RODRIGUES, Camila Cristine Torres dos Reis [1], ARAÚJO, Graziela [2]
RODRIGUES, Camila Cristine Torres dos Reis; ARAÚJO, Graziela. Cambios sistémicos asociados con puente cardiopulmonar (CPB). Revista científica multidisciplinaria base de conocimiento. año 03, Ed. 05, vol. 02, pp. 36-54, mayo de 2018. ISSN:2448-0959
Resumen
Introducción: el puente cardiopulmonar (CPB) hecho posible nuevas curas en enfermedades del corazón, pero hay complicaciones que se pueden accionar durante o después de la cirugía. Objetivo: Relacionar los principales trastornos sistémicos asociados con derivación cardiopulmonar; identificar los principales trastornos hematológicos; definir cambios inmunológicos y correlacionando las implicaciones renales y pulmonares. Materiales y métodos: se trata de una revisión de la literatura científica bases de datos de SciELO, LILACS y en PUBMED que abarca publicaciones nacionales e internacionales en el periodo de 1993 a 2014. Resultados y discusión: a pesar de la modernidad el cuerpo reconoce ECC como sistema de estaño, generar una respuesta inmune que puede evolucionar rápidamente a un síndrome de respuesta inflamatoria sistémica (señores) y también una respuesta hematológica a través de la coagulación de la sangre, es esencial para prevenir trombosis anticoagulate paciente durante la cirugía con CEC, el tiempo que el paciente durante el postoperatorio, es susceptible a la hemorragia por varios factores. Problemas de riñón y el pulmón se observan comúnmente después de CPB por una multitud de factores, algunos casos evolucionan rápidamente a Insuficiencia Renal aguda (IRA), mientras que la disfunción pulmonar sigue siendo la mayor causa de morbilidad después de la operación. Reflexiones finales: el CEC debe usarse cuando es la única forma de recurso operativo para pacientes del corazón, porque hay complicaciones asociadas con esta técnica para aumentar las tasas de morbilidad y mortalidad. Sin embargo, existe una interrelación compleja de la intervención quirúrgica, la anestesia y la CCA que es difícil asignar todas las complicaciones para el uso exclusivo de la CCA.
Palabras clave: Perfusión extracorpórea, corazón y pulmón, complicaciones sistémicas.
Introducción
Cirugía cardíaca con derivación cardiopulmonar puesto que el siglo XX fue uno de los mayores logros en el área de la salud, ya que trajo un gran avance en medicina, significativamente reducir el número de muertes y que la posibilidad de nuevas curas en enfermedades del corazón 16.
En 1953, John h. Gibbon realiza la primera cirugía exitosa de corazón utilizando la técnica del bypass cardiopulmonar (CPB). Este procedimiento está destinado a tomar la función temporal del corazón y los pulmones cuando el paciente somete a un procedimiento quirúrgico. Por lo tanto, un conjunto de máquinas, dispositivos y circuitos mantener circulación activa, mientras que estos órganos están excluidos de circulação43.
Según Lima23 (1997), no todos los pacientes sometidos a cirugía cardíaca utilizando la técnica de circulación extracorpórea, porque aunque es un método que ha mejorado enormemente en los resultados, se sabe que ciertos inconvenientes todavía existen, tales como: reacción inflamatoria, hemodilución, movimiento, morbilidad, además de aumento de los costos. Por lo tanto, cuando sea posible, utilizar otras técnicas sin la ayuda de la CCA a la menor agresión al paciente.
Con la aparición de la CCA, nuevos estudios han aparecido vinculados a una fisiología diferente. Sin embargo, estas habilidades han beneficiado no sólo las cirugías cardiovasculares, sino también todas las especialidades, obtención de conceptos para el cuidado de los pacientes durante la cirugía e incluyendo el período posterior post-operatório17.
Por desgracia, una de las principales características de los pacientes sometidos a cirugía cardíaca con CEC es la facilidad del órgano sistemas son afectados por los cambios en la función del sistema cardiovascular. Una variedad de complicaciones puede ocurrir después de cirugía de corazón, en frecuencia se encuentran: hemorragia, disfunción respiratoria, bajo débito cardiaco, disfunción renal y cambios neurológicos infecções43.
Así, el objetivo de este estudio fue relacionar los principales trastornos sistémicos asociados con el uso de puente cardiopulmonar; identificar los principales trastornos hematológicos; definir cambios inmunológicos y correlacionando las implicaciones renales y pulmonares del paciente de puente cardiopulmonar.
Materiales y métodos
Se trata de una revisión de la literatura con investigación bibliográfica utilizando bases de datos científicas de SciELO y LILACS, PUBMED. Los elementos encontrados fueron leídos y seleccionaron, publicaciones nacionales e internacionales que cubre en el periodo de 1993 a 2014.
Las palabras clave usadas en la búsqueda fueron: perfusión extracorpórea, corazón, pulmón, cambios sistémicos.
MARCO TEÓRICO
Puente cardiopulmonar (Cpb)
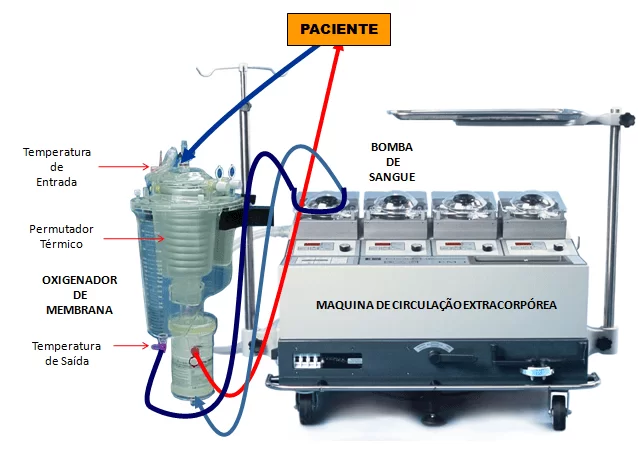
Durante la CEC, funciones bombeo del corazón se realizan por una bomba mecánica y las funciones de los pulmones se sustituyen por un dispositivo capaz de realizar intercambio de gases con la sangue20.
En este contexto, para el buen entendimiento de las complicaciones sistémicas relacionadas con este procedimiento, es necesario el básico la comprensión en el circuito de la sangre durante el bypass cardiopulmonar.
Así, en CEC, se desvía sangre desoxigenada desde el corazón y los pulmones a la aurícula derecha del paciente, a través de tubos colocados en la vena Cava superior e inferior. Por un hilo común, la sangre venosa se lleva el oxigenador, depósito de membrana semipermeable para la separación de oxígeno arterial y la realización de comercio gasosas8.
El oxigenador, la sangre se bombea a un punto en el sistema de la sangre del paciente, generalmente el ascendente de la aorta, donde viaja a través del sistema sanguíneo y se distribuye a todos los órganos, dando oxígeno a los tejidos para llevar a cabo procesos de la vida y que recoge la produce dióxido de carbono en ellos. Después circula a través del sistema capilar de los tejidos, la sangre hacia el sistema de la parte superior e inferior arcos las venas, donde se continuamente extenderá a la CCA por el final de la cirurgia14.
Para la realización de cirugía cardíaca con CEC algunos procedimientos han sido adoptados a lo largo de la historia para mejor, como hipotermia, el uso de soluciones cardioplégicas y hemodilución.
La hipotermia se asoció con circulación extracorpórea, con el objetivo de reducir las necesidades metabólicas de los pacientes y, por tanto, su consumo de oxígeno, ofreciendo protección adicional al cuerpo, especialmente los órganos vitales, prevención de lesiones de anóxia7. Él actualmente trabaja en central hipotermia es inducida por el enfriamiento de la sangre con agua y hielo en el intercambiador de calor del oxigenador, para que a través de la sangre fría la circulación en los órganos se produce enfriamiento. La revocación de la hipotermia, es decir, recalentar al paciente obtiene circulando agua caliente en el intercambiador de calor43.
Soluciones cardioplégicas, ricas en potasio, se utilizan para prevenir las lesiones del miocardio, llevando a una parada casi instantánea de corazón, sin consumo de energía. Otras cosas, para la protección miocardio el uso juicioso de soluciones cardioplégicas e hipotermia, por lo que, después del procedimiento quirúrgico, se producen en el estado normal de homeostasis metabólica7.
Antes del inicio de la CEC, para llenar el depósito del oxigenador y el resto de los componentes del circuito, proceso conocido como desareação, uso de celulares, no soluciones de solutos cristaloides o coloides (llamada solución o primer) así ocurre una dilución de la sangre. Estudios han demostrado que esto mejora la oxigenación de hemodilución durante la perfusión, reduciendo la cantidad total de sangre necesaria para cada paciente, durante y después de la operación, preservando a un mayor número de plaquetas, así como reducir la pérdida de sangre post-operatórias3.
Las complicaciones sistémicas Post CEC
Circulación extracorpórea debido a la multiplicidad de componentes mecánicos y las interacciones con la sangre produce varios cambios en el cuerpo humano que generan grandes desviaciones de la fisiología, o poco después de la perfusión o post-operatoria temprana 31, 50.
A pesar de todo la modernidad de los equipos en uso, más tiempo de CEC, mayores las posibilidades de complicaciones. Además, las condiciones intrínsecas tales como edad, peso, uso de medicamentos, enfermedades, entre otras, pueden comprometer el estado final del paciente. Se sabe, por ejemplo, que los pacientes ancianos y los niños menores de tres meses tienen peor pronóstico, puesto que están en mayor riesgo de hipotermia, porque los niños pequeños son más propensos a la dispersión del calor y ancianos anestesiado el límite para vasoconstricción es el nivel de temperatura más baja en adultos jovens24 más.
Cleveland13 (2001) no reportaron una mortalidad de 2,9% en la cirugía con CEC y 2,3% CEC, por otra parte, pacientes operados sin CEC presentó 10.6% de complicaciones, en comparación con 14% de los operados con CEC.
Una variedad de complicaciones puede ocurrir después de la cirugía del corazón y grandes vasos, algunos relacionados con la anestesia, manejo otros relacionados con la cirugía y otras relacionadas con puente cardiopulmonar. A menudo, es difícil asignar una complicación particular a un procedimiento específico, dependiendo de la interrelación de los procedimientos en el quirófano. Por lo tanto, subraya que las complicaciones más frecuentes son las complicaciones inmunológicas, hematológicas, pulmonares y renais16.
Desordenes hematológicos
Los trastornos hemorrágicos relacionados con CEC invariablemente enfrentan a los cambios de la coagulación de la sangre, una vez que la sangre circula a través de tuberías y aparatos que son superficies no endoteliales. Y, aunque son materiales compatibles, sin embargo, son las superficies extrañas, capaces de estimular al mismo tiempo, en mayor o menor medida, sistemas de coagulación y imunológico36.
Ocurre, por lo tanto, un desequilibrio de la hemostasia de la sangre durante el CPB es el más común es la aparición de eventos trombóticos, mientras que después de la CEC se divulga generalmente hemorragia Marcos.
Así, durante la CEC, las vías intrínsecas y extrínsecas de la cascada de coagulación se activa, el primero a través del factor XII en contacto con la superficie artificial y el segundo por la liberación de factor tisular (TF), ambos que culminó con la formación de un coágulo.
Además, cuando la sangre es aspirada del campo quirúrgico y volvió a darme un circuito by-pass, una serie de otros elementos, tales como: fragmentos de coágulos o grasa, tromboplastina del tejido y materiales de desecho, aumenta el riesgo de trombose29.
El CEC induce aún cambiando la fibrinolisis con disminución en la formación de plasmina, que favorece la aparición de trombos36. De esta manera, la Asociación de estos factores indica la importancia de heparinización paciente al comienzo de la perfusión para evitar la coagulación de la sangre previniendo los eventos trombóticos9.36.
La heparina diluyente de la sangre es el más utilizado para este propósito, porque tiene pocos efectos secundarios, sin molestias y no hay un antídoto específico, protamina, que se utiliza al final de la perfusión para neutralizar el efecto anticoagulante de la heparina porque el sangrado post quirúrgico puede ocurrir porque el sangrado efecto de la heparina. Es válido mencionar que acción de heparina simple neutralización por dosis adecuadas de administración de la protamina restaura la actividad hemostática sólo parcial, no pudiendo recuperar inmediatamente la función hemostática de pacientes sometidos a CEC45.
Por otra parte, hay varias causas para el sangrado post CEC, tales como: hemodilución, consumo de la coagulación de los factores, el cambio cuantitativo y cualitativo de las plaquetas, la hipotermia, la inmunorespuesta del anfitrión en la formación de complejos heparina-protamina y hemostasia quirúrgica inadecuada. Algunos pacientes necesitan, por lo tanto, re-intervención porque el sangrado en el período postoperatorio temprano y a menudo no se puede identificar la causa del sangrado en cirugía 1, 28.
El paciente durante y después de la CEC puede desarrollar trombocitopenia debido varios factores, como: depósito de plaquetas sobre las superficies internas de tuberías, oxigenadores y filtros; resultado de la acción de la heparina utilizada para la anticoagulación; total reducción de la capacidad debido al contacto con las superficies no endoteliales circuitos y aparatos; hiponatremia por dilución efecto sobre las plaquetas debido a la hemodilución; Además el secuestro de numerosos plaquetas por el bazo y el fígado27.
Según Ascione2 et al. (2001), en estudios prospectivos con grupos aleatorios de bajo riesgo preoperatorio se encontró sangrado marco 1.6 veces mayor en el grupo con derivación cardiopulmonar que sin puente cardiopulmonar. Se indica que menos del 20% de los pacientes sin CEC necesita transfusión de sangre, en comparación con más de la mitad del grupo con CEC.
Otros estudios han demostrado que la arteria coronaria (CABG) injerto de puente sin puente cardiopulmonar tiene ventajas en relación con RM con bypass cardiopulmonar, comparado con menos sangrado postoperatorio y menor necesidad de transfusión de concentrado de glóbulos rojos, minimizando el morbo hospitalares1 factores y costos.2. Así que en la actualidad, las cirugías de MRI se realizan sin CPB.
Se sabe que aproximadamente 10 a 20% de los pacientes que se someten a la función CEC excesiva sangrado poco después de la cirugía, requieren de 5 a 10% en las primeras horas poco después de la cirugía de recambio sanguínea6.
Según Souza43 et al. (2006) la interacción compleja de varios factores (Hemodilución, hipotermia, trauma, interacción de la plaqueta de perfusión con endotelial no emerge, la deposición de fibrinógeno en los tubos, reduciendo el número y actividad de las plaquetas en circulación y favor de la liberación de un número de plaquetas activación de sustancias) la ocurrencia de trastornos de la hemostasia y coagulación.
Además de los propios cambios mencionados, CPB hemorrágica también promueve la hemólisis de los eritrocitos debido principalmente a la desviación de la circulación normal por el uso de cánulas que forma y también por la agitación inadecuada calibración de las bombas de rodillo de los centros Sistema. Sin embargo, para equipos quirúrgicos que utilizan el sistema de succión cardiotomia o cardiotômica, encargado de aspirar la sangre extravasada en el campo operativo, esta práctica es la mayor causa de hemólisis, porque cuando el aire es aspirado con sangre a través de los daños de la aspiradora se le ocurre a la vermelhas11 de células.51.
Hemólisis aguda culmina en marcos de hemoglobinemia y hemoglobinuria, que pueden influir en la filtración glomerular para la obstrucción de los glomérulos, glomerulares generando una falla renal34.
Cambios inmunológicos
Cuando el corazón se queda sin sangre durante la CEC, es decir se paró al instante, asociados con la interacción con materiales extraños al cuerpo se produce como consecuencia de la activación de la respuesta inmune con posibles repercusiones para las complicaciones futuras9.
La sangre en contacto con las superficies artificiales del circuito de perfusión activa el sistema del complemento, así como la respuesta inflamatoria. Con el complemento sistema de activado son liberados de las anafilatoxinas C3a y C5a que estimulan la producción de citocinas y varios mediadores del proceso inflamatorio. Además, los glóbulos blancos también se activan por poder quimiotáctico de las anafilatoxinas, con la consiguiente vasocontrição y aumento de la permeabilidad vascular, llevando a la acumulación de agua en el interstício29, 38, 49.
Este proceso es la coagulación de la sangre también activado y mayor adhesión de neutrófila a las células endoteliales, que es una condición esencial en todos los procesos que conducen a lesiones tecidual10.
Así, los neutrófilos se activan y liberan sustancias que contribuyen a la formación de la reacción inflamatoria generalizada. Durante la perfusión, neutrófilos tienden a acumularse en los pulmones, donde sus productos tóxicos producen aumento de la permeabilidad vascular y edema intersticial. Además, otros leucocitos activan liberación radicales libres de oxígeno que en ciertas circunstancias puede producir oclusión microvascular30.
Esta cascada de reacciones inflamatorias son síndrome de respuesta inflamatoria sistémica (señores) y puede manifestarse en menor o mayor grado, siendo más evidente nociva y en personas de edad avanzada y neonatos17.
Los señores también llaman el síndrome de pós-perfusão, características clínicas muy similares a shock séptico. Clínicamente lo señores pós-CEC se caracteriza por la debilitación de la función pulmonar, renal, corazón, cerebro, presencia de taquicardia, hipotensión arterial, fiebre, leucocitosis, hemorragia trastornos, susceptibilidad a las infecciones, cambios en permeabilidad vascular conduce a la acumulación de líquido intersticial, vasoconstricção y hemólise35.
La frecuencia de manifestaciones clínicas del SRIS después de CEC varía entre 22% y 27,5%, aunque ha sido evaluado por distintos métodos15. En 1993 un estudio informó la incidencia de 27,5% del SRIS en niños en los que el criterio de diagnóstico utilizado fue adaptada de la definición de SRIS en pacientes clínicos41.
En las cirugías de la RM se observó los señores en el cuerpo de la respuesta protectora alrededor del 11%, con una alta tasa de mortalidad del 41% 25.
Otros datos relevantes, es que el CEC es seguido por síndrome de dificultad respiratoria agudo (SDRA) con frecuencia de 0,4% en la población adulta, y hay una alta mortalidad associada15, 28.
Según Torrati47 et al. (2012) la CEC produce una respuesta inflamatoria sistémica a la vista de los cambios en la permeabilidad vascular y disminución en la presión oncótica, con liberación de sustancias que afectan la coagulación y la respuesta inmune, conduciendo a las complicaciones en el período postoperatorio inmediato.
En algunos pacientes, la respuesta exacerbada la defensa sistema del organismo se produce por la liberación de sustancias vasodilatadoras como la bradicinina, y su acción paraliza vasculatura arteriolar, que complica la salida de perfusão29. Porque su motor de vasoativo produce aumento de la permeabilidad vascular y vasodilatación arteriolar, favoreciendo la extravasación de líquido al intersticio, y bradicinina seguirá siendo alta durante la CEC porque su sitio pulmonar metabolismo se excluye de la processo38.
Algunos pacientes pueden desarrollar resistencia a las heparina o hipersensibilidad las reacciones causadas por complejo heparina-protamina, agravando las respuestas protectoras del sistema imunológico22.
Un estudio comparativo de la RMN con y sin CEC identificaron una respuesta inflamatoria por aumento de las concentraciones de proteína C reactiva (PCR) y fibrinógeno 12:00 am después del procedimiento. La RM con evidencia bioquímica de CEC de principios Pro-trombótico no estado después de la cirugía, sin embargo, ninguna evidencia de un aumento en el número de eventos trombóticos. Este estado puede ser una consecuencia de la Pro-trombótico Dame un circuito by-pass, respuesta compensatoria a la sangría o ambos32.
Cabe mencionar que la respuesta inflamatoria desencadenada por la CEC es significativamente menor cuando el tiempo de infusión es de menos de 70 minutos52.
Cambios renales
Insuficiencia renal en el período post CEC es un evento serio que se relaciona con la alta tasa de mortalidad y morbilidad. A pesar de toda la evolución de la tecnología en puente cardiopulmonar, renal continúa mostrando alta incidencia, el desarrollo de esta complicación y multifatorial44 complejo.
En los primeros momentos del marco común de la CCA de hipotensión debido a una multitud de factores tales como: la reducción de la perfusión flujo hemodilución con reducción de la viscosidad de la sangre y el aumento de la bradicinina vasodilatadores. Después de este período, el cuerpo inicia una respuesta compensatoria que a menudo resulta en hipertensión. Así, la vasoconstricción producida por hipotermia, la elevación de la resistencia vascular sistémica y la ausencia de pulsatilidad de la circulación contribuye a este hipertensiva43 respuesta.
Sin embargo, como consecuencia de la vasoconstricción renal, se produce una reducción en el flujo sanguíneo renal, los riñones que predispone a isquemia y lesión. De esta manera, se reduce la energía disponible a los mecanismos de la actividad normal del riñón, haciendo reabsortivas y renais48 de funciones secretoras.
Además, la hemodilución con soluciones de cristaloides, en exceso, predispone al paciente a la formación de edema, debido a la reducción de la presión osmótica-coloido del plasma, disminuyendo la reabsorción de los capilares peritubulares, resultando en un medio acuoso y diuresis Rica en electrolitos y pueden culmina en un desequilibrio de hidroeletrolítico39.
La hemólisis causada en la CEC produce vasoconstricción por liberación de productos de vasoativos del interior de las células y porque es una molécula grande, la hemoglobina se filtra con dificultad y puede cristalizar en los túbulos renales, causando obstrucción y necrosis tubular34, 37.
Otros factores también son responsables de la producción de disfunción renal, enfermedad renal, incluyendo el uso de fármacos nefrotóxicos, agentes de isquemia renal, vasoconstricción severa, hipotermia extrema y hemodilución profunda44.
En pacientes ancianos el riesgo de desarrollar insuficiencia renal aguda trastornos más a menudo, porque este grupo de pacientes viene más a menudo con otras enfermedades como: diabetes, enfermedad vascular periférica, marginal de reserva renal y fiebre Henoch-Schönlein. Por lo tanto, una medida cautelar es importante añadir manitol a la solución, con el objetivo de proteger contra la lesión isquémica del tejido renal47.
Sin embargo, existen varias evidencias que los efectos deletéreos de puente cardiopulmonar en los riñones, incluyendo la producción de insuficiencia renal aguda, están relacionados con la duración de la infusión. Esto fue comprobado en el estudio de Taniguchi44 et al., (2007) que identificó la influencia negativa del tiempo de CEC en la función renal de la creatinina sérica mayor, la variación de la creatinina sérica y una incidencia más alta de la diálisis en pacientes con un tiempo CEC mayor de 90 minutos.
La insuficiencia renal en cirugía cardíaca tiene una incidencia entre 3.5% y 31.0%, con mayor tasa de mortalidad de 0.4% a 4,4% a 1.3% al 22,3%; y la necesidad de la terapia Dialítica está presente en el 0,3% a 15.0% de los casos, y en estos, la tasa de mortalidad alcanza el 25.0% 88.9% 26.
La cirugía cardiaca con la ayuda de la CCA tienen algunas implicaciones típico y algunos más grandes y más frecuentes que otros. Entre ellos está incluida la insuficiencia renal con el proceso de evolución a la insuficiencia renal aguda (IRA) que se produce en promedio 7% al 30%. Se cree que factores genéticos, como la ateroesclerosis, la diabetes y la hipertensión incluso pueden contribuir en la disfunción renal poco después operatório46.
Cambios pulmonares
En los últimos años, el avance y la sofisticación de las técnicas de infusión y equipos, hubo una reducción de las complicaciones pulmonares. Sin embargo, aún constituye la causa más importante de la morbilidad postoperatoria con tan rápida evolución que se resiste a todos los terapêuticas39 de medidas.
El paciente experimentó una cirugía cardíaca con CEC suelen presentar un grado de disfunción pulmonar con disminución de la capacidad funcional residual de los pulmones. Se produce en los pulmones, un aumento en la fuga de agua intersticial causada por las células inflamatorias, llenado alveolar, que conduce a la inactivación del surfactante y el colapso de algunas regiones y la capacidad pulmonar reducida. Además, la exposición a la hipotermia durante la CEC también afecta la función pulmonar negativamente, causando lesiones en el endotelio pulmonar12.
Otro factor que contribuye a post de disfunción pulmonar CEC son las dosis de anestésicos y sedantes que comúnmente Oprima ventilación, reducción de la capacidad residual para trabajar alrededor de 20% 5.40.
Así, la fisiopatología de la disfunción pulmonar es multifactorial, con la combinación de los efectos generados por la anestesia, la incisión quirúrgica, tiempo de isquemia, trauma quirúrgico en el bypass cardiopulmonar y la activación del sistema inmune. Estos factores presentan una gran importancia en la aparición de complicaciones respiratorias en el postoperatorio de cirugía cardiaca 4.21.33.
Múltiples complicaciones pulmonares ocurren en el postoperatorio de cirugía cardiaca, entre las que destaca de la atelectasia con un promedio entre 60% incidencia 90% de los casos, un número 6 veces mayor que las cirugías de corazón sin CEC18, 33.
La atelectasia pulmonar es la principal causa de la hipoxia que se produce después de la cirugía con CEC, provocando una reducción en el intercambio de gases y principales problemas pulmonares tales como: compresión del parénquima pulmonar, absorción del aire alveolar y compromiso surfactante5 función.42.
Entre todos los órganos afectados por el post cirugía CEC, el pulmón tiende a ser más comprometido. Aunque se produzcan varios factores asociados con el aumento del agua intersticial, la más importante es el depósito de neutrófilo en la microcirculación pulmonar, principal sitio de secuestro de neutrófilo activado. Estas células liberan enzimas lisosomales y radicales libres de oxígeno, causando lesión endotelial directa y mediante la alteración de la permeabilidad vascular, con la consiguiente acumulación de agua en el intersticial pulmonar38.
Los estudios demuestran la CEC como una de las principales causas de la lesión pulmonar debido a la resistencia de vía aérea mayor y posible aumento de la disfunción diafragmática y toda cirugía cardiaca plantea pulmonar daño, sin embargo el CEC es maior21.
Sin embargo, el estudio de Montes34 et al. (2004) informa que no hubo diferencias significativas en la función pulmonar, 72 horas después de la cirugía, pacientes operados con y sin CEC, los cuales tuvieron una reducción.
Muchos estudios muestran que el tiempo de guardia en la sala de operaciones es mayor en pacientes que utilizaron el CEC 22.28.43, 53… Algunos autores afirman incluso que pacientes que usan el CEC crean mayor dependencia de ventilación mecánica en el post-cirúrgico1 el.38. Sin embargo, este tema es aún controversial ya que hay datos que no muestran diferencias significativas al comparar los grupos con y sin CEC. Asimismo, algunos datos indican que no hay ninguna diferencia en tiempo medio a la extubación entre pacientes operados con y sin CEC 11.29.
Consideraciones finales
Incluso con el gran desarrollo de la CCA en sus más de 50 años de historia en Brasil, todavía hay muchas implicaciones observadas el uso de esta técnica, que a pesar de ser la única forma de recursos operativos para corazón muchos procedimientos pueden tener un impacto en complicaciones graves, siendo responsable de extender la duración de la estancia con los costos de hospital mayor, así como causas importantes de morbilidad y mortalidad.
En grandes cirugías ya que hay una interrelación compleja de la intervención quirúrgica cardiaca, anestesia y la CEC (sobre todo en relación al tiempo de la cirugía), así como factores relacionados con el paciente y por lo tanto cuestionable etiología de cambios sistémicos.
Referencias
1. ATIK, Fernando Antibas; SAMPATH, Leonardo Augusto; Fábio B. Jatene, JÚNIOR, José Octavio C. Auler; OLIVEIRA, Sérgio Almeida. La revascularización miocárdica sin derivación cardiopulmonar reduce al mínimo la necesidad de sangrado y transfusión postoperatoria. ARQ. Bras. Cardiol. Vol. 83 Nº 4 Sao Paulo de octubre de 2004.
2. ASCIONE R, WILLIAMS S, LLOYD CT, SUNDARAMOORTHI T, PITSIS AA, ANGELINI G d. reducida prostoperative sangre pérdida y transfusión requisito después de operaciones coronarias de corazón: un estudio de ensayos. J Thorac Cardiovasc Surg 2001; 121:689-96.
3. ADAMS, James Davis. Inmediatamente después de cirugía cardiaca. Brasilia, 2013.
4. ARP AMBROZIN, DI GIACOMO CATANEO AJM. Aspectos de la función pulmonar después de la arteria coronaria bypass injerto relativos a riesgo preoperatorio. Rev Bras Cir Cardiovasc. 2005; 20 (4): 408-15.
5. AULER JUNIOR, José Octavio Costa; GALAS, Filomena Regina Barbosa Gomes; HAJJAR, Ludhmila Abraham; FRANCA, Zelda. Ventilación mecánica intraoperatoria. São Paulo, 2007.
6. BARROSO, Roberto Cardoso; MENDONDÇA, de Jose Teles; CARVALHO, Ramos Marcos; Costa Rika Kakuda; SANTOS, José Akil. Evaluación de protamina en heparina de neutralización después de puente cardiopulmonar. Rev Bras Cir Cardiovasc vol. 17 Nº 1 São Paulo enero 2002/Mar…
7. BIAZZOTTO, Camilla B.; BRUDNIEWSKI, Márcio; SCHMIDT, Andrew P.; Junior, José Otávio Auler costa. Hipotermia períoda perioperatorio. Rev Bras Anestesiol 2006; 56:1: 89-106.
8. BISCEGLI, J. F; ANDRADE, A. J. P; PAULISTA, P. P. DARLINGTON, S. A; SOUZA, L. C. (B); RUEDA, J.; TOFFANO, R. M.; PICCINI, b. evaluación clínica de un oxigenador de membrana bajo volumen ("cebado") de relleno. São Paulo, 1999.
9. BRASIL L; GOMES W J; SOLOMON R; FRANCISCO J H P; BLANCO J N R, BUFFOLO y corticoesteroide uso como inhibidor de la respuesta inflamatoria sistémica inducida por el bypass cardiopulmonar. Rev Bras Cir Cardiovasc 1999; 14 (3): 254-68.
10. BORIWIEC JW, HAGMAN TH PEKNA M, P VENGE, THELIN s. circulación citocinas y enzimas derivadas de granulocitos durante cirugía cardíaca compleja: un estudio clínico con especial referencia a circuitos de bypass cardiopulmonar de recubrimiento de heparina-de. SCAND J Thorac Cardiovasc Surg 1995; 29 (4): 167-74.)
11. CASTRO, Reginaldo Parmar; CROTI, Ulises Alexander; MACHADO, Maurice de Nassau; MUTILLO, Harold González; Rincón Omar Yesid Prieto; Policarpo, Sebastião Rodrigues; FOX, Renata Geron; Braille, Domingo Marcolino. Modificación de la técnica de ultrafiltración en el tratamiento quirúrgico convencional de defectos congénitos del corazón. Rev Bras Cir Cardiovasc vol. 21 Nº 1 São José do Rio Preto enero 2006/Mar.
12. CLARK SC. Lesión pulmonar después de puente cardiopulmonar. Perfusión. 2006; 21 (4): 225-8.
13. CLEVELAND JC, LW SHROYER, CHEN AY, PETERSON Y GROVER, FL. Coronaria de la apagado-bomba puente injerto disminuye riesgo ajustada mortalidad y morbilidad. Ann Thorac Surg 2001; 72:1282-9
14. COLAFRANCESCHI, Alexander sicilianos; Monteiro, Andrey José de Oliveira; CANALE, Leonardo Secchin; CAMPOS, Luiz Antonio de Almeida; MONTERA, Marcelo Westerlund; SILVA del da de Paulo Roberto Dutra; FERNANDES, Marcelo Ramalho; PINTO, Alexander de Araújo; Resortes, Stelmar Moura; Mezquita, Evandro Tinoco. ¿Asistencia circulatoria con oxigenación de membrana extracorpórea (ECMO) en adultos: un concepto de quiebra u olvidados? ARQ. Bras. Cardiol. Vol. 91 no. 1 San Pablo julio de 2008.
15. COSTA SOARES, Leonardo Dug; RIBAS, Denise; PRIMAVERA, Regine; SILVA, Jean Marcelo Ferreira da; MIYAGUE, Nelson Itiro. Perfil clínico de respuesta inflamatoria sistémica después de la cirugía cardiaca pediátrica con derivación cardiopulmonar. ARQ Bras Cardiol 2010; 94 (1): 127-133.
16. DIENSTMANN, Carolina; CAREGNATO, Rita Catalina Aquino. Circulación extracorpórea en cirugía cardíaca: un campo de trabajo para la enfermera. Reverendo SOBECC, São Paulo. Ene/mar. 2013; 18 (1): 35-43.
17. El domingo, M Braille. Puente cardiopulmonar. Rev Bras Cir Cardiovasc vol. 25 Nº 4 Sao Jose do Rio la Preto octubre 2010/Dec…
18. LC DE FIGUEIREDO, AGUILAR S, RCS ABDALA, ABDALA, CAV DE GH. CPAP a 10 cmH2O durante el bypass cardiopulmonar mejora intercambio gaseoso posoperatorio. Rev Bras Cir Cardiovasc. 2008; 23 (2): 209-15.
19. FONSECA, J.W. G; BISCEGLI, J. F; RUEDA, J.; POLANSKY, M. R; AKIKUBO, r. diseño y desarrollo de un termómetro para la circulación. II muestra SES, São Paulo 2008.
20. GARCIA, Walter J.; SABA, John C.; BUFFOLO, Enio. 50 años de puente cardiopulmonar en Brasil: j. Hugo Felipozzi, el pionero de puente cardiopulmonar en Brasil. Rev Bras Cir Cardiovasc vol. 20 núm. 4 Sao Jose do Rio la Preto octubre 2005/diciembre…
21. GUIZILINI S, GARCIA WJ, FARESIN SM, DW BOLZAN, ALVES FA, CATANI R, et al. Evaluación de la función pulmonar en pacientes sometidos a revascularización miocárdica con y sin circulación extracorpórea. Rev Bras Cir Cardiovasc. 2005; 20 (3): 310-6.
22. JOÃO Paulo Ramos, David; JAIN, Fernando haría. Atención inmediata en el postoperatorio de cirugía cardiaca. Rio de Janeiro (RJ) 2003.
23. LIMA, Leonardo Edwards. Cirugía cardiaca menos invasiva. ¿Un fenómeno de moda o un método del futuro? Comentario editorial. Hospital La Pitiè-París, Francia, 1997.
24. HIJO del lobo, José Glauco; Cochinillo, Maria Claudia de Azevedo; MUCHACHO del lobo, Heraldo Guedis; Smith, John Paul Holland; MAGALHÃES, George Aguilar; LEO SON, Carmelo Sen Ram; FEITOSA, José Francisco Acacio; Oliveira Martins; LAVOR, Arnobius; SOARES FILHO, Odair; Borges, Elita; ABREU, de José Sebastião; DIOGENES, Tereza Cristina Pinheiro; BARRETO, José Erirtônio hazaña; PAES Junior, José Nogueira. A la izquierda cirugía de revascularización coronaria sin CEC y no manipulación de la aorta en pacientes más de 75 años. Rev Bras Cir Cardiovasc 2002; 17 (3): 208-214.
25. Luciano Brandão Machado; NEGRI, Elnara Marcia; BONAFÉ, Wanderley Wesley; SANTOS, Luciana de Moraes; MALBOUISSON, Luis Marcelo Sá; CARMONA, María José Carvalho. Evaluación de los niveles de la función de citoquinas y pulmonar de los pacientes sometidos a cirugía cardíaca con derivación cardiopulmonar. Rev Bras Anestesiol 2011 de artículo científico; 61:3: 275-285.
26. BUCKS GJ MA MARRÓN, CHAN WY, HORTON D, TREW P, WHITWORTH JA. Falta renal aguda después de cirugía cardiaca: incidencia, los resultados y factores de riesgo. Aust N Z JMed 1995; 25:284-9.
27. SAMPATH, Leonardo Augusto; ATIK, Fernando Antibas; Moreira, Luiz Felipe; HUEB, Alejandro Ciappina; JATENE, Fabio Biscegli; AULER JUNIOR, José Octavio; OLIVEIRA, Sérgio Almeida. Factores de riesgo de sangrado postoperatorio después de cirugía cardiaca en pacientes adultos. Rev Bras Cir Cardiovasc 2004; 19 (3): 280-286.
28. MILOT J, J PERRON, LACASSE Y, LETOURNEAU L, PC de CARTIER, MALTAIS f. incidencia y predictores de ARDS después de cirugía cardiaca. 2001; 119 (3): 884-8.
29. Mota, André Lupp; Rodrigues, Alfredo José; ÉRVORA, Paulo Roberto Barbosa. Puente cardiopulmonar en adultos en el siglo XXI. ¿Ciencia, arte o empirismo? Rev Bras Cir Cardiovasc 2008; 23 (1): 78-92.
50 h MOURA, Hemilton Vieira; POMERANTZEFF, Pablo M.; García, José Walter. Síndrome de respuesta inflamatoria sistémica en la circulación extracorpórea: papel de las interleuquinas. Rev Bras Cir Cardiovasc 2001; 16 (4): 376-87.
31. NOGUEIRA, Celia R. S. R.; HUEB, Whady; Michou TAKIUTI, E.; GIRARDI, Nadia B. M.; NAKANO, Teryo; FERNANDES, Fábio; Felipe da s., PAULITSCH, Aécio GOIS t. f.; LEE, Neuza H. M.; STOLF, Noedir A.. Calidad de vida después de la revascularización miocárdica quirúrgica con y sin circulación extracorpórea. Artículo original. São Paulo, SP – Brasil, 2008.
32. PAULITSCH, Felipe da Silva. Cambios hemostáticos y clínicas de cirugía de revascularización miocárdica con y sin bypass cardiopulmonar: un estudio prospectivo randomizado. São Paulo, 2009.
33. PADOVANI, Cauê; CAVENAGHI, Odette Mauad. Reclutamiento alveolar en los pacientes en el postoperatorio inmediato de cirugía cardiaca. Rev Bras Cir Cardiovasc vol. 26 Nº 1 São José do Rio Preto enero/marzo 2011.
34. PUENTES, José Carlos Vieira Dorsa; SILVA, Guilherme Viotto Rao; BENFATTI, Ricardo Dhanashree; MACHADO, Natalia Pereira; PONTELLI, Renato; PUENTES, Jagan Rosaleda Cury. Factores de riesgo en el desarrollo de insuficiencia renal aguda después de la cirugía de revascularización miocárdica con CEC. Rev Bras Cir Cardiovasc 2007; 22 (4): 484-490.
35. SALLES, M.J.; SPROVIERI, S.R.; BEDRIKOW, R; PEREIRA, C.; CARDENUTO, S.L; AZEVEDO, P.R.; SILVA, T. M; GOLIN, v. revisión de.75, sepsis síndrome de respuesta inflamatoria sistémica y el estudio de la terminología y Fisiopatología. São Paulo, 1999.
36. SANTOS, Ari-Tadeo de la azucena; SPLETTSTOSSER, Juan Carlos; WARPECHOWSHI, Pablo; GAIDZINSKI, Mariana Maříž Pinto. Cardíaca y antifibrinolíticos en cirugía con bypass cardiopulmonar. Bras de Reverendo. Anestesiol. Vol. 57 Nº 5 Campinas septiembre 2007/octubre…
37. SANTOS, Fernando Oliveira; SILVEIRA, Marco Antonio; MAIA, Roberto Barreto; MONTEIRO, Marcelo Dantas Chao; MARTINELLI, Reinaldo. Falta Renal aguda después de cirugía de bypass de la arteria coronaria con bypass cardiopulmonar-incidencia, factores de riesgo y mortalidad. Salvador, BA. 2003.
38. SAVARIS, Laurel. Imunoinflamatória respuesta a la derivación cardiopulmonar: Estado. Bras de Reverendo. Anestesiol 1998; 48:2: artículo 126-136.
39. SOARES, Gustavo Mattos Teixeira; Fernández, Diego Costa de Souza; GONÇALVES, Mariana Paula Cunha; ALVES, Thales George das; DAVID, Lee Phlegon; HENRIQUES, Karina Mabel Castro; RIANI, Larissa Rodrigues. Prevalencia de las principales complicaciones postoperatorias en cirugía cardiaca. Rev Bras Cardiol. 2011; 24 (3): 139-146.
40. SANGANI, Dante Fanganiello; IASBECH, José Alberto; OLIVEIRA, Sérgio Almeida. Postoperatorio en cirugía cardiaca de adultos. São Paulo, 1998.
41. SEGHAYE MC, J DUCHATEAU, RG GRABITZ, FAYMONVILLE ML, MESSMER BJ, BURO-RATHSMANN K, et al. Complemento de activación durante el bypass cardiopulmonar en lactantes y niños: relación con múltiple postoperatorio fallo del sistema del órgano. Thorac Cardiovasc Surg. 1993; 106 (6): 978-87
42. SILVA, Naila Luisa Saiki; PIOTTO, Raquel Ferrari; BABU, Marcelo Adriano Ingraci; CROTI, Ulises Alexander; Braille, Domingo m. inhalación solución salina hipertónica como coadyuvante de la fisioterapia respiratoria para reversión de atelectasias en el postoperatorio cirugía cardiaca pediátrica. Rev Bras Cir Cardiovasc v. 21 n. 4 Sao Jose do Rio Preto/dez… 2006.
43. Souza, María Helena; ELIAS, Decio. Fundamentos de la derivación cardiopulmonar. Segunda edición, Río de Janeiro, Brasil, 2006.
44. TANIGUCHI, Fábio Papa; SHARMA, Ademar Rosa de; Martins, Antonio Sérgio. Tiempo de derivación cardiopulmonar como factor de riesgo para la insuficiencia renal aguda. Braz J Cardiovasc Surg 2007; 22 (2): 201-205.
45. TANAKA KA, THOURANI VH, WILLIAMS WH, duque PG, LEVY JH, GUYTON RA, heparina, PUSKAS JD-anticoagulante en pacientes sometidos a CEC y cirugía de revascularización de CEC, 2007.
46. TEIXEIRA SOARES, Gustavo Mattos; Fernández, Diego Costa de Souza; GONÇALVES, Mariana Paula Cunha; ALVES, Thales George das; DAVID, Lee Phlegon; HENRIQUES, Karina Mabel Castro; RIANI, Larissa Rodrigues. Prevalencia de las principales complicaciones postoperatorias en cirugía cardiaca. Río de Janeiro, 2011.
47. TORRATI, Fernanda Gaspar; DANTAS, Rosana Ap. Spadoti. Bypass cardiopulmonar y las complicaciones en el postoperatorio inmediato de cirugía cardiaca. ACTA paul. personal de enfermería. Vol. 25 no. 3 Sao Paulo, 2012.
48. UTLEY, J.R. EFECTOS RENALES DE PUENTE CARDIOPULMONAR –. EN GRAVLEE, G.P.; DAVIS, R.F.; UTLEY, J.R. extracorpórea. Principios y Williams práctica & Wilkins, Baltimore, 1993.
49. Uva, Joaquim Miguel Sennfelt de Sousa. Estudio prospectivo aleatorio de cirugía coronaria con y sin circulación extracorpórea. PORTO, 2009.
50. VEGNI, Ronaldo; BRAGA, Gustavo Ferreira de Fabricio; FREITAS, Marcia; DRUMOND, Luis Eduardo; PENNA, Guillermo; Y K, José; NOBLE, Gustavo Freitas; KALICHSZTEIN, Marcelo; JAPIASSÚ, Andre Miguel. Complicaciones después de la arteria coronaria bypass cirugía del injerto en pacientes de edad avanzada. Rio de Janeiro (RJ), Brasil, 2008.
51. JUNIOR de VIEIRA, Francisco Ubaldo; VIEIRA, Reinaldo Wilson; COSTA, Eduardo Tavares; ANTUNES, Nilson; PETRUCCI JUNIOR, Orlando; Pedro OLIVEIRA, Paulo Martins; SON SEN, Rua da Mota; VILARINHO, acuesta de Sousa; Severino, Elaine Soraya Babu. Reflujo de visualización en la sangre más limpia y reservorio de cardiotomia en derivación cardiopulmonar. Rev Bras Cir Cardiovasc vol. 24 núm. 4 Sao Jose do Rio la Preto octubre 2009/diciembre…
52. CW WHITTEN, COLINA GE, IVY R, GREILICH PE, LIPTON JM. ¿Influye la duración del bypass cardiopulmonar o pinzamiento aórtico, en ausencia de sangre o administración de productos sanguíneos, la respuesta de IL-6 a la cirugía cardiaca? Anesth Analg. 1998; 86 (1): 28-33
[1] Curso de Ciencias de la vida de estudiante
[2] Maestro de maestros del curso de la biomedicina