ARTIGO ORIGINAL
RODRIGUES, Camila Juliano Salvador [1], SILVEIRA, Elita Ferreira da [2], VARGAS, Rafael da Silveira [3], GIACOMO, Giordano Gatti de [4], BIANCHIN, Marino Muxfeldt [5]
RODRIGUES, Camila Juliano Salvador. Et al. Marcadores de células-tronco cancerígenas associados ao desenvolvimento e fenótipo agressivo no câncer de pâncreas. Revista Científica Multidisciplinar Núcleo do Conhecimento. Ano 05, Ed. 10, Vol. 12, pp. 102-122. Outubro de 2020. ISSN:2448-0959, link de acesso em: https://www.nucleodoconhecimento.com.br/saude/cancer-de-pancreas, DOI: 10.32749/nucleodoconhecimento.com.br/saude/cancer-de-pancreas
RESUMO
Contexto: As células-tronco cancerígenas, também conhecidas como células iniciantes do tumor, são sugeridas como responsáveis pela resistência a medicamentos e desenvolvimento do câncer devido, em parte, à sua capacidade de se auto-renovar e se diferenciar em linhagens heterogêneas das células cancerosas. Objetivo: Este estudo foi projetado para investigar o papel das células-tronco cancerígenas no câncer de pâncreas. Métodos: Uma análise clínicapatológica retrospectiva foi realizada em 112 pacientes diagnosticados com adenocarcinoma ductal pancreático entre 2005 e 2010, e a imuno-histoquímica foi realizada com anticorpos contra CD133, CD24 e OCT4. A coloração nuclear, citoplasmática ou membrana positiva para cada anticorpo foi classificada em intensidade de coloração, sendo classificada em grupos de coloração baixo/moderado ou forte. Os resultados foram analisados em relação aos parâmetros clínico-ológicos de cada paciente. Resultados: Houve uma relação estabelecida entre a coloração dos marcadores com algumas variáveis associadas ao pior prognóstico, sendo os três marcadores presentes na maioria das células tumorais e associados à progressão do tumor. Supomos que as células-tronco cancerígenas estão presentes desde o início do início do tumor e estão intrinsecamente relacionadas ao desenvolvimento do tumor. Embora a presença de células-tronco tenha sido associada à biologia molecular de vários tumores, sua expressão no câncer de pâncreas ainda não foi relatada clinicamente. Conclusão: A presença de células-tronco e seu papel na tumorigênese do câncer de pâncreas podem ser considerados como fatores prognósticos valiosos, embora o mecanismo envolvido precise de uma investigação mais aprofundada. O aumento de insights sobre o papel das células-tronco do câncer e da carcinogênese pode, em última análise, gerar novas ideias para abordagens diagnósticas e terapêuticas baseadas molecularmente.
Palavras-chave: Células-tronco de câncer, câncer de pâncreas, Antígeno AC133, Antígeno CD24, OCT4.
INTRODUÇÃO
Apesar do progresso no diagnóstico e tratamento do câncer nas últimas décadas, continua sendo uma das causas de morte mais comuns em todo o mundo. Embora potencialmente curável quando diagnosticado precocemente, o diagnóstico precoce continua sendo um desafio na prática clínica diária. Muitos cânceres são diagnosticados em estágio tardio, quando as opções terapêuticas não são mais eficazes (BARBOSA et al., 2018).
O adenocarcinoma ductal pancreático (ADP) é uma doença altamente agressiva geralmente diagnosticada em estágio avançado e para a qual poucas terapias eficazes estão disponíveis. É uma neoplasia cuja incidência é quase igual à sua mortalidade. A razão pela qual o câncer de pâncreas tem um prognóstico tão ruim e por que tem uma resposta terapêutica tão baixa à quimioterapia e radioterapia são perguntas que motivaram a busca de uma resposta que possa modificar o curso dessa doença. Apesar dos avanços nas técnicas cirúrgicas, que hoje são consideradas a única opção curativa, a taxa média de sobrevivência de 5 anos é inferior a 5% (1-3%) (BARBOSA et al., 2018; SOTO et al., 2006). Considera-se a neoplasia com o pior prognóstico de mais de 60 tipos de cânceres, fato evidenciado por sua taxa de incidência quase igualando a taxa de mortalidade (SAKORAFAS et al., 2000). Deve-se notar que a detecção precoce do câncer, em um estágio que ainda pode ser curado, está associada a uma maior eficácia terapêutica e é atualmente uma das formas de melhorar o resultado de pacientes diagnosticados com câncer de pâncreas (ALLEGRA; TRAPASSO, 2012).
A biologia molecular do câncer de pâncreas está diretamente relacionada à sua rápida progressão e baixa resposta terapêutica. Está bem documentado que o aparecimento de uma célula tumoral é o resultado de um acúmulo de mutações em seu DNA capaz de alterar morfológica e funcionalmente suas propriedades normais (FANG et al., 2013; RICCI-VITIANI et al., 2007). O desencadeamento desse processo e sua evolução molecular, culminando na formação da célula tumoral e suas características pertinentes, caracterizam o processo de carcinogênese. É bem compreendido na literatura que o desenvolvimento de uma neoplasia envolve um conjunto de mudanças moleculares que levam não apenas ao surgimento e sobrevivência de uma célula tumoral, mas à sua capacidade de invadir tecidos adjacentes e formar metástases distantes (LI; JIAO, 2003).
Entre os processos mais recentemente implicados na carcinogênese e progressão do tumor, as alterações nas células-tronco do câncer (CSCs) ainda são pouco estudadas no câncer de pâncreas sem resultados satisfatórios, e merecem maiores esforços para elucidar seus efeitos e relação na aquisição de um fenótipo maligno pancreático. Evidências recentes sugerem que os CSCs desempenham um papel crucial não apenas na geração e manutenção de diferentes tecidos, mas também no desenvolvimento, progressão e resistência terapêutica de diferentes tipos de tumores (BALIC et al., 2012).
Os CSCs pertencem a um grupo diferenciado de células dentro de um tumor com propriedades auto renovadores e diferenciadas, semelhantes às células-tronco normais, dando origem a linhas de células tumorais heterogêneas que formam um tumor. Eles podem dividir e originar várias células que compõem tumores, perpetuando assim seu crescimento e oferecendo resistência à quimioterapia por mecanismos ainda não bem compreendidos. Por isso, representam um importante alvo de pesquisa (TAI, 2005).
A agressividade intrínseca do câncer de pâncreas, com sua alta capacidade de invasão local, alto potencial metastático, diagnóstico tardio e resistência terapêutica, parece estar parcialmente relacionada à população de CSCs que compõem esses tumores (HU; FU, 2012). Além disso, mostrou-se que o PDAC contém não apenas uma população homogênea de CSCs, mas diversas subpopulações que podem estar envolvidas na progressão do tumor. Até agora, os CSCs pancreáticos identificados constituem uma minoria das células componentes tumorais (cerca de 1-5%), e têm uma alta capacidade de auto renovação (ANSARI et al., 2012). O aspecto clínico mais importante, no entanto, é que esses CSCs são altamente resistentes à quimioterapia e radioterapia, resultando em resistência e rápida recidiva da doença. Atualmente, um dos grandes desafios da oncologia é identificar e estudar as características desses CSCs, especialmente no PDAC, no qual poucas descobertas foram feitas (KOBAYASHI; NORONHA, 2015).
MATERIAIS E MÉTODOS
SELEÇÃO DE CASOS E AMOSTRAS DE TUMOR
As amostras de tecido foram de uma coorte de 112 cânceres pancreáticos consecutivos diagnosticados de 2005 a 2010, selecionados a partir dos cuidados de rotina do Hospital de Clínicas de Porto Alegre (HCPA), pelo Departamento de Patologia e Grupo do Trato Biliar e pâncreas. As análises imunohistoquímica foram realizadas em blocos de tecidos embutidos em parafina já armazenados no Departamento de Patologia do HCPA, após aprovação do Comitê Científico e do Comitê de Ética em Pesquisa em Saúde da instituição. As seguintes variáveis foram registradas a partir de prontuários: idade, sexo, grau de tumor, estado do linfonodo, ocorrência de metástase, tratamento recebido (tipo de cirurgia, radioterapia e quimioterapia), sobrevida livre de doenças e sobrevida geral.
ANÁLISE IMUNOHISTOQUÍMICO DE TISSUE MICROARRAY (TMA)
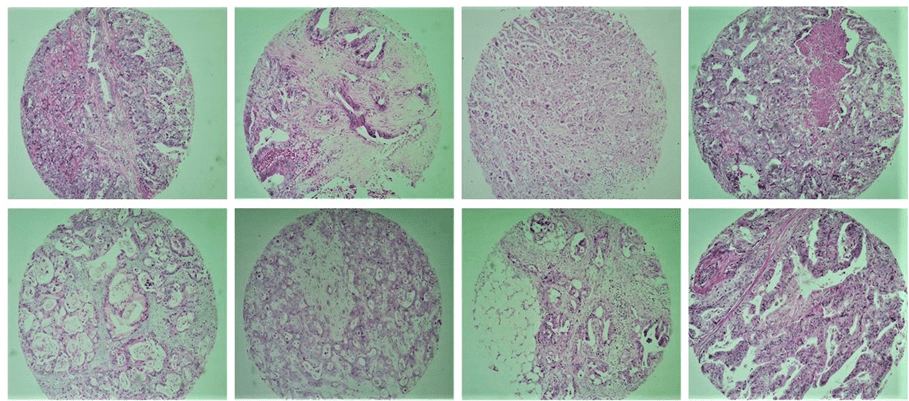
Tissue Microarray (TMA) matriz é uma técnica descrita pela primeira vez por Kononen et al. (1998) e é uma grande ferramenta para patologia investigativa. Trata-se de agrupar em um único bloco um número razoável de amostras de tecido, permitindo assim o estudo da expressão imunohistoquímica de marcadores moleculares, com grande uso do material, presença de controle interno e tempo e custo-benefício. Essa técnica também permite a padronização das reações, representação eficiente através do uso de diferentes áreas do tumor, estudo de grandes números de amostras simultaneamente, facilidade de interpretação e pesquisa em larga escala de fatores prognósticos ou preditivos do câncer (Figura 1).
Fig. 1. Exemplifica algumas amostras de tecido tumoral incluídas no estudo pela técnica TMA
ANÁLISE ESTATÍSTICA
Para verificar a associação entre variáveis imunohistoquímica e intensidade de imunorreação com as variáveis de caracterização dos indivíduos, utilizou-se uma abordagem não paramétrica com o teste exato de Fisher. Para verificar a associação da idade variável numérica com variáveis imunohistoquímica e intensidade, u foi utilizado o teste U Mann-Whitney.
A associação entre marcadores de células-tronco e diferentes características clinicopatológicas dos pacientes foi [incluindo idade, sexo, diferenciação tumoral, estágio, categoria Tumor-Nó-Metástase (TNM) e ressecção tumoral] avaliada pelos testes de coeficiente de correlação ou χ2 de Pearson, conforme apropriado. Para intensidade, as categorias foram dicotomizadas em baixa/moderada intensidade (0-2+) ou alta intensidade (≥3+).
O método Kaplan-Meier foi usado para estimar a probabilidade de sobrevivência. As curvas de sobrevivência foram comparadas utilizando-se o teste de log-rank, que afirma sob a hipótese nula de que as funções de sobrevivência não diferem umas das outras.
O tempo de sobrevida geral foi medido desde o momento da cirurgia ou biópsia até a data da morte (em decorrência de qualquer causa) ou até o último seguimento. O tempo de sobrevida livre de doenças foi medido a partir da data do diagnóstico histológico ou da cirurgia até a data do primeiro evento de falha livre da doença (definido como recaída locorregional), doença distante ou morte em decorrência de qualquer causa. A significância foi estabelecida em P < 0,05. Todas as análises estatísticas foram realizadas utilizando-se r (versão 3.6.0).
RESULTADOS
Análises imunohistoquímicas indicaram a presença de marcadores de superfície de células-tronco tumorais para os três anticorpos analisados em células PDAC. No estudo, foram incluídos 112 pacientes com câncer de pâncreas: 59 (52,6%) homens e 53 (47,4%) mulheres, com idade mediana no diagnóstico de 63 anos (faixa, 36-93 anos, SD ± 10,3) e um período médio de acompanhamento pós-diagnóstico de 16,2 meses.
Não houve diferença significativa entre os sexos ao comparar a intensidade do sinal de anticorpos. Cinquenta pacientes (48,08%) morreu durante o período de seguimento.
Entre todos os pacientes incluídos, 16 (15,2%) estavam em estágio patológico I, 32 (30,4%) estavam no estágio patológico II, 25 (23,8%) estavam no estágio patológico III, e 32 (30,4%) estavam no estágio patológico IV. Nos casos em que as informações sobre o grau tumoral estavam disponíveis, 2,8% dos carcinomas eram bem diferenciados, 62,8% eram moderadamente diferenciados e 34,2% eram pouco diferenciados.
Quanto ao estágio TNM, 11,2% eram T1 (tumor menor que 2 cm), 38,3% eram T2 (tumor maior que 2 cm ou tecidos vizinhos invasores), 19,6% eram T3 (tumor de qualquer tamanho invadindo tecidos próximos, mas sem comprometer o plexo celíaco ou artéria mesentérico superior), 21,5% eram T4 (tumor de qualquer tamanho comprometendo órgãos vitais e plexo celíaco ou artéria mesentérico superior) , e 9,3% eram Tx (a extensão do tumor é desconhecida). Para o envolvimento do linfonodo, 31,7% estavam no estágio N0 (sem metástase do linfonodo), 31,7% eram N1 (metástase do linfonodo regional), 6,5% eram N2 (mais de uma cadeia de linfonodos afetados) e 29,9% eram Nx (não estimáveis). Quanto à presença de metástase, 66,6% estavam no estágio M0 (sem metástases distantes), 30,2% eram M1 (metástase distante) e 3,6% eram Mx (não inestimável).
Cerca de 75,9% das amostras foram obtidas a partir do tecido tumoral pancreático, e cerca de 26% foram de amostras de metástase, com o fígado (65,7%) sendo o local mais afetado, seguido pelos linfonodos (14,2%), peritônio (8,5%) e outros (11,4%).
O tratamento paliativo foi dado a 68 indivíduos, ou 76,40% do total de pessoas analisadas.
Quanto à localização do tumor, 81,6% dos tumores estavam localizados na cabeça do pâncreas, 22,9% no corpo e 6,4% na cauda.
A Tabela 1 resume a análise descritiva geral dos indivíduos envolvidos no estudo.
Mesa 1. Análise Descritiva Geral
| Variáveis | N | % |
| Sexo | ||
| Fêmea | 53 | 47.4 |
| Masculino | 59 | 52.6 |
| Idade | ||
| 35-59 anos | 37 | 33.9 |
| 60-69 anos | 39 | 35.8 |
| 70-93 anos | 33 | 30.3 |
| Morte (n=104) | ||
| Não | 54 | 51.9 |
| Sim | 50 | 48.1 |
| Tratamento cirúrgico (n=108) | ||
| Paliativo | 42 | 38.9 |
| Cirurgia parcial | 19 | 17.6 |
| Dpt # | 47 | 43.5 |
| Tratamento cirúrgico (n=89) | ||
| Não | 21 | 23.6 |
| Sim | 68 | 76.4 |
| Diferenciação tumoral (n = 105) | ||
| Bem diferenciado | 3 | 2.9 |
| Moderado diferenciado | 66 | 62.8 |
| Pobre diferenciado | 36 | 34.3 |
| Amostra/Amostra (n=108) | ||
| Metástase | 26 | 24.1 |
| Pâncreas | 82 | 75.9 |
| Estágio patológico do tumor T (n=107) | ||
| T1 | 12 | 11.2 |
| T2 | 41 | 38.3 |
| T3 | 21 | 19.6 |
| T4 | 23 | 21.5 |
| Tx | 10 | 9.4 |
| Estágio patológico tumoral N (n= 107) | ||
| N0 | 34 | 31.8 |
| N1 | 34 | 31.8 |
| N2 | 7 | 6.5 |
| Nx | 32 | 29.9 |
| Estágio patológico tumoral M (n = 109) | ||
| M0 | 72 | 66.1 |
| M1 | 33 | 30.2 |
| Mx | 4 | 3.7 |
| Estágio geral patológico do tumor (n=105) | ||
| 1 | 16 | 15.2 |
| 2 | 32 | 30.5 |
| 3 | 25 | 23.8 |
| 4 | 32 | 30.5 |
| MTX (n=35) | ||
| Fígado | 23 | 65.7 |
| Linfonodos | 5 | 14.3 |
| Peritônio | 3 | 8.6 |
| Outros | 4 | 11.4 |
| Localização: Cabeça de Tumor | ||
| Sim | 89 | 81.7 |
| Localização: Cauda do Tumor | ||
| Sim | 7 | 6.4 |
| Localização: Corpo tumoral | ||
| Sim | 25 | 22.9 |
| Total | 112 | 100.0 |
#DPT: Duodenopancreatectomia
IMUNOSTAINING CD133 EM CÉLULAS-TRONCO CANCERÍGENAS EM CÉLULAS DE ADENOCARCINOMA DUCTAL PANCREÁTICO
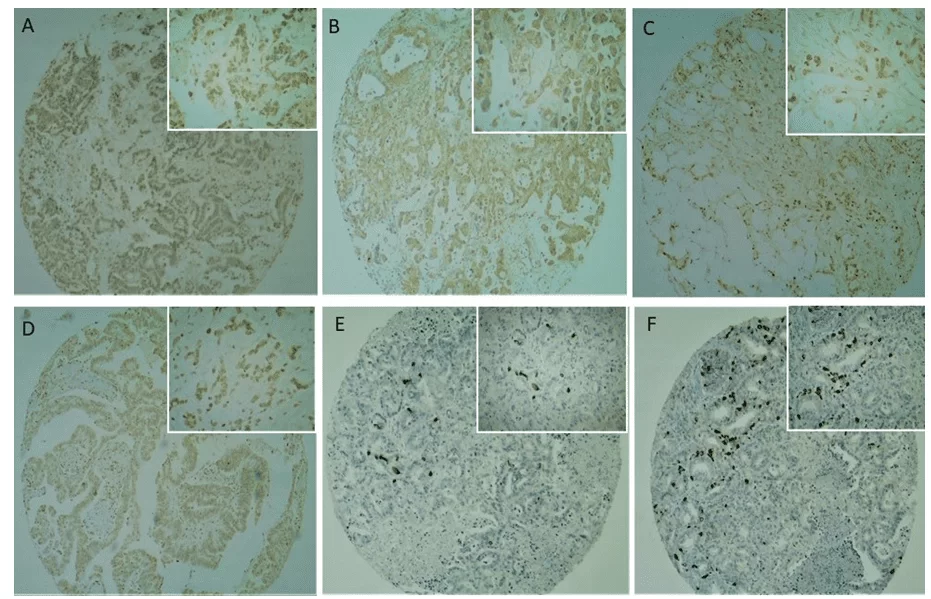
A imunocoloração CD133 esteve presente na membrana plasmática e citoplasma em intensidade moderada a forte (Figuras 2C e 2D), com intensidade predominantemente forte. Foi confirmada uma reação positiva ou negativa com o controle positivo (placenta) utilizado no estudo. Não foi observada imunorreatividade CD133 no epitélio ductal pancreático normal (Figura 2).
Fig. 2. Análise imunohistoquímica de marcadores de células-tronco de câncer em amostras de câncer pancreático TMA. (2A, 2B) A expressão CD24 foi observada principalmente no citoplasma das células tumorais. (2C, 2D) A expressão CD133 foi observada principalmente na membrana e citoplasma das células tumorais, raramente nucleares. (2E, 2F) A expressão OCT4 foi observada no núcleo das células tumorais, com expressão focal e forte intensidade. O campo de ampliação mais baixo (40x) está representado no painel global e no campo de ampliação mais alto (100x) no painel reduzido.
Em relação ao tratamento cirúrgico, 95,1% dos pacientes em tratamento 1 (desvio bileodigestivel) foram CD133-positivos, 70,0% dos pacientes em tratamento 2 (cirurgia parcial) foram CD133-positivos, e 81,2% dos pacientes submetidos ao tratamento 3 (duodenopancreatectomia total) foram CD133-positivo. Houve associação significativa (P = 0,019) entre o tratamento cirúrgico e o sinal CD133. Além do tratamento cirúrgico, apenas o tipo amostral foi significativamente associado ao sinal CD133, com nível de significância de 5%.
O grau de diferenciação do tumor (bom, moderado ou ruim) não mostrou associação significativa com a imunocoloração cd133 positiva, embora tenha sido observado que, à medida que o grau do tumor progredia, a intensidade de coloração aumentava (83,7% em tumores mal diferenciados). Também não houve associação significativa entre a encenação do TNM e a imunocoloração CD133 positiva, mas em estágios posteriores a rotulagem se intensifica, embora a presença de CSCs desde os estágios iniciais seja observada aqui. Isso corrobora a hipótese de que os CSCs estão presentes desde o início do processo de carcinogênese.
A Tabela 2 mostra a análise descritiva das variáveis juntamente com a verificação de sua associação com a imunorreatividade CD133, dada pelo teste exato de Fisher.
Mesa 2. Associação de variáveis com CD133 positivo.
| IHC CD133 positivo | p-valor* | ||||
| Não | Sim | ||||
| N | % | N | % | ||
| Sexo | 1,000 | ||||
| Fêmea | 8 | 15.1 | 45 | 84.9 | |
| Masculino | 9 | 15.5 | 49 | 84.5 | |
| Idade | 1,000 | ||||
| 35-59 anos | 6 | 16.2 | 31 | 83.8 | |
| 60-69 anos | 6 | 15.0 | 34 | 85.0 | |
| 70-93 anos | 5 | 14.7 | 29 | 85.3 | |
| Morte (n=106) | 0,192 | ||||
| Não | 6 | 11.1 | 48 | 88.9 | |
| Sim | 11 | 21.1 | 41 | 78.9 | |
| Tratamento Cirúrgico (n=109) | 0,019 | ||||
| Paliativo | 2 | 4.9 | 39 | 95.1 | |
| Cirurgia Parcial | 6 | 30.0 | 14 | 70.0 | |
| DPT # | 9 | 18.7 | 39 | 81.3 | |
| Tratamento Paliativo (n= 91) | 0,474 | ||||
| Não | 4 | 18.2 | 18 | 81.8 | |
| Sim | 8 | 11.6 | 61 | 88.4 | |
| Grau de Diferenciação (n=107) | 0,084 | ||||
| Bem diferenciado | 2 | 66.7 | 1 | 33.3 | |
| Moderado diferenciado | 9 | 13.4 | 58 | 86.6 | |
| Pobre diferenciado | 6 | 16.2 | 31 | 83.8 | |
| Amostra/amostra (n=107) | 0,028 | ||||
| Metástase | 7 | 29.2 | 17 | 70.9 | |
| Pâncreas | 9 | 10.9 | 74 | 89.2 | |
| Estágio T (n=109) | 0,587 | ||||
| T1 | 3 | 25.0 | 9 | 75.0 | |
| T2 | 5 | 12.5 | 35 | 87.5 | |
| T3 | 4 | 19.0 | 17 | 81.0 | |
| T4 | 2 | 8.0 | 23 | 92.0 | |
| Tx | 2 | 18.2 | 9 | 81.8 | |
| Estágio N (n=109) | 0,830 | ||||
| N0 | 4 | 11.4 | 31 | 88.6 | |
| N1 | 6 | 17.6 | 28 | 82.4 | |
| N2 | 1 | 16.7 | 5 | 83.3 | |
| Nx | 5 | 14.7 | 29 | 85.3 | |
| Estágio M (n=106) | 0,132 | ||||
| M0 | 8 | 11.3 | 63 | 88.7 | |
| M1 | 9 | 25.7 | 26 | 74.3 | |
| Mx | 0 | – | 5 | 100.0 | |
| Estágio geral (n=107) | 0,133 | ||||
| 1 | 2 | 12.5 | 14 | 87.5 | |
| 2 | 5 | 15.6 | 27 | 84.4 | |
| 3 | 1 | 4.0 | 24 | 96.0 | |
| 4 | 9 | 26.5 | 25 | 73.5 | |
| MTX (n=34) | 0,645 | ||||
| Fígado | 7 | 30.4 | 16 | 69.6 | |
| Linfonodos | 3 | 60.0 | 2 | 40.0 | |
| Peritônio | 1 | 25.0 | 3 | 75.0 | |
| Outros | 1 | 20.0 | 4 | 80.0 | |
| Localização: Cabeça de Tumor | 0,186 | ||||
| Sim | 12 | 13.2 | 79 | 86.8 | |
| Localização: Cauda do Tumor | 0,071 | ||||
| Sim | 3 | 42.9 | 4 | 57.1 | |
| Localização: Corpo tumoral | 1,000 | ||||
| Sim | 4 | 16.0 | 21 | 84.0 | |
*Teste exato de Fisher
#DPT: Duodenopancreatectomia
A Tabela 3 mostra os valores p e associações de variáveis com intensidade quando a coloração do CD133 foi positiva. Pelo teste exato de Fisher (P = 0,036), apenas o estágio M apresentou associação significativa com a intensidade do CD133; ou seja, tumores que já metástases estão fortemente manchados para CD133.
Mesa 3. Valores P de associação com intensidade.
| Variáveis | Grupos | p-valor* | ||
| IHC CD133 – Intensidade quando positiva |
IHC CD24 – Intensidade quando positiva |
IHC OCT4 – Intensidade quando positiva |
||
| Sexo |
Fêmea | 0,222 | 0,438 | 0,619 |
| Masculino | ||||
| Morte | Não | 1,000 | 0,235 | 0,627 |
| Sim | ||||
| Tratamento Cirúrgico |
Paliativo | 0,815 | 0,732 | 0,620 |
| Cir. Parcial | ||||
| Dpt # | ||||
| Tratamento Paliativo | Não | 0,136 | 0,027 | 0,619 |
| Sim | ||||
| Grau de Diferenciação | Bem diferenciado | 0,266 | 0,442 | 0,407 |
| Moderado diferenciado | ||||
| Pobre diferenciado | ||||
| Espécime/Amostra | Metástase | 0,848 | 0,201 | 0,488 |
| Pâncreas | ||||
| Estágio T | T1 | 0,611 | 0,992 | 1,000 |
| T2 | ||||
| T3 | ||||
| T4 | ||||
| Tx | ||||
| Estágio N |
N0 | 0,560 | 0,920 | 0,180 |
| N1 | ||||
| N2 | ||||
| Nx | ||||
| Estágio M |
M0 | 0,036 | 0,350 | 0,078 |
| M1 | ||||
| Mx | ||||
| Estágio Geral | 1 | 0,337 | 0,380 | 0,218 |
| 2 | ||||
| 3 | ||||
| 4 | ||||
| MTX | Fígado | 0,094 | 0,037 | 1,000 |
| Peritônio | ||||
| Linfonodos | ||||
| Outros | ||||
*Teste exato de Fisher
#DPT: Duodenopancreatectomia
IMUNOSTAINING CD24 EM CÉLULAS-TRONCO CANCERÍGENAS EM CÉLULAS ADENOCARCINOMA DUCTAL PANCREÁTICAS
A imunocoloração CD24 (Figuras 2A e 2B) esteve presente na membrana plasmática e citoplasma tanto fraco/moderado (41,6%) e forte (58,3%) intensidades, mas em uma intensidade mais fraca quando comparado ao CD133 (Figuras 2C e 2D). As reações positivas e negativas foram confirmadas com o controle positivo (placenta) utilizado no estudo. A Tabela 4 mostra a análise descritiva das variáveis juntamente com a verificação de sua associação com a positividade do CD24, dada pelo teste exato de Fisher. Um sinal de CD24 positivo foi visto em 98,3% dos homens, mas não houve associação entre sexo e positividade CD24 (P = 0,343). Apenas o tipo de amostra coletada e o tratamento paliativo estiveram significativamente associados ao sinal CD24, em nível de significância de 5% (P = 0.010 e 0,042, respectivamente).
Mesa 4. Associação de variáveis com CD24 positivo.
| IHC CD24 positivo | p-valor* | ||||
| Não | Sim | ||||
| N | % | N | % | ||
| Sexo | 0,343 | ||||
| Fêmea | 3 | 5.7 | 50 | 94.3 | |
| Masculino | 1 | 1.7 | 58 | 98.3 | |
| Idade | 0,159 | ||||
| 35-59 anos | 3 | 8.1 | 34 | 91.9 | |
| 60-69 anos | 0 | – | 40 | 100.0 | |
| 70-93 anos | 1 | 2.9 | 34 | 97.1 | |
| Morte (n=107) | 0,618 | ||||
| Não | 3 | 5.4 | 52 | 94.6 | |
| Sim | 1 | 1.9 | 51 | 98.1 | |
| Tratamento Cirúrgico (n=110) | 0,399 | ||||
| Paliativo | 3 | 7.1 | 39 | 92.9 | |
| Cirurgia Parcial | 0 | – | 20 | 100.0 | |
| Dpt # | 1 | 2.1 | 47 | 97.9 | |
| Tratamento Paliativo (n=91) | 0,042 | ||||
| Não | 3 | 13.6 | 19 | 86.4 | |
| Sim | 1 | 1.4 | 68 | 98.6 | |
| Grau de Diferenciação (n=108) | 1,000 | ||||
| Bem diferenciado | 0 | – | 3 | 100.0 | |
| Moderado diferenciado | 3 | 4.4 | 65 | 95.6 | |
| Pobre diferenciado | 1 | 2.7 | 36 | 97.3 | |
| Amostra/amostra (n=108) | 0,010 | ||||
| Metástase | 1 | 4.0 | 23 | 95.9 | |
| Pâncreas | 2 | 2.4 | 82 | 97.6 | |
| Estágio T (n=110) | 0,705 | ||||
| T1 | 0 | – | 12 | 100.0 | |
| T2 | 1 | 2.4 | 40 | 97.6 | |
| T3 | 1 | 4.8 | 20 | 95.2 | |
| T4 | 1 | 4.0 | 24 | 96.0 | |
| Tx | 1 | 9.1 | 10 | 90.9 | |
| Estágio N (n=110) | 0,881 | ||||
| N0 | 1 | 2.9 | 34 | 97.1 | |
| N1 | 2 | 5.9 | 32 | 94.1 | |
| N2 | 0 | – | 7 | 100.0 | |
| Nx | 1 | 2.9 | 33 | 97.1 | |
| Estágio M | 1,000 | ||||
| M0 | 3 | 4.2 | 69 | 95.8 | |
| M1 | 1 | 2.9 | 34 | 97.1 | |
| Mx | 0 | – | 5 | 100.0 | |
| Estágio Geral (n=108) | 0,913 | ||||
| 1 | 1 | 6.2 | 15 | 93.8 | |
| 2 | 1 | 3.1 | 31 | 96.9 | |
| 3 | 1 | 3.8 | 25 | 96.2 | |
| 4 | 1 | 2.9 | 33 | 97.1 | |
| MTX (n=37) | 1,000 | ||||
| Fígado | 1 | 4.3 | 22 | 95.7 | |
| Linfonodos | 0 | – | 5 | 100.0 | |
| Peritônio | 0 | – | 4 | 100.0 | |
| Outros | 0 | – | 5 | 100.0 | |
| Localização: Cabeça de Tumor | 0,550 | ||||
| Sim | 3 | 3.3 | 89 | 96.7 | |
| Localização: Cauda do Tumor | 1,000 | ||||
| Sim | 0 | – | 7 | 100.0 | |
| Localização: Corpo tumoral | 1,000 | ||||
| Sim | 1 | 4.0 | 24 | 96.0 | |
*Teste exato de Fisher
#DPT: Duodenopancreatectomia
Não foi observada imunorreatividade CD24 no epitélio ductal pancreático normal. Um sinal de CD24 positivo foi observado em 98,6% dos pacientes submetidos ao tratamento paliativo, o que foi significativo (P = 0,042). Devido ao seu estágio de tumor avançado, eles tinham um sinal CD24 mais forte em comparação com indivíduos que foram submetidos à duodenopancreatectomia total. O sinal cd24 foi mais forte em indivíduos submetidos ao tratamento paliativo como opção de tratamento (98,6%) quando comparado com aqueles que não o fizeram (13,6%).
O grau de diferenciação e estadiamento do tumor não mostrou associação significativa com a coloração CD24 positiva, nem houve diferenças significativas entre tumores mal diferenciados ou em estágio avançado em comparação com tumores bem diferenciados e em estágio inicial em relação ao CD24 positivo.
A Tabela 3 mostra a associação das variáveis com intensidade quando o CD24 foi positivo. Apenas a presença de metástase (MTX) esteve significativamente associada à intensidade, onde o fígado e o peritônio apresentaram forte positividade quando comparados à metástase em outros locais, como linfonodos e outros tecidos.
IMUNOSTAINING OCT4 EM CÉLULAS-TRONCO CANCERÍGENAS EM CÉLULAS DE ADENOCARCINOMA DUCTAL PANCREÁTICO
A imunocoloração OCT4 mostrou um padrão diferente em relação aos outros anticorpos testados. A frequência de casos positivos não foi tão alta quanto observada com os outros dois anticorpos testados, mas quando positiva, sua intensidade foi muito forte (Figuras 1E e 1F). A imunossuagem ocorreu no núcleo celular tumoral em 31,5% dos casos e não manchou 68,7% dos tumores analisados. Não foi observada imunorreatividade OCT4 no epitélio ductal pancreático normal. Nenhuma variável foi significativamente associada ao sinal OCT4, em nível de significância de 5%. A média de idade do grupo OCT4-positivo foi de 62,62 anos e 63,23 anos no grupo OCT4-negativo. Entretanto, não houve diferença significativa entre os grupos em relação à idade (P = 0,547).
Embora não estatisticamente significante, um achado interessante da análise de coloração OCT4 é que quanto mais diferenciado o tumor, maior a intensidade de coloração, enquanto tumores pouco diferenciados apresentaram baixa intensidade de coloração (66,6% vs 21,6%). As células positivas para OCT4 têm maior potencial de diferenciação.
ANÁLISE DE SOBREVIVÊNCIA
Sobre as curvas de sobrevivência e sua relação com os três marcadores, todos os grupos apresentaram curvas muito semelhantes, de modo que o teste de registro-rank não indica nenhuma diferença significativa entre as curvas em relação aos sinais positivos dos três anticorpos. As curvas Kaplan-Meier para intensidade de CD133, CD24 e OCT4, confirmadas pelos valores p do teste de classificação de registro, nenhuma das curvas de sobrevivência difere significativamente em relação à intensidade. Portanto, a positividade dos marcadores não altera a sobrevida dos pacientes incluídos no estudo.
DISCUSSÃO
Os CSCs têm sido recentemente associados à progressão do câncer e usados para identificar os fatores e metas prognósticas para a terapia em vários tipos de câncer (DEAN et al., 2005). É notável que o papel dos CSCs não é bem compreendido ou caracterizado no câncer de pâncreas. Além disso, poucos relatórios foram publicados sobre os padrões e efeitos da presença de CSCs. Considerando essa falta de dados, analisamos retrospectivamente a expressão de CSCs em amostras de câncer pancreático utilizando imunohistoquímica e verificamos seu papel na progressão do tumor e resistência terapêutica no adenocarcinoma pancreático ductal.
A biologia molecular do câncer de pâncreas está diretamente relacionada à sua rápida progressão e baixa resposta terapêutica. Está bem documentado que o aparecimento de uma célula tumoral é o resultado de um acúmulo de mutações em seu DNA capaz de alterá-la morfologicamente e funcionalmente (FANG et al., 2013; RICCI-VITIANI et al., 2007). O gatilho desse processo e toda a sua evolução, culminando na formação da célula tumoral e suas características pertinentes, caracterizam o processo de carcinogênese, já é significativamente elucidado para diversos tipos de neoplasias. No entanto, para certos tipos de câncer, como o câncer de pâncreas, o processo permanece incerto (KOBAYASHI; NORONHA, 2015).
A maioria dos tumores malignos segue uma história natural que pode ser dividida em quatro estágios: transformação maligna, crescimento de células tumorais, invasão local e metástase. O processo de carcinogênese, ou transformação maligna, ocorre em vários estágios e resultados devido ao acúmulo de alterações genéticas e mutações, que são desencadeadas por diversos fatores, incluindo fatores ambientais como radiação e produtos químicos (AYOB; RAMASAMY, 2018). No entanto, para que esse processo de carcinogênese progrida, pode ser necessário ter certas células com as características das células-tronco, como o potencial de autoconexão e regeneração, bem como um alto índice de proliferação.
Evidências recentes sugerem que as células-tronco desempenham um papel crucial não apenas na geração e manutenção de diferentes tecidos, mas também no desenvolvimento e progressão de certos tipos de tumores (BALIC et al., 2012). Para vários tumores sólidos, eles têm sido mostrados para abrigar uma subpopulação distinta de células tumorais que têm características de células-tronco e, portanto, são chamadas células-tronco tumorais (TCTs) ou células tumorigênicas (MATSUDA et al., 2012). As células-tronco cancerígenas parecem ser capazes de iniciar e impulsionar o crescimento do tumor em tumores sólidos. CD133, CD24 e OCT4 são recentemente relatados marcadores prospectivos para CSCs, expressos em uma variedade de tumores; no entanto, pelo nosso conhecimento, nenhuma tentativa foi feita para detectar sua expressão em amostras de câncer de pâncreas (MAEDA et al., 2008).
Pode-se observar que as células-tronco tumorais, ou marcadores de superfície de células-tronco tumorais como CD133, CD24 e OCT4 estão presentes em células tumorais de câncer pancreático, confirmando a relação intrínseca entre o fenótipo maligno pancreático e a presença de células-tronco. Não foi observada diferença significativa entre a expressão de anticorpos e o grau de diferenciação do tumor, assumindo que as células-tronco tumorais estão presentes desde o início do tumor. Deve-se notar que para os anticorpos CD133 e CD24, a porcentagem de células tumorais que expressam marcadores aumentou à medida que o tumor progredia. Assim, os tumores mais agressivos e pouco diferenciados apresentaram maior positividade para a presença do anticorpo. Por outro lado, a expressão do anticorpo OCT4 foi maior e mais intensa em tumores bem diferenciados; assim, quanto mais diferenciado o tumor, maior a rotulagem. As células que possuem o marcador de células-tronco para o anticorpo OCT4 têm um maior potencial de diferenciação (VILLODRE et al., 2016). Esta pode ser a razão pela qual o OCT4 difere em termos de expressão dos outros marcadores que foram testados, embora essas diferenças não tenham sido estatisticamente significativas.
O marcador OCT4 só está presente focalmente em amostras de tumores que foram positivas. Este achado está de acordo com a teoria de que os CSCs representam apenas uma parcela muito pequena da população total de células tumorais (PHI et al., 2018). Por exemplo, células positivas cd133 foram detectadas em 0,7-6,1% (RICCI-VITIANI et al., 2007), 1.8-24.5% (O’BRIEN et al., 2007) de células primárias de câncer de cólon, e em 0,7-3,2% das células primárias de câncer pancreático usando análise citométrica de fluxo (HERMANN et al., 2007). A coloração imunohistoquímica revelou a expressão CD133 em 1-3% dos espécimes de carcinoma hepatocelular (MA et al., 2007).
Embora a rotulagem e expressão tenham sido observadas com uma frequência relativamente alta em todos os graus de direção tumoral, por exemplo, tumores expressos rotulagem para células-tronco cancerígenas independentemente do grau de diferenciação, alguns achados favorecem a hipótese de que o número de células-tronco em tumores é maior em tumores com comportamento mais agressivo e com pior prognóstico. Essa hipótese é sustentada pelo fato de que o CD133 foi mais frequentemente expresso em indivíduos submetidos apenas ao tratamento paliativo (95,1%) com associação significativa (valor p < 0,05) entre a presença de anticorpos e tratamento paliativo. Quando se relata que um paciente foi submetido apenas ao tratamento paliativo, supõe-se que o tumor estava em estágio significativamente avançado e sem possibilidade de intervenção cirúrgica curativa e, portanto, apenas o tratamento paliativo foi realizado. Da mesma forma, pode-se exagerar que os tumores mais agressivos em estágios posteriores expressam maior rotulagem para o anticorpo de células-tronco tumorais CD133. Diversos estudos clínicos têm investigado a relação entre a expressão CD133 e os desfechos clínicos dos tumores; no entanto, os resultados são controversos. Por exemplo, a expressão CD133 está relacionada ao prognóstico ruim do câncer de cólon e hepatocarcinoma (CAI et al., 2018).
Em relação ao estágio TNM, a rotulagem dos três anticorpos (CD133, CD24 e OCT4) não mudou ao longo da progressão. É notável que as células-tronco tumorais estavam presentes desde o estágio inicial e que elas não aumentam durante a encenação. A prevalência dos três anticorpos e suas associações com as variáveis foi geralmente elevada, embora nem todos os anticorpos tivessem um nível de significância inferior ao de P < 0,05.
Todas as variáveis que contribuíram para um prognóstico desfavorável, como a localização do tumor na cabeça pancreática, idade avançada e presença de metástases foram todas associadas à alta prevalência especialmente para a expressão de CD133 e CD24. Além disso, isso corroborava com a ideia de que as células-tronco tumorais quando presentes estão associadas à rápida progressão do tumor e resistência terapêutica. As células-tronco cancerígenas têm certas características semelhantes às das células-tronco normais do organismo, como a capacidade de se autorregenerar e pluripotência, dando origem a linhas de células tumorais heterogêneas que formam o mesmo tumor (TAI et al., 2005). As células-tronco cancerígenas provavelmente compartilharão muitas das propriedades das células-tronco normais que proporcionam uma longa vida útil, incluindo aquiescência relativa, resistência a drogas e toxinas através da expressão de vários transportadores, uma capacidade ativa de reparação de DNA e uma resistência à apoptose. Portanto, os tumores podem ter uma população incorporada de células pluripotentes resistentes a medicamentos que podem sobreviver à quimioterapia e repovoar o tumor (MARQUES et al., 2010).
Para definir se os CSCs previam o desfecho clínico, realizamos a análise de sobrevivência de Kaplan-Meier e mostramos que os grupos apresentavam curvas muito semelhantes. Assim, o teste de registro-rank não indica diferença significativa entre as curvas em relação à presença dos três anticorpos. Embora estejam associadas a variáveis prognósticos piores, como metástase e opções terapêuticas de tratamento paliativo, não se pode fazer associação entre a presença de células-tronco tumorais e a sobrevivência do paciente neste caso; portanto, a presença de CSCs não prevê pior sobrevivência.
A descoberta de células-tronco cancerígenas em tumores sólidos mudou nossa visão da carcinogênese. Que as células-tronco tumorais estão envolvidas no desenvolvimento do tumor e a progressão é um fato, uma vez que sua presença foi significativa na grande maioria dos tecidos analisados e, recentemente, muitos estudos associaram a presença de células-tronco tumorais ao desenvolvimento de vários tipos de câncer.
CONSIDERAÇÕES FINAIS
O processo de tumorigênese, até onde o assunto é conhecido até agora, envolve a progressiva aquisição de múltiplas mutações aberrantes que culminam na expansão e proliferação de subpopulações celulares mais agressivas, contribuindo para a progressão e crescimento do tumor. Embora essa teoria seja bem estabelecida, a identificação de células capazes de causar a progressão do tumor ainda é objeto de muitos estudos para caracterizar melhor o processo de carcinogênese e identificar essas células.
Grande parte das informações que obtemos e usamos para o diagnóstico, prognóstico e tratamento de neoplasias pancreáticas deriva de populações heterogêneas com diferentes graus de maturação e diferenciação. Está se tornando cada vez mais urgente caracterizar os CSCs para a avaliação e caracterização da rota cancerígena dos tumores mais agressivos. A consequência direta é o desenvolvimento de estratégias terapêuticas que possam atuar nos CSCs e a possibilidade de determinar, por um método de fácil acesso, quais pacientes serão os mais beneficiados com esse tipo de tratamento.
REFERÊNCIAS
ALLEGRA, E.; TRAPASSO, S. Cancer stem cells in head and neck cancer. Onco Targets Ther., v.5, p.375-83, 2012.
ANSARI, D.; CHEN, B.C.; DONG, L.; ZHOU, M.T.; ANDERSSON, R. Pancreatic cancer: translational research aspects and clinical implications. World J Gastroenterol., v.18, n.13, p.1417-24, 2012.
AYOB, A.Z.; RAMASAMY, T.S. Cancer stem cells as key drivers of tumour progression. J Biomed Sci., v.25, n.20, 2018.
BALIC, A.; DORADO, J.; ALONSO-GÓMEZ, M.; HEESCHEN, C. Stem cells as the root of pancreatic ductal adenocarcinoma. Exp Cell Res., v.318, n.6, p.691-704, 2012.
BARBOSA, I.R.; SANTOS, C.A.; SOUZA, D.L.B. Pancreatic cancer in Brazil: mortality trends and projections until 2029. Arq. Gastroenterol., v.55, n.3, p.230-6, 2018.
CAI, X.; LI, J.; YUAN, X.; XIAO, J.; DOOLEY, S.; WAN, X., WHENG, W.; LU, L. CD133 expression in cancer cells predicts poor prognosis of non-mucin producing intrahepatic cholangiocarcinoma. J Transl Med., v.16, n.50, 2018.
DEAN, M.; FOJO, T.; BATES, S. Tumour stem cells and drug resistance. Nat Rev Cancer., v.5, n.4, p.275-84, 2005.
FANG, Y.; YAO, Q.; CHEN, Z.; XIANG, J.; WILLIAM, F.E.; GIBBS, R.A.; CHEN, C. Genetic and molecular alterations in pancreatic cancer: implications for personalized medicine. Med Sci Monit., v.19, p.916-26, 2013.
HERMANN, P.C.; HUBER, S.L.; HERRLER, T.; AICHER, A.; ELLWART, J.W.; GUBA, M.; BRUNS, C.J.; HEESCHEN, C. Distinct populations of cancer stem cells determine tumor growth and metastatic activity in human pancreatic cancer. Cell Stem Cell., v.1, n.3, p.313-23, 2007.
HU, Y.; FU, L. Targeting cancer stem cells: a new therapy to cure cancer patients. Am J Cancer Res., v.2, n.3, p.340-56, 2012.
KOBAYASHI, N.C.C.; NORONHA, S.M.R. Cancer stem cells: a new approach to tumor development. Rev Assoc Med Bras., v.61, n.1, p.86-93, 2015.
KONONEN, J.; BUBENDORF, L.; KALLIONIMENI, A.; BÄRLUND, M.; SCHRAML, P.; LEIGHTON, S.; TORHORST, J.; MIHATSCH, M.J.; SAUTER, G.; KALLIONIMENI, O.P. Tissue microarrays for high-throughput molecular profiling of tumor specimens. Nat Med., v.4, n.7, p.844-7, 1998.
LI, D.; JIAO, L. Molecular epidemiology of pancreatic cancer. Int J Gastrointest Cancer., v.33, n.1, p.3-14, 2003.
MA, S.; CHAN, K.W.; HU, L.; LEE, T.K.W.; WO, J.Y.H.; NG, I.O.L.; ZHENG, B.J.; GUAN, X.Y. Identification and characterization of tumorigenic liver cancer stem/progenitor cells. Gastroenterology, v.132, n.7, p.2542-56, 2007.
MAEDA, S.; SHINCHI, H.; KURAHARA, H.; MATAKI, Y.; MAEMURA, K.; SATO, M.; NATSUGOE, S.; AIKOU, T.; TAKAO, S. CD133 expression is correlated with lymph node metastasis and vascular endothelial growth factor-C expression in pancreatic cancer. Br J Cancer., v.98, n.8, p.1389-97, 2008.
MARQUES, D.S.; SANDRINI, J.Z.; BOYLE, R.T.; MARINS, L.F.; TRINDADE, G.S. Relationships between multidrug resistance (MDR) and stem cell markers in human chronic myeloid leukemia cell lines. Leuk Res., v.34, n.6, p.757-62, 2010.
MATSUDA, Y.; KURE, S.; ISHIWATA, T. Nestin and other putative cancer steam cell markers in pancreatic cancer. Med Mol Morphol., v.45, n.2, p.59-65, 2012.
O’BRIEN, C.A.; POLLETT, A.; GALLINGER, S.; DICK, J.E. A human colon cancer cell capable of initiating tumour growth in immunodeficient mice. Nature, v.445, n.7123, p.106-10, 2007.
PHI, L.T.H.; SARI, I.N.; YANG, Y.G.; LEE, S.H.; JUN, N.; KIM, K.S.; LEE, Y.K.; KWON, H.Y. Cancer Stem Cells (CSCs) in Drug Resistance and their Therapeutic Implications in Cancer Treatment. Stem Cells Int., n.5416923, 2018.
RICCI-VITIANI, L.; LOMBARDI, D.G.; PILOZZI, E.; BIFFONI, M.; TODARO, M.; PESCHLE, C.; DE MARIA, R. Identification and expansion of human colon-cancer-initiating cells. Nature, v.445, p.111-5, 2007.
SAKORAFAS, G.H.; TSIOTOU, A.G.; TSIOTOS, G.G. Molecular biology of pancreatic cancer; oncogenes, tumor suppressor genes, growth factors, and their receptors from a clinical perspective. Cancer Treat Rev., v.26, n.1, p.29-52, 2000.
SOTO, J.L.; BARBERA, V.M.; SACEDA, M.; CARRATO, A. Molecular biology of exocrine pancreatic cancer. Clin Transl Oncol., v.8, p.306-12, 2006.
TAI, M.H.; CHANG, C.C.; OLSON, L.K.; TROSKO, J.E. Oct4 expression in adult human stem cells: evidence in support of the stem cell theory of carcinogenesis. Carcinogenesis, v.26, n.2, p.495-502, 2005.
VILLODRE, E.S.; KIPPER, F.C.; PEREIRA, M.B.; LENZ, G. Roles of OCT4 in tumorigenesis, cancer therapy resistance and prognosis. Cancer Treat Rev., v.51, p.1-9, 2016.
[1] Mestrado em Ciências Médicas, Programa de Pós-Graduação em Medicina: Ciências Médicas, Universidade Federal do Rio Grande do Sul (UFRGS), Brasil.
[2] Doutor em Ciências Fisiológicas pela Universidade Federal do Rio Grande (FURG).
[3] MSc em Genética e Biologia Molecular da Universidade Federal do Rio Grande do Sul (UFRGS), Brasil.
[4] Estudante de Medicina de Graduação na Universidade Federal do Rio Grande (FURG).
[5] Doutor em Ciências Biológicas (Bioquímica) pela Universidade Federal do Rio Grande do Sul (UFRGS), com doutorado em neurociência sanduíche – Universidade da Califórnia Irvine.
Inscrições: setembro de 2020.
Aprovado em outubro de 2020.