REVIEW ARTICLE
TAVARES, Marcela Marçolla [1]
TAVARES, Marcela Marçolla. Verwendung von Kolloiden und Kristalloiden in der perioperativen Periode schwerer Patienten: Kontroversen. Multidisziplinäre Kern Fachzeitschrift des Wissens. Jahrgang 05, Ed. 01, Vol. 01, S. 05-21. Januar 2020. ISSN: 2448-0959, Zugangslink: https://www.nucleodoconhecimento.com.br/gesundheit/kolloid-und-kristalloide
ZUSAMMENFASSUNG
Da das Management des Flüssigkeitsaustauschs die Prognose des Patienten beeinflusst, hat sich die Grundlagen- und klinische Forschung mit den verschiedenen Aspekten befasst, die zur Verabreichung von Flüssigkeiten und Volumen in der perioperativen Periode beitragen. Es gibt immer noch keinen Konsens darüber, wann und in wem eine perioperative hämodynamische Optimierung angegeben werden soll. Zusätzliche Probleme wie die relative Rolle der Kristalloid- und Kolloid-Verhältnisoptimierung wurden nicht gelöst. Diese Arbeit besteht aus einer Literaturrezension, die zwischen Februar und Oktober 2019 durchgeführt wurde, in der eine Konsultation zu verschiedenen wissenschaftlichen Publikationen durchgeführt wurde, die im Internet durch Konsultationinsprechung in den Datenbanken: ScienceDirect, UptoDate, Medline/PubMed, Lilacs, sciELO, mit den Begriffen Perioperative Fluidtherapie, Hemodynamik, Volume Reposition, Crystalloid, Colloid durchgeführt wurden. Daraus wurde beobachtet, dass Flüssigkeiten wie jedes andere Medikament angewendet werden sollten, unter Berücksichtigung ihrer individuellen Indikationen und Einschränkungen, was die Grundlage des Konzepts der Zieltherapie ist – ein neues Konzept, das die Festlegung von Inklusionskriterien für die Flüssigkeitsoptimierung durch den Patienten fördert. In diesem Zusammenhang sind vorteilhafte Aspekte des perioperativen Volumenersatzes durch iso-onkotische Lösungen verständlich, obwohl zusätzliche randomisierte kontrollierte Studien erforderlich sind, um ihre Relevanz für das Ergebnis zu beweisen.
Schlagworte: Perioperative Fluidtherapie, Hämodynamik, Volumenersatz.
1. EINFÜHRUNG
Da das Management des Flüssigkeitsaustauschs die Prognose des Patienten beeinflusst, hat sich die Grundlagen- und klinische Forschung mit den verschiedenen Aspekten befasst, die zur Verabreichung von Flüssigkeiten und Volumen in der perioperativen Periode beitragen. Die Grundlagenforschung verbesserte das Wissen über die Funktion der endotheliale Gefäßbarriere und ihre funktionellen Veränderungen, die für die vaskuläre Extravasation verantwortlich sind. Klinische Studien, die unterschiedliche Ansätze zur Flüssigkeitskontrolle proklamieren, haben widersprüchliche Ergebnisse gezeigt und beziehen sich in den meisten Fällen nicht auf die physiologische Grundlage der Gefäßbarriere. Basierend auf der Metaanalyse der letzten 30 Jahre wurden eine Reihe von Studien durchgeführt, um die Sterblichkeit und chirurgische Morbidität durch absichtliche und präventive Manipulation der perioperativen Hämodynamik zu reduzieren, was eine Tendenz der wissenschaftlichen Gemeinschaft zeigt, zu klären, ob eine hämodynamische Optimierung tatsächlich von Vorteil is[2]t.
Es ist verantwortlich für Studien, die sich hauptsächlich auf klinische Ziele konzentrierten, um die volumetrische Therapie in der perioperativen Periode zu leiten. Eine Argumentation sollte jedoch im Allgemeinen aus physiologischen Fakten und signifikanten und vergleichbaren Studien abgeleitet werden. So fasst diese Überprüfung das relevante Wissen über die Wirkung verschiedener intravenöser Flüssigkeiten und über die hämodynamische Überwachung zusammen. Da es in diesem Bereich noch keinen Konsens von großem Interesse für alle Anästhesisten gibt, zielt dieser Artikel darauf ab, einige Vor- und Nachteile der Hauptflüssigkeiten zu klären, die beim perioperativen Volumenersatz verwendet werden.
Die relative Rolle der Optimierung der kristalloiden versus kolloiden Beziehung, obwohl nicht gelöst, gibt es Beweise, die ausgewogene Lösungen mit einer Elektrolytkonzentration ähnlich der im Plasma gefunden begünstigt, und große Mengen von Salzlösung sollte vermieden werden, da sie hyperchloremische Azidose induziere[3]n.
2. MATERIAL UND METHODEN
Diese Arbeit besteht aus einer Literaturrezension, die zwischen Februar und Oktober 2019 durchgeführt wurde, in der eine Konsultation zu verschiedenen wissenschaftlichen Publikationen durchgeführt wurde, die im Internet durch eine Suche aus den Datenbanken von ScienceDirect, UptoDate, Medline/PubMed, Lilacs, sciELO, hauptsächlich mit den Begriffen Perioperative Fluidtherapie, Hämodynamik, Volemic Reposition, Crystalloid, Colloid, durchgeführt wurden.
Die Kriterien für die Aufnahme in diese Studie waren wissenschaftliche Artikel, die die Hauptunterschiede zwischen Kolloiden und Kristalloiden sowie deren Hauptindikationen in der perioperativen Periode beschreiben. Mehrere Studienmodalitäten zwischen 1980 und 2019 wurden überprüft, darunter randomisierte und multizentrische prospektive Studien, Metaanalysen, retrospektive Beobachtungsstudien und Literaturrezensionen.
3. BEWERTUNG
3.1 DIE PHYSIOLOGIE DER FLUID-KOMZENTRALISIERUNG
Das Gesamtkörperwasser für eine Person von 75 kg beträgt ca. 45 L (60%). Zwei Drittel davon (30 L) sind intrazelluläres Wasser. Das restliche Drittel (15 L) im extrazellulären Fach wird zwischen den intravaskulären (3 L) und extravaskulären (12 L) Fächern (Abb. 1) aufgeteil[4]t. Das gesamtinvaskuläre Volumen beträgt ca. 5 L und hat zelluläre Komponenten (rote und weiße Blutkörperchen und Blutplättchen: 40%[2 L]) und nichtzellulär (Plasma: 60[3 L]%). Plasma ist eine wässrige Lösung von anorganischen Ionen (überwiegend Natriumchlorid), einfachen Molekülen wie Harnstoff und größeren organischen Molekülen wie Albumin und Globulinen.
BILD 01: Erläuterndes Modell der Flüssigkeitsverteilung im Körper

Wie in Abbildung 01 dargestellt, wird festgestellt, dass ein großer Teil des flüssigkeitsgroßen Volumens im intrazellulären Medium konzentriert ist und aus Glysatlösung besteht.
Erhöhte vaskuläre Permeabilität durch entzündliche Aktivierung mit eingeschränkter Endothelzellfunktion kann aus einer Vielzahl von Gründen bei größeren chirurgischen Eingriffen auftreten[5]. Insbesondere chirurgische Gewebetraumata, Gewebehypoperfusion aufgrund unzureichender Flüssigkeitstherapie, Ischämie-Verletzung/Reperfusion, Sepsis (lokal oder Blut) und Die Anwendung eines herzpulmonalen Bypasss (z. B. Herz-Lungen-Bypass) werden als entzündliche Reize anerkannt, die die Gefäßfunktion beeinträchtigen können[6].
3.2 VOLUME REPLACEMENT
Volumenersatz sollte angezeigt werden, wann immer es notwendig ist: 1) Blutverlust während der Operation zu ersetzen, 2) Ersetzen Sie Verluste durch Schwitzen und Urinproduktion 3) Präoperative Darmoperationen und 4) Aufrechterhaltung der dritten Platzverluste[7].
Es wird unter dem dritten Raum als ein Von Randall 1952 vorgeschlagener Begriff verstanden, um die Situation zu beschreiben, in der außerzelluläre Flüssigkeit in einem Bereich des Körpers verloren geht oder entführt wird, wo sie nicht am Austausch teilnimmt und folglich nicht den Wasserbedarf des Patienten erfüll[8]t.
3.3 PERIOPERATIVE HÄMODYNAMISCH OPTIMIERTE STRATEGIE
Die Patienten, die von dieser Therapie profitieren könnten, sind Patienten mit hohem Risiko gemäß dem Revised Cardiac Risk Index und dem Präoperativen Kardiopulmonaden-Übungstes[6]t[9],[10]
Laut einer systematischen Literaturrecherche zur perioperativen Optimierung bei Patienten mit hohem chirurgischen Risiko wurden wichtige Faktoren gefunden, die helfen würden, Patienten zu identifizieren, die am meisten von der perioparatorischen Flüssigkeitsoptimierung profitieren würde[11]n. Die Ergebnisse sind in Tabelle 01 auf der Grundlage der Studien von Mangano et al. beschrieben. Poldermans et al. (1999) und Shoemaker et al. (1988).
TABELLE 01 – Inklusionskriterien für die perioperative Optimierung
| Histórico de enfermidade cardíaca ou pulmonar severa, como por exemplo DPOC, infarto agudo do miocárdio, e insuficiência cardíaca. |
| Cirurgias extensas que envolvam anastomoses do trato gastrointestinal (por exemplo, esofagectomia). |
| Perda massiva e abrupta de sangue (>2,5L) |
| Idade maior ou igual a 70 anos com reserve fisiológica limitada em um ou mais órgãos vitais. |
| Septicemia |
| Insuficiência Respiratória (PaO2 <60 mmHg e FIO2 >0.4) |
| Acometimento abdominal agudo como pancreatite, perfuração de vísceras ou sangramentos do TGI. |
| Insuficiência Renal Aguda |
| Doença vascular em estágio avançado |
Quelle: Tote; 2006: Grounds
Basierend auf einer Studie mit 30 schweren Patienten, die Herzoperationen unterzogen wurden, wurde nachgewiesen, dass trotz der Zunahme des Herzindex und des renalen Blutflusses mit beiden Flüssigkeiten keine der Flüssigkeiten die Nierensauerstoffversorgung verbesserte, da beide eine Hämodilution induzierten. GFR stieg im Kristalloid (28%), aber nicht in der Kolloidgruppe, wie in Abbildung 02 dargestellt[12].
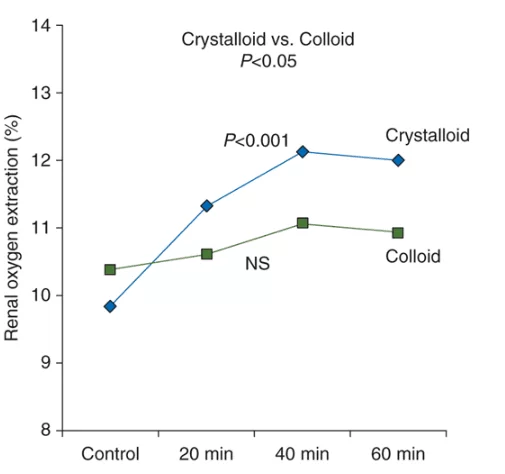
Die gleiche Studie zeigte, dass die Verwendung von Kristalloiden die Filtrationsrate erhöhte (24%) sowie die renale Sauerstoffextraktion (23%), auch ohne die Vaskuläre Versorgung der Komponente zu erhöhen, was darauf hindeutet, dass der Anstieg der GFR – der Hauptdeterminant des Sauerstoffverbrauchs – nicht mit einer proportionalen Erhöhung des Anteils des Sauerstoffs an die Nieren einherging. Mit anderen Worten, ihre Ergebnisse fassen in Derographie (Abbildung 02) zusammen, dass die kristalloide erhöhte Renalsauerstoffextraktion (P 0,001) 20, 40 und 60 min nach Bolus, im Gegensatz zu Kolloid (NS), was auf eine gestörte Nierensauerstoffversorgung im zweiten Fall hindeutet. Die Veränderung der renalen Sauerstoffextraktion war in der kristalloiden Gruppe signifikant (P 0,05) ausgeprägter als in der Kolloidgruppe[11].
BILD 02: Auswirkungen von Kristalloid (10 ml/kg) und Kolloidinfusion (20 ml/kg) auf die Renalsauerstoffextraktion nach einer Herzoperation
3.4 DIE ART DER FLÜSSIGKEIT FÜR DIE HÄMODYNAMISCHE OPTIMIERUNGSSTRATEGIE
Zahlreiche Präsentationen von Lösungen stehen für den Volumenaustausch zur Verfügung, sie variieren je nach Zusammensetzung der Ionen und dem Vorhandensein oder Fehlen organischer Verbindungen. So haben wir die Anwesenheit von Kolloiden und Kristalloiden.
Kolloide gelten als Plasmaexpander, weil sie weniger Kapillarverlust und weniger Lungenödem eimasieren als Kristalloide. Sie reduzieren die Expression von Entzündungsmediatoren, verbessern die Mikrozirkulation und Sauerstoffversorgung des Gewebes und fördern eine Reanimation mit höherem Volumen als Kristalloide. Jedoch, Nebenwirkungen (CS) wurden bereits beobachtet[5].
Die Kristalloide hingegen verlassen das intravaskuläre Fach früher und in größerer Menge als Kolloide, so dass ein größeres Volumen erforderlich ist, um Defizite aufzufüllen (3- bis 4-fache des Volumens der Kristalloide)[6]. Einige der Hauptmerkmale von Kristalloiden sind in Tabellen 02 und Kolloide in Tabelle 03 dargestellt[3].
TABELLE 2 – Hauptkristalloide und ihre Osmolaritäten und Konzentrationen von Natrium (Na+) und Kalium (K+)
| Cristaloide | Osmolaridade (mOsm/L) | Na+ | K+ |
| Glucose 5% | 252 | — | — |
| Glucose 25% | 1260 | — | — |
| Glucose 50% | 2520 | — | — |
| Sodium chloride 0.9% | 308 | 154.0 | 154.0 |
| Sodium chloride and glucose | 264 | 31.0 | 31.0 |
| Ringer’s solution | 309 | 147.0 | 156.0 |
| Compound sodium lactatea | 278 | 131.0 | 111.0 |
| Plasmalyte B | 298.5 | 140 | 98 |
| Normasol | 280 | 140 | 98 |
Quelle: Adapted from Grocott. 2005: Et al
In einer prospektiven blinden Studie an elektiven Patienten, die eine nicht-kardiale Chirurgie, eine intraoperative Flüssigkeitsreanimation mit Kolloidanwendung (6% HES), die Inzidenz von postoperativer Übelkeit und Erbrechen, starken Schmerzen, periorbitalen Ödemen und Doppelsicht hatten, wurde reduzier[13]t.
Bei Patienten, die sich einer größeren Bauchoperation unterziehen, wenn sie allein Kristalloide erhielten, führten sie zu einer Darmflüssigkeitsansammlung im Vergleich zu Patienten, die auch Kolloide erhielten (6% HES[14]). Dies führt zu einem erhöhten Gewebeödem. Die Verbindung von Gewebeödemen mit beeinträchtigter Perfusion und Sauerstoffversorgung ist umstritten[15]
TABELLE 3: Hauptkolloide und ihre jeweiligen Werte der Gewichtsdurchschnitt-Molekulargewicht (PMMP), gewichtete durchschnittliche Molekularzahl (NMMP) und Natrium (Na+) und Chlor (Cl-) Konzentrationen
| Solução | Coloide | PMMP(Da) | NMMP (Da) | Na+(mmol/L) | Cl- (mmol/L) |
| Gelofusine (4%) | Succinylated gelatin | 30,000 | 22,600 | 154 | 125 |
| Haemaccel (3.5%) | Polygeline | 35,000 | 24,300 | 145 | 145 |
| Voluven | Tetrastarch | 130,000 | 60,000 | 154 | 154 |
| Pentaspan | Pentastarch | 264,000 | 63,000 | 154 | 154 |
| HAES-steril 6% or 10% | Pentastarch | 200,000 | 60,000 | 154 | 154 |
| EloHase 6% | Hexastarch | 200,000 | 60,000 | 154 | 154 |
| Hespan 6% | Hetastarch | 450,000 | 70,000 | 150 | 150 |
| Hextend | Hetastarch | 670,000 | 70,000 | 143 | 124 |
| Gentran 40 | Dextran 40 | 40,000 | 25,000 | 154 | 154 |
| Gentran 70 | Dextran 70 | 70,000 | 39,000 | 154 | 154 |
| Rheomacrodex | Dextran 40 | 40,000 | 25,000 | 154 | 154 |
| Macrodex | Dextran 70 | 70,000 | 39,000 | 154 | 154 |
Angepasst von Grocott; Mythen, mythen, mythen. 2005: GAN
Andererseits führen große Mengen an Salzlösung zu hyperchloremischer Azidose und dem Zustand der[16] Hyperkoagulobilität, der noch stärker nac[17]hgewiesen wird als die, die normalerweise bei der Infusion anderer Kristalloide zu beobachten is[18]t.
3.5 RATIONALE VERWENDUNG VON FLUIDEn IM PERIOPERATIVEN PERIOD
Mehr als die Art der verwendeten Flüssigkeit gibt es eine immer deutlichere Sorge, die wirklichen Anzeichen eines Flüssigkeitsaustauschs in der perioperativen Periode zu identifizieren.
Eine der am weitesten verbreiteten Strategien ist Goal-Driven Therapy (GOT), die wiederholt verwendet wurde, um die Ergebnisse der hämodynamischen Optimierung deutlich zu verbessern, sowohl kurz- als auch langfristig, Der TGO-[19]A[20]nsatz konzentriert sich auf die Maximierung (Optimierung) der Herzleistung (CO) durch inkrementelle Flüssigkeitsverabreichun[21]g.
Der 2016 durchgeführte nationale Konsens kam zu dem Schluss, dass der Erfolg in der Ziel-Guided-Therapie (GOT) und anderen restriktiven Strömungsstrategien nahelegen, dass die perioperative Flüssigkeitsplanung betonen sollte, dass die Flüssigkeitstherapie nur dann verabreicht wird, wenn es eine klar[22]e Indikation anhand der in Tabelle 01 dargestellten Aufnahmekriterien gibt.
Darüber hinaus gibt es in Bezug auf die gezielte therapeutische Strategie 9 Studien, in denen eine auf ein Ziel ausgerichtete therapeutische Strategie auch verwendet wurde, um hämodynamische Variablen im Zusammenhang mit dem Fluss von chirurgischen, intra- und postoperativen Patienten zu maximiere[23]n. Die Studien ergaben, dass die Behandlungsstrategie Magen-Darm-Komplikationen und die Dauer des Krankenhausaufenthalts sowohl [24]auf der Station als auch auf der Intensivstation reduzierte[25].
Gleichzeitig mit beginne der Therapie ist es wichtig zu betonen, dass die Bewertung der Reaktionsfähigkeit vor der Flüssigkeitsverabreichung nach dem Beginn der Reaktionsfähigkeit nicht nur bei der Detektion von Flüssigkeitsbedürftigen helfen, sondern auch unnötige und schädliche Flüssigkeitsüberlastung vermeiden kann. Diese Auswertung besteht beispielsweise darin, funktionale dynamische Parameter wie Veränderungen der Herzleistung bei vorlastmodifizierenden Manövern – wie z.B. passive Erhöhung der unteren Gliedmaßen – zu beobachte[20]n.
Bei chirurgischen Hochrisikopatienten verringerte die Verwendung eines hämodynamischen Protokolls zur Aufrechterhaltung der Gewebeperfusion die postoperative Organsterblichkeit und das Versage[26]n. Die Überwachung der Herzleistung durch Berechnung des Sauerstofftransports und -verbrauchs half auch bei der Therapieführun[18]g.
4. ABSCHLIEßENDE ÜBERLEGUNGEN
Das ideale Ersatzregime wäre eine, die die Sterblichkeit verringerte und die Lebensqualität verbesserte, mehrfaches Organversagen und Blutkonsum verringerte und kostengünstig war. Diese Regelung ist offensichtlich noch nicht erreicht worden. Da es keine evidenzbasierte Richtlinie gibt, wird in der Praxis eine Kombination von Kristalloiden und Kolloiden verwendet, und es ist wichtiger zu wissen, wie man ersetzt, als zu wissen, was ersetzt werden soll.
Im Allgemeinen sollten Flüssigkeiten wie jedes andere Medikament angewendet werden, unter Achtung ihrer individuellen Indikationen und Einschränkungen. In diesem Zusammenhang sind vorteilhafte Aspekte des perioperativen Volumenersatzes durch iso-onkotische Lösungen verständlich, obwohl zusätzliche randomisierte kontrollierte Studien erforderlich sind, um ihre Relevanz für das Ergebnis zu beweisen. Zusammenfassend könnte eine rationale Strategie für die Verabreichung von Flüssigkeiten darin bestehen, Patienten, die sich einer operationellen Operation mit geringem Risiko unterziehen, mit einem vernachlässigbaren intravakulären Volumenverlust mit kristalloider Infusion zu behandeln und eine Kombination aus kristalloider und kolloider Verabreichung zu verwenden, die sorgfältig auf der Grundlage hämodynamischer Messungen titriert wird.
Schließlich kommen wir zu dem Schluss, dass eine zielorientierte Therapie in der perioperativen Phase mit einer Verringerung der Komplikationen und der Dauer des Krankenhausaufenthalts verbunden ist. Die positiven Effekte von OT können erreicht werden, wodurch die Schwierigkeiten bei der Aufnahme in die Intensivstationen vermieden werden.
5. REFERENZEN
BRANDSTRUP, B.; SVENDSEN, P. E.; RASMUSSEN, M.; et al. Which goal for fluid therapy during colorectal surgery is followed by the best outcome: near-maximal stroke volume or zero fluid balance? British Journal of Anaesthesia. United Kingdom, v. 109, n.2 , p. 191–199, 17 jun. 2012. Disponível em: <https://ac-els-cdn.ez3.periodicos.capes.gov.br/S000709121732888X/1-s2.0-S000709121732888X-main.pdf?_tid=bde7ae63-beb3-46c9-9adc-e0f04482d0cf&acdnat=1539636094_9a27cfa1829cc5679acd68973a0e7357>. Acesso em: 15 out. 2019.
BUNDGAARD-NIELSEN, M.; HOLTE, K.; SECHER, N. H.; KEHLET, H. Monitoring of peri-operative fluid administration by individualized goal-directed therapy. Acta Anaesthesiologica Scandinavica. USA v. 51, n. 3, p. 331–340, mar. 2007. Wiley/Blackwell (10.1111). Disponível em: <http://doi.wiley.com/10.1111/j.1399-6576.2006.01221.x>. Acesso em: 16 out. 2019.
GOW, K. W.; PHANG, P. T.; TEBBUTT-SPEIRS, S. M.; et al. Effect of crystalloid administration on oxygen extraction in endotoxemic pigs. Journal of Applied Physiology. USA, v. 85, n. 5, p. 1667–1675, nov. 1998. American Physiological SocietyBethesda, MD . Disponível em: <http://www.physiology.org/doi/10.1152/jappl.1998.85.5.1667>. Acesso em: 15 out. 2019.
GROCOTT, M. P. W.; MYTHEN, M. G.; GAN, T. J. Perioperative Fluid Management and Clinical Outcomes in Adults. Anesthesia & Analgesia. USA, v. 100, n. 4, p. 1093–1106, 2005. Disponível em: <https://insights.ovid.com/crossref?an=00000539-200504000-00032>. Acesso em: 15 out. 2019..
GURGEL, S. T.; DO NASCIMENTO, P. Maintaining Tissue Perfusion in High-Risk Surgical Patients. Anesthesia & Analgesia. USA, v. 112, n. 6, p. 1384–1391, 2011. Disponível em: <http://www.ncbi.nlm.nih.gov/pubmed/21156979>. Acesso em: 16 out. 2019..
HAMILTON, M. A.; CECCONI, M.; RHODES, A. A Systematic Review and Meta-Analysis on the Use of Preemptive Hemodynamic Intervention to Improve Postoperative Outcomes in Moderate and High-Risk Surgical Patients. Anesthesia & Analgesia. USA, v. 112, n. 6, p. 1392–1402, 2011. Disponível em: <http://www.ncbi.nlm.nih.gov/pubmed/20966436>. Acesso em: 16 out. 2019.
HOLTE, K.; SHARROCK, N. E.; KEHLET, H. Pathophysiology and clinical implications of perioperative fluid excess. British Journal of Anaesthesia. United Kingdom, v. 84, n. 4, p. 622-632, oct. 2002. Disponível em: <https://www.ncbi.nlm.nih.gov/pubmed/12393365>. Acesso em: 16 out. 2019.
KELLUM, J. A. Saline-induced hyperchloremic metabolic acidosis. Critical care medicine. New York, v. 30, n. 1, p. 259–61, 2002. Disponível em: <http://www.ncbi.nlm.nih.gov/pubmed/11902280>. Acesso em: 15 out. 2019.
LEE, T. H.; MARCANTONIO, E. R.; MANGIONE, C. M.; et al. Derivation and Prospective Validation of a Simple Index for Prediction of Cardiac Risk of Major Noncardiac Surgery. Circulation. Dallas, v. 100, n. 10, sep. 1999. Disponível em: < https://www.ncbi.nlm.nih.gov/pubmed/10477528>. Acesso em: 15 out. 2019.
LORENTZ, M. N. Reposição volêmica perioperatória. Rev Med Minas Gerais. Minas Gerais, v. 20, n. 4, p. 47–56, 2018. Disponível em: <http://rmmg.org/artigo/detalhes/1025>. Acesso em: 15 out. 2019.
MANGANO, D. T.; LAYUG, E. L.; WALLACE, A.; TATEO, I. Effect of Atenolol on Mortality and Cardiovascular Morbidity after Noncardiac Surgery. New England Journal of Medicine. Canada, v. 335, n. 23, p. 1713–1721, 1996. Massachusetts Medical Society . Disponível em: <http://www.nejm.org/doi/abs/10.1056/NEJM199612053352301>. Acesso em: 15 out. 2019.
MORETTI, E. W.; ROBERTSON, K. M.; EL-MOALEM, H.; GAN, T. J. Intraoperative Colloid Administration Reduces Postoperative Nausea and Vomiting and Improves Postoperative Outcomes Compared with Crystalloid Administration. Anesthesia & Analgesia. USA, v. 96, n. 2, p. 611–617, 2003. Disponível em: <https://insights.ovid.com/crossref?an=00000539-200302000-00056>. Acesso em: 15 out. 2019.
MYTHEN, M. G.; WEBB, A. R. Perioperative plasma volume expansion reduces the incidence of gut mucosal hypoperfusion during cardiac surgery. Archives of surgery. Chicago, v. 130, n. 4, p. 423–9, 1995. Disponível em: <http://www.ncbi.nlm.nih.gov/pubmed/7535996>. Acesso em: 16 out. 2019.
ØSTGAARD, G.; REED, R. K. Interstitial fluid accumulation does not influence oxygen uptake in the rabbit small intestine. Acta Anaesthesiologica Scandinavica. USA, v. 39, n. 2, p. 167–173, 1995. Wiley/Blackwell (10.1111). Disponível em: <http://doi.wiley.com/10.1111/j.1399-6576.1995.tb04037.x>. Acesso em: 15 out. 2019.
PEARSE, R.; DAWSON, D.; FAWCETT, J.; et al. Early goal-directed therapy after major surgery reduces complications and duration of hospital stay. A randomised, controlled trial [ISRCTN38797445]. Critical Care. New York, v. 9, n. 6, p. R687, 2005. Disponível em: <http://www.ncbi.nlm.nih.gov/pubmed/16356219>. Acesso em: 16 out. 2019.
PEREL, A.; HABICHER, M.; SANDER, M. Bench-to-bedside review: Functional hemodynamics during surgery – should it be used for all high-risk cases? Critical Care. New York, v. 17, n. 1, p. 203, 2013. BioMed Central. Disponível em: <http://ccforum.biomedcentral.com/articles/10.1186/cc11448>. Acesso em: 15 out. 2019.
POLDERMANS, D.; BOERSMA, E.; BAX, J. J.; et al. The Effect of Bisoprolol on Perioperative Mortality and Myocardial Infarction in High-Risk Patients Undergoing Vascular Surgery. New England Journal of Medicine. Canada, v. 341, n. 24, p. 1789–1794, 1999. Massachusetts Medical Society. Disponível em: <http://www.nejm.org/doi/abs/10.1056/NEJM199912093412402>. Acesso em: 15 out. 2019.
RAOBAIKADY, R.; DINESH, S.; HACKING, M.; WIGMORE, T. Cardiopulmonary exercise testing as a screening test for perioperative management of major cancer surgery: a pilot study. Critical Care. New York, v. 11, n. Suppl 2, p. 250, 2007. BioMed Central. Disponível em: <http://ccforum.biomedcentral.com/articles/10.1186/cc5410>. Acesso em: 15 out. 2019.
RIELLA MC, RIELLA CV, PACHALY MA, RIELLA LV. Metabolismo da água. In: Riella MC, org. Princípios de nefrologia e distúrbios hidroeletrolíticos. 5ª ed. Rio de Janeiro, Brasil: Guanabara Koogan; 2010. p. 105-38.
RUTTMANN, T. G.; JAMES, M. F.; VILJOEN, J. F. Haemodilution induces a hypercoagulable state. British Journal of Anaesthesia. United Kingdom, v. 76, n. 3, p. 412–414, 1996. Oxford University Press. Disponível em: <http://linkinghub.elsevier.com/retrieve/pii/S0007091217435483>. Acesso em: 16 out. 2019.
SHOEMAKER, W. C.; APPEL, P. L.; KRAM, H. B.; WAXMAN, K.; LEE, T. S. Prospective trial of supranormal values of survivors as therapeutic goals in high-risk surgical patients. Chest. Glenview, v. 94, n. 6, p. 1176–86, 1988. Disponível em: <http://www.ncbi.nlm.nih.gov/pubmed/3191758>. Acesso em: 16 out. 2019.
SILVA, E. D.; PERRINO, A. C.; TERUYA, A.; et al. Brazilian Consensus on perioperative hemodynamic therapy goal guided in patients undergoing noncardiac surgery: fluid management strategy – produced by the São Paulo State Society of Anesthesiology (Sociedade de Anestesiologia do Estado de São Paulo – SAESP). Brazilian Journal of Anesthesiology (English Edition). São Paulo v. 66, n. 6, p. 557–571, 2016. Sociedade Brasileira de Anestesiologia. Disponível em: <https://linkinghub.elsevier.com/retrieve/pii/S0104001416301750>. Acesso em: 15 out. 2019.
SINCLAIR, S.; JAMES, S.; SINGER, M. Intraoperative intravascular volume optimisation and length of hospital stay after repair of proximal femoral fracture: randomised controlled trial. BMJ (Clinical research ed.). London, v. 315, n. 7113, p. 909–12, 1997. Disponível em: <http://www.ncbi.nlm.nih.gov/pubmed/9361539>. Acesso em: 16 out. 2019.
SKYTTE LARSSON, J.; BRAGADOTTIR, G.; KRUMBHOLZ, V.; et al. Effects of acute plasma volume expansion on renal perfusion, filtration, and oxygenation after cardiac surgery: a randomized study on crystalloid vs colloid. British Journal of Anaesthesia. United Kingdom, v. 115, n. 5, p. 736–742, 2015. Oxford University Press. Disponível em: <https://linkinghub.elsevier.com/retrieve/pii/S0007091217310759>. Acesso em: 15 out. 2019.
SUBRAMANIAM, B.; SUBRAMANIAM, K.; PARK, K. W. Volume Replacement Strategies and Outcome. International Anesthesiology Clinics. USA, v. 48, n. 1, p. 115–125, 2010. Disponível em: <https://insights.ovid.com/crossref?an=00004311-201004810-00009>. Acesso em: 16 out. 2019.
TOCANTINS, L. M.; CARROLL, R. T.; HOLBURN, R. H. The Clot Accelerating Effect of Dilution on Blood and Plasma. Relation to the Mechanism of Coagulation of Normal and Hemophilic Blood. Blood. Washington, v. 6, n. 8, 1951. Disponível em: <http://www.bloodjournal.org/content/6/8/720.short?sso-checked=true>. Acesso em: 15 out. 2019.
TOTE, S. P.; GROUNDS, R. M. Performing perioperative optimization of the high-risk surgical patient. British Journal of Anaesthesia. United Kingdom, v. 97, n. 1, p. 4–11, 2006. Oxford University Press. Disponível em: <http://linkinghub.elsevier.com/retrieve/pii/S0007091217351772>. Acesso em: 15 out. 2019.
ANHANG – REFERENZEN IN FUßNOTE
2. Hamilton, 2011.
3. Holte, 2002.
4. Grocott, 2005.
5. Brandstrup, 2012.
6. Lorentz, 2018.
7. Subramaniam, 2010.
8. Riella, 2010.
9. Lee, 1999.
10. Raobaikady, 2007.
11. Tote, 2006.
12. Skytte Larsson, 2015.
13. Moretti, 2003.
14. ØStgaard, 1995.
15. Gow, 1998.
16. Kellum, John.
17. Ruttmann, 1996.
18. Tocantins et al. 1951
19. Gurgel; Nascimento, 2011.
20. Hamilton, Cecconi, Rhodes, 2011.
21. Perel, Habicher, Sander, 2003.
22. Silva, Et al. 2016.
23. Bundgaard-Nielsen, 2007.
24. Mythen, 1995.
25. Sinclair, Stephen. James, Sally. Singer, Merrill, 1997.
26. Pearse, Ruppert, 2005.
[1] Medizinisch. Postgraduierter in Intensivmedizin für Erwachsene.
Gesendet: Dezember, 2019.
Genehmigt: Januar 2020.


