RECENSIONE ARTICOLO
TAVARES, Marcela Marçolla [1]
TAVARES, Marcela Marçolla. Uso di Colloidi e Cristalloidi nel periodo perioperatorio di pazienti gravi: Controversia. Rivista scientifica multidisciplinare di nucleo di conoscenza. Anno 05, Ed. 01, Vol. 01, pp. 05-21. gennaio 2020. ISSN: 2448-0959, Collegamento di accesso: https://www.nucleodoconhecimento.com.br/salute/colloidi-e-cristalloidi
RIEPILOGO
Poiché la gestione della sostituzione dei fluidi influenza la prognosi del paziente, la ricerca di base e clinica ha affrontato i vari aspetti che contribuiscono alla somministrazione di fluidi e volume nel periodo perioperatorio. Non c’è ancora consenso su quando e in quale indicare l’ottimizzazione emodinamica perioperatoria. Ulteriori problemi, ad esempio il ruolo relativo dell’ottimizzazione del rapporto cristalloide rispetto al rapporto colloide, non sono stati risolti. Questo lavoro consiste in una revisione della letteratura, condotta tra febbraio e ottobre 2019, in cui è stata effettuata una consultazione a varie pubblicazioni scientifiche, presenti su Internet, attraverso la consultazione nelle banche dati: ScienceDirect, UptoDate, Medline/PubMed, Lilacs, sciELO, con i termini Perioperative Fluid therapy, Hemodynamics, Volume Reposition, Crystalloid, Colloid. Da questo, è stato osservato che i fluidi dovrebbero essere applicati come qualsiasi altro farmaco, rispettando le loro indicazioni e limitazioni individuali, che è la base del concetto di terapia guidata dall’obiettivo – un nuovo concetto che incoraggia l’inquadramento del paziente dei criteri di inclusione per l’ottimizzazione del fluido. Riferendosi a questo, gli aspetti vantaggiosi della sostituzione del volume perioperatorio con soluzioni iso-oncotiche sono comprensibili, anche se sono necessari ulteriori studi controllati randomizzati per dimostrare la sua rilevanza per il risultato.
Parole chiave: Terapia del fluido perioperatorio, Emodinamica, Sostituzione del volume.
1. INTRODUZIONE
Poiché la gestione della sostituzione dei fluidi influenza la prognosi del paziente, la ricerca di base e clinica ha affrontato i vari aspetti che contribuiscono alla somministrazione di fluidi e volume nel periodo perioperatorio. La ricerca di base ha migliorato le conoscenze sulla funzione della barriera vascolare endoteliale e sulle sue alterazioni funzionali responsabili della stravagazione vascolare. Studi clinici che proclamano diversi approcci al controllo dei fluidi hanno mostrato risultati contrastanti e, nella maggior parte dei casi, non si riferiscono alla base fisiologica della barriera vascolare. Sulla base della meta-analisi degli ultimi 30 anni, ci sono stati una serie di studi condotti per ridurre la mortalità e la morbilità chirurgica mediante manipolazione deliberata e preventiva dell’emodinamica perioperatoria, evidenziando una tendenza della comunità scientifica a chiarire se l’ottimizzazione emodinamica sia effettivamente vantaggios[2]a.
È responsabile di studi che si sono concentrati principalmente sugli obiettivi clinici per guidare la terapia volumetrica nel periodo perioperatorio. Tuttavia, un ragionamento dovrebbe generalmente essere derivato da fatti fisiologici e studi significativi e comparabili. Pertanto, questa revisione riassume le conoscenze pertinenti sull’effetto dei diversi fluidi endovenosi e sul monitoraggio emodinamico. Poiché non c’è ancora consenso su questo argomento di grande interesse per tutti gli anestesisti, lo scopo di questo articolo è quello di chiarire alcuni vantaggi e svantaggi dei principali fluidi utilizzati nella sostituzione del volume perioperatorio.
Il ruolo relativo di ottimizzare la relazione cristalloide contro colloide, anche se non risolto, ci sono prove che favorisce soluzioni equilibrate con una concentrazione di elettroliti simile a quella trovata nel plasma, e grandi volumi di soluzione salina dovrebbero essere evitati, in quanto inducono ipercloremiche acidoi[3]s.
2. MATERIALE E METODI
Questo lavoro consiste in una revisione della letteratura, condotta tra febbraio e ottobre 2019, in cui è stata effettuata una consultazione a varie pubblicazioni scientifiche, presenti su Internet, attraverso una ricerca, dai database di ScienceDirect, UptoDate, Medline/PubMed, Lilacs, sciELO, principalmente con i termini Terapia del fluido perioperatorio, Emodinamica, Ridisposizione Volemica, Cristalloide, Colloid.
I criteri per l’inclusione in questo studio sono stati articoli scientifici che descrivono le principali differenze tra colloidi e cristalliidi, nonché le loro principali indicazioni nel periodo perioperatorio. Sono state esaminate diverse modalità di studi tra il 1980 e il 2019, tra cui studi prospettici randomizzati e multicentrici, meta-analisi, studi osservazionali retrospettivi e revisioni della letteratura.
3. RECENSIONE
3.1 LA FISIOLOGIA DELLA COMPARTIMENTAZIONE DEI FLUIDI
L’acqua totale del corpo per un individuo di 75 kg è di circa 45 L (60%). Due terzi di questo (30 L) è acqua intracellulare. Il restante terzo (15 L) nel compartimento extracellulare è diviso tra i compartimenti intravascolari (3 L) e extravascolari (12 L) (Fig. 1)[4]. Il volume intravascolare totale è di circa 5 L e ha componenti cellulari (globuli rossi e bianchi e piastrine: 40%) [2 L]e non cellulari (plasma: 60%[3 L]). Il plasma è una soluzione acquosa di ioni inorganici (prevalentemente cloruro di sodio), molecole semplici come l’urea e molecole organiche più grandi come albumina e globuline.
FIGURA 01: Modello esplicativo di distribuzione dei fluidi nel corpo

Come mostrato nella Figura 01, si nota che gran parte del volume liquido è concentrata nel mezzo intracellulare, essendo composta da soluzione glicosate.
Aumento della permeabilità vascolare a causa dell’attivazione infiammatoria con funzione delle cellule endoteliali alterata può verificarsi per una serie di motivi durante le procedure chirurgiche più grand[5]i. In particolare, trauma tissutale chirurgico, ipoperfusione tissutale a causa di una terapia fluida inadeguata, lesione/reperfusione di ischemia, sepsi (locale o sangue) e uso di bypass cardiopolmonare (ad esempio, bypass cardiopolmonare) sono riconosciuti come stimoli infiammatori che possono compromettere la funzione vascolare[6].
3.2 SOSTITUZIONE DEL VOLUME
La sostituzione del volume deve essere indicata ogni volta che è necessario: 1) sostituire la perdita di sangue durante l’intervento chirurgico, 2) Sostituire le perdite con sudorazione e produzione di urina 3) Interventi chirurgici intestinali preoperatori e 4) manutenzione di terza perdita di spazi[7]o.
È inteso dal terzo spazio come un termine proposto da Randall nel 1952, per descrivere la situazione in cui il fluido extracellulare viene perso o rapito in una zona del corpo dove non partecipa agli scambi, e di conseguenza non soddisfa le esigenze idriche del paziente[8].
3.3 PERIOPERATIVO HEMODINAMICA
I pazienti che potrebbero beneficiare di questa terapia sono quelli ad alto rischio secondo l’indice di rischio cardiaco rivisto e il test di esercizio cardiopolmonare preoperatori[6]o[9],[10]
Secondo una revisione sistematica della letteratura sull’ottimizzazione perioperatoria nei pazienti ad alto rischio chirurgico, sono stati trovati fattori importanti che aiuteranno a identificare i pazienti che trarrebbero il massimo beneficio dall’ottimizzazione dei fluidi perioparator[11]i. I risultati sono descritti nella tabella 01, sulla base degli studi di Mangano et al. (1996), Poldermans ealtri. (1999) e Shoemaker et al. (1988).
TABELLA 01 – Criteri di inclusione per l’ottimizzazione perioperatoria
| Histórico de enfermidade cardíaca ou pulmonar severa, como por exemplo DPOC, infarto agudo do miocárdio, e insuficiência cardíaca. |
| Cirurgias extensas que envolvam anastomoses do trato gastrointestinal (por exemplo, esofagectomia). |
| Perda massiva e abrupta de sangue (>2,5L) |
| Idade maior ou igual a 70 anos com reserve fisiológica limitada em um ou mais órgãos vitais. |
| Septicemia |
| Insuficiência Respiratória (PaO2 <60 mmHg e FIO2 >0.4) |
| Acometimento abdominal agudo como pancreatite, perfuração de vísceras ou sangramentos do TGI. |
| Insuficiência Renal Aguda |
| Doença vascular em estágio avançado |
Fonte: Tote; Motivi (2006)
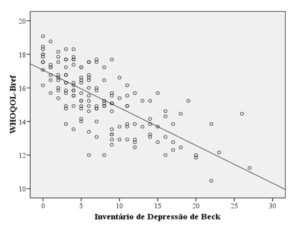
Sulla base di uno studio che ha coinvolto 30 pazienti gravi che hanno subito interventi chirurgici cardiaci, è stato dimostrato che nonostante l’aumento dell’indice cardiaco e del flusso sanguigno renale con entrambi i fluidi, nessuno dei fluidi ha migliorato l’ossigenazione renale, perché sia l’emodiluzione indotta. GFR è aumentato nel cristalloide (28%), ma non nel gruppo colloide, come mostrato nella Figura 0[12]2.
Lo stesso studio ha mostrato che l’uso di cristalliidi ha aumentato il tasso di filtrazione (24%) così come l’estrazione renale di ossigeno (23%), anche senza aumentare l’apporto vascolare del componente, suggerendo che l’aumento del GFR – il principale determinante del consumo di ossigeno – non è stato accompagnato da un aumento proporzionale della frazione di ossigeno fornita ai reni. In altre parole, i loro risultati riassumono nel grafico (figura 02) che il cristalloide ha aumentato l’estrazione di ossigeno renale (P <.001) 20, 40 e 60 min dopo il bolus, a differenza del colloide (NS), suggerendo una compromissione dell’ossigenazione renale nel secondo caso. Il cambiamento nell’estrazione dell’ossigeno renale è stato significativamente (P <,05) più pronunciato nel gruppo cristalloide rispetto al gruppo colloid[11]e.
FIGURA 02: Effetti dell’infusione cristallina (10 ml/kg) e colloide (20 ml/kg) sull’estrazione renale dell’ossigeno dopo la cardiochirurgia
3.4 IL TIPO DI FLUIDO PER LA STRATEGIA DI OTTIMIZZAZIONE EMODINAMICA
Numerose presentazioni di soluzioni sono disponibili per la sostituzione del volume, variano a seconda della composizione degli ioni e della presenza o assenza di composti organici. Quindi abbiamo la presenza di colloidi e cristalloidi.
I colloidi sono considerati espansori di plasma perché causano meno perdita capillare e meno edema polmonare rispetto ai cristalliidi. Riducono l’espressione di mediatori infiammatori, migliorano la microcircolazione e l’ossigenazione dei tessuti e promuovono una maggiore rianimazione del volume rispetto ai cristalliidi. Tuttavia, effetti collaterali (CS) sono già stati osservat[5]i.
I cristalliidi, d’altra parte, lasciano il compartimento intravascolare prima e in quantità maggiore rispetto ai colloidi e, quindi, è necessario un volume maggiore per ricostituire i deficit (da 3 a 4 volte il volume dei cristalliidi[6]). Alcune delle principali caratteristiche dei cristalliidi sono presentate nelle tabelle 02 e colloidi nella tabella 0[3]3.
TABELLA 2 – Cristallilidi principali e le loro osmolarie e concentrazioni di sodio (Na) e potassio (K
| Cristaloide | Osmolaridade (mOsm/L) | Na+ | K+ |
| Glucose 5% | 252 | — | — |
| Glucose 25% | 1260 | — | — |
| Glucose 50% | 2520 | — | — |
| Sodium chloride 0.9% | 308 | 154.0 | 154.0 |
| Sodium chloride and glucose | 264 | 31.0 | 31.0 |
| Ringer’s solution | 309 | 147.0 | 156.0 |
| Compound sodium lactatea | 278 | 131.0 | 111.0 |
| Plasmalyte B | 298.5 | 140 | 98 |
| Normasol | 280 | 140 | 98 |
Fonte: Adattato da Grocott. Et al (2005)
In uno studio cieco e prospettico in pazienti elettivi che hanno avuto la chirurgia non-cardiaca, la rianimazione dei fluidi intraoperatoria con uso colloide (6% HES), l’incidenza di nausea e vomito postoperatori, forti dolori, edema periorbitale e doppia visione è stata ridott[13]a.
Nei pazienti sottoposti a un importante intervento chirurgico addominale, quando hanno ricevuto solo cristalliidi, hanno provocato l’accumulo di liquidi intestinali rispetto a quelli che hanno ricevuto anche colloidi (6% HES[14]). Questo porta ad un aumento dell’edema tissutale. L’associazione di edema tissutale con alterazione perfusione e ossigenazione è controversa[15]
TABELLA 3: Principali colloidi e relativi valori delle concentrazioni Peso Molecolare Medio Ponderato (PMMP), Numero Molecolare Medio Ponderato (NMMP) e Sodio (Na) e Clorine (Cl-)
| Solução | Coloide | PMMP(Da) | NMMP (Da) | Na+(mmol/L) | Cl- (mmol/L) |
| Gelofusine (4%) | Succinylated gelatin | 30,000 | 22,600 | 154 | 125 |
| Haemaccel (3.5%) | Polygeline | 35,000 | 24,300 | 145 | 145 |
| Voluven | Tetrastarch | 130,000 | 60,000 | 154 | 154 |
| Pentaspan | Pentastarch | 264,000 | 63,000 | 154 | 154 |
| HAES-steril 6% or 10% | Pentastarch | 200,000 | 60,000 | 154 | 154 |
| EloHase 6% | Hexastarch | 200,000 | 60,000 | 154 | 154 |
| Hespan 6% | Hetastarch | 450,000 | 70,000 | 150 | 150 |
| Hextend | Hetastarch | 670,000 | 70,000 | 143 | 124 |
| Gentran 40 | Dextran 40 | 40,000 | 25,000 | 154 | 154 |
| Gentran 70 | Dextran 70 | 70,000 | 39,000 | 154 | 154 |
| Rheomacrodex | Dextran 40 | 40,000 | 25,000 | 154 | 154 |
| Macrodex | Dextran 70 | 70,000 | 39,000 | 154 | 154 |
Adattato da Grocott; Mia volta, mia allora, mia figlia. GAN (2005)
D’altra parte, grandi quantità di soluzione salina portano all’acidosi ipercloremica e[16] allo stato di ipercoagulobilità anc[17]ora più evidenti di quelli normalmente riscontrati nell’infusione di altri cristalliid[18]i.
3.5 USO RAZIONALE DEI FLUIDI NEL PERIOD PERIOPERATIVO
Più che il tipo di fluido utilizzato, c’è una preoccupazione sempre più chiara di identificare le reali indicazioni di sostituzione del fluido nel periodo perioperatorio.
Una delle strategie più diffuse è la terapia guidata dagli obiettivi (GOT), che è stata ripetutamente utilizzata per migliorare significativamente i risultati dell’ottimizzazione emodinamica, sia a breve che a lungo termine, L’approccio [19]T[20]GO si concentra sulla massimizzazione (ottimizzazione) dell’uscita cardiaca (CO) mediante somministrazione incrementale dei fluid[21]i.
Il consenso nazionale condotto nel 2016 ha concluso che il successo nella terapia guidata dagli obiettivi (GOT) e in altre strategie strategiche strategiche restrittive suggerisce che la pianificazione dei fluidi perioperatoria dovrebbe sottolineare che la terapia fluida viene somministrata solo quando vi è una chia[22]ra indicazione utilizzando i criteri di inclusione presentati nella tabella 01.
Inoltre, per quanto riguarda la strategia terapeutica mirata, ci sono 9 studi in cui una strategia terapeutica diretta a un obiettivo è stata utilizzata anche per massimizzare le variabili emodinamiche legate al flusso di pazienti chirurgici, intra e postoperator[23]i. Gli studi hanno rilevato che la strategia di trattamento riduceva le complicazioni gastrointestinali e la durata della degenza osp[24]edaliera, sia nel reparto che nelle unità di terapia intensiv[25]a.
Concomitante con l’avvio della terapia, è importante sottolineare che, una volta avviata, la valutazione della reattività prima della somministrazione dei fluidi può non solo aiutare nel rilevamento di pazienti che necessitano di liquidi, ma anche evitare sovraccarichi di liquidi inutili e nocivi. Questa valutazione consiste, ad esempio, nell’osservare parametri dinamici funzionali come i cambiamenti nella produzione cardiaca durante le manovre di precaricamento, come l’elevazione passiva degli arti inferior[20]i.
Nei pazienti chirurgici ad alto rischio, l’uso di un protocollo emodinamico per mantenere la perfusione tissutale ha diminuito la mortalità e l’insufficienza dell’organo postoperatori[26]o. Il monitoraggio della produzione cardiaca calcolando il trasporto e il consumo di ossigeno ha anche aiutato a guidare la terapi[18]a.
4. CONSIDERAZIONI FINALI
Il regime di sostituzione ideale sarebbe uno che ha diminuito la mortalità e migliorato la qualità della vita, diminuito l’insufficienza di organi multipli e l’uso del sangue, ed era a basso costo. Questo programma, ovviamente, non è ancora stato raggiunto. Poiché non esiste una linea guida basata su prove, in pratica viene utilizzata una combinazione di cristalliidi e colloidi, ed è più importante sapere come sostituire che sapere cosa sostituire.
Generalmente, i fluidi dovrebbero essere applicati come qualsiasi altro farmaco, rispettando le loro indicazioni individuali e limitazioni. Riferendosi a questo, gli aspetti vantaggiosi della sostituzione del volume perioperatorio con soluzioni iso-oncotiche sono comprensibili, anche se sono necessari ulteriori studi controllati randomizzati per dimostrare la sua rilevanza per il risultato. Riassumendo le argomentazioni citate in precedenza, una strategia razionale di somministrazione di liquidi potrebbe essere quella di trattare i pazienti sottoposti a chirurgia a basso rischio con trascurabile perdita di volume intravascolare con infusione cristallinidea e utilizzare una combinazione di somministrazione cristallide e colloide, accuratamente titonata sulla base di misurazioni emodinamiche.
Infine, concludiamo che la terapia guidata dall’obiettivo nel periodo perioperatorio è associata a riduzioni delle complicanze e della durata del ricovero. Gli effetti benefici di OT possono essere raggiunti, evitando così le difficoltà di ammissione alle unità di terapia intensiva.
5. RIFERIMENTI
BRANDSTRUP, B.; SVENDSEN, P. E.; RASMUSSEN, M.; et al. Which goal for fluid therapy during colorectal surgery is followed by the best outcome: near-maximal stroke volume or zero fluid balance? British Journal of Anaesthesia. United Kingdom, v. 109, n.2 , p. 191–199, 17 jun. 2012. Disponível em: <https://ac-els-cdn.ez3.periodicos.capes.gov.br/S000709121732888X/1-s2.0-S000709121732888X-main.pdf?_tid=bde7ae63-beb3-46c9-9adc-e0f04482d0cf&acdnat=1539636094_9a27cfa1829cc5679acd68973a0e7357>. Acesso em: 15 out. 2019.
BUNDGAARD-NIELSEN, M.; HOLTE, K.; SECHER, N. H.; KEHLET, H. Monitoring of peri-operative fluid administration by individualized goal-directed therapy. Acta Anaesthesiologica Scandinavica. USA v. 51, n. 3, p. 331–340, mar. 2007. Wiley/Blackwell (10.1111). Disponível em: <http://doi.wiley.com/10.1111/j.1399-6576.2006.01221.x>. Acesso em: 16 out. 2019.
GOW, K. W.; PHANG, P. T.; TEBBUTT-SPEIRS, S. M.; et al. Effect of crystalloid administration on oxygen extraction in endotoxemic pigs. Journal of Applied Physiology. USA, v. 85, n. 5, p. 1667–1675, nov. 1998. American Physiological SocietyBethesda, MD . Disponível em: <http://www.physiology.org/doi/10.1152/jappl.1998.85.5.1667>. Acesso em: 15 out. 2019.
GROCOTT, M. P. W.; MYTHEN, M. G.; GAN, T. J. Perioperative Fluid Management and Clinical Outcomes in Adults. Anesthesia & Analgesia. USA, v. 100, n. 4, p. 1093–1106, 2005. Disponível em: <https://insights.ovid.com/crossref?an=00000539-200504000-00032>. Acesso em: 15 out. 2019..
GURGEL, S. T.; DO NASCIMENTO, P. Maintaining Tissue Perfusion in High-Risk Surgical Patients. Anesthesia & Analgesia. USA, v. 112, n. 6, p. 1384–1391, 2011. Disponível em: <http://www.ncbi.nlm.nih.gov/pubmed/21156979>. Acesso em: 16 out. 2019..
HAMILTON, M. A.; CECCONI, M.; RHODES, A. A Systematic Review and Meta-Analysis on the Use of Preemptive Hemodynamic Intervention to Improve Postoperative Outcomes in Moderate and High-Risk Surgical Patients. Anesthesia & Analgesia. USA, v. 112, n. 6, p. 1392–1402, 2011. Disponível em: <http://www.ncbi.nlm.nih.gov/pubmed/20966436>. Acesso em: 16 out. 2019.
HOLTE, K.; SHARROCK, N. E.; KEHLET, H. Pathophysiology and clinical implications of perioperative fluid excess. British Journal of Anaesthesia. United Kingdom, v. 84, n. 4, p. 622-632, oct. 2002. Disponível em: <https://www.ncbi.nlm.nih.gov/pubmed/12393365>. Acesso em: 16 out. 2019.
KELLUM, J. A. Saline-induced hyperchloremic metabolic acidosis. Critical care medicine. New York, v. 30, n. 1, p. 259–61, 2002. Disponível em: <http://www.ncbi.nlm.nih.gov/pubmed/11902280>. Acesso em: 15 out. 2019.
LEE, T. H.; MARCANTONIO, E. R.; MANGIONE, C. M.; et al. Derivation and Prospective Validation of a Simple Index for Prediction of Cardiac Risk of Major Noncardiac Surgery. Circulation. Dallas, v. 100, n. 10, sep. 1999. Disponível em: < https://www.ncbi.nlm.nih.gov/pubmed/10477528>. Acesso em: 15 out. 2019.
LORENTZ, M. N. Reposição volêmica perioperatória. Rev Med Minas Gerais. Minas Gerais, v. 20, n. 4, p. 47–56, 2018. Disponível em: <http://rmmg.org/artigo/detalhes/1025>. Acesso em: 15 out. 2019.
MANGANO, D. T.; LAYUG, E. L.; WALLACE, A.; TATEO, I. Effect of Atenolol on Mortality and Cardiovascular Morbidity after Noncardiac Surgery. New England Journal of Medicine. Canada, v. 335, n. 23, p. 1713–1721, 1996. Massachusetts Medical Society . Disponível em: <http://www.nejm.org/doi/abs/10.1056/NEJM199612053352301>. Acesso em: 15 out. 2019.
MORETTI, E. W.; ROBERTSON, K. M.; EL-MOALEM, H.; GAN, T. J. Intraoperative Colloid Administration Reduces Postoperative Nausea and Vomiting and Improves Postoperative Outcomes Compared with Crystalloid Administration. Anesthesia & Analgesia. USA, v. 96, n. 2, p. 611–617, 2003. Disponível em: <https://insights.ovid.com/crossref?an=00000539-200302000-00056>. Acesso em: 15 out. 2019.
MYTHEN, M. G.; WEBB, A. R. Perioperative plasma volume expansion reduces the incidence of gut mucosal hypoperfusion during cardiac surgery. Archives of surgery. Chicago, v. 130, n. 4, p. 423–9, 1995. Disponível em: <http://www.ncbi.nlm.nih.gov/pubmed/7535996>. Acesso em: 16 out. 2019.
ØSTGAARD, G.; REED, R. K. Interstitial fluid accumulation does not influence oxygen uptake in the rabbit small intestine. Acta Anaesthesiologica Scandinavica. USA, v. 39, n. 2, p. 167–173, 1995. Wiley/Blackwell (10.1111). Disponível em: <http://doi.wiley.com/10.1111/j.1399-6576.1995.tb04037.x>. Acesso em: 15 out. 2019.
PEARSE, R.; DAWSON, D.; FAWCETT, J.; et al. Early goal-directed therapy after major surgery reduces complications and duration of hospital stay. A randomised, controlled trial [ISRCTN38797445]. Critical Care. New York, v. 9, n. 6, p. R687, 2005. Disponível em: <http://www.ncbi.nlm.nih.gov/pubmed/16356219>. Acesso em: 16 out. 2019.
PEREL, A.; HABICHER, M.; SANDER, M. Bench-to-bedside review: Functional hemodynamics during surgery – should it be used for all high-risk cases? Critical Care. New York, v. 17, n. 1, p. 203, 2013. BioMed Central. Disponível em: <http://ccforum.biomedcentral.com/articles/10.1186/cc11448>. Acesso em: 15 out. 2019.
POLDERMANS, D.; BOERSMA, E.; BAX, J. J.; et al. The Effect of Bisoprolol on Perioperative Mortality and Myocardial Infarction in High-Risk Patients Undergoing Vascular Surgery. New England Journal of Medicine. Canada, v. 341, n. 24, p. 1789–1794, 1999. Massachusetts Medical Society. Disponível em: <http://www.nejm.org/doi/abs/10.1056/NEJM199912093412402>. Acesso em: 15 out. 2019.
RAOBAIKADY, R.; DINESH, S.; HACKING, M.; WIGMORE, T. Cardiopulmonary exercise testing as a screening test for perioperative management of major cancer surgery: a pilot study. Critical Care. New York, v. 11, n. Suppl 2, p. 250, 2007. BioMed Central. Disponível em: <http://ccforum.biomedcentral.com/articles/10.1186/cc5410>. Acesso em: 15 out. 2019.
RIELLA MC, RIELLA CV, PACHALY MA, RIELLA LV. Metabolismo da água. In: Riella MC, org. Princípios de nefrologia e distúrbios hidroeletrolíticos. 5ª ed. Rio de Janeiro, Brasil: Guanabara Koogan; 2010. p. 105-38.
RUTTMANN, T. G.; JAMES, M. F.; VILJOEN, J. F. Haemodilution induces a hypercoagulable state. British Journal of Anaesthesia. United Kingdom, v. 76, n. 3, p. 412–414, 1996. Oxford University Press. Disponível em: <http://linkinghub.elsevier.com/retrieve/pii/S0007091217435483>. Acesso em: 16 out. 2019.
SHOEMAKER, W. C.; APPEL, P. L.; KRAM, H. B.; WAXMAN, K.; LEE, T. S. Prospective trial of supranormal values of survivors as therapeutic goals in high-risk surgical patients. Chest. Glenview, v. 94, n. 6, p. 1176–86, 1988. Disponível em: <http://www.ncbi.nlm.nih.gov/pubmed/3191758>. Acesso em: 16 out. 2019.
SILVA, E. D.; PERRINO, A. C.; TERUYA, A.; et al. Brazilian Consensus on perioperative hemodynamic therapy goal guided in patients undergoing noncardiac surgery: fluid management strategy – produced by the São Paulo State Society of Anesthesiology (Sociedade de Anestesiologia do Estado de São Paulo – SAESP). Brazilian Journal of Anesthesiology (English Edition). São Paulo v. 66, n. 6, p. 557–571, 2016. Sociedade Brasileira de Anestesiologia. Disponível em: <https://linkinghub.elsevier.com/retrieve/pii/S0104001416301750>. Acesso em: 15 out. 2019.
SINCLAIR, S.; JAMES, S.; SINGER, M. Intraoperative intravascular volume optimisation and length of hospital stay after repair of proximal femoral fracture: randomised controlled trial. BMJ (Clinical research ed.). London, v. 315, n. 7113, p. 909–12, 1997. Disponível em: <http://www.ncbi.nlm.nih.gov/pubmed/9361539>. Acesso em: 16 out. 2019.
SKYTTE LARSSON, J.; BRAGADOTTIR, G.; KRUMBHOLZ, V.; et al. Effects of acute plasma volume expansion on renal perfusion, filtration, and oxygenation after cardiac surgery: a randomized study on crystalloid vs colloid. British Journal of Anaesthesia. United Kingdom, v. 115, n. 5, p. 736–742, 2015. Oxford University Press. Disponível em: <https://linkinghub.elsevier.com/retrieve/pii/S0007091217310759>. Acesso em: 15 out. 2019.
SUBRAMANIAM, B.; SUBRAMANIAM, K.; PARK, K. W. Volume Replacement Strategies and Outcome. International Anesthesiology Clinics. USA, v. 48, n. 1, p. 115–125, 2010. Disponível em: <https://insights.ovid.com/crossref?an=00004311-201004810-00009>. Acesso em: 16 out. 2019.
TOCANTINS, L. M.; CARROLL, R. T.; HOLBURN, R. H. The Clot Accelerating Effect of Dilution on Blood and Plasma. Relation to the Mechanism of Coagulation of Normal and Hemophilic Blood. Blood. Washington, v. 6, n. 8, 1951. Disponível em: <http://www.bloodjournal.org/content/6/8/720.short?sso-checked=true>. Acesso em: 15 out. 2019.
TOTE, S. P.; GROUNDS, R. M. Performing perioperative optimization of the high-risk surgical patient. British Journal of Anaesthesia. United Kingdom, v. 97, n. 1, p. 4–11, 2006. Oxford University Press. Disponível em: <http://linkinghub.elsevier.com/retrieve/pii/S0007091217351772>. Acesso em: 15 out. 2019.
APPENDIX – REFERENCES IN FOOTNOTE
2. Hamilton, 2011.
3. Holte, 2002.
4. Grocott, 2005.
5. Brandstrup, 2012.
6. Lorentz, 2018.
7. Subramaniam, 2010.
8. Riella, 2010.
9. Lee, 1999.
10. Raobaikady, 2007.
11. Tote, 2006.
12. Skytte Larsson, 2015.
13. Moretti, 2003.
14. ØStgaard, 1995.
15. Gow, 1998.
16. Kellum, John.
17. Ruttmann, 1996.
18. Tocantins et al. 1951
19. Gurgel; Nascimento, 2011.
20. Hamilton, Cecconi, Rhodes, 2011.
21. Perel, Habicher, Sander, 2003.
22. Silva, Et al. 2016.
23. Bundgaard-Nielsen, 2007.
24. Mythen, 1995.
25. Sinclair, Stephen. James, Sally. Singer, Merrill, 1997.
26. Pearse, Ruppert, 2005.
[1] Medico. Post-laurea in Medicina di Terapia Intensiva per Adulti.
Inviato: Dicembre 2019.
Approvato: gennaio 2020.