ARTICLE ORIGINAL
SILVA, Ítalo Fernando Penha da [1], SERRUYA JÚNIOR, José Maria Henriques [2], GÓES, Tayonara Borges Gonçalves [3], NORONHA, Bruno Gomes de [4], DIAS, Cláudio Alberto Gellis de Mattos [5], DENDASCK, Carla Viana [6], OLIVEIRA, Euzébio de [7], FECURY, Amanda Alves [8]
SILVA, Ítalo Fernando Penha da. Et al. Profil de sensibilité aux antimicrobiens des uropathogènes dans un laboratoire de Macapá, Amapá, Amazonie brésilienne. Revista Científica Multidisciplinar Núcleo do Conhecimento. An 06, Ed. 02, Vol. 04, p. 81-102. février 2020. ISSN: 2448-0959, Lien d’accès: https://www.nucleodoconhecimento.com.br/sante/sensibilite-aux-antimicrobiens, DOI: 10.32749/nucleodoconhecimento.com.br/sante/sensibilite-aux-antimicrobiens
RÉSUMÉ
Les infections des voies urinaires (IVU) représentent un problème de santé mondial. La résistance microbienne, due à la pression sélective des antibiotiques, a une influence directe sur l’évolution et l’impact de ces infections. L’objectif de ces travaux était d’identifier le profil de susceptibilité antimicrobienne des uropathogènes isolés dans des échantillons d’uroculture provenant d’un laboratoire privé de la ville de Macapá/AP. Il s’agit d’une étude quantitative, rétrospective et transversale, à l’aide d’une base de données de laboratoire. Les données ont été recueillies à partir des résultats des urocultures avec antibiogramme analysés de janvier à décembre 2019. La présente étude a évalué 3 510 urocultures, réalisées au cours de la période d’étude, dont 1 269 avaient une croissance bactérienne, soit l’équivalent de 36,15 %. Parmi les résultats positifs, nous avons trouvé les bactéries Escherichia coli (66,59%), Staphylococcus aureus (32,62%), colonies mixtes de E. coli et S. aureus (0,47%), Staphylococcus saprophyticus (0,24%) et Serratia marcescens (0,08%). Le sexe masculin était responsable de 16,35 % (n = 574) des urocultures analysées, tandis que la population féminine était de 83,65 % (n = 2936). Lors de l’analyse de la distribution de bactéries isolées par sexe, les mâles ont été considérés comme un facteur protecteur avec 42% moins de chances de présenter des bactéries dans l’urine. La bactérie E. coli était l’agent pathogène prédominant dans ces infections chez les deux sexes et dans tous les groupes d’âge.
Mots-clés: Uroculture, Sensibilité, Résistance, Antimicrobiens, Antibiotiques, Amazonie.
INTRODUCTION
Une infection des voies urinaires (IVU) signifie) désigne la réponse inflammatoire dans les voies urinaires (urètre, vessie, rein ou prostate), déterminée par un agent microbien (bactéries et/ou virus et/ou champignon et/ou parasite) avec des manifestations cliniques allant de la bactérie asymptomatique au choc septique. Le type d’informatique peut être classifié par son emplacement anatomique : élevé ou bas, symptomatique ou asymptomatique, compliqué ou simple, récurrent ou sporadique (JÚNOR et coll.; 2010).
Aux États-Unis, elles ont représenté environ 2 % des consultations avec les services d’urgence en 2014, soit un total de 2,3 millions de personnes (WIJTING, 2019). Au Brésil, les UDI sont considérées comme les infections bactériennes les plus courantes, responsables de 80 consultations cliniques sur 1 000, et peuvent avoir des particularités entre les sexes (OLIVEIRA; SANTOS, 2018). On estime que près de la moitié des femmes éprouveront au moins un épisode de cystite au cours de leur vie et un tiers d’entre elles avant l’âge de 24 ans (EAU, 2018).
L’agent étiologique le plus commun est les bactéries gramnégatives, Escherichia coli étant le plus fréquent. Les autres bactéries impliquées sont Proteus mirabilis, Klebsiella pneumoniae, Pseudomonas aeruginosa, Enterococcus spp., Enterobacter spp., Streptocoque du groupe B et Staphylococcus saprophyticus (MARTINS et al, 2016).
Le diagnostic des IVUs est basé sur les signes et symptômes cliniques présentés par le patient et l’analyse de l’échantillon d’urine, confirmant la présence de leukocyria et de bactéries significatives (MARTINS et al, 2016). L’incidence élevée de ces infections et la nécessité de commencer le traitement avant que les résultats des résultats microbiologiques deviennent disponibles mènent souvent à l’adoption de la thérapie empirique (CUNHA et al, 2016).
Bien que les avantages de l’utilisation d’antibiotiques soient évidents, leur utilisation abusive ou leur surutilisation ont contribué au problème croissant de résistance chez les bactéries uropathogènes, qui est une grave menace pour la santé publique. Dans les services d’urgence, 20 à 50 % des antibiotiques prescrits se sont révélés inutiles ou inappropriés (EAU, 2018). Contrairement à d’autres médicaments, l’utilisation non ingérable d’antimicrobiens a un impact négatif non seulement sur le patient qui les reçoit, mais aussi sur l’écosystème, lors de la sélection d’agents pathogènes multirésistants (BRASIL, 2019).
Le Rapport mondial de suivi sur la résistance aux antibiotiques publié par l’Organisation mondiale de la Santé a montré qu’une résistance accrue des principales bactéries aux céphalosporines et aux fluoroquinolones est un grave problème de santé dans le monde entier (KANG et al, 2018).
Toute cette exposition augmente le risque d’effets indésirables, d’interactions médicamenteuses indésirables, d’acquisition d’infections concomitantes par d’autres pathogènes multirésistants, champignons et Clostridium difficile, en plus de l’augmentation significative des coûts de soins (directs et indirects) (BRASIL, 2019).
Des études nationales et internationales ont montré une plus grande résistance aux antimicrobiens couramment utilisés. En outre, la connaissance du modèle de résistance des uropathogènes est importante pour guider le choix antimicrobien idéal dans l’approche initiale du patient, parce que les variations dans le spectre microbien et les modèles de susceptibilité peuvent se produire dans différentes régions, et l’utilisation précédente des antimicrobiens est un prédicteur important de la résistance (CUNHA et al, 2016; OLIVEIRA et al., 2020).
Toutefois, des études nationales et internationales ont démontré une résistance croissante aux antimicrobiens couramment utilisés, résultant d’un changement du profil bactérien, reflétant directement la qualité des soins dispensés. Il en est résulté des initiatives mondiales de prévention et de contrôle de la résistance microbienne dans les services de santé afin d’orienter des stratégies et des actions visant à détecter, prévenir et contrôler la propagation des micro-organismes résistants (BRASIL, 2019).
Parmi ces mesures, l’identification des agents pathogènes les plus courants dans la communauté, ainsi que leur profil de sensibilité à l’utilisation d’antimicrobiens, vise à assurer l’effet pharmacothérapeutique maximal; réduire l’apparition d’effets indésirables chez les patients; prévenir la sélection et la propagation de micro-organismes résistants et réduire les coûts de soins.
BUT
Identifier les uropathogènes les plus fréquents dans les urocultures, ainsi que leur profil de sensibilité aux antibiotiques chez les patients externes à Macapá, Amapá, Brésil, visant à améliorer l’efficacité dans l’approche initiale du patient.
MÉTHODOLOGIE
Il s’agit d’une étude quantitative, rétrospective et transversale. Les données des patients qui ont fait analyser l’uroculture de janvier 2019 à décembre 2019 ont été utilisées au Laboratoire médical Dr Paulo J. Albuquerque, situé à Avenida Leopoldo Machado, Centro, Macapá-AP, Brésil. Les données ont été recueillies et organisées en février et mars 2020 et correspondent à la production de tests d’uroculture et d’antibiogramme pour le diagnostic de IVU. L’information a été obtenue en consultation avec la base de données des dossiers d’essai du laboratoire, en utilisant les résultats des urocultures de la clinique externe, du service ou de la communauté. Initialement, l’information a été organisée en utilisant Microsoft Excel 2010 et a été analysée et traitée par l’outil BIOESTAT 5.0. Les données des patients des deux sexes et de tous les groupes d’âge qui ont pratiqué des urocultures dans ce laboratoire de janvier 2019 à décembre 2019 ont été incluses dans l’étude.
Cette étude a été approuvée par le Comité d’éthique de la recherche (CEP/UNIFAP) sous inscription no 4 203 509 et les données recueillies ne seront utilisées qu’aux fins de la cette étude, préservant ainsi l’anonymat de la population échantillonnée.
RÉSULTATS
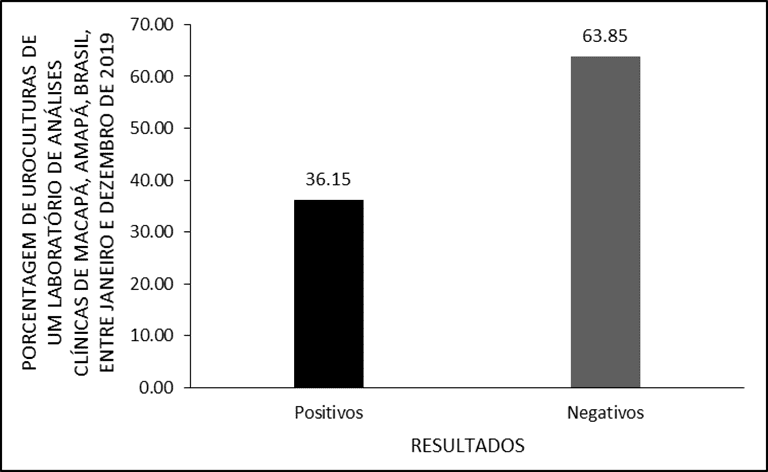
La présente étude a évalué 3.510 urocultures, réalisées entre janvier et décembre 2019 dans un laboratoire d’analyse clinique de la ville de Macapá, amapá, au Brésil, dont 1 269 ont connu une croissance bactérienne, soit l’équivalent de 36,15 % (figure 1).
Figure1 Résultats des urocultures d’un laboratoire d’analyse clinique de la ville de Macapá/AP, de janvier à décembre 2019.
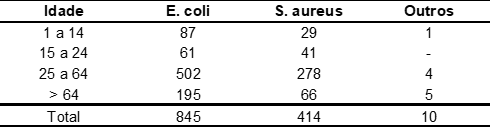
Parmi les résultats positifs, nous avons trouvé les bactéries Escherichia coli (66,59%), Staphylococcus aureus (32,62%), colonies mixtes de E. coli et S. aureus (0,47%), Staphylococcus saprophyticus (0,24%) et Serratia marcescens (0.08%) représentés au tableau 1.
Tableau 1. Bactéries isolées dans les urocultures d’un laboratoire d’analyse clinique de la ville de Macapá/AP de janvier à décembre 2019

Le sexe masculin était responsable de 16,35 % (n = 574) des urocultures analysées, tandis que la population féminine était de 83,65 % (n = 2936). Lors de l’analyse de la répartition des bactéries isolées selon le sexe, les mâles ont été considérés comme un facteur protecteur avec 42 % moins de chances de présenter des bactéries dans l’urine (Odds Ratio = 0[IC 0,480-0,716],58 p<0,05) et les femelles se sont montrées être un facteur de risque avec 1,7 fois plus de chances d’avoir des résultats positifs (p<0,05). Cependant, il n’y avait aucune association en comparant le risque d’infection spécifiquement par E. coli ou S. aureus dans chaque genre (OR = 0,76[IC: 0,537-1,090]5 p = 0,137). Les bactéries S. saprophyticus, S. marcescens et colonies mixtes ont été exclues de ces calculs, car elles ne représentent pas un échantillon significatif.
L’âge des patients variait entre 1 et 106 ans, l’âge moyen dans l’échantillon étudié était de 41 ans et la médiane était de 39 ans. En outre, la population avec des résultats positifs a eu un âge moyen et médian plus élevé que la population avec le résultat négatif, 42 et 38 ans, respectivement. La répartition par groupe d’âge de la population étudiée a été décrite dans le tableau 2.
Tableau 2. Répartition par âge de la population étudiée à partir d’un laboratoire d’analyse dans la ville de Macapá/AP, de janvier à décembre 2019.

Comme le montre le tableau 3, le groupe d’âge entre 25 et 64 ans a concentré la majorité des cas positifs avec 61,47 % (n = 784) dans la population générale.
Tableau 3. Répartition par âge chez les patients selon des bactéries isolées individuellement d’un laboratoire d’analyse de la ville de Macapá/AP, de janvier à décembre 2019.
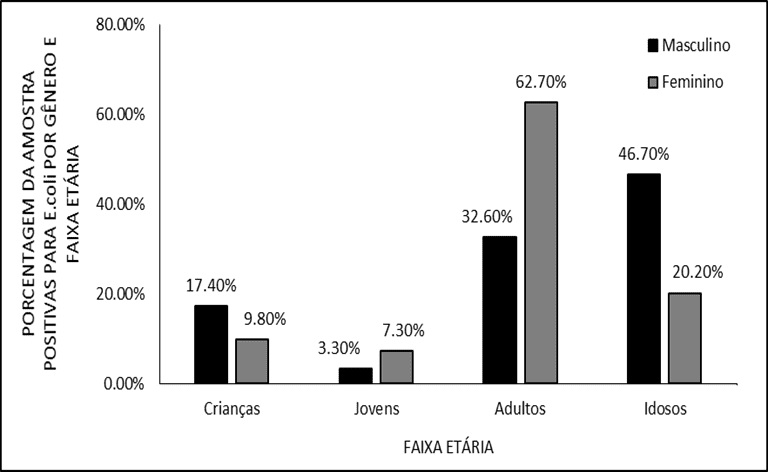
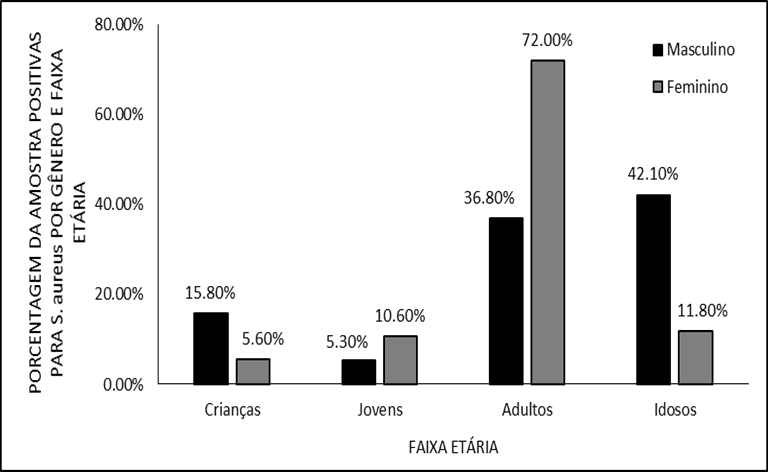
En observant chaque sexe isolément, les femmes ont été plus touchées entre 25 et 64 ans (E. coli 62,7 %; S. aureus 72,0 %) tandis que chez les hommes, les patients âgés (> 64 ans) ont eu un plus grand nombre de cas (E. coli 46,7 %; S. aureus 42,1%). Ces résultats avaient une signification statistique (p<0,05) et sont représentés aux figures 2 et 3.
Figure 2. Distribution d’échantillons positifs pour E. coli selon le sexe et le groupe d’âge.
Figure 3. Distribution d’échantillons positifs pour S. aureus selon le sexe et le groupe d’âge.
Parmi les résultats positifs pour E. coli, 20 antibiotiques répandus dans la pratique clinique ont été testés, ceux-ci sont énumérés dans le tableau 4.
Tableau 4. Sensibilité antimicrobienne et profil de résistance des bactéries E. coli (n = 845) en antibiogrammes provenant d’un laboratoire d’analyse clinique de la ville de Macapá/AP
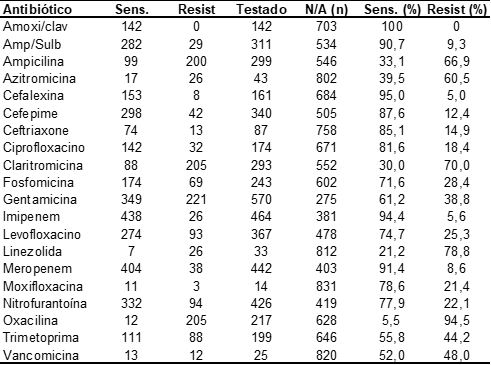
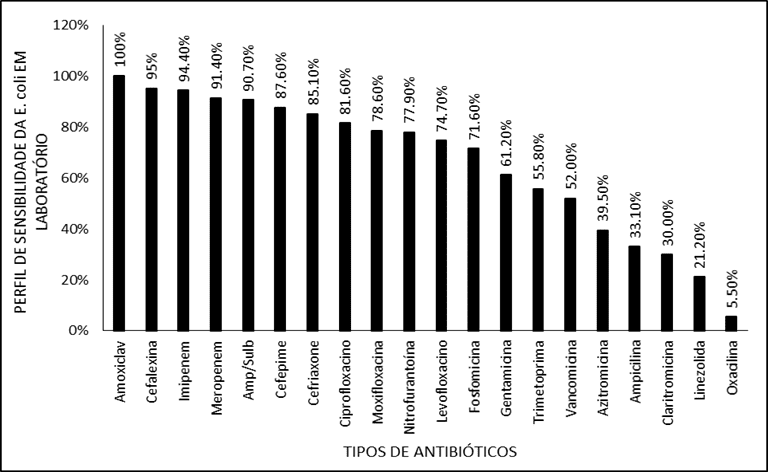
Antibiotiques ayant le taux de sensibilité le plus élevé contre E. coli. étaient: Amoxicillin avec clavulanate (100,0%), Cephalexin (95,0%), Imipenem (94,4%), Meropenem (91,4%), Ampicillin avec Sulbactan (90,5%) et Cefepime (87,5%). La distribution dans l’ordre décroissant de sensibilité était représentée à la figure 4.
Figure 4. Affiche le profil de sensibilité de E. coli à différents antibiotiques en laboratoire.
Parmi les résultats positifs pour S. aureus, 20 antibiotiques répandus dans la pratique clinique ont été testés, qui sont énumérés dans le tableau 5.
Tableau 5. Sensibilité antimicrobienne et profil de résistance de s. aureus (n = 414) en antibiogrammes provenant d’un laboratoire d’analyse clinique de la ville de Macapá/AP
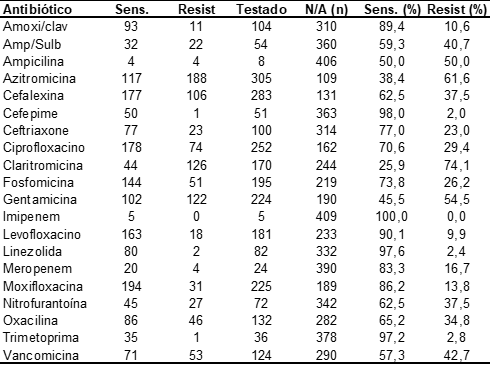
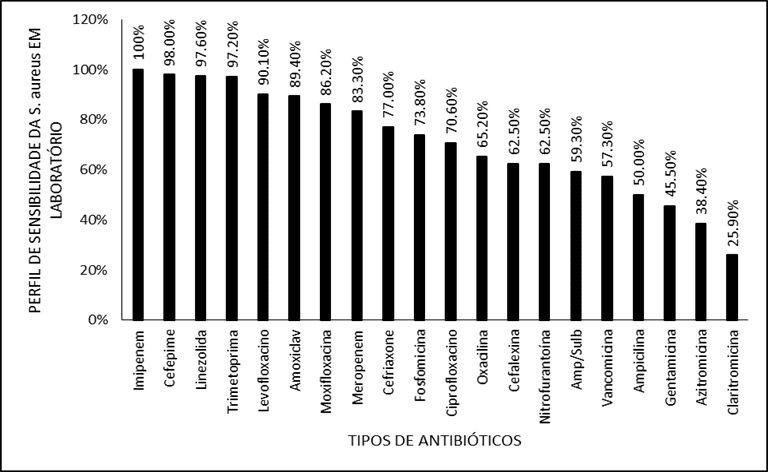
Les antibiotiquesayant l’indice de sensibilité le plus élevé étaient : Imipenem (100,0 %), Cefepime (98,0 %), Linezolid (97,6 %), Trimethoprima (97,2 %), Amoxicilline avec clavulanate (89,4 %) et Levofloxacine (90.1%) La distribution dans l’ordre décroissant de sensibilité était représentée à la figure 5.
La figure 5 montre le profil de sensibilité de E. coli à différents antibiotiques en laboratoire.
DISCUSSION
L’étiologie et le profil de la résistance bactérienne dans les urocultures des patients traités dans une communauté selon l’âge et le sexe sont importants dans la décision de la thérapie antimicrobienne empirique. Les résultats positifs de 36,15 % obtenus dans la recherche ont des rapports similaires chez plusieurs auteurs.
Santos et coll. (2017) ont trouvé 25,7% de résultats positifs de tests culturels avec antibiogramme dans un laboratoire privé de São Paulo. En 2019, au Laboratoire central de santé publique de Macapá (LACEN), les chercheurs ont analysé 2 078 tests et constaté 13,9 % d’urocultures positives (SANTOS; PORCY; MENEZES, 2019). De même, dans un laboratoire de Santa Catarina, 3 232 tests ont été analysés, où 16 % des patients ont obtenu des résultats positifs pour une infection urinaire (MACHADO et coll., 2019). À Ceará, dans un laboratoire qui a fréquenté l’hôpital et la population communautaire, un total de 835 échantillons ont été observés avec 26,52 % des analyses positives (FIGUEREDO; CRUZ; PITA, 2020).
Des chercheurs d’un hôpital pédiatrique du Pará ont analysé 2 222 urocultures chez des enfants de moins de 10 ans avec 9 % de positif (BRÍGIDO, 2020). Résultat divergent de celui trouvé par Marks et coll. (2020) dans un hôpital pédiatrique de Santa Catarina, qui a obtenu 46,2% d’urocultures positives. Des valeurs plus élevées ont été trouvées dans l’unité de soins intensifs de l’hôpital municipal de Santarém/PA, avec des taux positifs d’uroculture de 63,4 %. En général, on s’attend à ce que les unités hospitalières enregistrent une prévalence plus élevée d’urocultures positives comparativement aux laboratoires où les utilisateurs proviennent de la communauté (TIAGO et al, 2020).
Au sujet de sa population, la présente étude a observé une plus grande participation des femmes (88 % des résultats positifs) et le groupe d’âge entre 15 et 64 ans a été plus touché. Un résultat similaire à ceux trouvés dans les études de Machado et coll. (2019), Brambilla et al (2019), Santos et al (2017), Cunha et al (2016) e Araújo e Queiroz (2012) qui ont déclaré 88,2 %, 89,7 %, 84 %, 79 %, 78 % de la participation des femmes, respectivement. Cependant, une plus faible proportion a été observée dans les œuvres de Santos, Porcy et Menezes (2019) et Bail et coll. (2017) avec 55% et 56% chacune. Selon Nóbrega (2015), l’IVU est la maladie urologique la plus fréquente chez les femmes et peut se manifester dans n’importe quel groupe d’âge.
Les facteurs comportementaux prédominent dans la méninge, comme le nombre de partenaires, la fréquence des rapports sexuels, l’utilisation du diaphragme et des spermicides. La génétique et l’anatomie pelvienne jouent également un rôle important puisque l’histoire maternelle de l’IVU récurrente, le cas précédent de l’IVU avant 15 ans et une distance plus courte entre l’urètre et l’anus sont rapportés comme facteurs de risque. Dans postmenopausal, d’autres changements sont mis en évidence, tels que l’insuffisance d’oestrogène, lactobacille vaginal diminué, cystocèle, chirurgie urogenital, volume résiduel post-annulation élevé et IVU précédent (HADDAD ; FERNANDES, 2018).
Selon Marks et coll. (2020), la prévalence féminine la plus élevée d’infection urinaire survient dès la première année de vie, parce qu’avant cela et surtout au cours des trois premiers mois, elle est plus fréquente chez les hommes. On le croit qu’il est dû à la muqueuse du foreskin favorisant l’adhérence bactérienne et le reflux urétéral de vesico qui peuvent être présents à cet âge chez les garçons. Cependant, dans le cas de l’infection dans l’environnement hospitalier, les hommes et les femmes sont affectés d’une manière variable selon les facteurs de risque qui sont associés et aussi sur l’état immunosuppresseur de chaque patient (JORGE; VIDAL, 2014).
Dans cette étude, les hommes représentaient 12 % des échantillons positifs, le groupe d’âge de plus de 64 ans étant le plus touché. Selon Fernandes (2020), la prévalence plus élevée dans la population âgée est justifiée par l’augmentation du volume de prostate qui entraîne l’incapacité de vider complètement la vessie. D’autres changements structurels tels que la sténose d’urètre, les tumeurs urinaires et l’hyperplasie prostatique bénigne, aussi bien que la présence des sondes urétales, éliminent les mécanismes inhérents de défense de l’individu, tels que la miction et la vidange appropriée de la vessie, facilitant l’entrée des micro-organismes intraluminaux dans ce système fermé.
Dans la présente étude, E. coli était l’agent pathogène le plus répandu (66,59 %) suivi de S. aureus (32,62%). Pendant ce temps, la colonisation mixte, S. saprophyticus et S. marcescens < 1,0% chacune. Ce résultat est similaire à une étude menée dans le même laboratoire de Macapá au cours de la période de 2017 qui a signalé la présence d’E. coli (65,4 %), S. aureus, (31,5 %) et Staphylococcus sp, (3.1%) dans leurs échantillons. En ce qui concerne la bactérie prédominante, les deux études ont des valeurs semblables à celles que l’on retrouve dans la littérature nationale et internationale (RODRIGUES et al., 2016; CASTILLO et al, 2019).
À Santa Catarina, Machado et coll. (2019) observé E. coli (62,4 %), suivi de Proteus sp. (17,3%), Klebsiella sp. (10,4%), Estafilococos sp. (8,9%) e Pseudomonas sp. (1%). Dans un laboratoire du Paraná, E a été trouvé. E. coli (60%), suivi de Klebsiella pneumoniae (12%), Morganella morganii (4%), Enterococcus sp (4%), Aeromonas hydrophila (4%) et Citrobacter koseri (4%) (BRAMBILLA, 2019). Une étude, menée au Laboratoire central du Rio Grande do Norte, a révélé E. coli responsable de 60,4%, Klebsiella spp. (14.2%), Staphylococcus spp. (7.2%), e Proteus spp. (4.8%) (CUNHA et al., 2016).
En milieu hospitalier, Bail et coll. (2019) décrit E. coli 56,7 % des cas, suivie de Klebsiella spp. avec 13,5%. Les autres entérobactéries détectées étaient Proteus mirabilis (4,8%), Enterobacter spp (2,9%), Citrobacter spp (2,9%), Pantoea agglomerans (1%) et Serratia marcescens (1%). Figueredo et coll. (2020) a observé, dans le cadre de l’hôpital, E. coli (40,52%); Klebsiella sp. (15,26%); Enterobacter sp. (14,73%); Streptococcus agalactiae (10%) e Proteus sp. (9,47%).
Tiago et coll. (2020), dans une population pédiatrique du Pará, ont observé E. coli avec 53,8%, Proteus mirabilis avec 13,5%, Klebsiella pneumoniae avec 9,6%, Pseudomonas aeruginosa avec 9,6% et Staphylococcus epidermidis avec 5,8% des cas positifs.
Une étude multicentrique portant sur neuf pays européens et le Brésil (étude ARESC) a évalué 3 018 cas d’infection urinaire chez les femmes; la prévalence la plus élevée était E. coli (76,7%), suivi d’Enterococcus faecalis (4%), Staphyloccocus saprophyticus (3,6%), Klebsiella pneumoniae (3,5%) et Proteus mirabilis (3.5%) (NABER, 2008).
Dans l’étude de résistance aux antibiotiques de la dimension nordique (NoDARS), la Finlande, l’Allemagne, la Lettonie, la Pologne, la Russie et la Suède ont prélevé des échantillons d’urine chez des femmes ambulatoires présentant des symptômes d’infection urinaire simple et ont trouvé E. coli responsable dans 77,2 % des cas (NY et coll., 2019).
Dans la littérature la plupart des micro-organismes isolés appartiennent à la famille des entérobactéries, aux résidents de l’intestin humain et considérés comme des causes importantes d’OV, de sang, d’infections hospitalières, de pneumonies et de diverses infections intra-abdominales. E. coli est l’agent pathogène le plus souvent associé aux OV pour tous les syndromes et groupes d’âge où sa transmission se fait par contact direct personne par personne et par voie fécale-orale. Issu du microbiote intestinal, il est adested et colonisé par les fibrias et les adhésines, empêchant son élimination par le flux urinaire (BAIL et autres 2019).
Le deuxième agent pathogène le plus répandu dans cette étude, S. aureus (32,62 %), est une bactérie grampositive et a une grande adaptation aux conditions environnementales et peut survivre à des sites acides, basiques et secs. Ces micro-organismes sont des bactéries anaérobies facultatives et ont un grand impact sur la santé publique, étant une cause importante d’infections chez l’homme et d’autres animaux. On le trouve souvent dans les narines et la peau humaines et sa relation avec l’UT en général est liée aux soins de santé (FRANÇA et al, 2020). La proportion élevée trouvée dans cette étude diffère d’une grande partie de la littérature et peut être une conséquence de la contamination des échantillons pendant la procédure de collecte effectuée par méthode manuelle (CASTILLO et al, 2019).
Les infections des voies urinaires polymicrobiennes sont peu fréquentes. La présence de deux bactéries ou plus dans la culture soulève des doutes quant à la fiabilité du test et suscite des soupçons de contamination possible de l’échantillon. La confirmation du diagnostic doit être effectuée avec l’acquisition d’échantillons d’urine en série, en observant la présence des mêmes agents pathogènes dans les échantillons subséquents (FIGUEREDO; CRUZ; PITA, 2020).
La résistance aux antibiotiques est devenue l’un des problèmes de santé publique les plus importants au monde. Cette augmentation, observée depuis les dernières années du siècle, a généré un mouvement mondial dans le but de limiter ses effets potentiellement catastrophiques. Les conséquences de la résistance aux antibiotiques sont difficiles à prévoir, mais on estime que d’ici 2050, elle sera la cause de la mort d’une dizaine de millions de personnes et assumera un coût économique énorme (ALFAYATE, MIGUELEZ; GARCIA-MARCOS, 2020).
La présente étude a évalué la susceptibilité à plusieurs antibiotiques communs dans la pratique médicale. La bactérie E. coli était sensible aux bêta-lactams : amoxicilline avec clavulanate (100.0%), cephalexin (95.0%), ampicilline et sulbactan (90.5%) – avec une faible sensibilité à l’ampicilline seule (33%) – et 3ème et 4ème génération cephalosporins avaient 85% et 87%. En outre, plus de 90% des cultures étaient sensibles aux carbapénèmes. La sensibilité aux fluoroquinolones était variée : Ciprofloxacine (81,4 %), moxifloxacine (78 %) et la lévofloxacine (74,7 %). Les médicaments de choix dans la plupart des lignes directrices, comme la nitrofurantoïne et la phosphomycine, présentaient une sensibilité modérée avec 77,9 % et 71,6 %, respectivement. Les macrolides se sont montrés de faible efficacité (<40%), même inclus dans les antibiogrammes, ces médicaments n’ont aucun rôle dans le traitement des IVUs.
Bien que cette étude ait montré un bon profil d’action des bêta-lactams, il est important de souligner que ces médicaments perdent leur efficacité en raison de souches productrices de bêta-lactamases à spectre étendu (ESBL). Ny et coll. (2018), Kim et coll. (2015) et Zavala-Cerna et coll. (2020) ont constaté une prévalence de 8,7 %, 25,6 % et 24,6 % dans leurs études. Le mécanisme de résistance est essentiellement dû à la transmission plasmide- médiatisée des gènes codant ces enzymes.
La résistance à l’ampicilline est déjà décrite dans plusieurs études, cependant, malgré le taux élevé de résistance, ce médicament est considéré comme un traitement de première ligne pour les bactéries sensibles chez les femmes enceintes en raison de son profil d’innocuité (MACHADO, 2018; BAIL, 2019; BRÍGIDO, 2020). Dans ce travail, il a été remarqué que l’ajout d’inhibiteurs de la bêta-lactamase était suffisant pour améliorer le profil d’action de cette classe de médicaments. La compréhension totale des types de bêta-lactamases produites par les souches et leur profil d’action suscite encore de nombreux doutes dans la communauté scientifique, car on ne sait pas comment le profil général des pathogènes bactériens réagira à l’application clinique de la nouvelle vague d’inhibiteurs de la bêta-lactamase (TOOKE, 2019).
European Association of Urology a indiqué que les aminopenicilines ne soient utilisées que dans des situations exceptionnelles, comme dans le traitement d’IVU compliquées, où elles devraient être associées à d’autres classes d’antibiotiques; tandis que les céphalosporines de 3e et 4e générations devraient être réservées aux cas de pyélonephrite et d’uréropse (EAU, 2018).
Fluoroquinolones sont largement utilisés dans le traitement empirique de l’infection urinaire (IVU), y compris les cas d’infections des voies urinaires élevées. Dans une importante revue de littérature, Lee et coll. (2016) ont souligné qu’au Japon et en Australie, la susceptibilité de E. coli à ces médicaments était d’environ 90%; aux Etats-Unis entre 70~88% et en Chine 74~84%. En outre, dans les pays d’Europe du Nord, 80 % ont été trouvés, tandis que d’autres régions européennes et certaines régions méditerranéennes ont fait preuve d’environ 60 % de susceptibilité. Ny et coll. (2018), en Russie et en Europe de l’Est, ont montré une sensibilité de 85%. Au Brésil, nous avons également trouvé des résultats variés en ce qui concerne la sensibilité de E. coli às fluoroquinolonas: Marks et al (2020) 96%, Brígido et al (2020) 85%, Machado et al (2019) 83%; enquanto Cunha et al (2016) 75%, Figueredo et al (2020) 71%; Bail et al (2020) 61%; Tiago et al (2020) 54,6%.
Selon Lee et coll. (2016), la susceptibilité des bactéries gramnégatives à la ciprofloxacine était beaucoup plus élevée chez les patients de moins de 20 ans que chez les patients plus âgés. La raison de cette observation peut être la plus faible exposition aux fluoroquinolones chez les jeunes individus, puisque ces médicaments n’ont pas un bon profil d’innocuité dans la population pédiatrique.
Aucune ligne directrice nationale ou internationale ne recommande l’utilisation de quinolonas comme première ligne chez les patients atteints d’une infection urinaire simple. En outre, il est déterminé qu’il y a augmentation significative de la manifestation des effets secondaires sérieux sur des systèmes musculo-squelettiques. À cet égard, l’utilisation de ces médicaments est interdite dans des conditions telles que : la prise en charge des infections autolimitatives, les patients ayant des antécédents d’effets indésirables, les greffes d’organes solides ou ceux qui utilisent continuellement des corticostéroïdes parce que dans ces groupes, le risque de tendinite et de rupture tendinite est exacerbé (ANVISA, 2018). Un rapport similaire a été publié par European Medicine Agency qui a suspendu la publicité, restreint l’utilisation et suggéré une surveillance accrue des professionnels de santé dans les effets néfastes des quinonines (EMA, 2019)
Bien que les résultats de cette étude aient démontré une sensibilité modérée à la phosphomycine (71,6 %) et la nitrofurantoine (77,9 %), depuis plus d’une décennie, ils sont considérés comme des antimicrobiens de choix pour le traitement empirique de la cystite aiguë simple (GUPTA et coll., 2011). La phosphomycine inhibe la synthèse peptidoglycane à un stade plus précoce que les antibiotiques bêta-lactam ou les glycopeptides et a un large spectre d’activité, y compris E. coli produisant de l’esbl. Nitrofurantoin, d’autre part, agit en endommageant l’ADN bactérien dans sa forme réduite très active. Naber et coll. (2008), au Brésil et en Europe, ont constaté une sensibilité de 87 % et de 96,4 % pour la phosphomycine et la nitrofurantoine, respectivement. Aujourd’hui encore, après la popularisation de son utilisation, la résistance est faible de 0 à 5 % (LEE et coll., 2016). En Russie et en Europe de l’Est, la sensibilité à la nitrofurantoine et à la phosphomycine était de 98,8 % et de 98,7 % (NY et coll., 2018); dans notre pays, Machado et coll. (2018) ont identifié que la sensibilité était de 95,1 % et 97,5 % et Cunha et coll. (2016) ont trouvé plus de 92 %.
La présente étude a observé la sensibilité au sulfamethoxazole-trimethoprim dans seulement 55.8%. Ce médicament a été utilisé pendant plus de 30 ans comme thérapie de première ligne pour les OV et la prophylaxie de la cystite récurrente. Cependant, la résistance aux antimicrobiens à cet agent a augmenté au fil des ans, approchant les 18-22% dans certaines régions des États-Unis et d’Europe. L’étude ARESC (NABER, 2008) a déjà observé des taux élevés de résistance de l’E. coli au sulfamethoxazole-trimethoprim (29%), confirmé par des études récentes en Russie et en Corée du Sud (NY et coll., 2018) et par Kim et coll. (2015) qui ont signalé une résistance comprise entre 22-32,6% et 39,4%. Au Brésil, Machado et coll. (2018), Bail et coll. (2019), Figueredo et coll. (2020) et Castillo et coll. (2019) ont trouvé 25 %, 35,7 %, 39,5 % et 62 % respectivement, ce qui rend leur utilisation empirique douteuse. Néanmoins, on rapporte que son profil de sensibilité a augmenté ces dernières années en raison de la réduction de sa prescription (KANG et coll., 2018).
Plusieurs initiatives mondiales ont mis en garde contre l’utilisation rationnelle d’antibiotiques suggérant la mise en œuvre de programmes d’éducation locaux, le contrôle de la prescription et de la vente d’antibiotiques et le soutien à la mise en œuvre de lignes directrices pour la prise en charge des maladies infectieuses. Qui a déclaré que seuls les antibiotiques résistants aux tests de sensibilité aux antimicrobiens (AST) supérieurs à 80 % devraient être prescrits. Par conséquent, tout médicament dont le taux de résistance est supérieur ou égal à 20 % ne doit pas être administré empiriquement compte tenu de l’inefficacité et de l’induction de l’émergence de nouvelles bactéries résistantes (FIGUEREDO; CRUZ; PITA, 2020; CUNHA, 2016; DORON & DAVIDSON, 2011; GUPTA et al, 2011).
La durée du traitement a également fait l’objet de débats au cours des dernières années, les lignes directrices récentes recommandent un traitement à dose unique ou des régimes plus courts, jusqu’à 5 jours. Un examen systématique a prouvé qu’il n’y avait aucune différence dans l’amélioration de symptôme entre les régimes de 3 jours et 5 à 10 jours d’utilisation d’antibiotiques chez les femmes avec la cystite simple. Les traitements plus longs sont sujets à plus d’effets secondaires et à l’abandon par l’utilisateur, mais ils sont liés à la répétition inférieure à court terme (MILO et al, 2005).
CONCLUSIONS
Les infections des voies urinaires sont toujours un problème de santé publique étant donné leur incidence élevée dans la population. Les femmes en âge de procréer sont les plus touchées en raison de facteurs anatomiques et comportementaux, mais la prévalence augmente chez les hommes après la 6ème décennie de vie.
La bactérie E. coli était l’agent pathogène prédominant dans ces infections chez les deux sexes et dans tous les groupes d’âge. Le profil de résistance de cette bactérie a quelques particularités au niveau local, telles qu’une bonne sensibilité aux bêta-lactams et une sensibilité modérée à la nitrofurantoïne et à la phosphomycine. Les résultats présentés montrent la nécessité de l’uroculture et des ASS pour que la thérapie soit adéquate et efficace, en évitant la prescription inappropriée de médicaments, qui en plus de ne pas traiter l’infection peut induire une résistance bactérienne.
Il est important de développer des recherches qui explorent le profil épidémiologique de la région parce qu’elle fournit un cadre théorique à la communauté médicale pour fonder ses décisions thérapeutiques en tenant compte du modèle de résistance locale, ce qui se traduit par de meilleurs soins, une réduction de la morbidité et la récurrence de ces infections.
RÉFÉRENCES
ALFAYATE MIGUELEZ, Santiago; GARCIA-MARCOS, Luis. Rational use of antimicrobials in the treatment of upper airway infections. J. Pediatr. (Rio J.), Porto Alegre , v. 96, supl. 1, p. 111-119, Mar. 2020
ARAÚJO, K.L; QUEIROZ, A.C; Análise do perfil dos agentes causadores de infecção do trato urinário e dos pacientes portadores, atendidos no Hospital e Maternidade Metropolitano-SP. J Health Sci Inst., v.30, n.1, p.7-12, 2012.
BAIL, Larissa et al. Perfil de sensibilidade de bactérias isoladas em uroculturas de pacientes atendidos em um hospital brasileiro. Cadernos da Escola de Saúde, v. 17, n. 2, p. 52-60, 2017.
BRAMBILLA, Gabriela Gonçalves; DA SILVA ECKER, Alessandra Barrochelli. Incidência de microrganismos em infecções no trato urinário e sua relação com o antibiograma em um laboratório da região do noroeste do paraná. REVISTA UNINGÁ, v. 56, n. 4, p. 85-97, 2019.
BRASIL, ANVISA. Agência Nacional de Vigilância Sanitária. PROJETO STEWARDSHIP BRASIL. Avaliação Nacional dos Programas de Gerenciamento do Uso de Antimicrobianos em Unidade de Terapia Intensiva Adulto dos Hospitais Brasileiros. Gerência de Vigilância e Monitoramento em Serviços de Saúde. Gerência Geral de Tecnologia em Serviços de Saúde. Brasília-DF, 2019.
BRASIL, ANVISA – Agência Nacional De Vigilância Sanitária. Risco de efeitos colaterais graves incapacitantes e potencialmente irreversíveis e restrições no uso – quinolonas e fluoroquinolonas sistêmicas e inalatórias. 2018.
BRÍGIDO, Heliton Patrick Cordovil et al. Perfil de resistência de agentes de infecção urinária em crianças internadas em um hospital de pediatria em Belém do Pará. Brazilian Journal of Health Review, v. 3, n. 4, p. 9808-9818, 2020.
CASTILLO, Naiara Campos Paixão de. et al. Resistência Bacteriana em Uroculturas de mulheres em Macapá: comparação dos resultados ambulatoriais e hospitalares. Revista Científica Multidisciplinar Núcleo do Conhecimento. Ano 04, Ed. 10, Vol. 13, pp. 128-165. Outubro de 2019. ISSN: 2448-0959
CUNHA, M. A., ASSUNÇÃO, G. L., MEDEIROS, I. M., & FREITAS, M. R. (2016). ANTIBIOTIC RESISTANCE PATTERNS OF URINARY TRACT INFECTIONS IN A NORTHEASTERN BRAZILIAN CAPITAL. Revista do Instituto de Medicina Tropical de São Paulo, 58, 2. doi:10.1590/S1678-9946201658002
DORON, S., & DAVIDSON, L. E. (2011). Antimicrobial stewardship. Mayo Clinic proceedings, 86(11), 1113–1123. https://doi.org/10.4065/mcp.2011.0358.
EAU GUIDELINES. Edn. presented at the EAU Annual Congress Copenhagen 2018. ISBN 978-94-92671-01-1. EAU Guidelines Office, Arnhem, The Netherlands.
European Medicines Agency (EMA). Disabling and potentially permanent side effects lead to suspension or restrictions of quinolone and fluoroquinolone antibiotics. 11 March 2019 EMA/175398/2019. Disponível em <https://www.ema.europa.eu/en/documents/referral/quinolone-fluoroquinolone-article-31-referral-disabling-potentially-permanent-side-effects-lead_en.pdf> Acesso em 12 out 2020.
FERNANDES, Thaís Siqueira. Infecção do trato urinário no idoso: revisão de literatura. Repositório de Trabalhos de Conclusão de Curso, 2020.
FIGUEREDO, Fernando Gomes; CRUZ, Ítalo Silva; PITA, Pablo. Avaliação do perfil de resistência bacteriana em uroculturas no cariri cearense–brasil. Avaliação do perfil de resistência bacteriana em uroculturas no cariri cearense–brasil, p. 1-388–416. Comunicação científica e técnica em medicina [recurso eletrônico] /Organizador Benedito Rodrigues da Silva Neto. – Ponta Grossa, PR: Atena, 2020
FRANÇA, Fabrício Rota et al. Incidência de infecção relacionada à assistência à saúde na unidade de terapia intensiva de um hospital de médio porte. Revista funec científica-multidisciplinar-ISSN 2318-5287, v. 9, n. 11, p. 1-12, 2020.
GOLDMAN, L., SCHAFER, A. I. Cecil: Medicina 24ª edição. Rio de Janeiro: Elsevier, 2014
GUPTA, Kalpana et al. International clinical practice guidelines for the treatment of acute uncomplicated cystitis and pyelonephritis in women: a 2010 update by the Infectious Diseases Society of America and the European Society for Microbiology and Infectious Diseases. Clinical infectious diseases, v. 52, n. 5, p. e103-e120, 2011.
HADDAD JM, FERNANDES DA. Infecção do trato urinário. São Paulo: Federação Brasileira das Associações de Ginecologia e Obstetrícia (Febrasgo); 2018. (Protocolo Febrasgo – Ginecologia, nº 63/Comissão Nacional Especializada em Uroginecologia e Cirurgia Vaginal).
IRONMONGER D, EDEGHERE O, GOSSAIN S, HAWKEY PM. Use of antimicrobial resistance information and prescribing guidance for management of urinary tract infections: survey of general practitioners in the West Midlands. BMC Infect Dis. 2016 May 24;16:226. doi: 10.1186/s12879-016-1559-2. PMID: 27221321; PMCID: PMC4877747.
JORGE, H. M. S.; VIDAL, E. C. F. Infecção do trato urinário hospitalar e suas implicações para a gestão do cuidar: revisão integrativa. Cadernos de Cultura e Ciência, Crato, v. 13, n. 1, p.39-48, 2014.
JÚNIOR, A. N., FILHO, M. Z., REIS, R. B. Urologia Fundamental. Sociedade Brasileira de Urologia (SBU) São Paulo: Planmark, 2010
KANG CI, KIM J, PARK DW, et al. Clinical Practice Guidelines for the Antibiotic Treatment of Community-Acquired Urinary Tract Infections. Infect Chemother. 2018;50(1):67–100. doi:10.3947/ic.2018.50.1.67
KIM, Woong Bin et al. Recent antimicrobial susceptibilities for uropathogenic Escherichia coli in patients with community acquired urinary tract infections: a multicenter study. Urogenital Tract Infection, v. 12, n. 1, p. 28-34, 2017.
LEE, Dong Sup et al. Role of age and sex in determining antibiotic resistance in febrile urinary tract infections, International Journal of Infectious Diseases, Volume 51, 2016, Pages 89-96, ISSN 1201-9712, https://doi.org/10.1016/j.ijid.2016.08.015.
MACHADO, Ariane Dhoyce; NAUMANN, Daniele Cristina; FERRAZZA, Magda Helena Soratto Heitich; TENFEN Adrielli; GUEVOHLANIAN-SILVA, Bárbara Yasmin; WEBER, Karla. Prevalência de infecção urinária em um laboratório de análises clínicas da cidade de Jaraguá do Sul, SC, no ano de 2017. RBAC, v. 51, n. 3, p. 213-8, 2019.
MARKS, Fernanda Ossani et al. Infecção do trato urinário: etiologia, perfil de sensibilidade e resistência aos antimicrobianos em hospital pediátrico. Research, Society and Development, v. 9, n. 8, 2020.
MARTINS, Milton de Arruda; CARRILHO, Flair José; ALVES, Venâncio Avancini Ferreira; CASTILHO, Euclides Ayres de; CERRI, Giovanni Guido. Clínica Médica: Doenças hematológicas, oncologia, doenças renais. 2ª edição. Barueri-SP. Editora Manole [S.l: s.n.], 2016.
MILO G, KATCHMAN EA, PAUL M, CHRISTIAENS T, BAERHEIM A, LEIBOVICI L. Duration of antibacterial treatment for uncomplicated urinary tract infection in women. Cochrane Database Syst Rev. 2005;(2):CD004682. Published 2005 Apr 18.
NABER KG, SCHITO G, BOTTO H, PALOU J, MAZZEI T. Surveillance study in Europe and Brazil on clinical aspects and Antimicrobial Resistance Epidemiology in Females with Cystitis (ARESC): implications for empiric therapy. Eur Urol. 2008;54(5):1164–75
NÓBREGA, M M. Bacteriúria em mulheres após estudo urodinâmico: fatores de risco e análise microbiológica. São Paulo, 2015. Dissertação de Mestrado. Faculdade de Ciências Médicas da Santa Casa de São Paulo – Curso de Pós-Graduação em Pesquisa em Cirurgia.
NY, Sofia et al. Antimicrobial resistance of Escherichia coli isolates from outpatient urinary tract infections in women in six European countries including Russia. Journal of global antimicrobial resistance, v. 17, p. 25-34, 2019. ISSN 2213-7165.
OLIVEIRA, Sergio Marcelino; SANTOS, Ludimylla Lins Gondim. Infecção do trato urinário: estudo epidemiológico em prontuários laboratoriais. Journal Health NPEPS. 2018; 3(1):198-210.
OLIVEIRA, M. K. R.; ALENCAR, S. S.; DIAS, C. A. G. M.; FECURY, A. A. Perfil epidemiológico da mortalidade dos setores intensivos de um hospital público de Macapá/AP. Temas em Saúde, v. 20, p. 163-177, 2020. https://temasemsaude.com/wp-content/uploads/2020/04/20209.pdf
RESENDE, J. A. et al. Infecção do trato urinário de origem hospitalar e comunitária: revisão dos principais micro-organismos causadores e perfil de susceptibilidade. Revista Científica Fagoc Saúde. Vol 1. 2016. ISSN: 2448-282X
RODRIGUES, S. C. S.; FECURY, A. A.; DIAS, C. A. G. M.; OLIVEIRA, E. Occurrence of Staphylococcus Aureus in Hospitals: A literature review. Revista Científica Multidisciplinar Núcleo do Conhecimento, v. 02, p. 33-42, 2016. https://www.nucleodoconhecimento.com.br/health/staphylococcus-aureus
SANTOS, Amanda Grossi et al. Prevalência de positividade bacteriana em exames de urina de um laboratório particular em itapevi. 2017. Revista Saúde em Foco – Edição nº 9 – Ano: 2017.
SANTOS, Maria José Amador dos; PORCY, Claude; DE OLIVEIRA MENEZES, Rubens Alex. Etiologia e perfil de resistência bacteriana em uroculturas de pacientes atendidos em um hospital público de Macapá-Amapá, Brasil. Um estudo transversal. REVISTA DIAGNÓSTICO E TRATAMENTO• VOLUME 24• EDIÇÃO 4, p. 135, 2019
TIAGO, Keyla Pereira et al. Frequência e resistência de uroculturas provenientes de pacientes internados na unidade de terapia intensiva do hospital municipal de Santarém-PA. RBAC, v. 52, n. 1, p. 64-70, 2020.
TOOKE, C. L., HINCHLIFFE, P., BRAGGINTON, E. et al. β-Lactamases and β-Lactamase Inhibitors in the 21st Century. Journal of molecular biology, 431(18), 3472–3500. https://doi.org/10.1016/j.jmb.2019.04.002
WIJTING, I. E. A. et al. Urinary tract infections in a university hospital: pathogens and antibiotic susceptibility. The Netherlands Journal of Medicine, v. 77, n. 6, p. 210-219, 2019.
ZAVALA-CERNA, Maria G. et al. The Clinical Significance of High Antimicrobial Resistance in Community-Acquired Urinary Tract Infections. Canadian Journal of Infectious Diseases and Medical Microbiology, v. 2020, 2020.
[1] Universitaire de la 11ème période du cours de médecine à l’Université fédérale d’Amapá (UNIFAP).
[2] Universitaire de la 11ème période du cours de médecine à l’Université fédérale d’Amapá (UNIFAP).
[3] Universitaire de la 11ème période du cours de médecine à l’Université fédérale d’Amapá (UNIFAP).
[4] Maîtrise en sciences forestières de l’Université fédérale du Rio Grande do Norte (UFRN). Doctorant à l’Université fédérale de Viçosa (UFV).
[5] Biologiste, Ph.D. en recherche théorique et comportementale, professeur et chercheur du cours de chimie de l’Institut d’éducation fondamentale, technique et technologique de l’Amapá (IFAP) et du Graduate Program in Professional and Technological Education (PROFEPT IFAP).
[6] Théologien, Docteur en psychanalyse, chercheur au Center for Research and Advanced Studies – CEPA.
[7] Biologiste, PhD en maladies topiques, professeur et chercheur du cours d’éducation physique, Université fédérale du Pará (UFPA).
[8] Biomédical, PhD en maladies topiques, professeur et chercheur du cours de médecine du campus de Macapá, Université fédérale d’Amapá (UNIFAP).
Publié: Février 2021
Approuvé : Février 2021