ARTICOLO ORIGINALE
FERREIRA, Fernanda Amorim [1], PARAÍBA, Isabella Maria Rios [2], ELIAS, Laíse de Souza [3]
FERREIRA, Fernanda Amorim. PARAÍBA, Isabella Maria Rios. ELIAS, Laíse de Souza. Effetto della melatonina sulla morfofisiologia cardiaca dei ratti indotta a iperlipidemia. Revista Científica Multidisciplinar Núcleo do Conhecimento. Anno 05, Ed. 10, Vol. 13, pp. 130-143. nell’ottobre 2020. ISSN: 2448-0959, Link di accesso: https://www.nucleodoconhecimento.com.br/nutrizione/effetto-della-melatonina
RIEPILOGO
Le iperlipidemie sono classificate come alterazioni metaboliche e sono correlate a malattie cardiovascolari, che evidenziano la malattia atertotica coronarica. Le malattie cardiovascolari hanno una notevole partecipazione ai tassi di mortalità in tutto il mondo e, di conseguenza, è stato l’obiettivo della ricerca che cerca l’innovazione terapeutica. La melatonina è un ormone prodotto in una fase ambientale di oscurità dalla ghiandola pineale che svolge, tra gli altri, una funzione antiossidante, i lipidica, antinfiammatoria, dimostrando così di essere una potente molecola nel trattamento delle malattie cardiovascolari. Pertanto, l’obiettivo di questo lavoro è valutare l’effetto della melatonina sullo stress ossidativo e sui parametri biochimici nei ratti indotti dall’iperlipidemia. Per questo, sono stati utilizzati 15 ratti albini maschi (Rattus norvegicus albinus), con 150 giorni di età, provenienti dal bioterio del dipartimento di morfologia e fisiologia animale dell’Università rurale federale di Pernambuco. Questi animali sono stati tenuti in gabbia, con alimentazione e acqua ad libitum, temperatura di 22 °C e illuminazione artificiale che stabilirà un fotoperiodo di 12 ore di luce e 12 ore di buio (ciclo invertito). In conclusione, studi hanno dimostrato che la melatonina ha effetti sulla riduzione della perossidazione lipidica, sui livelli di creatina chinasi (CK) e sulla riduzione della glutatione ridotta. Come farmaco economico e ben tollerato, la melatonina può essere una nuova opzione terapeutica per le malattie cardiovascolari e gli individui con iperlipidemia.
Parole chiave: Aterosclerosi, melatonina, cuore, iperlipidemia, stress ossidativo.
INTRODUZIONE
Le iperlipidemie sono alterazioni metaboliche che si verificano quando i livelli lipidici circolanti superano i limiti di normalità nel flusso sanguigno (BEVILACQUA et al., 2007). Questa produzione non regolamentata può causare gravi problemi, tra cui malattie cardiovascolari (CVD), come ipertensione, aterosclerosi, oltre a danni a diversi organi e tessuti, caratterizzando così un grave problema di salute pubblica (EMET et al., 2016).
I CVD hanno una notevole partecipazione ai tassi di mortalità in tutto il mondo e, di conseguenza, sono stati oggetto di ricerca che cerca innovazioni terapeutiche. (SIMKO et al., 2016). Così, negli ultimi decenni, la ricerca di nuovi farmaci per il trattamento dell’iperlipidemia ha valutato il ruolo delle sostanze che agiscono nel controllo dell’aumento del profilo lipidico e dell’infiammazione, oltre a proteggere l’endotelio vascolare dallo stress ossidativo (JOCKERS et al., 2016). Tra queste sostanze, la melatonina ha ricevuto molte ripercussioni sul trattamento delle lesioni in vari organi, tra cui il cuore (YANG et al., 2014).
La melatonina (N-acetil-5-metossitriptalina) (MEL) è un ormone neuroendocrino prodotto dalla ghiandola pineale (HARDELAND et al., 2006). La sua secrezione è regolata dal ciclo luce/oscurità ambientale attraverso il nucleo soprachiasmatico (SKENE et al., 2006). Da quando la sua biosintesi è iniziata di notte, dai fotorecettori retini che inviano segnale alla ghiandola pineale, stimolando la produzione e il rilascio di melatonina (GOOLEY et al., 2003). Il meccanismo d’azione del MEL dipende dai recettori a membrana chiamati MT1, MT2 e MT3, che si esprimono sia individualmente che insieme in vari tessuti e organi, i primi due sono espressi sia nel cuore che nell’arteria del ratto (CAHILL; GRACE; BESHARSE, 1991) (LI; ZHANG; TANG, 2013).
Presentando recettori ampiamente distribuiti dal corpo, mel può essere responsabile di una serie di eventi fisiologici (FARÍAS; ZEPEDA; CALAF, 2012). Inizialmente la sua funzione era limitata alla regolazione del ciclo sonno/veglia (SUN; HUANG; QU, 2015) tuttavia, nel corso degli anni sono state riportate anche altre funzioni, come il suo ruolo antiossidante e antinfiammatorio, nella regolazione del metabolismo lipidico e glucosio,(AGIL et al., 2011) (ESPINO; Pariente; RODRIGUEZ, 2011) e il suo effetto cardioprotettivo, avendo un ruolo importante sulle malattie cardiache (TAN et al., 1998), come lesioni da ischemia-riperfusione del miocardio, aterosclerosi, ipertensione e insufficienza cardiaca. (FAVERO et al., 2012) (BENOVA et al., 2013) (DOMINGUEZ; ABREU-GONZALEZ; REITER, 2014).
Studi su ratti hanno rilevato che MEL ha prodotto un effetto cardioprotettivo contro la cardiotossicità indotto da agenti chemioterapici e recentemente l’ampiezza dell’effetto protettivo cardiaco esercitato dal MEL (SUN; GUSDON, QU, 2016). Inoltre, la melatonina è stata trovata efficace nel ridurre gli effetti dell’ischemia indotta sul cuore dei ratti (YU et al., 2014), abbassando la frequenza cardiaca, riducendo i livelli di proteine della creatina chinasi, (FAVERO et al., 2016), conservazione della microstruttura cardiomiocita (LIN et al., 2018), riduzione delle aritmie cardiache e ossidazione lipidica derivante da processi ischemici cardiaci( TARE et al., 2014), oltre a migliorare la funzione cardiaca e il flusso sanguigno (ZHANG et al., 2017).
In considerazione del crescente aumento dell’iperlipidemia (KANG; KOH; LEE, 2011) e di conseguenza malattie cardiovascolari (HARDELAND, 2015) e che la melatonina svolge una funzione antiossidante, (PANDI-PERUMAL et al., 2013) (COMMENTZ; HELMKE, 1995), (REITER et al., 2013) antinfiammatorio e abbassamento lipidico (ALLEGRA et al., 2003), è necessario studiare l’efficacia dell’effetto della melatonina sulla morfofisiologia cardiaca nei ratti indotti dall’iperlipidemia. Pertanto, questa ricerca può contribuire allo sviluppo di metodi terapeutici complementari nel trattamento dell’iperlipidemia e delle malattie cardiovascolari. Il presente studio mirava a valutare l’effetto della melatonina sulla morfofisiologia cardiaca dei ratti indotti all’iperlipidemia.
1. MATERIALI E METODI
1.1 GRUPPI SPERIMENTALI
Abbiamo usato 15 ratti albini maschi (Rattus norvegicus albinus), 150 giorni, del bioterio del Dipartimento di Morfologia e Fisiologia Animale dell’Università Rurale Federale di Pernambuco. Questi animali sono stati tenuti in gabbie, con alimentazione e acqua ad libitum, temperatura di 22 °C e illuminazione artificiale che ha stabilito un fotoperiodo di 12 ore di luce e 12 ore di buio (ciclo invertito). Gli animali sono stati pesati e divisi casualmente in tre gruppi sperimentali: GC: ratti senza induzione di iperlipidemia; GI: ratti indotti all’iperlipidemia e trattati con placebo; GM: ratti indotti all’iperlipidemia e trattati con melatonina.
1.2 INDUZIONE DI IPERLIPIDEMIA
Per indurre l’iperlipidemia, Triton WR 1339 è stato somministrato per via intraperitoneale per trenta giorni, noto anche come tyloxapol, un detergente non anionico di struttura polimerica, ad una dose di 400mg/kg di peso corporeo, sciolto in NaCl allo 0,9%. Questa sostanza è stata utilizzata in studi sperimentali perché è in grado di causare iperlipidemia negli animali. Le analisi biochimiche sono state utilizzate per seguire l’iperlipidemia dopo il terzo giorno di induzione, secondo i kit labtest®, seguendo i cataloghi specificati: LDL, HDL, trigliceridi e colesterolo totale. Gli animali non indotti all’iperlipidemia (CG) hanno ricevuto dosi equivalenti di soluzione salina allo stesso modo.
1.3 SOMMINISTRAZIONE DI MELATONINA
La melatonina è stata somministrata per via orale (VO), quindi 10 mg/kg di melatonina sono stati sciolti in 200 microlitri di alcol. Poi, alle 7:00 del .m., questa soluzione è stata diluita nell’acqua potabile degli animali, vale la pena notare che le bottiglie sono state rivestite con un foglio di alluminio per proteggere il contenuto di luminosità.
1.4 ANALISI BIOCHIMICA
Campioni di sangue sono stati raccolti nei periodi precedenti l’induzione e dopo il trattamento. Per l’analisi prima del periodo di induzione, i ratti sono stati mobilitati dal contenimento meccanico e dal sangue raccolto dalla puntura caudale laterale con l’uso di catetere (24G). Per l’analisi dopo l’induzione e il suo rispettivo trattamento, il sangue è stato raccolto per puntura cardiaca. Il materiale è stato centrifugato, il sovrapprezzo confezionato in Eppendorf e tenuto in un congelatore a -20 °C fino al momento dei dosaggi. A tal fine è stato utilizzato il kit Labtest®, seguendo lo specifico catalogo: proteina CK (133-1/500).
1.5 ANALISI DELLO STRESS OSSIDATIVO: PEROSSIDAZIONE LIPIDICA E GLUTATIONE RIDOTTO
La perossidazione lipidica è stata stimata misurando i livelli di sostanze reattive dell’acido tiobarbiturico (TBARS), mentre la riduzione del glutatione (GSH) è stata determinata misurando gruppi di solfatidro non proteici. Per questo, frammenti del cuore sono stati macerati in KCl, 1,15% in una proporzione di 10 ml/1g fino alla completa omogeneizzazione del materiale raccolto. L’omogeneato è stato trasferito in una provetta, alla quale sono stati aggiunti 2 ml di reggente (0,375% acido tiobarbiturico e 75% acido tricloroacetico) a ciascun mL della miscela. I tubi duplicati sono stati sigillati e riscaldati in un bagno d’acqua (100 °C) per 15 minuti. L’overnum è stato separato e l’assorbanza misurata a 535 nm.
1.6 PROCEDURE ETICHE
L’esperimento è stato sviluppato in conformità con i principi etici nella sperimentazione animale, secondo la legge n. 11.794 dell’8 ottobre 2008, e il progetto è stato approvato dalla Commissione etica sull’uso degli animali (CEUA) dell’Università rurale federale di Pernambuco (UFRPE – numero di processo 23082.015842/2014) (ALLEGATO A).
1.7 ANALISI STATISTICA
Le analisi statistiche sono state effettuate utilizzando il metodo non parametrico Kruskal-Wallis, dove i mezzi sono stati confrontati con il test Wilcoxon-Mann Whitney, il 95% della significatività.
2. RISULTATI E DISCUSSIONE
Il danno ossidativo indotto nelle cellule e nei tessuti è stato correlato a processi fisiologici e all’eziologia di varie malattie, come l’invecchiamento, e malattie croniche come diabete, cancro e aterosclerosi, dove si osserva spesso l’aumento del contenuto delle più importanti specie reattive di ossigeno (EROs) nel contesto biologico (ROSEN et al., 2001) (HIGASSHI et al., 2014).
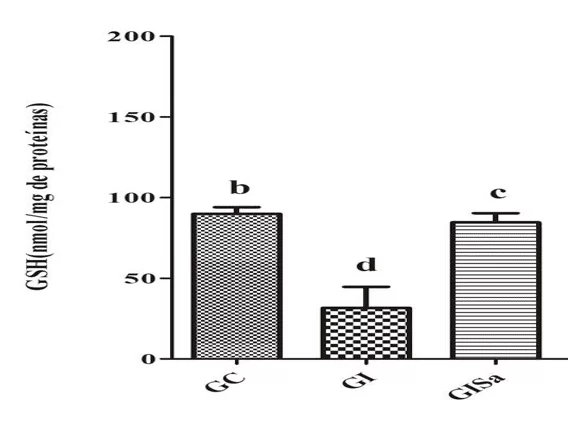
Le analisi dei livelli di TBARS nel tessuto cardiaco dopo aver indotto iperlipidemia hanno rivelato valori elevati rispetto al gruppo di controllo. Tuttavia, il trattamento con melatonina ha attenuato i livelli di TBAR, presentando valori simili al GC (Figura 1). L’analisi dei tessuti dei livelli di GSH nel gruppo indotto e trattato con melatonina era superiore a quella degli animali nel gruppo GI, mostrando anche valori simili a quelli del gruppo di controllo (Figura 2). Con ciò, ci siamo resi conto che la melatonina era in grado di ridurre il danno ossidativo.
Questo ormone ha la capacità di rapire specie reattive di ossigeno (EROs) e azoto (ERN), agendo per prevenire danni ossidativi (ALVES et al., 2014) oltre a stimolare l’espressione degli enzimi antiossidanti (PANDI-PERUMAL et al., 2013) attraverso la crescita dell’espressione del Keap1-Nrf2 (MANCHESTER et al., 2015).
ONK (2016) ha rilevato che l’uso di 20 mg/kg di melatonina ha comportato una diminuzione dei livelli di TBARS. Allo stesso modo, Debosree Ghosh (2015) ha dimostrato che la dose minima di 10 mg / kg di melatonina era necessaria per proteggere dall’aumento della perossidazione lipidica nei globuli rossi dei ratti.
Sono stati riportati numerosi studi che dimostrano l’effetto isolato della melatonina sulla promozione dei livelli di GSH, ad esempio, sono stati dimostrati livelli aumentati di GSH negli animali con danno epatico indotto dalla tioacetamide (TAA) e trattati con melatonina (10 mg/kg) Czechowska (2015) e Goc (2017), osservato alti livelli di GSH nel tessuto epatico di animali trattati con 10 mg/kg di MEL da solo o in combinazione con nitroprusside di sodio (SNP), un farmaco antipertensivo con effetti tossici, rispetto all’amministrazione isolata dell’SNP.
Nel nostro studio, il gruppo indotto all’iperlipidemia e trattato con melatonina, ha dimostrato una riduzione dei livelli di proteine Ck rispetto al gruppo iperlipidemico (GI), tuttavia, in relazione al gruppo di controllo, non è stata osservata alcuna alterazione significativa (tabella 1).
La creatina chinasi (CK) è un enzima che svolge un ruolo importante nella generazione di energia per il metabolismo muscolare. È presente prevalentemente nel tessuto muscolare, ma si trova anche nel tessuto cerebrale (BRANCACCIO et al., 2008). Tra le molecole utilizzate come marcatore di danno cardiaco, la creatina chinasi (CK) è spesso descritta come il miglior marcatore indiretto di danno al tessuto muscolare (FOSCHINI et al., 2017). Questa riduzione dei livelli di CK può essere attribuita agli effetti di stabilizzazione della membrana dati dal MEL. Studi in vitro dimostrano che la MEL è in grado di inibire l’internalizzazione della fosfatidilserina, dell’espressione di Bax e della xantina ossidasi, causando così la stabilizzazione del bistrato lipidico (KOCIC et al., 2017).
Ghaeli (2015), riferisce che nei pazienti con infarto del miocardio con sovralivellamento del segmento ST sottoposto all’intervento coronaico percutaneo primario, la somministrazione di melatonina più il trattamento standard hanno notevolmente diminuito il livello di creatina chinasi-MB. Inoltre, MEL ha ancora effetti antinfiammatori e anti-apoptotici, essendo così in grado di agire nel controllo delle malattie cardiovascolari (CHEN et al., 2016).
3. CONCLUSIONE
In conclusione, studi hanno dimostrato che la melatonina ha effetti sulla riduzione della perossidazione lipidica, sui livelli di creatina chinasi (CK) e sull’aumento della riduzione del glutatione nei ratti indotti dall’iperlipidemia.
RIFERIMENTI
AGIL, A, Navarro-Alarcon M, Ruiz R, et al. Beneficial effects of melatonin on obesity and lipid profile in young Zucker diabetic fatty rats. J Pineal Res 2011; 50:207–212.
ALLEGRA, M.; REITER, R. J.; TAN, D. X.; et al. The chemistry of melatonin’s interaction with species. J. Pineal Res., v.34, n.1, p. 1–10, 2003.
ALVES, R.S.C. et al. A melatonina e o sono em crianças. Pediatria. v. 1, p. 587-594,2004.
BRANCACCIO, P.; Maffulli, N.; Buonauro, R. Serum enzyme monitoring in sports medicine. Clin Sports Med 2008. 27:1-1.
BENOVA, T, Viczenczova C, Radosinska J, et al. Melatonin attenuates hypertension-related proarrhythmic myocardial maladaptation of connexin-43 and propensity of the heart to lethal arrhythmias. Can J Physiol Pharmacol 2013; 91:633–639.
BEVILACQUA, MR, GIMENO SGA, BEVILACQUA MR, Matsumura LK, et al. Hiperlipidemias e Fatores Dietéticos: Estudo Transversal Entre Nipo-Brasileiros. Arq Bras Endocrinol Metab. 2007 mar/out; 51/4: 547-558.
CAHILL, GM, Grace MS, Besharse JC. Rhythmic regulation of retinal melatonin: metabolic pathways, neurochemical mechanisms, and the ocular circadian clock. Cell Mol Neurobiol 1991; 11:529–560.
CHEN, S,J. et al. Melatonin enhances interleukin-10 expression and suppresses chemotaxis to inhibit inflammation in situ and reduce the severity of experimental autoimmune encephalomyelitis. Int Immunopharmacol. v.31, p.169-77, 2016.
COMMENTZ, J. C.; HELMKE, K. Precocious puberty and decreased melatonin1583 secretion due to a hypothalamic hamartoma. Horm.Res. v.44, n. 6, p. 271-275,1584 1995.
CZECHOWSKA, G. et al. Protective effects of melatonin against thioacetamide induced liver fibrosis in rats. J Physiol Pharmacol. v.66, p.567-79, 2015.
DEBOSREE Ghosh; Sudeshna Paul, Aindrila Chattopadhyay, Debasish Bandyopadhy. Melatonin and aqueous curry leaf extract in combination protects against lead induced oxidative stress mediated injury to rat heart: a new approach. Journal of Pharmacy Research 2015,9(12),618-634.
DOMINGUEZ -Rodriguez A, Abreu-Gonzalez P, Reiter RJ. The potential usefulness of serum melatonin level to predict heart failure in patients with hypertensive cardiomyopathy. Int J Cardiol 2014; 174:415–417.
EMET M, Ozcan H, Ozel L, Yayla M, Halici Z, Hacimuftuoglu A. A review of melatonin, its receptors and drugs. Eur J Med. 2016; 48(2):135-41.
ESPINO J, Pariente JA, Rodriguez AB. Role of melatonin on diabetes-related metabolic disorders. World J Diabetes 2011; 2:82–91.
FARIAS JG, Zepeda AB, Calaf GM. Melatonin protects the heart, lungs and kidneys from oxidative stress under intermittent hypobaric hypoxia in rats. Biol Res. 2012; 45(1):81-5.
FAVERO G, Rodella LF, Reiter RJ, et al. Melatonin and its atheroprotective effects: a review. Mol Cell Endocrinol 2014; 382:926–937.
FAVERO G, Franceschetti L, Buffoli B, Moghadasian MH, Reiter RJ, Rodella LF, et al. Melatonin: Protection against age-related cardiac pathology. Ag Res Rev. 2016; 22: S1568-1637. 16.
FOSCHINI D, Prestes J, Charro MA. Relação entre exercício físico, dano muscular e dor muscular de início tardio. Rev Bras Cineantropom Desempenho Hum 2007;9(1):101-6.
GHAELI P, Vejdani S, Ariamanesh A, et al. Effect of melatonin on cardiac injury after primary percutaneous coronary intervention: a randomized controlled trial. Iran J Pharm Res 2015; 14:851–855.
GOC, Z. et al. Protective effects of melatonin on the activity of SOD, CAT, GSH-Px and GSH content in organs of mice after administration of SNP. Chin J Physiol. v.1, p. 28-34 2017.
GOOLEY, JJ, Lu J, Fischer D, Saper CB. A broad role for melanopsin in nonvisual photoreception. J Neurosci 2003; 23:7093–7106.
HARDELAND, R, Pandi-Perumal SR, Cardinali DP. Melatonin. Int J Biochem Cell Biol. 2006; 38:313–316.
HARDELAND, R. Antioxidative protection by melatonin: multiplicity of mechanisms from radical detoxification to radical avoidance. Endocrine. v. 27, p. 111-118, 2015.
HIGASSHI; T Maruhashi, K Noma, Y Kihara Oxidative stress and endothelial dysfunction: Clinical evidence and therapeutic implications, Trends in Cardiovascular Medicine Volume 24, Issue 4, May 2014, Pages 165-169.
JOCKERS, R, Delagrange P, Dubocovich ML, Markus RP, Renault N, Tosini G, et al. Update on melatonin receptors: IUPHAR Review. Br J Pharmacology. 2016; 173:2702-25.
KANG, J. W.; KOH, E. J.; LEE, S. M. Melatonin protects liver against ischemia and reperfusion injury through inhibition of toll-like receptor signaling pathway. J Pineal Res. v.50, p. 403-411, 2011.
KOCIC, G., Tomovic, K., Kocic, H., et al., 2017. Antioxidative, membrane protective and antiapoptotic effects of melatonin, in silico study of physico-chemical profile and efficiency of nanoliposome delivery compared to betaine. RSC Adv. 7, 1271–1281.
LI, X.; ZHANG, M.; TANG, W. Effects of melatonin on streptozotocin-induced retina neuronal apoptosis in high blood glucose rat. Neurochem Res. v.38, p.669- 76, 2013.
LIN, X, Zhao T, Lin CH et al. Melatonin provides protection against heat strokeinduced myocardial injury in male rats. J Pharm Pharmacol. 2018 Jun;70(6):760-767.
MANCHESTER LC, et al. Melatonin: an ancient molecule that makes oxygen metabolically tolerable. J Pineal Res. v.59, p. 403-19, 2015
ONK D, et al. Melatonin Attenuates Contrast-Induced Nephropathy in Diabetic Rats: The Role of Interleukin-33 and Oxidative Stress. Mediators Inflamm. v.2016, p. 508-28, 2016.
PANDI-PERUMAL, S. R. et al. Melatonin antioxidative defense: therapeutical implications for aging and neurodegenerative processes. Neurotox Res. v.23, p.267-300, 2013.
REITER, R. J. et al. Melatonin as an antioxidant: biochemical mechanisms and pathophysiological implications in humans – Acta Biochim. Pol.v. 50, p. 1129-1146, 2003.
RODRIGUEZ C, et al. Regulation of antioxidant enzymes: a significant role for melatonin. J Pineal Res. 2004;36(1):1–9.
ROSEN, P P Nawroth, G King, W Möller, H J Tritschler, L Packer. The role of oxidative stress in the onset and progression of diabetes and its complications: a summary of a Congress Series sponsored by UNESCO-MCBN, the American Diabetes Association and the German Diabetes Society – May-Jun 2001;17(3):189-212.
SIMKO F, Baka T, Paulis L, Reiter RJ. Elevated heart rate and non dripping heart rate as potential targets for melatonin: a review. J Pineal Res. 2016; 61:127-37.
SKENE, DJ, Arendt J. Human circadian rhythms: physiological and therapeutic relevance of light and melatonin. Ann Clin Biochem. 2006; 43:344–353.
SUN H, Huang FF, Qu S. Melatonin: a potential intervention for hepatic steatosis. Lipids Health Dis. 2015; 14:75.
SUN H, Gusdon AM, Qu S. Effects of melatonin on cardiovascular diseases: progress in the past year. Curr Opin Lipidol. 2016; 27(4):408-13.
TAN DX, Manchester LC, Reiter RJ, et al. Ischemia/reperfusion-induced arrhythmias in the isolated rat heart: prevention by melatonin. J Pineal Res. 1998; 25:184–191.
TARE M, Parkington HC, Wallace EM et al. Maternal melatonin administration mitigates coronary stiffness and endothelial dysfunction, and improves heart resiliência to insult in growth restricted lambs. 2014
YANG Y, Sun Y, Yi W, Li Y, Fan C, Xin Z, et al. A review of melatonin as a suitable antioxidant against myocardial ischemia-reperfusion injury and clinical heart diseases. J Pineal Res. 2014;57(4):357-66. doi: 10.1111/jpi.12175.
YU L, Sun Y, Cheng L, Jin Z, Yang Y, Zhai M, et al. Melatonin receptor mediated protection against myocardial ischemia/reperfusion injury: role of SIRT1. J Pineal Res. 2014; 57(2):228-38.
ZHANG, Y. et al. Melatonin protects against arsenic trioxide-induced liver injury by the upregulation of Nrf2 expression through the activation of PI3K/AKT pathway. Oncotarget. 2017.
ALLEGATO
Figura 1: Valutazione dei livelli di TBARS (nmol / mg di proteina) nel tessuto cardiaco degli animali nei diversi gruppi sperimentali) * I mezzi seguiti dalla stessa lettera non differiscono in modo significativo dal test Kruskal-Wallis con il test post-hoc di Dunn (p < 0,05). CG: controllo; GI: indotto a iperlipidemia; GIM: indotto a iperlipidemia e trattato con melatonina.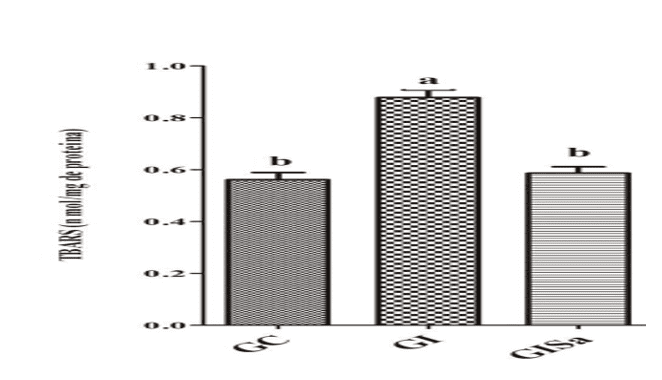
Figura 2. Valutazione dei livelli di GSH (nmol / mg di proteina) nel tessuto cardiaco degli animali nei diversi gruppi sperimentali) * I mezzi seguiti dalla stessa lettera non differiscono in modo significativo dal test di Kruskal-Wallis con il test post-hoc di Dunn (p < 0,05). CG: controllo; GI: indotto a iperlipidemia; GIM: indotto a iperlipidemia e trattato con melatonina.
Tabella 1: Analisi biochimica dei gruppi sperimentali [1] Laureato in Nutrizione presso il Centro Universitario Uninassau.
[1] Laureato in Nutrizione presso il Centro Universitario Uninassau.
[2] Studente magistrale in Nutrizione comunitaria e sanità pubblica presso FCNAUP Laureato in Nutrizione presso il Centro Universitario Di Uninassau.
[3] Consulente di orientamento. Dottorato di ricerca in Bioscienze Animali. Laurea magistrale in Bioscienze Animali. Specializzazione in Morfologia. Laurea in Scienze Biologiche.
Inviato: agosto, 2020.
Approvato: ottobre 2020.