REVUE INTÉGRATIVE
SILVA, Poliane Cardoso da [1], MORAIS, Lauandecy Maria Domingas Costa de [2], LEAL, Kamila Soares [3]
SILVA, Poliane Cardoso da. MORAIS, Lauandecy Maria Domingas Costa de. LEAL, Kamila Soares. Les répercussions de l’édition génétique chez l’homme par la technique «CRISPR-CAS9». Revista Científica Multidisciplinar Núcleo do Conhecimento. An 06, Ed. 09, Vol. 05, p. 85 à 107. Septembre 2021. ISSN: 2448-0959, Lien d’accès: https://www.nucleodoconhecimento.com.br/droit/technique-crispr-cas9
RÉSUMÉ
L’édition génétique par le biais du système CRISPR-Cas9 a permis des avancées majeures dans le domaine du génie génétique, y compris la capacité de modifier génétiquement des embryons humains ayant un potentiel de reproduction, ce qui s’est récemment produit en Chine. Ainsi, de nombreuses controverses surgissent sur le sujet qui soulève des dilemmes scientifiques, éthiques et juridiques, un problème qui a conduit la présente étude avec la question suivante: Quelles sont les principales répercussions scientifiques, éthiques et juridiques découlant de l’édition génétique chez l’homme grâce à l’application de la technique CRISPR-Cas9? Ainsi, l’objectif était d’étudier ces impacts afin de tisser les réflexions appropriées sur le sujet dans le scénario actuel, en considérant la protection du patrimoine génétique due au principe de dignité de la personne humaine. Nous avons également cherché à aborder ces aspects de manière interdisciplinaire, afin d’élever le droit selon des perspectives anthropocentriques. Pour mener à bien l’étude, nous avons utilisé des recherches théoriques et bibliographiques intégratives et documentaires, opérationnalisées par la recherche d’articles académiques dans des indexeurs nationaux et internationaux, des sites officiels de consultation de la législation, ainsi que des livres mis à jour, disponibles dans l’environnement physique et numérique. Il a été obtenu que le système CRISPR-Cas9 est extrêmement prometteur compte tenu de ses applications pour la thérapie génique, cependant, l’application de l’édition de gènes dans les cellules reproductrices humaines est au milieu d’incertitudes scientifiques avec des résultats inattendus, tels que le mosaïcisme et les mutations aléatoires; en ce qui concerne les questions normatives, le patrimoine génétique est protégé aux niveaux national et international en ce qui concerne les cellules embryonnaires humaines, car l’ADN humain est considéré comme un bien inhérent à l’humanité et aucun changement n’est transmis aux générations futures; en ce qui concerne les implications éthiques, la modification de la composition naturelle de l’être humain signifie la rupture d’une limite qui nuit au principe d’autodétermination de l’individu, tout en permettant d’entrevoir des pratiques eugéniques et d’accroître la ségrégation sociale. Il est conclu que les possibilités apportées par l’édition génétique à travers la technique explorée sont inévitables et, par conséquent, il appartient au système juridique de chercher à se mettre à jour sur sa prédiction, ces mises à jour devraient, avant tout, tenir compte des principes éthiques qui guident la bioéthique et le biodroit. Il est souligné que des recherches plus concluantes devraient guider de telles interventions.
Mots-clés : Édition génétique, Répercussions, Dignité de la personne humaine.
1. INTRODUCTION
La découverte de moyens plus pratiques pour l’édition génétique chez l’homme a provoqué une grande fanfare dans l’environnement scientifique, principalement en raison de l’annonce de la naissance des premiers humains génétiquement modifiés, un fait qui s’est produit en Chine, grâce à l’utilisation de la technique « CRISPR-Cas9 » – Clustered Regulary Interepaced Short Palindromic Repeats, le terme fait référence aux fragments du ruban d’ADN.
L’édition génétique de la technique CRISPR-Cas9 provient de l’application des fonctions exercées par une véritable machinerie observable au niveau moléculaire, où les segments d’ADN sont modifiés, selon Amabis et Martho (2010) L’ADN est la structure qui porte toutes les informations héréditaires des organismes vivants simples ou pluricellulaires, sa structure en double hélice est composée de milliers de nucléotides joints séquentiellement dont les suivis forment les gènes , les endroits qui indiquent l’expression des caractéristiques de chaque individu, par exemple, la couleur des yeux, la forme du visage, peuvent même avoir des anomalies qui s’expriment dans les maladies héréditaires.
Ainsi, maîtriser la manipulation génétique signifie contrôler l’expression du génotype et du phénotype des organismes, c’est-à-dire leur composition génétique et son extériorisation. Il est substantiel d’annoncer que les premiers résultats avec CRISPR-Cas9 sont prometteurs compte tenu des possibilités offertes par la thérapie génique (ORMON et al., 2017).
Cependant, il est nécessaire de souligner les divergences présentes dans l’environnement scientifique, car il n’y a pas de consensus concernant de telles manipulations, puisque certaines études ont indiqué des effets secondaires susceptibles d’entraîner des pertes telles que des mutations nocives dans d’autres gènes, l’apparition de cancers et d’autres changements non mesurés, ajoutant à cela le fait que les changements définitifs dans l’ADN ont un impact sur les générations futures dans leurs dimensions biologiques et sociales (CLEMENTE, 2020).
Dans la conjoncture actuelle, les incertitudes scientifiques conduisent à des dilemmes éthiques et juridiques concernant le thème, compte tenu des principes qui guident la bioéthique et le biodroit. En ce qui concerne la législation nationale, il existe la réglementation des activités de génie génétique, à travers la loi sur la biosécurité (n ° 11.105/2005), ce dispositif scelle les pratiques d’interventions génétiques impliquant des cellules germinales et des embryons humains (BRASIL, 2005). De même, il existe une protection internationale du patrimoine génétique, par le biais de dispositifs visant à la protection universelle du matériel génétique en tant qu’unité fondamentale appartenant aux êtres humains (UNESCO, 1997).
Dans ce contexte, la présente étude visait à étudier d’une certaine manière les principales répercussions scientifiques, éthiques et juridiques de l’édition génétique chez l’homme à travers la technique CRISPR-Cas9, afin de tisser les réflexions nécessaires sur le sujet dans le scénario actuel, en considérant la protection du patrimoine génétique due au principe de dignité de la personne humaine. Nous avons également cherché à aborder ces aspects de manière interdisciplinaire, afin d’élever le droit selon des perspectives anthropocentriques.
La présente étude est d’une grande importance pour l’environnement académique et social car elle cherche à mieux connaître les nuances impliquées dans un thème controversé, actuellement d’une grande répercussion pour le biodroit et les domaines connexes, comme il convient à un thème multidisciplinaire. C’est un sujet impliquant les droits de l’homme et les droits fondamentaux, tels que la dignité de la personne humaine face à des innovations technologiques caractérisées par des mécanismes de plus en plus présents dans le monde postmoderne et qui, par conséquent, constituent les faits générateurs du droit actuel et futur, dont le dynamisme exige une attention maximale et une délibération constante.
Pour mener à bien l’étude, nous avons utilisé des recherches théoriques et bibliographiques intégratives et documentaires, opérationnalisées par la recherche d’articles académiques dans des indexeurs nationaux et internationaux, des sites officiels de consultation de la législation, ainsi que des livres mis à jour, disponibles dans l’environnement physique et numérique.
Ce travail suit une organisation présentant comme résultats et discussions les axes thématiques suivants : l’édition génétique ; technique CRISPR-Cas9; la protection du patrimoine génétique humain; les limites scientifiques de la technique CRISPR-Cas9 chez l’homme et les implications éthiques entourant ladite technique, enfin la dernière section apporte les considérations générales comme un produit des investigations menées.
2. DÉVELOPPEMENT
2.1 L’ÉDITION GÉNÉTIQUE
Le génie génétique permet l’édition du matériel génétique humain par le transfert de séquences génétiques qui seront recombinées avec d’autres segments d’ADN, une activité qui nécessite un contrôle et une régulation appropriés afin d’éviter les risques pour la vie humaine, car le principe de la dignité humaine est respecté (MALUF, 2020, p. 59).
Les pratiques de modification de l’organisme par l’édition génomique impliquent une amélioration de celui-ci, lui donnant des caractéristiques souhaitables, comme l’a déclaré Scarmanhã; Silva et Garé:
A engenharia genética realiza processos de manipulações genéticas, objetivando que elementos sejam duplicados, transferidos ou mesmo isolados dos genes originais. Assim, com estes procedimentos, é possível obter seres com genética melhorada com qualidade e aprimoramento de funções (SCARMANHÃ; SILVA; GARÉ, 2019, p. 05).
Dans cette dimension, les applications du génie génétique peuvent être réalisées dans n’importe quel organisme animal ou humain, ce que Clemente (2020) assure, dans la mesure où les applications de l’édition génétique sont initialement limitées aux cellules somatiques, c’est-à-dire aux cellules non germinales, qui sont présentes dans la majeure partie du corps humain et diffèrent et se spécialisent dans divers tissus et organes, tandis que les cellules gamétiques sont essentielles à la reproduction d’un nouvel être. En résumé, les changements dans les cellules germinales peuvent être transmis aux générations futures, au contraire, les changements dans les cellules somatiques ne restent que chez les individus qui les ont dans leur composition.
Compte tenu de ces possibilités, le caractère dynamique des sciences qui tend toujours à progresser, avec le génie génétique ne s’est pas produit différemment, dit Beriam (2017) que encore en 2015 a commencé à intensifier les débats sur l’altération génétique des cellules germinales humaines, ou l’édition génétique des ovules, des spermatozoïdes et des embryons (ovules fécondés), il y avait donc la possibilité de manipuler le matériel génétique des embryons humains.
En ce qui concerne l’édition génétique chez l’homme, la législation nationale tend à interdire les pratiques connexes, par le biais de la loi sur la biosécurité, qui établit des normes pour l’utilisation des techniques de génie génétique et la dissémination d’organismes génétiquement modifiés – OGM dans l’environnement (BRASIL, 2005).
Il existe une interdiction d’altération génétique dans les cellules embryonnaires ou germinales des êtres humains, en lisant l’article 8 du dispositif susmentionné, d’autres interdictions concernant la manipulation impliquant des cellules germinales sont notées:
Art. 6º Fica proibido:
I – Implementação de projeto relativo a OGM sem a manutenção de registro de seu acompanhamento individual;
II – Engenharia genética em organismo vivo ou o manejo in vitro de ADN/ARN natural ou recombinante, realizado em desacordo com as normas previstas nesta Lei;
III – engenharia genética em célula germinal humana, zigoto humano e embrião humano;
IV – Clonagem humana; (…) (BRASIL, 2005).
Il convient de noter que la loi susmentionnée considère l’application du génie génétique dans l’édition de cellules germinales humaines comme un crime, prévoyant à l’article 24 qu’un tel comportement, ainsi que tout acte de violation du matériel génétique humain in vivo qui ne vise pas à l’inversion des défauts génétiques et qui est en dehors des diktats légaux, entraînera une peine de détention de 1 (un) à 3 (trois) ans et une amende, le clonage humain et l’utilisation d’embryons humains sont également pénalisés en désaccord avec les prévisions légales :
Art. 24. Utilizar embrião humano em desacordo com o que dispõe o art. 5º desta Lei:
Pena – detenção, de 1 (um) a 3 (três) anos, e multa.
Art. 25. Praticar engenharia genética em célula germinal humana, zigoto humano ou embrião humano:
Pena – reclusão, de 1 (um) a 4 (quatro) anos, e multa.
Art. 26. Realizar clonagem humana:
Pena – reclusão, de 2 (dois) a 5 (cinco) anos, e multa.
Art. 27. Liberar ou descartar OGM no meio ambiente, em desacordo com as normas estabelecidas pela CTNBio e pelos órgãos e entidades de registro e fiscalização:
Pena – reclusão, de 1 (um) a 4 (quatro) anos, e multa. (BRASIL, 2005).
Il reste clarifié la position de la loi réglementant les activités liées à l’altération génétique des organismes, cela est autorisé chez d’autres êtres vivants non humains et dans les cellules humaines non embryonnaires ou reproductrices. D’autre part, la biotechnologie moderne développe des procédures de manipulation génétique plus controversées et révolutionnaires (REIS; OLIVEIRA, 2019).
Toujours selon les auteurs, parmi les techniques révolutionnaires issues des innovations biotechnologiques, plus particulièrement dans le domaine du génie génétique se distingue la technique d’édition de gènes appelée CRISPR-Cas9, qui permet de remplacer des segments dans la bande d’ADN en corrigeant d’éventuelles erreurs ou défauts génétiques en insérant des caractéristiques souhaitées ou plus bénéfiques. Cette possibilité éveille à une réflexion sur les risques découlant de la manipulation de l’être humain suivant ses intérêts, comme la possibilité de pratiques eugéniques (REIS ; OLIVEIRA, 2019).
2.2 LA TECHNIQUE CRISPR-CAS-9
Selon Sander et Joung (2014), le système CRISPR-Cas9 a émergé de l’ingénierie moléculaire du système immunitaire des bactéries, ce qui permet l’édition de n’importe quel gène par fragmentation de l’ADN par une enzyme de restriction appelée « Cas9 », qui est dirigée par un ARN transporteur, et a la capacité de s’apparier avec des séquences de bases azotées spécifiques.
Corroborant la même compréhension ci-dessus, Boel et al., (2016) a comparé la technique à un éditeur de texte, en partant du point où l’ADN est du code écrit, et comme tout autre peut présenter des erreurs dans sa structure, ainsi que les outils d’identification des erreurs écrites, la technique reconnaît des séquences nucléotidiques spécifiques dans l’ADN cible, ainsi que des supports de coupure pour les sélectionner.La figure 3 illustre comment le mécanisme d’édition génétique se déroule à travers le système CRISPR-Cas9.
Figure 3 : système CRISPR – Cas9
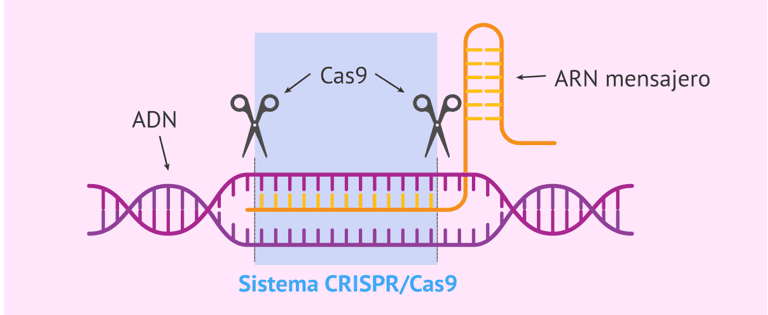
Dans ce contexte, Clemente se réfère à deux moments principaux du mécanisme d’édition mentionné ici, à savoir, le stade de reconnaissance et de clivage où la molécule d’ADN est coupée, suivi de la phase de réparation de l’ADN:
O processo de edição divide-se em duas etapas, sendo a primeira relacionada ao reconhecimento e clivagem da molécula de DNA e, a segunda, destinada ao reparo da mesma. Uma vez seccionados, os nucleotídeos são acionados mecanismo celulares endógenos, naturais de reparação do DNA. O processo de edição utiliza-se então, desses recursos, para promover modificações pretendidas. Assim, o reparo pode ocorrer por ligação das extremidades não homólogas (mecanismo útil quando se pretende silenciar a ação dos genes) ou também, por reparo dirigido por moldes. Nessa situação, é possível inserir, nas moléculas, juntamente com a ferramenta de edição, moldes de DNA externo. Assim, pode-se fornecer moldes externos contendo genes selecionados, ao novo seguimento de DNA a ser formado no local da clivagem (CLEMENTE, 2020, p. 15).
Il est entendu que la cellule a des mécanismes de réparation internes qui sont activés par l’action du système CRISPR-Cas9, où elle utilise de tels moyens pour provoquer des changements d’intérêt, ces changements peuvent se produire à partir d’un moule inséré dans le processus ou par l’utilisation des extrémités déjà présentes dans la bande d’ADN.
La technique discutée ici a été prometteuse en raison de sa simplicité, de sa rapidité et de son efficacité dans la manipulation génétique, comme l’indique Clemente (2020), les avantages de cette technique représentent une véritable révolution dans les traitements de santé, en particulier en ce qui concerne les maladies graves d’origine héréditaire, qui sont souvent incurables. Par conséquent, une attente positive est générée par rapport aux nouvelles alternatives thérapeutiques.
Les applications de l’édition de gènes chez l’homme offrent de nombreux avantages allant de la recherche plus fondamentale à la recherche plus avancée, permettant plusieurs améliorations pour l’homme, parmi les innovations peuvent être citées: la compréhension de la différenciation cellulaire dans le processus de développement du corps humain, le fonctionnement de gènes particuliers encore dans la phase embryonnaire de l’organisme, la compréhension des maladies d’origine génétique, fournir la production de médicaments spécifiques tels que les pathologies, les progrès de la thérapie génique (traitement du cancer), entre autres mécanismes qui sont encore en phase d’étude (CLEMENTE 2020).
Toujours en ce qui concerne les applications, il convient de mettre l’accent sur l’édition génétique des nouveau-nés conditions de malformation congénitale héréditaire, au moins 6% des nouveau-nés présentent de graves problèmes génétiques, grâce au mécanisme CRISPR-Cas9 identifie les segments d’ADN qui sont responsables de ces pathologies, il est donc possible de rechercher des traitements préventifs (CLEMENTE, 2020).
Les avantages s’appliquent toujours à la physiologie du système immunitaire. De nombreux gènes sont directement liés à la résistance de certains individus aux agents pathogènes infectieux, l’identification de ces sites dans le génome signifie étendre leurs avantages à d’autres organismes et favoriser une immunisation efficace. Il est souligné que de telles procédures sont déjà une réalité (ORMOND et al., 2017).
2.3 LA PROTECTION DU PATRIMÔMNIO GÉNÉTIQUE
Les progrès biotechnologiques augmentent et gagnent de plus en plus d’espace, ce qui en déduit la nécessité de promouvoir une protection efficace du génome humain, visant à la préservation des générations futures (NAVES; GOIATÁ, 2017).
Cette protection repose sur des thèmes complexes, car de nombreux conflits surgissent, des intérêts économiques aux discussions éthiques philosophiques et religieuses, mais la large capacité humaine à appliquer des moyens technologiques pour la modification des systèmes biologiques exige un contrôle approprié basé sur « la réglementation et l’établissement de mesures concrètes de préservation par l’utilisation appropriée et consciente des ressources biologiques » (NASCIMENTO; BRITO, 2021, p. 5).
Le patrimoine génétique correspond à toute « information d’origine génétique d’espèces végétales, animales, microbiennes ou autres, y compris les substances dérivées du métabolisme de ces êtres vivants » (BRASIL, 2015), ce concept a été adopté par la loi 13 123 de mai 2015, qui réglemente la disposition constitutionnelle sur la préservation de l’intégrité du patrimoine génétique, ainsi que les mesures de protection et d’accès au patrimoine génétique, établies dans la Convention sur la diversité biologique qui a été proposée unilatéralement aux nations lors de la Conférence des Nations Unies sur l’environnement et le développement en 1992.
Ainsi, le patrimoine génétique est toute unité héréditaire présente dans les organismes monocellulaires ou pluricellulaires, ainsi que dans les substances résultant de leurs activités métaboliques. Par conséquent, leur protection repose sur les gènes animaux, les plantes de micro-organismes et les humains. Toutefois, les droits et obligations prévus par la loi sur l’accès au patrimoine génétique ne s’appliquent pas au matériel humain, tel que décrit à l’article 4.
Ainsi, cette règle n’inclut pas les règles concernant l’accès au patrimoine génétique humain. Ceci est justifié par les lignes directrices et les interdictions apportées par la loi sur la biosécurité, dont les interdictions se concentrent sur les comportements impliquant l’altération de cellules embryonnaires, le clonage et toute modification du matériel génétique in vivo en désaccord avec les normes actuelles (BRASIL, 2005).
Il convient de souligner les interdictions de se concentrer sur la modification ou la manipulation des cellules embryonnaires, c’est-à-dire des cellules reproductrices, mais il existe une lacune concernant l’application de techniques de modification génétique dans les cellules somatiques, qui, par le processus de mitose, diffèrent pour former des tissus et d’autres organes humains. C’est subtilement subtilement dans les normes et les normes réglementaires qu’ils peuvent être soumis à des processus d’altération des gènes.
En fait, jusqu’à quelques années, il n’y avait pas de normes réglementaires relatives à de tels mécanismes, mais l’Agence nationale de surveillance de la santé – Anvisa, réglementée en 2018, par le biais du RDC n ° 260, les règles pour l’essai clinique de produits de thérapies expérimentales avancées, y compris la thérapie génique, selon Anvisa (2018), cela a comme produit biologique ADN ou ARN recombinant visant à la modification de l’expression génétique à cette fin traitement, traitement préventif ou diagnostique. »
Par conséquent, la thérapie génique effectuée dans des cellules humaines non reproductrices est devenue manipulable, mais le but est exclusivement médical, une thérapie qui implique un traitement ou une prévention.
Dans ce contexte, il est souligné que la norme réglementait de telles procédures à des niveaux expérimentaux « expérimentaux » étant, selon Anvisa elle-même (2018) « dans le but de prouver l’innocuité et l’efficacité ». Cependant, en 2020, la même agence a enregistré la première thérapie génique au Brésil pour le traitement de l’amyotrophie spinale – AME (NOVARTIS, 2020).
Étant donné que les applications biotechnologiques imprègnent tous les groupes et royaumes d’organismes vivants, le sujet est orienté vers la protection du matériel génétique humain, qui fait l’objet d’une protection nationale par le biais de la sécurité susmentionnée et des normes internationales par le biais du système de protection des droits de l’homme.
Les droits de l’homme sont envisagés en fonction de leurs dimensions de protection, d’une manière simple, nous parlons de droits de première dimension qui protègent les libertés individuelles, de droits de deuxième dimension dont la protection relève des droits sociaux et de la troisième dimension relative aux droits trans-individuels, mais une quatrième dimension a prévu les droits relatifs aux questions de biotechnologie, le génie génétique et ses implications éthiques et juridiques malgré la conservation de la vie humaine (GORCZEVSKI, 2009).
Les droits de l’homme de la quatrième génération et leur réglementation sont apparus en raison des nouveaux problèmes découlant des progrès technologiques et scientifiques, qui n’avaient pas été rencontrés jusque-là, mais ils étaient parfaitement prévisibles, en particulier ceux qui sont pertinents pour la recherche sur le génome humain et sa manipulation (NETO, 1998).
Ainsi, anticipant les implications des progrès scientifiques et technologiques en matière de manipulation génétique, la 29e Conférence générale de l’UNESCO a adopté en 1997 le document proposé par le Comité international de bioéthique, qui a été conçu comme la « Déclaration universelle du génome humain et des droits de l’homme ».
La Déclaration universelle du génome humain et des droits de l’homme visait à mettre l’accent sur la dignité de la personne humaine face à la recherche liée à l’intervention génétique, les droits des personnes subissant un traitement ou un diagnostic qui affectent leur génome et à établir les limites à respecter par les nations qui effectuent de telles recherches. Dans ce contexte, la lettre indique que « le génome humain sous-tend l’unité fondamentale de tous les membres de la famille humaine ainsi que la reconnaissance de sa dignité et de sa diversité inhérentes » (UNESCO, 1997).
Ainsi, la protection du patrimoine génétique proposée par l’UNESCO prévoit la protection de l’individualité humaine, ce qui est conforme aux aspects scientifiques de l’ADN, puisque le matériel génétique est universellement composé de la même structure moléculaire et remplit les mêmes fonctions physiologiques, mais il s’agit d’un code unique et exclusif pour chaque individu. Même s’il transporte des informations de ses ascendants, il fonctionne comme un texte, décrivant les caractéristiques physiques de chaque individu. C’est ce qui relie toute la famille humaine, tout en conférant l’originalité de chaque personne, comme une empreinte digitale.
Ainsi, le dispositif reconnaît que le contenu génétique de chaque personne est un patrimoine appartenant à toute l’humanité, dont la diversité doit être respectée et reconnue, sinon il viole le principe de la dignité de la personne humaine, qui gouverne chaque nation sur la base d’un régime démocratique. En ce sens, Naves et Goiatá (2017, p. 03) conviennent que « la protection des données génétiques humaines est la protection du patrimoine génétique lui-même et la continuité de l’espèce dans des conditions dignes ».
Corroborant la disposition légale susmentionnée, elle échappe à toute discrimination due à la composition génétique d’une personne donnée, de sorte qu’une telle violation cause une atteinte aux droits de l’homme et aux autres libertés fondamentales (UNESCO, 1997).
Dans cette dimension, le Brésil, en harmonie avec les dispositions de protection internationale du génome, la lettre magna CF/88, en son article 225 §1er alinéa II, a confié aux pouvoirs publics le devoir de « préserver la diversité et l’intégrité du patrimoine génétique. du pays et superviser les entités dédiées à la recherche et à la manipulation du matériel génétique » (BRASIL, 1988), la disposition légale susmentionnée a cependant été réglementée avec la promulgation de la loi sur la biosécurité, qui réglemente les normes de sécurité et les activités d’instruments d’inspection impliquant organismes génétiquement modifiés – OGM et leurs dérivés, et crée le Conseil National de Biosécurité – CNBS, ainsi que la restructuration de la Commission Technique Nationale de Biosécurité – CTNBio, prévoit la Politique Nationale de Biosécurité – PNB (BRASIL, 2005).
2.4 LIMITES DE L’ÉDITION GÉNÉTIQUE CHEZ L’HOMME À PARTIR DE LA TECHNIQUE CRISPR-CAS9
La protection du patrimoine génétique est très valable pour faire les prédictions appropriées à travers les perspectives de la biotechnologie et du génie génétique, des mécanismes les plus archaïques de l’édition génomique aux plus modernes et les plus efficaces, ouvert une fenêtre pour un avenir de grandes découvertes et la capacité d’améliorer la vie sur terre.
Cependant, il faut se rendre compte qu’une telle fenêtre est une arme à double tranchant, car l’homme peut utiliser les ressources scientifiques au profit de l’environnement et de la santé humaine, c’est aussi dans son plan l’alternative de les appliquer uniquement pour des intérêts économiques, sans mesurer les impacts.
Il est encore nécessaire de vérifier le fait qu’il existe encore un contrôle total de l’opérationnalisation et des résultats de certaines techniques, comme observé dans le cas de l’utilisation du mécanisme CRISPR-Cas9.
En ce sens, les possibilités découlant des progrès biotechnologiques ont révolutionné la façon de considérer les gènes, en particulier en ce qui concerne les aspects scientifiques et économiques, compte tenu de l’expansion des études et de la valorisation du contenu génétique, désormais reconnu comme un élément fondamental des progrès biotechnologiques (NASCIMENTO; BRITO, 2021).
Bien que la technique d’édition génétique du mécanisme CRISPR-Cas9 se soit avérée rapide, efficace et économique, la littérature rapporte certaines limites, ce qui implique naturellement des risques, ou des effets secondaires.
Par conséquent, dans le contexte scientifique à partir duquel émergent les expériences et les études, il y a la présentation de résultats controversés concernant les interventions en relation avec le matériel génétique.
Il est souligné que dans le domaine scientifique, il existe deux types de controverses, qui sont internes, découlant de questions non concluantes, incomplètes ou trop complexes; externes, liées à des préoccupations, des jugements de valeur, des croyances, des conceptions religieuses, philosophiques, culturelles ou éthiques (HODSON, 2018). Cette dimension traite des résultats non concluants ou imparfaits, qui sont liés aux incertitudes des expériences scientifiques, ainsi que de leurs impacts, en particulier en ce qui concerne l’édition génétique chez l’homme.
Selon Thompson et al., (2019) certains dans des expériences avec des embryons soumis à l’édition génétique se sont produits ce que l’on peut appeler un mosaïcisme qui résulte d’une erreur dans la découpe du suivi d’intérêt, une telle erreur peut résulter de deux possibilités, une coupe infructueuse par nucléase (Cas9 qui effectue un clivage), ou due à une réparation incorrecte de celui-ci. Le résultat est l’apparition d’au moins trois types de cellules, qui sont, avec le matériel génétique d’origine, celles modifiées avec des mutations et celles qui ont été correctement modifiées, c’est-à-dire que l’organisme commence à avoir une composition génétique contenant différents ensembles d’ADN.
Dans ce contexte, cet effet est lié à un patchwork ou à une mosaïque, faisant allusion à la « fragmentation génomique » de l’organisme. Il est important de souligner la présence de mutations dans les cellules où les réparations ne se sont pas produites, il est important que la plupart des mutations soient des sélétérias, c’est-à-dire qu’elles conduisent à des déficiences congénitales d’origine génétique, telles que plusieurs syndromes.
Il est souligné que si le mosaïcisme peut ou non se produire l’expression de gènes indésirables, cependant, une fois présent dans la composition de l’individu, il est possible qu’il soit transféré aux générations futures (CLEMENTE, 2020).
Un autre facteur qui nécessite de la prudence et une grande prudence est la possibilité de modificationsaléatoires « off-tarfegt », sont des mutations accidentelles où l’enzyme manque la cible de coupe, se produisant par un événement non déterminé dans Cas9, ce qui conduit à des actions atypiques et involontaires (MARTI-GUITIERREZ et al., 2017).
Devant l’exposé Ormond et al. (2017) soutiennent que de tels incidents sont minimes compte tenu de la capacité de la technique à guérir une multitude de maladies, dont les effets négatifs sont certains et dévastateurs. Et pourtant, l’émergence de résultats imprévus n’est pas une règle, puisque l’ADN lui-même est capable de résister à un certain niveau de mutations.
Il en déduit que les manipulations génétiques dans l’ADN humain n’ont pas présenté de résultats avec une certitude à cent pour cent sur l’application de la technique CRISPR-Cas9, qui peut entraîner des dommages tels que des mutations nocives dans d’autres gènes et d’autres changements non mesurés, car la science elle-même ne connaît pas la totalité des effets de l’expression des gènes.
Cependant, Ormom et al. (2017) affirment qu’en ce qui concerne l’édition de gènes in vitro ne devrait pas être la cible d’obstacles, à condition qu’elle soit liée à des protocoles éthiques, juridiques et de sécurité, tels que l’autorisation du donneur et une supervision appropriée. Il est tout à fait approprié de financer publiquement de telles recherches.
En ce qui concerne la poursuite des applications techniques dans les lignées germinales humaines ayant un potentiel de reproduction, au moins quatre points devraient être pris en considération, à savoir : « a) une justification médicale convaincante, b) une base de données probantes à l’appui de son utilisation clinique, c) une justification éthique et d) un processus public transparent pour demander et intégrer les contributions des parties prenantes » (ORMON et al., 2017, p. 01).
L’auteur conclut que, compte tenu des questions scientifiques pour lesquelles aucune réponse n’a encore été obtenue, l’édition de gènes de la lignée embryonnaire humaine ayant une capacité de reproduction ne devrait pas être effectuée, de telles pratiques sont totalement inadéquates (ORMON et al., 2017).
La situation inverse s’est produite en Chine en 2015, où un groupe de chercheurs sous la supervision du scientifique Junjiu Huang de l’Université Sun Yat-sen a mené des études sur des embryons humains en utilisant la technique CRISPR-Cas9, visant à corriger une mutation présente dans le gène HBB, dont la fonction est de coder la protéine bêta-globine (LIANG et al., 2015).
La plus controversée est survenue en 2018 avec l’annonce de la naissance des jumelles Lulu et Naná, les premiers humains génétiquement modifiés, où le scientifique Jiankui He a utilisé le mécanisme CRISPR-Cas9 pour modifier les gènes CCR5, rendre les enfants immunisés contre le virus VIH (CÁRDENAS-KRENZ, 2018).
Selon les médias, le scientifique a été condamné par la justice chinoise, lorsqu’il a assumé la programmation génétique d’un autre enfant, donc, même sans règles prohibitives en ce qui concerne l’édition génétique des humains, mais compte tenu du dégoût social, le chercheur a été condamné à 3 ans de prison (JUNQUEIRA, 2019).
Sur de telles controverses, il n’y a pas d’autres informations, la Chine est une nation extrêmement fermée. Par conséquent, il n’y a pas d’études ou de nouvelles sur la façon dont ces enfants sont, ni sur la façon dont le troisième bébé est, s’il a survécu ou présenté une anomalie.
2.5 IMPLICATIONS ÉTHIQUES CONCERNANT L’ÉDITION GÉNÉTIQUE CHEZ L’HOMME
En ce qui concerne les implications éthiques, l’échec / les limitations / les échecs ou même l’application réussie de l’édition génomique à partir de CRISPR-Cas9, génèrent des répercussions (ORMON et al., 2017). Dans ce scénario, Sandel (2013, p. 84) met en garde contre l’existence inévitable de dilemmes et de controverses, car il y a des progrès technologiques et scientifiques, mais l’évolution de la société ne se produit pas au même rythme.
Quant aux aspects négatifs, il est considéré entre l’exposition des individus à des interventions à potentiel nocif face à l’incertitude de tels risques surmontant les bénéfices, comme c’est le cas dans le cas de l’édition d’embryons humains, dont les effets seront encore déterminés (ORMON et al., 2017).
Un point crucial dans le débat éthique se réfère à l’autonomie des individus, même face au succès de la technique, selon Ormon et al., (2017) cette technologie a des incidences majeures en générant un être génétiquement modifié sans leur consentement.
À ce stade, il serait nécessaire de considérer que les parents sont les personnes les plus appropriées pour décider de la vie de leurs enfants, mais c’est un sujet controversé, car il se réfère à la composition génétique de quelqu’un, un être individuel qui exprimera ses caractéristiques génotypiques et vivra avec eux pour toujours.
Dans cette dimension Hayden (2016), affirme que les parents, y compris, exercent déjà un contrôle immense sur leurs enfants, comme la possibilité d’un dépistage génétique pendant les soins prénataux, où il est possible de vérifier l’apparition d’anomalies dans l’ADN comme c’est le cas de la trisomie 21 – syndrome de Down, et aussi en ce qui concerne le choix de prendre ou non une grossesse jusqu’à la fin, comme dans certains pays.
Dans ce contexte, le nombre de mouvements opposés à ce contrôle a augmenté, comme ceux qui considèrent la conception elle-même comme un acte immoral, pour faire naître quelqu’un qui n’a jamais demandé à naître, selon Benatar (2015, p. 60), le principal défenseur de l’idée, la procréation peut sembler quelque chose d’innocent, mais elle est en réalité très nuisible, car un enfant né est la cible de tous les maux et des choses terribles qui peuvent arriver, Bien que tout le monde ne souffrira pas de grandes horreurs, personne n’est à l’abri de dommages graves, la meilleure façon de protéger un enfant des choses terribles de la vie est de ne pas les avoir.
À cela s’ajoute le fait qu’il existe des rapports d’individus qui, même s’ils ont des maladies génétiques rares et « désavantageuses » telles que l’albinisme et le nnisme, déclarent qu’ils ne voudraient pas que leur contenu génétique soit modifié pour devenir des personnes normales (HAYDEN, 2016).
Il y a aussi la possibilité d’intervenir en choisissant des gènes qui expriment des conditions pathologiques, comme l’affirme Sandel (2013, p. 86), l’auteur rapporte le cas d’un couple de femmes sourdes, qui par la procréation assistée a permis la conception d’un enfant également sourd, un tel intérêt consistait dans la défense que la surdité ne serait pas une condition préventive d’une vie comme une autre. En fait, l’enfant est né avec la surdité.
Il reste un grand dilemme concernant les limites de l’édition génétique pour le traitement des conditions considérées comme anormales par le bon sens, selon Haydem (2016), de nombreuses personnes sourdes ne considèrent pas leur état comme une maladie ou une carence, refusant même des interventions telles que l’implant cocloto et empêchent également leurs enfants également sourds d’être soumis à des traitements.
Corroborant, Lamphier et al. (2015) souligne qu’en plus des risques liés à l’eugénisme, il existe des problèmes liés à d’éventuels dommages à la lignée humaine elle-même, puisque l’altération du matériel génétique implique le transfert héréditaire de caractéristiques, cela signifie la modification irréversible d’un être humain et de ses descendants.
En outre, Habermas (2016) ajoute de la préoccupation à la compréhension éthique de soi de l’espèce, c’est-à-dire les aspects subjectifs et existentiels de la personne qui a été génétiquement modifiée sous le jugement d’autrui.
L’auteur susmentionné s’est consacré à soulever la question et à entourer la violation de l’autodétermination des individus, malgré la certitude claire qu’un embryon n’a pas de caractère volontaire, qu’il est en plein développement et qu’il deviendra un être doté de valeurs, de désirs et inversement, selon les mêmes termes, cette intervention eugénique « limite la configuration autonome de la vie de l’individu et sape les relations fondamentalement symétriques entre les personnes libres et égales » (HABERMAS, 2016, p. 15).
Il y a un conflit clair et remarquable dans ce processus biotechnologique avec le caractère propice de la bioéthique, parmi lesquels on peut mentionner, le principe d’autonomie, selon Maluf (2020, p. 155) est lié à la capacité d’auto-gouvernance des individus. L’interférence dans les gènes d’embryons aptes à la reproduction signifierait, dans les limites éthiques et légales brésiliennes, la violation de ce principe.
Un autre principe « dans la ligne de mire » de l’édition génétique est la dignité même de la personne humaine, pour Maluf (2020, p.155) ceci en harmonie avec le principe du caractère sacré, ils prévoient la protection de la vie humaine dans toute sa dimension.
Dans ce point d’accord, il est important de discuter de la controverse entourant l’émergence de la personnalité, qui, selon Venosa (2007, p. 230) dans le système juridique brésilien, est utile pour élever les droits de chaque individu, sur ce thème rayonner des divergences autour de l’enfant à naître.
Cette controverse persiste en raison de la lecture apportée par l’article 2 du Code civil de 2002, où il stipule que la personnalité d’une personne commence par la naissance avec la vie, mais la loi défend les droits de l’enfant à naître (BRASIL, 2002). Sur ces points, il est souligné qu’il s’agit de droits dans la sphère civile, alors que la loi sauve tout droit de l’enfant à naître.
Cependant, la définition de l’enfant à naître ne correspond pas à ce qui n’est encore qu’un embryon, car le fait d’être conçu et non né correspond à l’embryon après nidation, c’est-à-dire après fixation dans la paroi interne de l’utérus. Ainsi, il n’est pas question de droits embryonnaires, cependant, Tartuce (2015) souligne l’importance d’une législation abritant la prédiction sur de telles technologies.
Dans ce chemin de réglage, Cervi se demande :
(…) diante das inovações biotecnológicas de edição genética embrionária, seria possível promover uma interpretação acerca de intimidade e identidade e dos direitos da personalidade em um momento até mesmo anterior ao nascimento com vida, ou antes, à própria consideração de ser o embrião nascituro? (CERVI, 2019, p. 13).
Au milieu d’un tel écart, l’auteur défend un recadrage des dispositions légales selon les inéluctables exigences modernes afin de protéger le principe consacré de la dignité humaine (CERVI, 2019).
On en déduit que les valeurs éthiques et culturelles sont liées à chaque peuple et nation, tandis que l’essence humaine et la composition humaine sont unies, en ce sens, Rodotá (2010) induit sur la possibilité d’éditer des embryons humains qui reçoivent un corps physique conçu selon la détermination de quelqu’un rabaisse contre les droits de l’homme.
2.5.1 QUESTIONS LIÉES À EUGENIA
L’aperçu et l’enchantement devant les perspectives de guérison de l’édition génétique deviennent une préoccupation, même au vu des interférences possibles visant des intérêts louches, basés sur des aspects culturels, considérant que le contrôle de la technique est utilisé dans le choix des caractéristiques physiques, telles que la taille, la couleur des yeux, les cheveux, la forme du visage, etc. (CERVI, 2019).
Ainsi, les préoccupations se tournent vers les risques des pratiques eugéniques, considérant l’intérêt de l’être humain ici qui est beau et éloigné de l’anormal ou du laid, pour Cervi (2019) le désir de beauté et de jeunesse a toujours accompagné l’homme, en étant la preuve, son besoin d’exprimer la perfection dans les œuvres d’art, ainsi que est vérifié dans les récits littéraires lorsqu’il décrit les caractéristiques de personnages jeunes et attrayants.
De manière simple, l’eugénisme consiste à sélectionner des individus à partir de leurs caractéristiques génétiques afin d’améliorer les descendants qui naîtront. En ce qui concerne l’édition génétique, Ormon et al. (2017) met en garde contre la possibilité qu’il soit utilisé pour la sélection de caractéristiques qui vont au-delà des intérêts thérapeutiques.
Pour Bobbio (2016), le concept développé en Angleterre au XIXe siècle, est associé aux théories de l’hérédité des biologiques raciaux et à l’interprétation subversive de la sélection naturelle proposée par Charles Darwin, selon laquelle le plus adapté survit, c’est-à-dire celui qui a les meilleures caractéristiques génétiques survivra. Selon l’endoctrinateur, de telles théories sont à l’origine de pratiques appliquées à tort dans des contextes politiques racistes: où la purification raciale était prêchée.
En fonction de cette observation, Ormon et al., (2017) à tous égards, l’eugénisme est une pratique dangereuse, renforçant les préjugés découlant de la définition de ce qui serait normal, ou acceptable dans la société, comme cela s’est produit historiquement, l’amélioration de l’ADN humain, sans l’objectif thérapeutique associé à une détermination génétique, qui, soutenue par l’État, a généré des conséquences désastreuses.
Par conséquent, l’amélioration génétique ne devrait jamais être utilisée pour renforcer le préjugé des stéréotypes, en particulier en sachant ce que la croyance en la suprématie d’une race peut causer, comme cela s’est produit dans l’Allemagne nazie, où l’on croyait que la race aryenne pour être supérieure aux autres devrait dominer, à cet égard Cervi (2019, p.05) déclare « la revendication du nettoyage ethnique et de la promotion de la race pure et de la beauté aryenne, a généré à son revers, beaucoup de tristesse, d’exclusion, de misère et de mort, ainsi que des sentiments de honte.
Ainsi, la possibilité de pratiques eugéniques suscite des inquiétudes quant à une éventuelle sélection d’individus et à leurs caractéristiques en tant que modèle déterminant, ce qui générerait une perte de diversité humaine.
2.5.2 IMPLICATIONS SOCIALES
Dans les impasses éthiques de l’édition génétique humaine, il convient de discuter brièvement des implications sociales dans le scénario possible d’individus dont les caractéristiques ont été préalablement choisies et déterminées artificiellement.
Notifiéement, la technique est limitée aux protocoles qui empêchent son application, mais dans une réalité possible dans laquelle sa mise en œuvre est réglementée, Ormon et al. (2017) avertissent que les conséquences sociales sont l’un des points les plus importants, compte tenu du succès car il est susceptible de rendre encore plus grandes les inégalités sociales déjà rencontrées aujourd’hui.
Il est souligné que même les procédures de santé légèrement plus complexes sont souvent limitées à ceux qui peuvent avoir de bonnes quantités, comme la procréation assistée, selon Cervi (2019) les procédures biotechnologiques d’application dans le domaine de la santé sont possibles pour un petit groupe de personnes, et il n’y a aucune perspective autour d’un large accès aux meilleures thérapies curatives.
C’est donc la question de Singer (2017, p.135) « qu’arrivera-t-il à ceux qui n’ont pas d’argent pour aller au supermarché génétique ? Vos enfants seront-ils prédestinés à la médiocrité ? »
Certes, chaque personne cherche le meilleur pour elle-même et pour la sienne, on sait que l’être humain ne mesure pas les efforts pour rechercher ce qui lui donne qualité de vie et sécurité. Ce qui semblait autrefois utopique aujourd’hui n’est pas si loin, mais pour ce qui est déjà marginalisé, l’avenir reste lourd d’incertitudes.
Selon Singer (2017) dans cette logique, le marché des gènes pourrait favoriser ceux qui ont un plus grand pouvoir d’achat pour insérer dans la lignée génétique de leurs descendants des gènes codant des caractéristiques pouvant favoriser l’intelligence, l’aptitude à la pratique de certains sports, entre autres (SINGER, 2017). L’auteur cite également l’exclusion de la « loterie génétique » pour désigner les impacts possibles causés par le choix artificiel de qualités souhaitables.
3. CONSIDÉRATIONS FINALES
La présente étude visait à apporter une approche interdisciplinaire marquant les principales répercussions scientifiques, éthiques, philosophiques et juridiques apportées par l’édition génétique chez l’homme à partir de la technique Crispr-Cas9, un tel mécanisme biotechnologique du génie génétique a ouvert de nouveaux précédents en ce qui concerne le traitement et la lutte des pathologies humaines jusqu’alors considérées comme insurmontables. Ainsi, il le voit comme une technologie inévitable dans la postmodernité.
Cependant, un univers de possibilités découle de l’application de la manipulation génétique à travers le système CRISPR-Cas9, qui a alerté la communauté scientifique, car il s’avère efficace, accessible et rapide, mais les expériences apportent encore d’autres résultats non concluants face à d’éventuelles erreurs dans les performances de l’outil, qui peuvent aboutir à des effets imprévisibles et délétères pour l’organisme.
Il s’intéresse également à l’utilisation d’objectifs louches tels que l’amélioration génétique humaine, une pratique réfutée avec véhémence pour susciter des idéaux eugénistes, qui dans le passé ont conduit à de véritables catastrophes sous la justification de la croyance en des races supérieures.
Considérant la difficulté évidente de l’être humain à obéir aux limites nécessaires à l’utilisation équilibrée des ressources environnementales, en visant un environnement écologiquement équilibré. On s’inquiète de l’inégalité sociale qu’une technique d’une telle ampleur peut causer, car de telles procédures seront certainement exhaustivement coûteuses, conduisant à une plus grande ségrégation entre les humains dont les parents ont été en mesure de payer pour les caractéristiques génétiques souhaitables et les prédispositions par rapport aux humains conçus dans le cadre de la loterie génétique.
Parmi les questions liées à la protection juridique qui gravitent autour du thème, on trouve que la composition génétique de chaque individu est un patrimoine de toute la famille humaine, telle que prévue par les organisations de protection internationale, qui la considèrent comme un bien inviolable, essentiel au maintien du principe de dignité de la personne humaine, et ne peut jamais être utilisé à des fins ségrégationnistes.
La protection du patrimoine génétique est également projetée au niveau national, afin d’interdire toute manipulation impliquant du matériel génétique humain, comme les procédures impliquant le clonage et les embryons humains. Il est interprété que l’interdiction incombe aux techniques d’édition liées au système CRISPR-Cas9. Il convient de mentionner la récente réglementation de la thérapie génique au niveau expérimental, dont la responsabilité réglementaire incombe à l’Agence nationale de surveillance de la santé – Anvisa.
Face à l’avenir avec l’amélioration inévitable et l’amélioration des mécanismes biotechnologiques, il reste un besoin juco-normatif concernant de telles pratiques, en se concentrant sur les considérations de la bioéthique, comme une question qui cherche à établir les moyens corrects pour l’application des procédures impliquant l’environnement et la santé humaine, en consolidant de plus en plus le biodroit et les principes qui le régissent.
RÉFÉRENCES
AGÊNCIA NACIONAL DE VIGILÂNCIA SANITÁRIA – ANVISA. Resolução da Diretoria Colegiada – RDC Nº 260, de 21 de Dezembro de 2018. Dispõe sobre as regras para a realização de ensaios clínicos com produto de terapia avançada investigacional no Brasil, e dá outras providências. Disponível em:< https://www.in.gov.br/materia/-/asset_publisher/Kujrw0TZC2Mb/content/id/57218930/do1-2018-12-28-resolucao-da-diretoria-colegiada-rdc-n-260-de-21-de-dezembro-de-2018-57218634> Acesso em 17 jun 2021.
AMABIS, J. M.; MARTHO, G. R. Biologia das células. v. 1. São Paulo: Moderna, 2010.
BOBBIO, N. Dicionário de Política. Brasília: Universidade de Brasília, 2016.
BRASIL. Constituição da República Federativa do Brasil de 1988. Disponível em: < http://www.planalto.gov.br/ccivil_03/Constituicao/Constituicao.htm>. Acesso em 28 jan 2021.
BRASIL. Lei Nº 11.105, de 24 de Março de 2005. Disponível em:< http://www.planalto.gov.br/ccivil_03/_Ato2004-2006/2005/Lei/L11105.htm>. Acesso em 28 jan 2021.
BRASIL. Lei nº 13.123, de 20 de maio de 2015. Regulamenta o inciso II do § 1º e o § 4º do art. 225 da Constituição Federal, o Artigo 1, a alínea j do Artigo 8, a alínea c do Artigo 10, o Artigo 15 e os §§ 3º e 4º do Artigo 16 da Convenção sobre Diversidade Biológica, promulgada pelo Decreto nº 2.519, de 16 de março de 1998; dispõe sobre o acesso ao patrimônio genético, sobre a proteção e o acesso ao conhecimento tradicional associado e sobre a repartição de benefícios para conservação e uso sustentável da biodiversidade; revoga a Medida Provisória nº 2.186-16, de 23 de agosto de 2001; e dá outras providências. Brasília, 20 de maio de 2015. Disponível em:< http://www.planalto.gov.br/ccivil_03/_ato2015-2018/2015/lei/l13123.htm> Acesso em 16 jun 2021.
BRITO, N. B. V., Nascimento, S. M. C. Herança da vida: reflexões ético-jurídicas acerca do Patrimônio Genético. Brasil, Editora Dialética, 2021.
BOEL, Annekatrien et al. BATCH-GE: Batch analysis of Next-Generation Sequencing data for genome editing assessment. Scientific reports, v. 6, n. 1, p. 1-10, 2016. Disponível em:< https://www.nature.com/articles/srep30330>. Acesso em 01 jun 2021.
CERVI, T. M. D. Dorian Gray Na Moldura Do Século Xxi: Reflexões Jurídicas Em Edição Genética Embrionária. RJLB, Ano 5 (2019), nº 3. Disponível em:< http://www.cidp.pt/revistas/rjlb/2019/3/2019_03_1703_1721.pdf> Acesso em 19 jun 2021.
CLEMENTE, G. T. Avanços e desafios na edição gênica em seres humanos. In NICOLETI, C. E. et al. Biodireito, Bioética e Filosofia em Debate. Almedina, São Paulo. 2020.
Conferência Geral da Organização das Nações Unidas para a Educação, Ciência e Cultura (UNESCO) 29.ª sessão. Declaração Universal do Genoma Humano e dos Direitos Humanos. 11 de novembro de 1997.
GORCZEVSKI, C. Direitos humanos, educação e cidadania: conhecer, educar, praticar. Santa Cruz do Sul: Edunisc, p. 16, 2009.
HABERMAS, J. O futuro da natureza humana. Tradução de Karina Jannini. 2ª ed. São Paulo: WMF Martins Fontes, 2016.
HAYDEN, C. E. Should you edit your children’s genes?. Nature News, v. 530, n. 7591, p. 402, 2016.
HODSON, D. Realçando p papel da ética e da política educação científica. In: Dália Melissa Conrado, Nei Nunes-Neto. Questões sociocientíficas: fundamentos, propostas de ensino e perspectivas para ações sociopolíticas. Brasil, Editora da Universidade Federal da Bahia, 2018.
JUNQUEIRA, D. China confirma o nascimento de terceiro bebê geneticamente modificado. Olhar Digital. Disponível em:< https://olhardigital.com.br/2019/12/31/ciencia-e-espaco/china-confirma-nascimento-de-terceiro-bebe-geneticamente-modificado/> Acesso em 19 jun 2021.
LAMPHIER, E. et al. Don’t edit the human germ line. Nature, v. 519, p. 410-411, mar. 2015. Disponível em:< https://www.nature.com/news/don-t-edit-the-human-germ-line-1.17111> Acesso em: 03 de mai 2021.
MALUF, A. C. R. F.D. Curso de bioética e biodireito. 3ª ed. Atlas. São Paulo. 2015.
NAVES, B. T. O.; GOIATÁ, S. R. Direitos Humanos, patrimônio genético e dados genéticos humanos: crítica à doutrina dos dados genéticos como interesse difuso. Revista de bioética y derecho, n. 40, p. 63-81, 2017.
NETO, F. V. L. Direitos humanos de 4ª Geração. DHNET, 1998. Disponível em < http://www.dhnet.org.br/direitos/textos/geracaodh/4_geracao.html> Acesso em 22 de mai de 2021.
NOVARTIS. Aprovado o registro da primeira terapia gênica para AME no Brasil. 18 Agosto 2020. Disponível em:< https://www.novartis.com.br/news/aprovado-o-registro-da-primeira-terapia-genica-para-ame-no-brasil> acesso em 17 jun 2021.
ORMOND, K. E. et al. Human germline genome editing. The American Journal of Human Genetics, v. 101, n. 2, p. 167-176, 2017.
REIS, É. V. B.; OLIVEIRA, B. T. Crispr-Cas9, Biossegurança E Bioética Uma Análise Jusfilosófica-Ambiental da Engenharia Genética. Veredas do Direito: Direito Ambiental e Desenvolvimento Sustentável, v. 16, n. 34, p. 123-152, 2019.
RODOTÁ, Stefano. La vida y las reglas: entre el derecho y el no derecho. Traduzido por Andrea Greppi. Madrid: Edi-torial Trotta, 2010.
SCARMANHÃ, B. O. S. G. SILVA, M. F. GARÉ, C. C. T. Os avanços biotecnológicos e da engenharia genética: sob a perspectiva da reprodução humana assistida e seus reflexos no direito de família. RJLB, Ano 5 (2019). Disponível em:< http://www.cidp.pt/revistas/rjlb/2019/3/2019_03_0259_0279.pdf> Acesso em 11 jun 2021.
SANDEL, M. Contra a perfeição: ética na era da engenharia genética. Rio de Janeiro: Civilização Brasileira, 2013.
SANDER, J. D.; JOUNG, J. Keith. CRISPR-Cas systems for editing, regulating and targeting genomes. Nature biotechnology, v. 32, n. 4, p. 347, 2014.
SINGER, P. Ética no mundo real: 82 breves ensaios sobre coisas realmente importantes. Traduzido por Desidério Murcho. Lisboa: Edições 70, 2017.
TARTUCE, F. Manual de Direito Civil. Vol. Único. 5ª Edição. Editora Método. São Paulo. 2015.
THOMPSON, Deborah J. et al. Genetic predisposition to mosaic Y chromosome loss in blood. Nature, v. 575, n. 7784, p. 652-657, 2019. Disponível em:< https://www.nature.com/articles/s41586-019-1765-3> Acesso em: 18 jun 2021.
VENOSA, S. S. Direito Civil-Parte Geral. 7 ed. São Paulo (SP): Atlas, 2007.
VILLAR, L. P. Empieza el primer proyecto de modificación genética de embriones humanos. Reproducción Asistida ORG. 2020. Disponível em: <https://www.reproduccionasistida.org/autorizacion-de-modificacion-de-embriones/> Acesso em: Acesso em 11 jun 2021.
[1] Académique du cours de baccalauréat en droit. ORCID: https://orcid.org/0000-0002-0096-7153
[2] Baccalauréat en droit. ORCID: https://orcid.org/0000-0001-7902-079X
[3] Conseiller d’orientation.
Soumis: Septembre, 2021.
Approbation : Septembre, 2021.


