ARTÍCULO ORIGINAL
RIBEIRO, Eliane de Oliveira Aranha [1], TABAL, Gabriella Bezerra [2], SOARES, Keuly Sousa [3], PRESTES, Gimol Benchimol Resende [4], SALINO, Alessandra Valle [5], QUEIRÓZ, Ana Karoline de Souza [6]
RIBEIRO, Eliane de Oliveira Aranha. Et al. Características Enfoque dental en el síndrome de Alagille: Reporte de caso. Revista Científica Multidisciplinar Núcleo do Conhecimento. Año 06, Ed. 03, Vol. 16, pp. 158-170. Marzo de 2021. ISSN: 2448-0959, Enlace de acceso: https://www.nucleodoconhecimento.com.br/odontologia-es/enfoque-dental
RESUMEN
El síndrome de Alagille (SA) es una enfermedad autosómica dominante, multisémica, compleja y poco frecuente con gran variación en la penetrancia de las características clínicas. Describir estas características, hallazgos orales y tratamiento dental de un paciente con SA, haciendo hincapié en la atención a adoptar, era el objetivo de este informe. Una paciente de 31 años asistió a la Clínica Dental de Pacientes Especiales de la Universidad Estatal de Amazonas (UEA) para recibir atención dental de rutina. En la anamnesis informó presentar el SA, ser trasplantado hígado y usar como medicamento Tacrolimus (Prograf®) continuamente. En el examen físico, se observó una piel ligeramente amarillenta, frente y nariz prominentes, y se observó exophthalmia pequeña. En el examen clínico intra-oral, se observó dentición amarillenta, presencia de reposo radicular de los 36 y cálculo dental en la región de los molares superior e inferior. El tratamiento propuesto y ejecutado fue exodontia, raspado supragingival, profilaxis y orientación de higiene bucal. El tratamiento dental ambulatorio se puede realizar en pacientes con SA, siempre que se observen las peculiaridades del síndrome. El papel del dentista en la promoción de la salud bucal es relevante, con el fin de evitar la presencia de focos infecciosos, especialmente en pacientes inmunosupresores.
Palabras clave: Síndrome de Alagille, características clínicas, tratamiento dental.
INTRODUCCIÓN
El síndrome de Alagille (SA) es una enfermedad autosómica dominante, multisímica y compleja con gran variación en la penetrancia de las características clínicas (MITCHELL et al., 2018). Afecta poco frecuentemente a 1 de cada 30/50.000 nacidos vivos y fue descrito por primera vez en 1970 basándose en hallazgos clínicos hepáticos, cardíacos y faciales, entre otros (GILBERT et al., 2019).
Según Sousa y Resende (2018), los cinco signos principales son: colestasa crónica (ictericia temporal, persistente o intermitente; picazón a partir de los 6 meses; xantomas en las áreas de fricción cutánea); facy dismórfico (frente saliente; ojos hundidos con hipertelorismo discreto; barbilla puntiaguda; nariz aplanada con punta en forma de bombilla); anomalías cardiovasculares (esnoosis de rama periférica de la arteria pulmonar, presente en el 90% de los casos, con o sin asociación con anomalías complejas); defectos de los arcos vertebrales (vértebras en el ala de mariposa); y el embrio posterior (signo presente en el 10% de la población general, consiste en el engrosamiento de la línea formada por membrana descemet y el ángulo de la cámara anterior del ojo, evidente por lámpara de hendidura o por gonioscopia). Se dice que está completo cuando hay presencia simultánea de al menos cuatro signos, mientras que la presencia de sólo tres de ellos caracteriza el síndrome como incompleto. Las enzimas alcalina fosfatasa y gamma-glutamiltransferasa (Gama GT o GGT) son muy altas en la mayoría de los casos.
Otros hallazgos clínicos menos frecuentes en el síndrome también fueron presentados por Alagille et al. (1987), como el hipogonadismo, el acortamiento de las falanges distales, la artritis poliarticular deformante, el retraso del crecimiento, el retraso mental, la insuficiencia renal (mesangiolipidosis, acidosis tubular renal, nefrocalcinosis) y el volumen y tono alterados de la voz.
El diagnóstico puede ser difícil debido a la expresividad variable de las manifestaciones clínicas (GUEGAN et al., 2012). Una gran parte de los pacientes afectados por el síndrome no tienen antecedentes familiares, lo que refuerza la característica de la penetrancia incompleta, además de la posibilidad de una nueva mutación genética (SOUSA; RESENDE, 2018). El pronóstico de la enfermedad y el riesgo de mortalidad dependen de la gravedad de la afectación de los órganos. La mortalidad temprana generalmente es causada por enfermedades cardíacas o enfermedades hepáticas graves y la mortalidad posterior a menudo es causada por accidentes cerebrovasculares (SALEH et al., 2016).
Con respecto a los rasgos faciales hay rasgos dismórficos leves pero reconocibles, incluyendo frente prominente, ojos profundos con hipertelorismo moderado, fisuras palpebrales oblicuas ascendentes, puente nasal deprimido, nariz recta con punta bulbosa, orejas grandes, mandíbula prominente y barbilla puntiaguda. En algunos niños, la forma de la cara es notablemente triangular. La frente prominente parece menos obvia en el adulto, mientras que la protuberancia de la mandíbula y la barbilla puntiaguda son más obvias. Se consideró que el fenotipo facial difiere en relación con si los ojos están cerrados o no. Aquellos que no tienen ojos profundos generalmente tienen fisuras de palpebral oblicua ascendentes estrechas, con notable hipertelorismo (CIOCCA; ÁLVAREZ, 2012).
En cuanto a la cavidad oral, los principales efectos se deben a disfunciones hepáticas: hipoplasia de esmalte, pigmentación dental debido a acumulación de bilirrubina, retraso generalizado en erupción, mayor susceptibilidad al desarrollo de caries, entre otros (SHEEHY et al., 2000; LIN et al., 2003; AMARAL et al., 2008).
La gravedad de este síndrome varía de individuo a otro, y puede presentar síntomas leves a la necesidad de trasplante hepático (TORRES et al. 2006).
La SA puede conducir a una enfermedad hepática terminal, que requiere tratamiento a través del trasplante de hígado. En el trasplante, la mayor complicación es la posibilidad de rechazo. Una de las principales causas de esto, además de la incompatibilidad tisular, es la infección pre y postoperatoria. La cavidad oral tiene bacterias patógenas que pueden producir bacteremia con el potencial de causar infecciones en otros órganos del cuerpo (AL-MUTAWA, 2002). Demostrar la relevancia del seguimiento y la preservación de la salud bucal de estos pacientes.
Por ello, el presente estudio pretende describir las características clínicas de esta patología, sus hallazgos orales y el tratamiento dental de un paciente con SA, destacando la atención a adoptar.
CASO CLÍNICO
Paciente A.C.C.S.F. 31 años, mujer de género, melanodermia, natural y procedente de Manaus-AM, asistió a la Clínica Dental de Pacientes Especiales de la Universidad Estatal de Amazonas (UEA) para recibir atención dental de rutina.
En la anamnesis informó presentar SA, ser trasplantado hígado, utilizando como medicamento Tacrolimus (Prograf®), medicamentos inmunosupresores que inhiben la activación de linfocitos T, y que hace uso de este fármaco desde el trasplante. Informó que tenía un “diente molesto”.
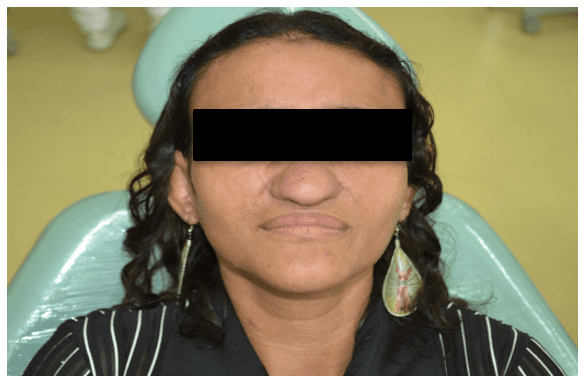
En el examen físico, se observó una piel, frente y nariz prominentes ligeramente amarillentas y una exophthalemia pequeña (Figura 1).
Figura 1 – Características clínicas faciales
En el examen clínico intra-oral, se observó dentición amarillenta, presencia de reposo radicular de 36 y cálculo dental en la región de los molares superior e inferior (Figura 2 y 3).
Figura 2 – Examen clínico inicial que muestra la presencia de reposo inferior izquierdo de la raíz (36)
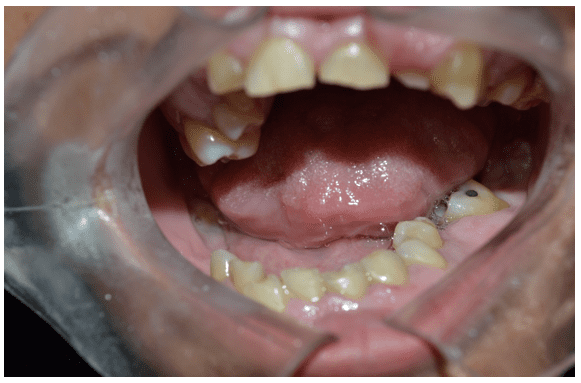
Figura 3 – Examen clínico inicial
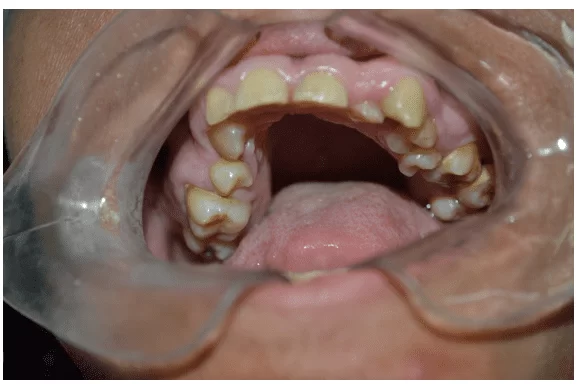
El tratamiento propuesto y ejecutado fue exodontia, raspado supragingival, profilaxis y orientación de higiene bucal. Para realizar los procedimientos, se solicitaron pruebas de laboratorio preoperatorias complementarias (recuento completo de sangre, coagulograma, creatinina y glucemia) y pruebas radiográficas. En la siguiente consulta, el paciente trajo las pruebas que estaban dentro de los estándares normales. La profilaxis antibiótica se realizó entonces con amoxicilina 2 gramos, 1 hora antes del procedimiento quirúrgico y la extirpación quirúrgica del elemento (Figura 4 y 5). En la siguiente consulta se realizó raspado supragingival, profilaxis y orientación de higiene bucal.
Figura 4 – Extirpación quirúrgica del diente 36.
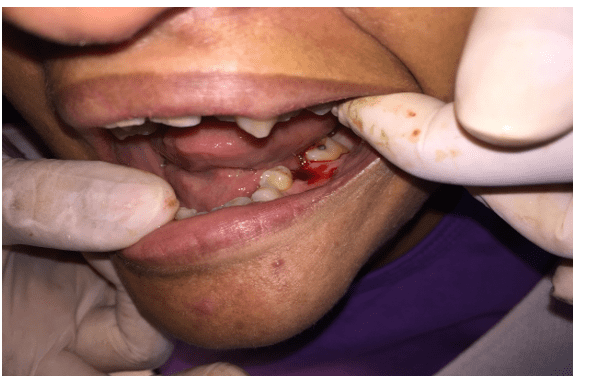
Figura 5 – Radiografía periapical de los molares inferiores.

DISCUSIÓN
A lo largo de los años, el número de cirugías de trasplante hepático ha aumentado y con esto, la supervivencia del paciente ha mejorado significativamente. Las terapias inmunosupresoras, utilizando fármacos como la ciclosporina, el tacrolimus y el sirolimus, actúan para evitar el rechazo del órgano recibido. El efecto inmunosupresor deseado es prevenir el rechazo del injerto por parte del sistema inmunitario, preservando al mismo tiempo el control de infecciones y neoplasias (PILLAI y LEVITSKY, 2009). Estos datos corroboran nuestro estudio, ya que el paciente en este informe tiene un grupo de edad y terapia farmacológica compatible con la literatura citada.
Las complicaciones más frecuentes que afectan a pacientes inmunosupresores se originan a partir de infecciones oportunistas, que tienden a evolucionar rápidamente a condiciones sistémicas agudas (OLCZAK et al., 2010; VIVAS, 2012). Después de realizar el trasplante, la paciente está subordinada a tratamientos inmunosupresores a lo largo de la vida, lo que puede promover el desarrollo de infecciones fúngicas y virales, siendo la candidiasis oral y las lesiones del herpes simple (SCULLY, 1992). Corresponde al dentista observar la presencia de estas alteraciones y tratarlas. Dependiendo de la gravedad, el medicamento inmunosupresor puede tener la dosis ajustada o incluso ser modificada por el médico.
Debido al tratamiento inmunosupresor o a los medicamentos utilizados, los pacientes trasplantados pueden presentar una variedad de lesiones orales. Este sitio donde podemos encontrar numerosos microorganismos, que pueden incluir los de origen viral o fúngico, neoplasias malignas, hiperplasia gingival, entre muchas otras alteraciones (SEYMOUR et al., 1997).
Saalman et al. (2010) describió un estudio en el que ocho niños trasplantados que usaban tacrolimus presentaban lesiones orales (edema y labios hendidos, queilitis angular y nódulos en la parte posterior de la lengua). Divergiendo de estos autores, se encuentra este informe, ya que no se observaron indicios de alteraciones orales en el examen clínico, incluso el paciente usando tracolimus.
Fármaco hiperplasia gingival asociado con el uso de ciclosporina y drogas que bloquean los canales de calcio como nyphedidin y amlodipino ya es un episodio bien conocido. Wright et al. (2005) presentado en su revisión bibliográfica sobre el aumento gingival relacionado con el uso de ciclosporina, que el predominio de esta alteración puede variar del 8 al 100% de los pacientes sometidos a cirugía de trasplante. Vivas (2002) realizó un estudio en el Hospital AC Camargo, São Paulo (SP), en el que de los 13 pacientes evaluados, 8 utilizaron ciclosporina y otros 5 pacientes utilizaron tracrolimus y bloqueadores de canales de calcio. Ningún paciente que tuvo hiperplasia gingival utilizó sólo tracolimus (1 nifedipine usada y los otros 4 amlodipino usados). Este informe corrobora la literatura, mostrando que el tracolimus no causa hiperplasia de las encías, sino más bien el canal de calcio que bloquea los fármacos que se utilizan de forma concomitante.
Las manifestaciones dentales no son una característica primaria del síndrome, pero ocurren invariablemente como una complicación de la colestasis a largo plazo y están relacionadas con la hiperbilirrubinemia.Como consecuencia de la colestática durante la odontogénesis, pueden surgir opacidades de esmalte, hipomineralización e hipoplasia de esmalte dental. Tanto la dentición primaria como la permanente pueden verse fuertemente afectadas si se desarrollan antes de la resolución de ictericia. Los autores informan de la presencia de cúspides de garra en dientes caducifolios y permanentes en pacientes con SA (PRAVEEN et al., 2011; CHATTERJEE y MASON, 2007). Otros reportan incisivos superiores macrodónticos y, en algunos casos, dientes caducifolios taurodonticos con cavidad pulpa agrandada (CALLEA et al., 2013; COZZANI y FONTANA, 2012).Y otros han observado que los pacientes con SA tienen hipodontia y xantomas orales (BERNICZEI-ROKYO et al., 2014). A diferencia de estas referencias, se encuentra este estudio de caso, ya que no se observó ninguno de estos cambios.
Una de las principales alteraciones dentales que se pueden encontrar en pacientes con enfermedades colestáticas es la pigmentación dental de bilirrubina. Estudios presentados por Hosey et al. (1995), Wondimu et al. (2001) y Lin et al. (2003), reveló una prevalencia de esta pigmentación intrínsica en el 50 al 61,3% de los pacientes. Estos datos son compatibles con el paciente, donde hubo un cambio, aunque leve, en la tinción dental.
La cavidad oral alberga sustancias patógenas que pueden causar inflamación aguda de órganos como neumonía, gastritis, úlceras pépticas y endocarditis infecciosa, que pueden ser perjudiciales para los pacientes trasplantados. Por lo tanto, se recomienda que el paciente realice consultas dentales preventivas.Antes de la cirugía, todas las cavidades cariosas deben ser tratadas y restauradas o removidas, el periodontum debe ser saludable y la higiene bucal debe ser muy buena. Se cree que los dientes infectados aumentan la carga inflamatoria sistémica general del cuerpo debido a la liberación de metabolitos bacterianos orales en el torrente sanguíneo y a través de respuestas inflamatorias e inmunológicas del huésped (OFFENBACHER et al., 2008). El tratamiento de pacientes con SA no diferencia la usal en ningún procedimiento, a menos que se cuide el cuidado profiláctico de antibióticos (TORRES et al., 2006). Esto debe llevarse a cabo en asociación con el médico, ya que puede haber una necesidad de prescripción específica de medicamentos (BERNICZEI-ROKYO et al., 2014). Ratificando estos estudios, el tratamiento dental quirúrgico del paciente se realizó con la prescripción de profilaxis antibiótica, así como pautas de higiene bucal.
Ajustar las afecciones orales, con la extirpación de focos odontogénicos antes del trasplante, puede reducir las complicaciones durante los procedimientos médicos necesarios para los receptores de órganos sólidos (GULLEÇ et al., 2003). La instrucción de higiene bucal es una estrategia eficaz para la reducción de microorganismos periodontopatógenos, reduciendo la incidencia de bacteremias y complicaciones posteriores durante el período de inmunosupresión, así como la eliminación de focos infecciosos locales, según el rendimiento dental realizado en el paciente de este estudio.
CONCLUSIÓN
El tratamiento dental ambulatorio se puede realizar en pacientes con SA, siempre que se observen las peculiaridades del síndrome. El papel del dentista en la promoción de la salud bucal es relevante, con el fin de evitar la presencia de focos infecciosos, especialmente en pacientes inmunosupresores. El dentista también debe ser consciente de los problemas cardiovasculares y hepáticos relacionados con el síndrome; tratamiento eficiente, contribuyendo al bienestar general del paciente.
REFERENCIAS
ALAGILLE, D. et al. Syndromic paucity of interlobular bile ducts (Alagille syndrome or arteriohepatic dysplasia): review of 80 cases. J Pediatr; v.110, p. 195-200, 1987.
AL-MUTAWA, S. et al. Oral findings in Alagille syndrome. Medical Principles and Practice, v.11, n. 3, p.161-163, 2002.
AMARAL TH, de Guerra CS, Bombonato-Prado KF, et al. Tooth pigmentation caused by bilirubin: a case report and histological evaluation. Spec Care Dentist., v. 28, n.6, p. 254–57, 2008.
BERNICZEI-ROYKO, A. et al. Medical and dental management of Alagille syndrome: a review. Med Sci Monit, v.20, p. 476-480, 2014.
CALLEA M, et al. Síndrome de Alagille: uma revisão. J Int Dent Med Research. v.6, n.1, p. 54–58, 2013.
CIOCCA, M.; ÀLVAREZ, F. Síndrome de Alagille. Arch Argent Pediatr, v. 110, n.6, p. 509-515, 2012.
CHATTERJEE, M.; MASON, C. Talon cusps presenting in a child with Alagille’s syndrome – a case report. J Clin Pediatr Dent., v. 32, n. 1, p. 61–64, 2007.
COZZANI, M.; FONTANA, M. Macrodontic maxillary incisor in alagille syndrome. Dent Res J., v. 9, n. 8, p. 251–254, 2014.
GILBERT, M. et al. Hum Mutat. 2019 Dec;40(12):2197-2220.
GUEGAN, K. et al. JAG1 mutations are found in approximately one third of patients presenting with only one or two clinical features of Alagille syndrome. Clin Genet., v. 82, p.33–40, 2012.
GULLEÇ, A.T. et al. Superficial fungical infections in 102 patients renal transplant recipients: a case control study. J Am Acad Dermatol.,v. 49, p.187-192, 2003.
HOSEY, M.T. et al. Oral findings in children with liver transplants. Int J Paediatr Dent., v. 5, n.1,p. 29-34, 1995.
LIN YT, LIN YT, CHEN CL. A survey of the oral status of children undergoing liver transplantation. Chang Gung Med J. v. 26, n.3, p. 184-188, 2003.
MITCHELL, E. et al. Alagille syndrome. Clin Liver Dis., v. 22, p.625–41, 2018.
OFFENBACHER, S. et al. Rethinking periodontal inflammation. J Periodontol, v. 79, p. 1577– 1584, 2008.
OLCZAK, B. et al. Oral candidiasis in immunosuppressed children and young adults after liver or kidney transplantation. Pediatr Dent. v. 32, n. 3, p.189-94, 2010.
PILLAI, A.A.; LEVITSKY J. Overview of immunosuppression in liver transplantation. World J Gastroenterol. v. 15, n.34, p. 4225-4233, 2009.
PRAVEEN P, et al. Cúspide de garra em um dente decíduo. J Dent Sci Res. v. 2, n.1, p. 34–40, 2011.
SAALMAN, R. et al. Long‐standing oral mucosal lesions in solid organ‐transplanted children‐a novel clinical entity. Transplantation 89: 606– 611. 2010.
SALEH, M. et al. Alagille syndrome: clinical perspectives. Appl Clin Genet., v.9, p.75-82, 2016.
SCULLY C. Oral Infectinos in the immunocompromised patient. Br Dent J. v.172, n.11, p. 401-407, 1992.
SEYMOUR, R.A. et al. Oral lesions in organ transplant patients. J Oral Pathol Med., v.26, n.7, p. 297-304, 1997.
SHEEHY EC, et al. Oral Health in children undergoing liver transplantation. Int J Pediatr Dent., v.10, n.2, p. 109-19, 2000.
SOUSA, A. C .M.; RESENDE, L. R. Síndrome de Alagille – relato de caso. Resid Pediatr. v.8, n.2, p.85-88, 2018.
TORRES, C.P. et al. Síndrome de Alagille: relato de caso. J. Health Sci. Inst., v. 24, n.2, p.149-153, 2006.
VIVAS, A. P. M. Avaliação de manifestações bucais em pacientes pediátricos submetidos ao transplante hepático.2012 Dissertação (Mestrado em Patologia Bucal) – Faculdade de Odontologia da Universidade de São Paulo, São Paulo, 2012.
WONDIMU, B.; NEMETH, A.; MODEER, T. Oral health in liver transplant children administered cyclosporin A or tacrolimus. International journal of paediatric dentistry, v. 11, n. 6, p. 424-429, 2001.
WRIGHT G., WELBURY RR., HOSEY MT. Cyclosporin‐induced gingival overgrowth in children. Int J Paediatr Dent., v.15, n.6, p. 403-411, 2005.
[1] Profesor de maestría en la Universidad Estatal de Amazonas.
[2] Estudiante de pregrado de la Universidad Estatal de Amazonas.
[3] Profesor especialista en la Universidad Estatal de Amazonas.
[4] Profesor de doctorado, Universidad Estatal de Amazonas.
[5] Profesor de doctorado, Universidad Estatal de Amazonas.
[6] Dentista, Especialista en Pacientes con Necesidades Especiales.
Enviado: Febrero de 2021.
Aprobado: Marzo de 2021.