ARTÍCULO DE REVISIÓN
CARNEIRO, Renato Brandi Pereira [1], KFOURI, Flávio de Ávila [2]
CARNEIRO, Renato Brandi Pereira. KFOURI, Flávio de Ávila. Membranas D-Ptfe Cytoplast® en regeneración ósea guiada en implantología. Revista Científica Multidisciplinar Núcleo do Conhecimento. Año 05, Ed. 09, Vol. 05, pp. 108-135. Septiembre de 2020. ISSN: 2448-0959, Enlace de acceso: https://www.nucleodoconhecimento.com.br/odontologia-es/regeneracion-osea, DOI: 10.32749/nucleodoconhecimento.com.br/odontologia-es/regeneracion-osea
RESUMEN
El aumento óseo vertical de la llanta alveolar es importante para obtener buenos resultados en rehabilitación con prótesis en implantes. Esta Revisión De Literatura buscó artículos que trataran el aumento óseo de los bordes alveolares usando membranas de citoplasto®, buscando evaluar la resistencia a la penetración bacteriana y la capacidad para crear y mantener el espacio. Para ello, se realizó una revisión de la literatura en las plataformas de búsqueda de Pubmed y Google scholar. Las investigaciones analizadas encontraron resultados similares entre la membrana d-PTFE, las mallas de titanio y las membranas e-PTFE, tanto en la ganancia ósea como en la calidad ósea. La capacidad de mantenimiento del espacio era evidente en los artículos en los que se utilizaba la membrana reforzada de titanio. La membrana d-PTFE presentaba una mayor capacidad de exposición al entorno oral sin comprometer el material del injerto. Los autores investigados en este estudio encontraron que las membranas d-PTFE reforzadas con titanio para los aumentos de la llanta alveolar augamble óseo son viables y permiten un cierto período de exposición al medio ambiente oral sin contaminación por injerto. Se necesitan más estudios con la membrana Cytoplast d-PTFE® para explorar sus características con procedimientos de aumento óseo vertical.
Palabras clave: Membranas artificiales, regeneración de tejido guiada, regeneración ósea.
1. INTRODUCCIÓN
Implantodontics revolucionó la odontología, permitiendo la restauración de la ausencia del órgano dental, artificialmente. A menudo, el Implantodontista, al planificar la rehabilitación con implantes, se enfrenta a poca altura o anchura del borde alveolar restante, lo que hace imposible posicionar de manera óptima los implantes de acuerdo con la planificación retrógrada realizada y para continuar la planificación puede utilizar la técnica de regeneración ósea guiada (ROG) para obtener un aumento óseo en la región que recibirá los implantes.
Los 4 principios biológicos necesarios para el éxito en la regeneración ósea guiada (es decir, PAEE) son: “i) cierre primario de la herida; (ii) angiogénesis para proporcionar el suministro de sangre necesario; (iii) creación y mantenimiento del espacio y iv) estabilidad de la herida” (WANG; BOYAPATI, 2006, págs. 8-11)
Urban et al. (2016) describió la técnica de colgajo donde hay liberación de periosteum hecho con incisiones perisomas y radiales y el avance de la solapa con sacudidas en la dirección coronal aumentando significativamente la superficie de la solapa, permitiendo el llenado con biomaterial y obteniendo el cierre primario de la herida.
Los investigadores observaron que si una membrana no está expuesta y permanece sin eventos durante 6 a 9 meses, se obtiene la formación ósea completa y que cuando hay fracaso, la mayoría de las veces fue debido a la exposición a la membrana y la consiguiente contaminación del injerto. (CUCCHI et al., 2017)
Urban et al., (2017) hizo hincapié en que la membrana debe fijarse con tornillos de lengua y vestibular para que quede inmóvil durante el proceso vertical de ROG.
Los investigadores describieron las 5 características de una membrana para la regeneración ósea guiada vertical: “(i) Biocompatibilidad; (ii) Creación y mantenimiento del espacio; (iii) Oclusividad y permeabilidad selectiva; (iv) Integración de tejidos; (v) Capacidad de gestión clínica.” (NAUNG; SHEHATA; VAN SICKELS, 2019, p. 2)
Muchas membranas se han propuesto para ROG, tanto absorbibles como no absorbibles y pueden ser colágeno, placenta humana, pericardio humano, tendón humano, hecho de ácido poliglicólico, ácido poliláctico, politetrafluoroetileno expandido o denso y malla de titanio. (NAUNG; SHEHATA; SICKELS VAN, 2019)
Lee y col. (2020) analizaron los efectos de L-PRF como membrana sobre ROG horizontal en alvéolos elevados en perros, después de 4 semanas compararon los resultados de L-PRF con otras membranas absorbibles y no absorbibles. Luego de otras 4 semanas de cicatrización ósea, se midió la cantidad de hueso nuevo para cada grupo mediante microscopía y tomografía microcomputada, verificando que el L-PRF juega un papel efectivo como membrana para el aumento lateral de la cresta.
Salomão et al. (2010) informaron que dos casos utilizaban una barrera de polipropileno (Bone Heal® – INP, São Paulo) sin la asociación de ningún material de relleno (injerto o implante biomaterial), se utilizó con el fin de mantener el coágulo atrapado con el fin de recuperar la arquitectura del borde alveolar y promover la neoformación ósea, con el fin de permitir la correcta instalación de un implante osteointegrable. Antes de colocar la barrera, el alveolo fue estimulado para estar completamente lleno de sangre.
Las membranas no absorbibles, cuando están expuestas, tienen una tasa de infección más alta que las membranas absorbibles. La membrana densa de PTFE evita el paso de bacterias incluso cuando se exponen utilizando enjuague bucal de clorhexidina (0,12%) y la aplicación de gel de clorhexidina (1%). (GHENSI et al., 2017)
La patente US7296998B2 de 2007 describe una lámina de material polimérico de politetrafluoroetileno polifórico hidrófilo (PTFE), que está sustancialmente sin explotar, tiene cavidades que tienen una profundidad menor que el espesor de la hoja. (CHADDICK; BARTEE, 2007).
2. PROPOSICIÓN
El objetivo de esta investigación es revisar la literatura más reciente sobre el uso de la membrana d-PTFE (Cytoplast® Osteogenics Biomedical, Texas) en la regeneración ósea guiada en implantodontia, abordando su resistencia a la penetración bacteriana y su capacidad para mantener el espacio.
3. REVISIÓN DE LA LITERATURA
Barber et al. (2007) notificaron dos casos de ROG con instalación simultánea de implantes y revestimiento de membrana d-PTFE (Cytoplast® Regentex GBR-200 o TXT-200 Osteogenics Biomedical, Lubbock, TX) sin refuerzo. Reportó una técnica de ROG donde dejó la membrana expuesta sin exponer los bordes durante 6 semanas en un caso de extracción e implantación inmediata del primer premolar superior. En el segundo informe del caso, un accidente de trauma mantuvo la membrana del Cytoplast® durante 4 semanas, eliminando y obteniendo fácilmente una capa consistente de tejido ostoides en la colocación de implantes en una región maxilar anterior 5 elementos sin complicaciones y migración epitelial ocurrió en el tejido ostoides en la semana 6, aumentando el ancho del tejido queratinizado antes de la lesión sufrida. Barber et al. (2007) señaló que “la densidad de la membrana d-PTFE impide la colonización de la flora huésped y evita la contaminación del biomaterial por debajo de la membrana”. También notó que con esta técnica la mucosa queratinizada sana por segunda intención, terminando su cierre con un área más grande. Concluyó que como el cierre primario en la membrana d-PTFE no es necesario, el cirujano puede tratar grandes defectos, preservar la papila interdental y preservar todo el ancho de la mucosa queratinizada, sin la preocupación de contaminación o infección bacteriana y también que el uso de membrana de Cytoplast® d-PTFE es la opción de tratamiento ideal para alveolos de exodontias sin cierre primario de la herida , debido a la simplicidad en su colocación y eliminación sin comprometer la calidad de la regeneración. (BARBER et al., 2007)
Hoffmann et al. (2008) investigó la regeneración clínica de alveolos de exodontia, utilizando membranas d-PTFE, sin el uso de material de injerto, para este fin, evaluó 276 alveolos de exodontias en 276 individuos (151 hombres y 125 mujeres; edad media, 50,2 años; edad: 24 a 73 años). El porcentaje de ganancia ósea obtenida después de ROG utilizando membrana de citoplasto ®, sin el uso de cierre primario de la herida. Antes de la extracción hizo una guía personalizada que podía fijarse a los dientes adyacentes con cinco agujeros donde a través de la sonda periodontal podía obtener mediciones de profundidad del alveolo después de la extracción. Después de la extracción, las aletas fueron elevadas y se colocó una membrana d-PTFE (Cytoplast® Regentex GBR-200) sin refuerzo de titanio en la extracción local. Las aletas fueron reposicionadas y suturadas en su lugar. No se obtuvo el cierre primario en las membranas. Las membranas se eliminaron después de 4 meses. Las uniones cemento-esmalte de los dientes adyacentes se utilizaron como puntos de referencia. Las mediciones se realizaron utilizando la guía, después de la extracción y 12 meses después de la cirugía en las mismas áreas, las variables descritas a nivel óseo se notificaron individualmente para todos los casos revisados y también en los grupos por factores de interés investigados: solo alveolo o lado a lado, mandíbula y región, ganancia ósea en defectos verticales se expresaron en medio y todavía se realizaron 10 biopsias de tejidos duros 12 meses después de la preservación del aoloteo durante la colocación del implante, obteniendo como resultado, ganancia ósea significativa de las muestras del núcleo óseo, regeneración significativa del volumen de los alveolos que se pudo observar mediante una evaluación histológica, indicando que el tejido recién formado en los sitios de extracción era principalmente hueso. No encontró ninguna influencia de género, fumar < 10 cigarrillos, edad o nivel óseo clínico en el porcentaje de ganancia ósea. Concluyó que el uso de la membrana del Cytoplast® d-PTFE condujo a la preservación de tejido blando y duro en sitios de exodontia.
Con respecto a los ensayos clínicos aleatorios, según la declaración CONSORT de 2010 (SCHULZ; ALTMAN et al., 2010):
Cuando se diseñan, llevan a cabo e informan adecuadamente, representan el estándar de oro en la evaluación de intervenciones de salud. Para evaluar con precisión un estudio, los lectores de un informe publicado necesitan información completa, clara y transparente sobre su método, tecnología y hallazgos. Por lo tanto, el Estado CONSORT de 2010 cumple los criterios mínimos, aunque esto no debe impedir que los autores incluyan otra información si lo consideran importante. (SCHULZ; ALTMAN, et al., 2010, p. 698)
Urban et al. (2014) evaluaron el uso de la membrana d-PTFE (Cytoplast® Ti-250) reforzada con titanio en combinación con una mezcla de hueso autógeno y BioOss®, para hacer esto veinte incrementos verticales en el reborde alveolar utilizando una membrana reforzada de d-PTFE con Cytoplast® Ti-250 Osteogenics Biomedical titanio, fijado con tachuelas de titanio Master Pin Control®, tornillos Messinger y / o Pro-Fix Tentin Screw®, Osteogenics Biomedical y una mezcla 1: 1 de hueso autólogo y Biooss® y cierre sin tensión con doble sutura de colchón horizontal y simple, no hubo exposición de la membrana. Como resultado, obtuvieron una ganancia ósea media de 5,45 mm y una desviación estándar de 1,93. La histología reveló que las partículas de Biooss® “estaban conectadas a una densa red de hueso recién formado, en todas las muestras, el espacio medular estaba bien perfundido con vasos sanguíneos y no se observó respuesta inflamatoria o reacción de cuerpo extraño”. (URBAN et al., 2017). Concluyeron que el uso de la membrana Cytoplast® Ti-200 es factible para la técnica de aumento del reborde alveolar vertical con hueso autólogo más Biooss® 1: 1 y cierre de herida sin tensión sin exposición de la membrana.
Ronda et al. (2014) llevaron a cabo un estudio prospectivo, aleatorizado y controlado diseñado para probar las membranas d-PTFE Cytoplast® Ti-250 y e-PTFE Goretex®, ambas reforzadas con titanio asociado a hueso autólogo y alollenados en gránulos mineralizados (Puros®, Zimmer Dental, Carlsbad CA, EE. UU.), 1: 1 en 23 pacientes que requirieron aumento óseo vertical de la cresta alveolar con procedimientos ROG para la colocación de implantes en mandíbulas atróficas posteriores (altura ósea disponible <7 mm). Los implantes se colocaron al nivel planeado, dejando los aparentes giros que estaban cubiertos por el biomaterial del injerto, y solo entonces se aleatorizó la membrana utilizada por el cirujano. El cierre de la herida se realizó sin tensión con doble sutura. Los resultados mostraron que no hubo diferencia significativa entre los porcentajes de ganancia ósea de los dos grupos. Las dos biopsias recogidas en el procedimiento de extracción de membranas mostraron dos regiones: “una de hueso laminar bien organizado y otra con pequeños huecos que albergan osteocitos y una parte coronal caracterizada principalmente por tejido óseo compuesto por trabéculas pequeñas e inmaduras”. (RONDA et al., 2014, p. 863). Concluyeron que, las membranas de d-PTFE y e-PTFE mostraron resultados clínicos idénticos en el tratamiento de defectos óseos verticales alrededor de los implantes, utilizando esta técnica y que el procedimiento de extracción de la membrana fue más fácil de realizar en el grupo de d-PTFE que que en el grupo e-PTFE, atribuido a las porosidades de la capa exterior que se adhieren al tejido conectivo, Ronda et al., (2014) enfatizaron que “aunque la presencia de una porción porosa de una de las membranas parece jugar un papel importante en la estabilización del dispositivo , favoreciendo su integración con los tejidos blandos, no parecía imprescindible para obtener la regeneración ósea ”.
Maridati et al., (2016) propuso y probó el manejo de las exposiciones a la membrana del Cytoplast® d-PTFE para lograr el éxito clínico final, informó de un caso, en un procedimiento de aumento óseo vertical de la llanta alveolar, un paciente de 63 años de edad donde instaló un implante de 3,4 x 11 mm, dejando algunos giros y el lado liso del implante expuesto, lleno de Biooss® y adaptó la membrana reforzada con titanio Cytoplast® fijación con 4 pines , acompañó una exposición de la membrana d-PTFE, aunque cerró la herida sin tensión. Hubo >3 mm sin signos de infección el día 14. La membrana se dejó en su lugar durante otras dos semanas. En la 4a semana se retiró la membrana y se posicionó un injerto conectivo del paladar para proteger el injerto óseo en el 7o mes, el abutman y la corona se atornillaron con éxito. Basado en el tiempo que debido a la membrana del citoplasto con alta densidad y poros menores que 0,2-0,3 micrómetros y haber sido ya probado en alveolos después de la exodontia antes, sin cierre primario de la herida sin tensión, en este estudio obtuvo buenos resultados tras la exposición de la membrana > 3 mm y posteriormente injertando tejido conectivo al extraer la membrana. Concluyeron que el control de la exposición de la membrana sin retirarla durante 4 semanas garantiza el mantenimiento del espacio adecuado debido a la resistencia de la membrana a la contaminación bacteriana.
Ghensi y col. (2017) demostraron que es posible manejar las exposiciones de la membrana Cytoplast® d-PTFE. En su reporte de caso, siguieron una exposición <3 mm de membrana d-PTFE reforzada con injerto autógeno y BioOss® 1: 1 Más tornillo de tienda, se obtuvo el cierre primario de la herida con liberación de periostio sin tensión, después de 14 días a la membrana estuvo expuesta, sin embargo, hubo evidencia de un sello epitelial en el sitio involucrado, sin aflojar la sonda ni supurar. El problema se solucionó con la continuación de los enjuagues bucales de clorhexidina (0,12%), aplicando gel de clorhexidina con una concentración del 1% dos veces al día hasta el procedimiento de reapertura y retirando cualquier placa una vez por semana en el consultorio donde siguió 4 meses hasta la remoción, rellenando el defecto vertical en la región de extracción del premolar y primer molar. Cuando se reabrió el sitio, el defecto original parecía haberse llenado, por lo que se insertaron dos implantes (CLC Conic; CLC Scientific, Vicenza, Italia), respectivamente 4 × 10 mm y 5 × 6 mm, en las posiciones del primer pre posición molar y molar. Observaron que debido a que las membranas de d-PTFE no absorbible tienen poros de 0,2 µm de diámetro, evitan la infiltración bacteriana y, incluso si la membrana está expuesta, el riesgo de complicaciones e infecciones es mucho menor que en e- PTFE. Esto hace que el cierre primario de tejidos blandos sea importante, pero no estrictamente necesario, ya que la membrana actúa como una barrera impenetrable para los alimentos y las bacterias y ha concluido que la exposición de la membrana de d-PTFE se puede manejar con un conocimiento profundo de los materiales involucrados y higiene bucal adecuada.
Cucchi y col. (2017) evaluaron las tasas de complicaciones y la ganancia ósea vertical después de ROG con membrana Cytoplast® Ti-250 reforzada con titanio en comparación con la malla de titanio cubierta por una membrana de colágeno absorbible. Se comparó la ganancia ósea vertical y las complicaciones después de ROG en mandíbulas posteriores atróficas con membrana Cytoplast® Ti-250XL y malla de titanio en mandíbulas posteriores, con colocación de implantes en 1 etapa, se analizaron 39 pacientes parcialmente desdentados con mandíbula posterior atrófica divididos aleatoriamente en dos Grupos de estudio: 20 pacientes fueron tratados con ROG de una etapa, es decir, con colocación de implantes simultáneamente, se utilizaron perforaciones corticales para permitir la angiogénesis y una mezcla de hueso autógeno y aloinjerto (EnCore®, Osteogenics, Biomedical, Lubbock, Texas), Solo en este momento se le entregó al cirujano la membrana para ser utilizada al azar, d-PTFE (Grupo A) y malla de titanio cubierta por membranas de colágeno reticulado (Grupo B), 19 pacientes, inicialmente había 40 pero 1 paciente de este grupo escapó, se fijaron con mini tornillos y cierre primario de herida sin tensión con doble sutura horizontal y vertical. Se registraron todas las complicaciones, distinguiendo entre “quirúrgicas” y “cicatrizantes” y entre “menores” o “mayores”. También se evaluaron la estabilidad primaria del implante y la ganancia ósea vertical. Obteniendo como resultado: En el grupo A, las tasas de complicaciones quirúrgicas, en estos casos parestesia temporal del nervio mentoniano y cicatrización fueron de 5.0% y 15.0%, respectivamente. En el grupo B, las tasas de complicaciones quirúrgicas y la curación fue del 15,8% y 21,1%, respectivamente, se siguieron durante 9 meses hasta la eliminación de las membranas. La ganancia ósea se midió con una sonda periodontal con divisiones de 1 mm y precisión de medición de 0,5 mm, que se midieron desde el hombro del implante hasta el hueso, antes de rellenar con biomaterial por vía bucal, lingual, mesial y distal, en cada implante y después de la regeneración se realizaron nuevas mediciones. Y concluyeron que los resultados preliminares de este estudio controlado aleatorio mostraron que las membranas de d-PTFE y las mallas de titanio cubiertas de membrana de colágeno producían resultados similares tanto en tasa como en tipos en términos de complicaciones de curación. Por el contrario, las membranas de d-PTFE mostraron una tasa promedio más baja de complicaciones quirúrgicas. En ambos grupos se logró una ganancia y formación de hueso vertical similares.
Herzberg (2017) describió 10 casos de aumento óseo vertical en el reborde alveolar en la región de un diente, por ser una zona crítica debido a que los dientes adyacentes a la región injertada, el colgajo pequeño, es más difícil de adaptar al aumento 3D logrado. Se realizó una incisión intrasulcular extendiéndose hasta dos dientes adyacentes y pasando por la cresta y relajante mesial de 10 mm, excepto cuando el aumento fue anterior, luego se realizó el relajante en la parte posterior de la incisión. Se instaló un implante en siete pacientes y tres ya tenían implantes, y se injertó con una mezcla 1: 1 de hueso autógeno con aloinjerto (Raptos®, Citagenix) y se cubrió con membrana reforzada de d-PTFE (Cytoplast® Ti-250AS, Osteogenics) mediante corte y adaptando y fijando con tornillos autorroscantes (Pro-Fix PFMF®, Osteogenics) y una membrana de colágeno (Remaix®) se colocó sobre la membrana de d-PTFE y se cerró la herida sin tensión. A los 6 meses no hubo exposición de la membrana de d-PTFE por lo que retiró la membrana y de los 10 pacientes uno perdió el injerto, dos perdieron 0.5 mm y uno perdió 1 mm, los otros tuvieron éxito sin pérdida. Observó que esta técnica es confiable y en sus referencias menciona que es común una pérdida ósea fisiológica de 0.47 a 1.16 mm durante el primer año con procedimiento vertical GBR utilizando membranas PFTE que se puede atribuir a la reabsorción de hueso inmaduro en la parte más coronal del hueso regenerado prefiriendo la colocación del implante en una segunda cirugía para que pueda ser corregido en este segundo momento. También atribuye la tasa de éxito al cierre de la herida quirúrgica, que en casos de regiones pequeñas ofrece un colgajo más pequeño, que es más difícil de adaptar al entorno aumentado. Concluyó que el ROG vertical en la región de 1 elemento dental, utilizando membrana Cytoplast, es un tratamiento confiable.
Hassan et al. (2017) en su estudio aleatorizado de la boca dividida comparó la membrana humano amnium/cório (MAC) con la membrana del Cytoplast® de 22 alveolos de extracción de 9 participantes en los aspectos: cantidad de preservación de las dimensiones de la cresta alveolar, siguiendo los procedimientos de conservación de la cresta, es decir, el cambio vertical de la altura de la cresta en milímetros, para ello construyeron un stent radiográfico con plano de referencia radiopaco con 5 agujeros que se pueden utilizar con sonda milimétrica y la medición en tomografía fueron realizadas mediciones por un profesional que desconocía el objetivo del estudio después de los residuos y 3,5 meses después de los residuos y los datos fueron utilizados para el análisis estadístico. También evaluó la calidad ósea mediante la recolección de muestras de hueso regenerado para análisis histológicos e histomorfométricos y molestias a través de la escala VAS. La aleatorización se realizó en el mismo lado o en el derecho y la izquierda. Los resultados fueron: Aumento horizontal medio de 2,54 (1,29) y 2,72 (1,01) para MAC y Cytoplast® respectivamente, siguiente con un aumento medio vertical de: -0,24 (0,91) y 1,18 (2,22) para Cytoplast. Concluyó que el área ósea mineralizada y el área de tejido blando no eran significativamente diferentes entre los dos tratamientos. Los sitios Mac tenían puntuaciones VAS postoperatorias significativamente más bajas en comparación con d-PTFE. El mac expuesto intencionalmente es igualmente eficaz en la preservación de la cresta en comparación con d-PTFE. Además, el uso de MAC puede ayudar a reducir las puntuaciones de VAS en el período postoperatorio y potencialmente resultar en una mejor calidad ósea disponible para la colocación del implante, como lo demuestra la mejora de las mediciones histomorfométricas.
Trobos et al. (2018) en su trabajo con cultivos in vitro, evaluaron la función barrera del Cytoplast® TXT200 d-PTFE y NeoGen® membranas e-PTFE contra bacterias de 2h, 12h y 48h. Su experimento utilizó tubos que tenían membranas adaptadas que permitían el contacto de una superficie de sobreb estéril con la superficie interna de la membrana y un cultivo de S. oralis en contacto con la superficie externa y al analizar el sobrenatant en el medio de cultivo de agar de sangre de caballo. Recoger material del interior de la membrana después de 48 horas de experimento a 37oC en estado de anaerobiosis y no hubo bacterias ni dentro de las membranas ni en el sobrenadante en contacto con las membranas. Sin embargo, d-PTFE favoreció la formación de más Biofilm de S. oralis en relación con el titanio y e-PTFE después de lavar con suero, externamente. Llegaron a la conclusión de que todas las membranas de PTFE eran barreras eficaces contra el paso bacteriano in vitro.
Gallo; Díaz-Báez (2019) con el propósito de describir el tratamiento de complicaciones como exposiciones e infecciones después de ROG vertical y horizontal con membrana Cytoplast®. Utilizando un nuevo protocolo de gestión de complicaciones reportado para este tipo de membrana. Para ello, evaluaron las complicaciones en la regeneración ósea realizadas con la membrana d-PTFE reforzada con titanio Cytoplast Ti-250, Osteogénicos Biomédicos entre 2000 y 2017 de 80 casos que presentaron complicaciones y casos tratados de exposición a la membrana inferior o igual a 3 mm sin infección y después de 2 meses de cirugía manteniendo durante 9 meses monitoreando la higiene del paciente semanalmente mediante la limpieza con clorhexidina y recomendando un ligero cepillado de membrana y la aplicación de clorhexidina en gel para evitar la acumulación exposición apareció antes de que la membrana se mantuviera durante 6 a 8 semanas, siguiendo el mismo protocolo de higiene y luego se retiró. Cuando hubo un informe de dolor y pus, optó por eliminar y curar inmediatamente el tejido granulomatoso y mantener el tejido duro, los pacientes fueron medicados con (amoxicilina/ac. Clavulánico 1g de 12/12h). El sextante con mayor número de complicaciones fue el maxilar anterior (43,75%), seguido de la mandíbula izquierda (20%). El 70% de los casos aparecieron después de 2 meses. Concluyó que este protocolo de gestión de complicaciones, que se propuso sobre la base de las 80 complicaciones, puede ayudar a prevenir la pérdida de todo el injerto y que la infección es la principal complicación que causa la pérdida del injerto. Concluyó que este nuevo protocolo de gestión de complicaciones ROG propuesto, basado en las 80 complicaciones observadas, puede ayudar a prevenir la pérdida total del injerto.
Koidou; Chatzopoulos; Johnson (2019) informó, una serie de casos en los que utilizó una membrana de colágeno retiletrated en el aloencherto y en el conjunto fijó una membrana de d-PTFE, que permaneció durante 6 semanas y fue extirpada atraumáticamente cuando se extrajo la membrana d-PTFE, tejido conectivo inmaduro y se observó que se convirtió en goma queratinizada 8 semanas después de la extracción y concluyó que el uso de una membrana d-PTFE en una membrana de colágeno en la degradación de la membrana absorbible y preserva su integridad.
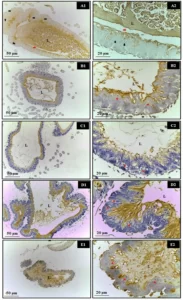
Cucchi et al. (2019) compararon los resultados de ROG entre la membrana Cytoplast® y la malla de titanio cubierta por la membrana Osseoguard® realizaron un estudio doble ciego que comparó los resultados histológicos e histomorfométricos del tejido óseo tomado de la región injertada de las mandíbulas posteriores con la mezcla 1: 1 de hueso autógeno y aloinjerto (EnCore® Osteogenics Biomedical), realizado decorticalización, utilizando en el grupo A 13 pacientes con membrana Cytoplast® Ti-250 XL d-PTFE y en el grupo B, 12 pacientes con malla Trinon Titanium®, Karlshure, Alemania cubierto con membrana de colágeno y fijado con dos o tres mini tornillos ProFix®. Suturada con doble capa horizontal y monocapa, obtenido cierre primario, esperado 9 meses. No hubo exposición, las muestras se fijaron en formalina tamponada con fosfato seguido de descalcificación Ácido clorhídrico y ácido fórmico, luego de descalcificar las muestras se deshidrataron en serie de baños graduados de alcohol y se embebieron en parafina, luego los cortes histológicos se tiñeron con hematoxilina y eosina. Los portaobjetos se escanearon (ScanScope CS®, Aperio Tecnologies, Leica Biosystems) en varios aumentos para evaluar las características del nuevo hueso formado, el material de injerto restante, la integración del material injertado con el nuevo hueso formado, el tejido blando y la inflamación local. La regeneración ósea en la porción coronal fue evidente en ambos grupos, y hubo un estrecho contacto entre el material injertado y el hueso, se encontró una formación activa de hueso evidente en todas las regiones del hueso injertado reflejada por altas densidades de osteocitos y trabeculado recién formado, asociado la intensa actividad de los osteoblastos en los frentes del crecimiento óseo. Se detectó reabsorción mediada por osteoclastos cerca del material del injerto, todas las biopsias contenían células de tejido conectivo con muchas venas. Los injertos se yuxtapusieron en todas las muestras y no hubo procesos inflamatorios ni reacciones inmunológicas en los sitios regenerados. Los datos histomorfométricos demostraron que ambas membranas impedían la migración de células no osteogénicas. En el grupo A, la proporción de tejido óseo, material de injerto y tejido blando fue del 39,7%; 8,6%; 52,1% y en el grupo B 42,1%; 9,6 y 48,3%, no encontraron diferencias significativas entre grupos. Concluyó que los resultados del estudio sugirieron que el uso de ROG con membrana d-PTFE Cytoplast® o malla Ti Trinon Titanium® en combinación con hueso autógeno y aloinjerto proporciona resultados similares tanto histológica como hitomorfométricamente.
Mertens et al. (2019) probó 4 técnicas in vitro diferentes para la estabilidad del volumen en un defecto del borde de la pared. Grupo 1: ROG con membrana de colágeno, xenoinjerto de partículas, Grupo 2: ROG con membrana de colágeno, xenoinjerto de partículas y pernos, Grupo 3: ROG con membrana reforzada con Cytoplast® Titanium Ti-250, xenoinjertos y pasadores de partículas, ROG Group 4 con bloque autógeno, membrana de colágeno, xenoinjerto de partículas, grabado con tomografías y probados. Para ello, creó los defectos en las mandíbulas de cerdo y realizó los procedimientos hasta que la solapa se cerró después de desmontar e hizo las mediciones: antes y después de la sutura, y calculó el cambio en mm y porcentaje y encontró como resultados que en los 4 grupos el cierre de la solapa llevó a una reducción de volumen, los grupos 2, 3, 4 tuvieron mejores resultados que el grupo 1 : colágeno sin pasador. Los grupos 3 y 4 son mejores que el grupo 2: colágeno y pin y grupo:3 d-PTFE mejor resultado que el grupo 4.Concluyeron que el cierre de la solapa tiene una influencia significativa en la estabilidad del injerto en defectos de 1 pared, la fijación adicional con pasadores mejora la estabilidad de la membrana ti-d-PTFE y el injerto de bloque mostró una mayor estabilidad que las membranas de colágeno, especialmente en la región del hombro del implante, y que los defectos de la estabilización del injerto de pared son incluso más importantes que en los defectos del contenedor automático.
Ibraheem et al. (2020), siguió RGB con membrana Cytoplast® con una exposición que se desarrolló durante el período de osificación del injerto. Para ello, informó un caso de aumento óseo con colocación simultánea de tres implantes en la región de los dientes 35,36,37, utilizando una membrana d-PTFE Cytoplast®, asociada a aloinjerto óseo LifeNet® Health, Virginia Beach, VA, giros expuestos 3-4,5 mm desde el lado vestibular y luego completados con una capa de BioOss®, y luego fijada la membrana d-PTFE con mini tornillos ProFix®. A los 21 días se retiró la sutura y hubo una exposición de 3 mm de la membrana, se indicó al paciente que pasara povidona yodada dos veces al día con un algodón, la exposición continuó aumentando, evolucionando a dehiscencia severa en la semana 16, pero los bordes de la membrana no estuvieron expuestos, no hubo evidencia de infección, la membrana fue removida revelando tejido fibroso cubriendo los implantes. Diez semanas después de que se quitó la membrana, se volvió a abrir y hubo hueso regenerado que cubría los tornillos de la cubierta. Se extrajo un núcleo con trépano para análisis histológico y se prepararon portaobjetos de tinción con hematoxilina / eosina, que revelaron un hueso viable denso y alrededor del hueso el material de relleno integral integrado. Llegaron a la conclusión de que la membrana Cytoplast®, cuando se expone, no necesariamente conduce a fallas si se maneja adecuadamente con intervalos de seguimiento cortos.
Mazzucchi et al., (2020) comparó muestras de la parte superior e inferior de la membrana d-PTFE en relación con los recuentos bacterianos de las dos superficies después de 28 días de conservación del alveolo de exodontias con exposición al medio ambiente oral. Los análisis microbiológicos y microscópicos revelaron que había una cantidad de bacterias en la capa interna, por debajo de los tejidos gingival perialveolar. Este hallazgo sugirió que las bacterias podían migrar a través de las encías adheridas a la membrana y colonizar la parte interna de la membrana, encontrando un camino entre la capa externa y los tejidos gingival que no se adhirieron a la superficie lisa de la membrana d-PTFE. Otra posibilidad es que la colonización se produce durante los procedimientos quirúrgicos: sin embargo, en ambas circunstancias, esto no afectó el proceso de curación, probablemente debido al pequeño número de bacterias presentes en el sitio.
4. DISCUSIÓN
Barber et al., (2007) y Ghensi et al., (2017) notificaron casos de ROG de alveolos exodontódicos que recibieron biomateriales y se utilizó la membrana del Cytoplast® d-PTFE como barrera. Barber et al. (2007), no obtuvo intencionalmente el cierre primario de la herida, que fue descrito por WANG et al. en 2006 como principio de PASS, afirmando ser innecesario debido a la densidad de la membrana d-PTFE que impide la contaminación del biomaterial por debajo de la membrana y mantuvo durante 6 semanas la membrana expuesta al entorno oral con control de higiene y concluyó que el cierre primario de la herida es innecesario en su discusión comentó que él y su equipo no tenían suficiente experiencia para comentar sobre la eficacia de mantener la membrana expuesta durante más de 6 semanas. Ghensi et al., (2017) exactamente 10 años más tarde, en su informe, a pesar de tener doble sutura y obtener inicialmente el cierre primario de la herida, informó de una exposición de la membrana donde siguió durante 4 meses. Ambos tuvieron éxito con ROG, confirmando que no había contaminación por injerto. Y Ibraheem et al., (2020) observó un aumento vertical de la exposición durante 4 meses, y obtuvo ROG, en este caso informe de que la membrana Cytoplast Ti-250 se fijó con tornillos.
Koidou et al. (2019) en su serie de estuches obtuvo ROG, utilizando membrana de Cytoplast®y una membrana de colágeno entre el injerto y la membrana, dejando la membrana expuesta intencionalmente. Hertzberg (2017) en su serie de estuches obtuvo ROG utilizando la membrana Cytoplast Ti-250 y se obtuvo una membrana de colágeno sobre la membrana d-PTFE que se fijó con pasadores de titanio y se obtuvo el cierre primario de la herida.
Hassan et al., (2017) se utilizó un modelo de estudio comparativo aleatorizado de la boca dividida que disminuye el sesgo porque es posible minimizar las variables interindividuales, ya que los participantes sirven como sus propios controles y, cuando están presentes, interfieren por igual en los tratamientos. Las membranas eran Cytoplast® y MAC, ROG se mantuvo manteniendo las membranas expuestas al ambiente oral durante 3,5 meses a pesar de no haber obtenido como resultado primario que la membrana del Cytoplast® resistió la penetración bacteriana mencionada en su conclusión de que el MAC expuesto intencionalmente es igualmente eficaz en la preservación de la cresta en comparación con d-PTFE y Hoffmann et al., (2008) en su estudio retrospectivo longitudinal, ROG realizado en 276 alveolos de exodontias, que debido a la población relativamente alta inscrita, reproduce una fuerte relación temporal de azar. Algunos detalles del estudio merecen ser destacados: primero el enmascaramiento y calibración del examinador que midió los defectos y luego la regeneración, y estandarizó las mediciones con casquetes individuales permitiendo 5 mediciones mapeando cada defecto, lo que aumenta la fiabilidad de los resultados. Al analizar los datos, las variables que describen la pérdida ósea fueron reportadas individualmente por todos los casos involucrados y también por separado en brazos por factores de interés investigados que eran: formato alveolo, maxilar superior o inferior y la ganancia ósea vertical se expresó en medios ± (DP) y valores mínimos, máximos y medios. Y se utilizaron muestras de prueba independientes para detectar algún efecto relacionado con el sexo o el tabaquismo en la pérdida ósea y se utilizó la correlación de Pearson para investigar la influencia de la edad en la ganancia ósea. No encontró ninguna influencia de las variables mencionadas anteriormente. Midió la ganancia ósea tridimensional, obteniendo una ganancia ósea vertical promedio de 6 mm, y también recogió muestras que demostraron que había regeneración ósea en el análisis histológico. En la descripción de la técnica enfatizó que no se obtuvo el cierre primario de la herida, la extracción de la membrana se realizó después de 4 meses, ambos autores mantuvieron las membranas expuestas incluyendo MAC durante un período entre 3,5 y 4 meses.
Dos experimentos han planteado evidencia relevante sobre las características de la impermeabilidad y la capacidad de integración en los tejidos de la membrana del Cytoplast®. Trobos et al., (2018) al probar la membrana d-PTFE en su experimento in vitro con S.oralis cultivo 2,12,24 y 48hs, concluyó que es impermeable a las bacterias ya Mazzucchi, et al., (2020) analizó las membranas tomadas de pacientes vivos y encontró bacterias en la parte inferior de la membrana en pequeñas cantidades pero no dañaron los injertos, argumentó que podrían haber penetrado en los bordes debido a la mala integración de los tejidos o durante la cirugía.
Gallo et al. (2019) al analizar las complicaciones en su estudio de 80 casos, informó de exposiciones a la membrana del Cytoplast®, que siguieron durante 9 meses guiando y acompañando a los pacientes con respecto a la higiene y el uso de clorhexidina 0,2% hasta la curación. Proponiendo un protocolo para el manejo de las exposiciones de membrana d-PTFE al medio oral, confirmó la resistencia a la penetración bacteriana, corroborando los resultados y recomendaciones de Ibraheem et al., (2020).
Ibraheem (2020) en su informe de caso hizo un ROG en una región de 3 elementos, y siguió una exposición >3 mm durante 10 meses y concluyó que la membrana Cytoplast®, cuando se expone, no necesariamente conduce al fracaso si se maneja adecuadamente con intervalos de seguimiento cortos, lo que confirma que el Cytoplast® membrana d-PTFE resiste la penetración bacteriana corroborando Maridati, et al. , (2016) que tuvo exposición a la membrana y siguió durante 4 meses y al retirar la membrana, también obtuvo ROG, este último autor no mencionó el uso de antiséptico, pero el uso de un antiséptico tópico parece desempeñar un papel importante en el pronóstico de las exposiciones para Gallo (2019) e Ibraheem (2020).
Urban et al., (2014), en su investigación, mediante la fijación de la membrana reforzada del Cytoplast® Ti-d-PTFE Ti 200 con Studs Master Pin Control®, Messinger y/o tornillos de carpa Pro-Fix Tentin Screw®, Osteogenics Biomedical, creó el andamio necesario para crear espacio. Al realizar perforaciones corticales, la liberación de la solapa y al obtener el cierre de la solapa sin tensión con doble sutura de edredón horizontal y simple, no hubo exposición de la membrana durante 9 meses, cumplió con los siguientes principios de PAEE de Wang, (2006): (i) cierre primario de la herida, (ii) angiogénesis y (iii) creación de espacio. Encontrar un resultado de una ganancia ósea de 5,45 mm con 1,93 desviación estándar confirmó que la capacidad de crear y mantener el espacio y la estabilización de la herida se cumplieron porque si la membrana del Cytoplast® d-PTFE no tuviera la capacidad de crear y mantener espacio y estabilizar la herida en hueso vertical aumenta, no habría alcanzado los aumentos óseos obtenidos por los autores , teniendo en cuenta que la angiogénesis y el cierre primario se lograron cuando describieron que no había exposición de la membrana ya Mertens et al., (2019) observó en su estudio con mandíbulas de cerdo que el acto de cerrar las aletas sin tensión con doble sutura, causó una disminución en el volumen vertical del injerto de partículas y también observó que el uso de Studs redujo la deformación del injerto de partículas y Herzberg et al., (2017) reconoció que a menudo el cierre primario de la herida es difícil de obtener como por ejemplo en las regiones de un diente.
Ronda et al., (2014) obtuvo resultados similares con dos membranas diferentes Ti-d-PTFE y Ti-e-PTFE en ROG, 116,8% y 119,7%, no hubo exposición de membranas, se instalaron implantes simultáneamente con ROG en 1 etapa y se realizó la descorticalización. Es posible notar que todos los principios de los PAEE se cumplieron en este estudio y Cucchi, (2017) en su estudio comparativo entre Cytoplast® membrana Ti-d-PTFE reforzada y malla de titanio cubierta con membrana de colágeno para ROG de mandíbulas posteriores y colocación de implantes de 1 etapa, obtuvo resultados similares en la ganancia ósea. Still Cucchi, (2019) continuando el trabajo de 2017 con análisis histológicos e histomorfométricos mostró una evidente regeneración ósea en las partes coronales de ambos grupos y el contacto íntimo entre el material del injerto óseo y el injerto sirvió como puente al hueso neoformado, determinando que hubo regeneración ósea tanto estudios aleatorios como enmascarados tanto en la distribución de pacientes como en las mediciones.
Oliveira (2015) en su artículo sobre Informes y series de casos señaló que a pesar de su importancia, los informes y la serie de casos están en riesgo de sesgo y que suelen publicar casos de éxito. Debido a que tenían un bajo riesgo de sesgo, los siguientes ensayos aleatorios: Ronda (2013) y Cucchi (2017) fueron seleccionados para ser agrupados en un gráfico “Trazado de bosque”. Iportante destaca que, para que pudieran haber sido publicados en la revista Clínical Oral Implant Research, como una consulta realizada en la página de presentación de la revista, el extracto sigue: “Los ensayos clínicos aleatorios deben ser reportados usando las directrices conSORT. También debe incluirse una lista de verificación de CONSORT 2010 en el material de presentación” (DIRECTRICES DEL AUTOR: 15/09/2020), por lo que una vez que cumplan con las directrices de prueba aleatorias, después de haber cumplido con los requisitos de la lista de verificación, pueden considerarse estándar de oro. Se agruparon en una “gráfica forestal” obtenida con el uso del software Review Manager 5.4 que podría realizarse debido a la baja heterogeneidad entre los estudios y los resultados cuantitativos de la ganancia ósea en mm, que podrían observarse en la prueba x2 e I2 presentada en los subtítulos con resultados 0,55 y 0% respectivamente, lo que sugirió que se utilizara el modelo de efecto fijo. Sólo confirma las conclusiones de los autores, pero demuestra un patrón que tiende a favorecer la membrana del citoplasto® en relación con la pantalla de titanio y la membrana e-PTFE en ganancia ósea / se entiende como capacidad para crear y mantener espacio también debido a que el injerto depende completamente de la membrana para permanecer en posición, por ejemplo si los estudios tenían el doble del total de intervenciones ya movería el rando negro fuera del eje 0, que también propone llevar a cabo estudios como estos con un muestreo mínimo de dos veces más alto. El software Review Manager 5.4 se utilizó para establecer metanálisis y simulaciones.
Figura 1. Trazado Forestal Ganancia media ósea d-PTFE x Control
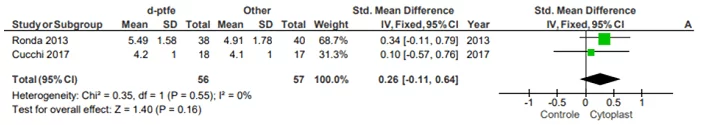
La forma en que Review Manager 5.4 realizó los cálculos fue descrita por Deeks y Higgins, (2010). Los tipos de datos encontrados en los resultados de ensayos clínicos aleatorizados fueron continuos, el método de análisis elegido fue la varianza inversa de efecto fijo y la medición del efecto en la diferencia media estándar y los intervalos de confianza del 95%.
Analizando los informes y series de casos en los que optaron por intentar dejar la membrana expuesta intencionalmente, basándose en la característica de impermeabilidad a las bacterias y la integración de los tejidos en la membrana y que obtuvieron la regeneración ósea y la ganancia ósea tanto en altura como en anchura y todavía algunas probadas por análisis histológicos e histomorfométricos, todavía había una brecha en la calidad de la integración de la membrana del Cytoplast® d-PTFE en los tejidos, si es lo suficientemente completo como para evitar que el colgajo de la mucosa permita el paso de bacterias en casos de exposición, el uso de clorhexidina en gel tópico y la eliminación mecánica de la placa en la parte superior de la membrana son esenciales en el control de las exposiciones y el control periodontal antes y después de la intervención quirúrgica son prácticas que pueden minimizar este riesgo. Se observó que hay evidencia y que requiere modelos de estudios con esta membrana que exploran estas propiedades.
5. CONCLUSIÓN
Después de analizar el trabajo científico de esta revisión, llegamos a la conclusión de que la membrana d-PTFE del Cytoplast® satisface las necesidades de una membrana para la preservación y el aumento del borde alveolar, permitiendo un período de exposición a la cavidad oral, sin infiltración de microorganismos en la región injertada siempre que el paciente esté acompañado por un rígido protocolo de higiene y los bordes de la membrana estén cubiertos por tejido y en casos de aumento vertical tornillos, Cytoplast Ti-250 es capaz de crear y mantener el espacio para que haya ROG cuando se obtiene el cierre de la herida primaria sin tensión realizada con la maniobra de incisión de liberación de periosteo.
REFERENCIAS
BARTEE, Chaddick M.; BARTEE, Barry K.. Hydrophilic high density PTFE medical barrier. Depositante: Chaddick M. Bartee, Barry K. Bartee. US7296998B2. Depósito: 21 set 2007.
BARBER, Dexter H.; LIGNELLI, John; SMITH, Brian M.; BARTEE, Barry K. Using a Dense PTFE Membrane Without Primary Closure to Achieve Bone and Tissue Regeneration. Journal of Oral and Maxillofacial Surgery, Estados Unidos, v. 65, n. 4, p. 748–752, abr. 2007. ISSN: 0278-2391. DOI: 10.1016/j.joms.2006.10.042.
CUCCHI, Alessandro; VIGNUDELLI, Elisabeta; NAPOLITANO, Aldo; MARCHETTI, Claudio; CORINALDESI, Giuseppe. Evaluation of complication rates and vertical bone gain after guided bone regeneration with non-resorbable membranes versus titanium meshes and resorbable membranes. A randomized clinical trial. Clinical implant dentistry and related research, Estados Unidos, v. 19, n. 5, p. 821–832, out. 2017. ISSN: 1523-0899. DOI: 10.1111/cid.12520.
CUCCHI, Alessandro; SARTORI, Maria, PARRILLI, Annapaola; ALDINI, Nicolò N.; VIGNUDELLI, Elisabetta; CORINALDESI, Giuseppe. Histological and histomorphometric analysis of bone tissue after guided bone regeneration with non-resorbable membranes vs resorbable membranes and titanium mesh.(Report). Clinical Implant Dentistry and Related Research, Estados Unidos, v. 21, n. 4, p. 693, ago. 2019. ISSN: 1523-0899. DOI: 10.1111/cid.12814.
DEEKS, Johnathan J.; HIGGINS, Julian P. T. Statistical algorithms in Review Manager 5: on behalf of the Statistical Methods Group of The Cochrane Collaboration, Cochrane Collaboration. p. 1–11, ago. 2010. Disponível em https://training.cochrane.org/handbook/statistical-methods-revman5. Acesso em: 08/07/2020.
GALLO, Pier; DÍAZ-BÁEZ, David. Management of 80 Complications in Vertical and Horizontal Ridge Augmentation with Nonresorbable Membrane (d-PTFE): A Cross-Sectional Study. The International journal of oral & maxillofacial implants, Estados Unidos, v. 34, n. 4, p. 927–935, jul. 2019. ISSN: 0882-2786. DOI: 10.11607/jomi.7214.
GHENSI, P;STABLUM, W; BETTIO, E; SOLDINI, M. C.;TRIPI,T. R.;SOLDINI, C. Menagemente of the exposure of a dense PTFE (d-PTFE) membrane in guided bone regeneration (GBR): A case report. Oral & Implantology, Itália, v. 10, n. 3, p. 335, jul. 2017. ISSN: 1974-5648. DOI: 10.11138/orl/2017.10.3.335.
HASSAN, Muyeenul M.; PRAKASAM, Sivaraman; BAIN, Carol; GHONEIMA, Ahmed; LIU Sean Shih-Yao. A Randomized Split-Mouth Clinical Trial on Effectiveness of Amnion-Chorion Membranes in Alveolar Ridge Preservation: A Clinical, Radiologic, and Morphometric Study. The International Journal of Oral & Maxillofacial Implants, Estados Unidos, v. 32, n. 6, p. 1389–1398, nov. 2017. ISSN: 0882-2786. DOI: 10.11607/jomi.5875.
HERZBERG, RAN. Vertical Guided Bone Regeneration for a Single Missing Tooth Span with Titanium-Reinforced d-PTFE Membranes: Clinical Considerations and Observations of 10 Consecutive Cases with up to 36 Months Follow-up. The International journal of periodontics & restorative dentistry, Estados Unidos, v. 37, n. 6, p. 893–899, nov. 2017. ISSN: 0198-7569. DOI: 10.11607/prd.3380.
HOFFMANN, Oliver.; BARTEE, Barry K.; BEAUMONT, Christian; KASAJ, Adrian;DELI, Giorgio; ZAFIROPOULOS, Gregor Georg. Alveolar bone preservation in extraction sockets using non-resorbable dPTFE membranes: a retrospective non-randomized study. Journal of periodontology, Estados Unidos, v. 79, n. 8, p. 1355–69, ago. 2008. ISSN: 0022-3492. DOI: 10.1902/jop.2008.070502.
IBRAHEEM, Ahmed Gamil; BLANCHARD, Steven B. Alveolar ridge augmentation around exposed mandibular dental implant with histomorphometric analysis. Clinical advances in periodontics, Estados Unidos, jan. 2020. ISSN: 2163-0097. DOI: 10.1002/cap.10090. Disponível em: https://aap.onlinelibrary.wiley.com/doi/epdf/10.1002/cap.10090. Acesso em: 15/09/2020.
KOIDOU, Vasiliki P.; CHATZOPOULOS, Georgios S.; JOHNSON, Deborah. The “Combo Technique”: A Case Series Introducing the Use of a d-PTFE Membrane in Immediate Postextraction Guided Bone Regeneration. J Oral Implantol., Estados Unidos, v. 45, n. 6 p. 486-493, dez. 2019.ISSN: 0160-6972. DOI: 10.1563/aaid-joi-D-19-00015.
LEE, Jun-Beom; LEE, Jung-Tae; HWANG, Sukhiun; CHOI, Jung-Yoo; YEO, In-Sung L. Leukocyte- and platelet-rich fibrin is an effective membrane for lateral ridge augmentation: An in vivo study using a canine model with surgically created defects. Journal of periodontology, Estados Unidos, v. 91, n. 1, p. 120–128, jan. 2020. ISSN: 0022-3492. DOI: 10.1002/JPER.19-0186.
MARIDATI, Paolo. C.;CREMONESI, Sergio; FONTANA, Filippo; CICCIÙ, Marco; MAIORANA, Carlo. Management of d-PTFE Membrane Exposure for Having Final Clinical Success. The Journal of oral implantology, Estados Unidos, v. 42, n. 3, p. 289–291, jun. 2016. ISSN: 0160-6972. DOI: 10.1563/aaid-joi-D-15-00074.
MAZZUCCHI, Giulia; LOLLOBRIGIDA, Marco; LAURITO, Domenica; DI NARDO, Dario; BERLUTTI, Francesca; PASSARIELLO, Claudio; SERAFINI, Giorgio; TESTARELLI, Luca; DE BIASE, Alberto G. Microbiological and FE-SEM Assessment of d-PTFE Membrane Exposed to Oral Environment after Alveolar Socket Preservation Managed with Granular nc-HA. The journal of contemporary dental practice, India, v. 21, n. 4, p. 404–409, 1 abr. 2020. ISSN: 1526-3711.
MERTENS, Christian; SEBASTIAN Braun; KRISAM, Johannes; HOFFMANN, Jürgen. The influence of wound closure on graft stability: An in vitro comparison of different bone grafting techniques for the treatment of one-wall horizontal bone defects. Clinical implant dentistry and related research, Estados Unidos. v. 21, n. 2, p. 284–291, 11 abr. 2019. ISSN: 1523-0899. DOI: 10.1111/cid.12728.
NAUNG, Noel. Ye.; SHEHATA, Ehab.; VAN SICKELS, Joseph. E. Resorbable Versus Nonresorbable Membranes: When and Why? Dental Clinics of North America, Estados Unidos v. 63, n. 3, p. 419–431, jul. 2019. ISSN: 0011-8532. DOI: 10.1016/j.cden.2019.02.008.
OLIVEIRA, Marco Aurélio Pinho; VELARDE, Guillermo Coca ; DE SÁ, Renato Augusto Moreira. Understanding the clinical research V: case report and series of case report. Femina, Brasil, v.43, n 5 p. 235-38, set. 2015. Disponível em: http://files.bvs.br/upload/S/0100-7254/2015/v43n5/a5320.pdf. Acesso em: 05/05/2020. ISSN: 0100-7203
REVIEW MANAGER 5.4 (Rev Man 5). The Cochrane Collaboration, set. 2015. Diponível em: https://training.cochrane.org/online-learning/core-software-cochrane-reviews/revman/reasons-downloading-revman-5. Acesso em: 05/06/2020.
RONDA, Marco; REBAUDI, Alberto; TORELLI, Lucio; STACCHI, Claudio. Expanded vs. dense polytetrafluoroethylene membranes in vertical ridge augmentation around dental implants: a prospective randomized controlled clinical trial. Clinical oral implants research, Dinamarca, v. 25, n. 7, p. 859–866, jul. 2014. ISSN: 0905-7161. DOI: 10.1111/clr.12157.
SALOMÃO, M.; F.K. ALVAREZ; J.T.T. SIQUEIRA. Guided bone regeneration after tooth extraction using membrane exposed to the oral environment. Case reports. Implantnews, Brasil, v. 7, n 6, p. 753-9. jun. 2010. ISSN: 2358-905.
SCHULZ, Knneth F.; ALTMANN, Douglas G.; MOHER, David; CONSORT. CONSORT 2010 Statement: updated guidelines for reporting parallel group randomised trials. International journal of surgery, Inglaterra v.9, n. 8, p. 672-677, 2011. ISSN: 1743-9191. DOI: 10.1016/j.ijsu.2011.09.004.
TROBOS, Margarita; JUHLIN, Annika; SHAH, Furqan A.; HOFFMANN, Maria; SAHLIN, Herman; DAHLIN, Christer. In vitro evaluation of barrier function against oral bacteria of dense and expanded polytetrafluoroethylene (PTFE) membranes for guided bone regeneration. Clinical Implant Dentistry and Related Research, Estados Unidos, v. 20, n. 5, p. 738–748, out. 2018. ISSN: 1523-0899. DOI: 10.1111/cid.12629.
URBAN, Istvan A.; MONJE, Alberto; NEVINS, Myron; NEVINS, Marc L; LOZADA Jamie L; WANG, Hom-Lay. Surgical Management of Significant Maxillary Anterior Vertical Ridge Defects. The International Journal of Periodontics & Restorative Dentistry, Estados Unidos, v. 36, n. 3, p. 329–337, mai. 2016. ISSN: 0198-7569. DOI: 10.11607/prd.2644.
URBAN, Istvan A.; MONJE, Alberto; LOZADA Jamie L; WANG, Hom-Lay. Principles for Vertical Ridge Augmentation in the Atrophic Posterior Mandible: A Technical Review. The International Journal of Periodontics & Restorative Dentistry, Estados Unidos, v. 37, n. 5, p. 639–645, set. 2017. ISSN: 0198-7569. DOI: 10.11607/prd.3200.
WANG, Hom. Lay.; BOYAPATI, Lakshmi. “PASS” principles for predictable bone regeneration. Implant Dentistry, Estados Unidos, v. 15, n. 1, p. 8–17, mar. 2006. ISSN: 1056-6163. DOI: 10.1097/01.id.0000204762.39826.0f.
ONLINELIBRARY.WILEY.COM. Author Guidelines: Research Reporting Guidelines. Clinical Oral Implants Research. Dinamarca. Disponível em: https://onlinelibrary.wiley.com/page/journal/16000501/homepage/ForAuthors.html. Acesso em: 15/09/2020. ISSN: 1600-0501
[1] Graduación en Odontología.
[2] consejero. Doctor en Ciencias. Máster Profesional en Odontología. Especialización en Implantodontia. Graduación en Odontología.
Artículo: Septiembre de 2020.
Aprobado: Septiembre de 2020.