ARTICLE ORIGINAL
RIBEIRO, Eliane de Oliveira Aranha [1], TABAL, Gabriella Bezerra [2], SOARES, Keuly Sousa [3], PRESTES, Gimol Benchimol Resende [4], SALINO, Alessandra Valle [5], QUEIRÓZ, Ana Karoline de Souza [6]
RIBEIRO, Eliane de Oliveira Aranha. Et al. Caractéristiques Approche dentaire dans le syndrome d’Alagille: rapport de cas. Revista Científica Multidisciplinar Núcleo do Conhecimento. An 06, Ed. 03, Vol. 16, p. 158-170. mars 2021. ISSN: 2448-0959, Access Link: https://www.nucleodoconhecimento.com.br/dentisterie/approche-dentaire
RÉSUMÉ
Le syndrome d’Alagille (SA) est une maladie dominante autosomique, multi-siemic, complexe et peu fréquente avec une grande variation dans la pénétration des caractéristiques cliniques. Décrire ces caractéristiques, les résultats oraux et le traitement dentaire d’un patient atteint de SA, en mettant l’accent sur les soins à adopter, était l’objectif de ce rapport. Une patiente de 31 ans s’est rendue à la Clinique dentaire des patients spéciaux de l’Université d’État d’Amazonas (UEA) pour des soins dentaires de routine. Dans l’anamnésie a rapporté présenter le SA, étant transplanté foie et l’utilisation comme médicament Tacrolimus (Prograf®) en permanence. À l’examen physique, une peau légèrement jaunâtre, le front et le nez proéminents ont été observés, et une petite exophthalmie a été observée. Dans l’examen clinique intra-oral, la dentition jaunâtre a été observée, présence du reste de racine des 36 et du calcul dentaire dans la région des molaires supérieures et inférieures. Le traitement proposé et exécuté était l’exodontie, le grattage supragingival, la prophylaxie et les directives d’hygiène buccodentaire. Le traitement dentaire ambulatoire peut être exécuté dans les patients présentant la SA, à condition que les particularités du syndrome soient observées. Le rôle du dentiste dans la promotion de la santé buccodentaire est pertinent, afin d’éviter la présence de foyers infectieux, en particulier chez les patients immunodéprimés.
Mots-clés: Syndrome d’Alagille, caractéristiques cliniques, traitement dentaire.
INTRODUCTION
Le syndrome d’Alagille (SA) est une maladie dominante autosomique, multisémique et complexe avec une grande variation dans la pénétration des caractéristiques cliniques (MITCHELL et al., 2018). Affecte rarement 1 naissance vivante sur 30/50.000 et a été décrite pour la première fois en 1970 basée sur des résultats cliniques hépatiques, cardiaques, faciaux, entre autres (GILBERT et autres, 2019).
Selon Sousa et Resende (2018), les cinq principaux signes sont: cholestase chronique (ictère temporaire, persistant ou intermittent; démangeaisons commençant à 6 mois; xantomas dans les zones de friction cutanée); facy dysmorphique (front saillant; yeux enfoncés avec hypertelorisme discret; menton pointu; nez aplati avec pointe en forme d’ampoule); anomalies cardiovasculaires (snoose périphérique de branche de l’artère pulmonaire, présente dans 90% des cas, avec ou sans association avec des anomalies complexes); défauts des arcs vertébraux (vertèbres dans l’aile papillon); et l’embryotoxon postérieur (signe présent dans 10% de la population générale, se compose de l’épaississement de la ligne formée par la membrane descemet et de l’angle de la chambre antérieure de l’oeil, évident par la lampe fendue ou par gonioscopy). Il est dit être complet quand il ya présence simultanée d’au moins quatre signes, tandis que la présence de seulement trois d’entre eux caractérise le syndrome comme incomplet. Les enzymes alcalines de phosphatase et de gamma-glutamyltransferase (GT ou alors GGT) sont très élevées dans la plupart des cas.
D’autres résultats cliniques moins fréquents dans le syndrome ont été également présentés par Alagille et al. (1987), comme l’hypogonadisme, le raccourcissement des phalanges distales, l’arthrite polyarticulaire déformante, le retardement de croissance, le retard mental, l’affaiblissement rénal (mésangiolipidose, acidose tubulaire rénale, néphrocalcinose) et le volume et le tonus modifiés de la voix.
Le diagnostic peut être difficile en raison de l’expressivité variable des manifestations cliniques (GUEGAN et al. 2012). Une grande partie des patients affectés par le syndrome n’ont pas d’antécédents familiaux, ce qui renforce la caractéristique de la pénétration incomplète, outre la possibilité d’une nouvelle mutation génétique (SOUSA; RESENDE, 2018). Le pronostic de la maladie et le risque de mortalité dépendent de la gravité de la participation des organes. La mortalité précoce est habituellement causée par une maladie cardiaque ou une maladie hépatique grave et la mortalité subséquente est souvent causée par des accidents vasculaires cérébraux (SALEH et al. 2016).
En ce qui concerne les dispositifs faciaux il y a des dispositifs dysmorphic doux mais reconnaissables, y compris le front proéminent, les yeux profonds avec l’hypertelorism modéré, les fissures palpebral obliques ascendantes, le pont nasal déprimé, le nez droit avec la pointe bulbeuse, les grandes oreilles, la mâchoire proéminente, et le menton pointu. Chez certains enfants, la forme du visage est remarquablement triangulaire. Le front proéminent semble moins évident chez l’adulte, tandis que la saillie de la mâchoire et du menton pointu sont plus évidentes. Il a été considéré que le phénotype facial diffère par rapport à savoir si les yeux sont fermés ou non. Ceux qui n’ont pas d’yeux profonds ont généralement des fissures palpebrals obliques ascendantes étroites, avec un hypertelorisme remarquable (CIOCCA; ÀLVAREZ, 2012).
En ce qui concerne la cavité buccale, les principaux effets sont dus à des dysfonctionnements hépatiques : hypoplasie de l’émail, pigmentation dentaire due à l’accumulation de bilirubine, retard généralisé dans l’éruption, plus grande susceptibilité au développement des caries, entre autres (SHEEHY et al., 2000; LIN et al., 2003; AMARAL et al., 2008).
La sévérité de ce syndrome varie de l’individu à l’autre, et peut présenter des symptômes doux au besoin de transplantation de foie (TORRES et al., 2006).
La SA peut mener à une maladie hépatique en phase terminale, nécessitant un traitement par transplantation hépatique. Dans la transplantation, la plus grande complication est la possibilité de rejet. Une des principales causes de ceci, en plus de l’incompatibilité de tissu, est l’infection pré- et postopératoire. La cavité buccale a des bactéries pathogènes qui peuvent produire la bactériémie avec le potentiel de causer des infections dans d’autres organes du corps (AL-MUTAWA, 2002). Démontrer la pertinence de surveiller et de préserver la santé buccodentaire de ces patients.
Par conséquent, la présente étude vise à décrire les caractéristiques cliniques de cette pathologie, ses résultats oraux et le traitement dentaire d’un patient atteint de SA, en mettant l’accent sur les soins à adopter.
CAS CLINIQUE
Patient A.C.C.S.F. 31 ans, sexe féminin, melanoderma, naturel et venant de Manaus-AM, a assisté à la clinique dentaire des patients spéciaux de l’Université d’État d’Amazonas (UEA) pour les soins dentaires de routine.
Dans l’anamnésie a rapporté présenter SA, étant transplanté foie, en utilisant comme médicament Tacrolimus (Prograf®), médicament immunosuppresseur qui inhibe l’activation des lymphocytes T, et qui fait usage de ce médicament depuis la transplantation. Il a déclaré avoir une « dent gênante ».
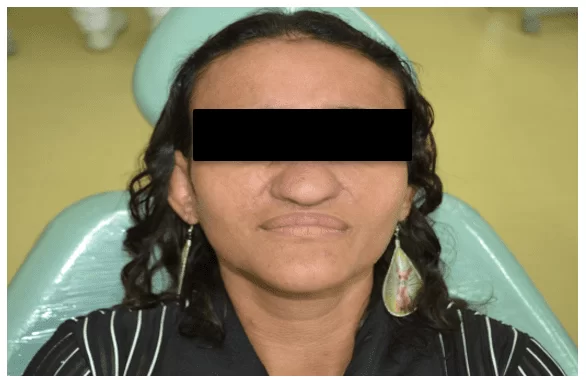
Lors de l’examen physique, on a observé une peau légèrement jaunâtre, un front et un nez proéminents et une petite exophtalémie (figure 1).
Figure 1 – Caractéristiques cliniques faciales
 Source: Archives personnelles
Source: Archives personnelles
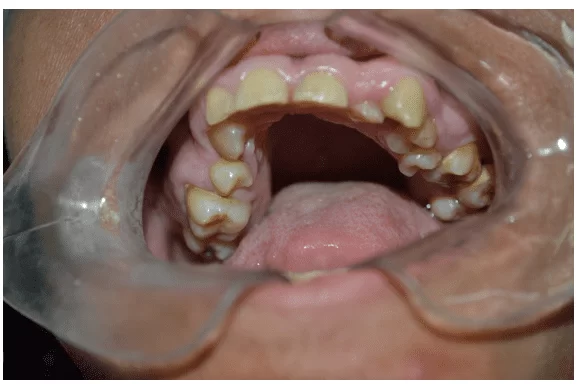
Dans l’examen clinique intra-oral, la dentition jaunâtre a été observée, présence du reste de racine de 36 et du calcul dentaire dans la région des molaires supérieures et inférieures (figure 2 et 3).
Figure 2 – Examen clinique initial montrant la présence d’un repose-racines inférieur gauche (36)
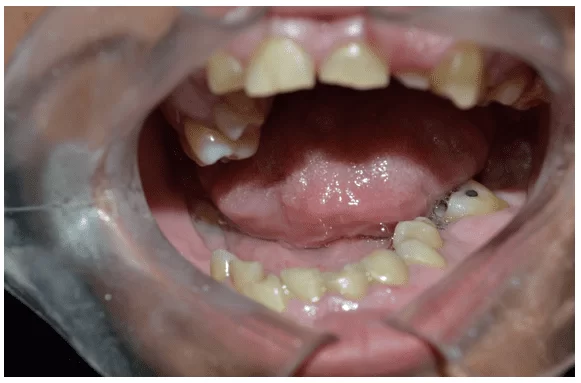
Figure 3 – Examen clinique initial
Le traitement proposé et exécuté était l’exodontie, le grattage supragingival, la prophylaxie et les directives d’hygiène buccodentaire. Pour effectuer les interventions, des tests préopératoires complémentaires en laboratoire (dénombrement complet du sang, coagulogramme, créatinine et glycémie) et des tests radiographiques ont été demandés. Lors de la consultation suivante, le patient a apporté les tests qui étaient dans les normes normales. La prophylaxie antibiotique a ensuite été effectuée avec l’amoxiciline 2 grammes, 1 heure avant l’intervention chirurgicale et l’ablation chirurgicale de l’élément (figure 4 et 5). Lors de la consultation suivante, des directives supragingivales en matière de grattage, de prophylaxie et d’hygiène buccodentaire ont été effectuées.
Figure 4 – Ablation chirurgicale de la dent 36.
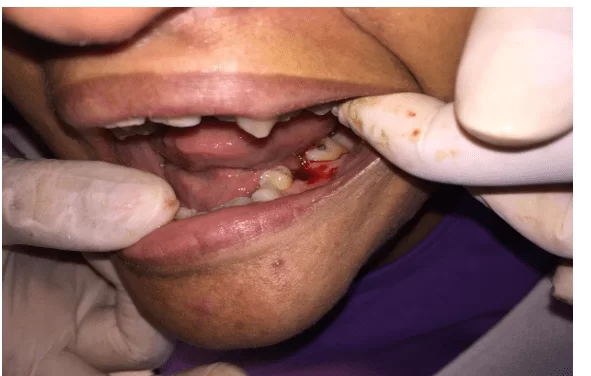
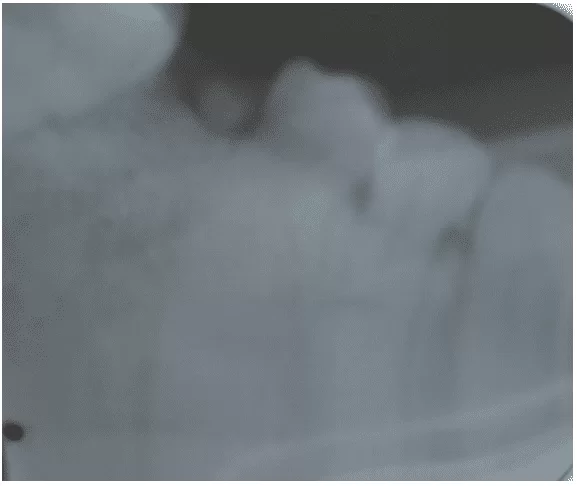
Figure 5 – Radiographie périapique des molaires inférieures.
DISCUSSION
Au fil des ans, le nombre de chirurgies de greffe du foie a augmenté et avec cela, la survie des patients s’est considérablement améliorée. Les thérapies immunosuppressrices, utilisant des drogues telles que la cyclosporine, le tacrolimus et le sirolimus, agissent pour empêcher le rejet de l’organe reçu. L’effet immunosuppresseur désiré est d’empêcher le rejet de la greffe par le système immunitaire, tout en préservant le contrôle des infections et des néoplasmes (PILLAI et LEVITSKY, 2009). Ces données corroborent notre étude, puisque le patient dans ce rapport a le groupe d’âge et la thérapie de drogue compatibles avec la littérature citée.
Les complications les plus fréquentes affectant les patients immunosuppressés proviennent d’infections opportunistes, qui ont tendance à évoluer rapidement vers des affections systémiques aiguës (OLCZAK et al., 2010; VIVAS, 2012). Après avoir effectué la greffe, le patient est subordonné aux traitements immunosuppresseurs tout au long de la vie, qui peuvent favoriser le développement des infections fongiques et virales, avec la candidose orale et les lésions de simplex d’herpès étant les plus communes (SCULLY, 1992). C’est au dentiste d’observer la présence de ces altérations et de les traiter. Selon la gravité, le médicament immunosuppresseur peut faire ajuster la dose ou même être modifié par le médecin.
En raison du traitement immunosuppresseur ou des drogues utilisées, les patients transplantés peuvent présenter une série de lésions orales. Ce site où l’on peut trouver de nombreux micro-organismes, qui peuvent inclure ceux d’origine virale ou fongique, malignités, hyperplasie gingivale, parmi beaucoup d’autres altérations (SEYMOUR et al., 1997).
Saalman et al. (2010) a décrit une étude dans laquelle huit enfants transplantés utilisant le tacrolimus ont présenté des lésions orales (oedème et lèvres de fissure, chéilite angulaire et nodules sur le dos de la langue). Divergeant de ces auteurs, ce rapport est trouvé, puisqu’aucune indication des altérations orales n’a été observée à l’examen clinique, même le patient utilisant le tracolimus.
L’hyperplasie gingivale de drogue liée à l’utilisation des drogues de cyclosporine et de canal-bloquant de calcium telles que nyphedidin et amlodipine est déjà un épisode bien connu. Wright et al. (2005) ont présenté dans leur revue de littérature sur l’augmentation gingivale liée à l’utilisation de cyclosporine, que la prédominance de cette modification peut varier de 8 à 100% de patients subissant la chirurgie de transplantation. Vivas (2002) a mené une étude à l’Hôpital AC Camargo, São Paulo (SP), dans laquelle sur les 13 patients évalués, 8 ont utilisé de la cyclosporine et 5 autres patients ont utilisé des inhibiteurs du tracrolimus et du canal calcique. Aucun patient qui a eu l’hyperplasie gingivale n’a employé seulement le tracolimus (1 nyfedipine employé et les 4 autres ont employé l’amlodipine). Ce rapport corrobore la littérature, montrant que le tracolimus ne cause pas l’hyperplasie de gomme, mais plutôt le canal de calcium bloquant des drogues qui sont employées simultanément.
Les manifestations dentaires ne sont pas une caractéristique primaire du syndrome, mais se produisent invariablement comme complication de la cholestasis à long terme et sont liées à l’hyperbilirubinemia.En raison du cholestatic pendant l’odontogenesis, des opacities d’émail, de l’hypominéralisation et de l’hypoplasie d’émail de dent peuvent surgir. La dentition primaire et permanente peut être fortement affectée si elle est développée avant la résolution de la jaunisse. Les auteurs rapportent la présence des cusps de griffe dans les dents à feuilles caduques et permanentes dans les patients présentant SA (PRAVEEN et al., 2011; CHATTERJEE et MASON, 2007). D’autres rapportent les incisives supérieures macrodontiques et, dans certains cas, les dents à feuilles caduques taurodontiques avec la cavité agrandie de pulpe (CALLEA et al., 2013; COZZANI et FONTANA, 2012). Et d’autres ont noté que les patients atteints de SA ont une hypodontie et des xantomas oraux (BERNICZEI-ROKYO et al., 2014). Contrairement à ces références, cette étude de cas est trouvée, puisqu’aucun de ces changements n’a été observé.
Une des principales altérations dentaires qui peuvent être trouvées dans les patients présentant des maladies cholestatic est la pigmentation de dent de bilirubin. Études présentées par Hosey et al. (1995), Wondimu et al. (2001) et Lin et al. (2003), a indiqué une prédominance de cette pigmentation intrinsèque dans 50 à 61.3% de patients. Ces données sont compatibles avec le patient, où il y avait un changement, même si doux, dans la coloration dentaire.
La cavité buccale abrite des substances pathogènes qui peuvent causer une inflammation aiguë d’organes tels que la pneumonie, la gastrite, les ulcères gastro-duodénaux et l’endocardite infectieuse, qui peuvent être nocives pour les patients greffés. Par conséquent, il est recommandé que le patient fait des consultations dentaires préventives.Avant la chirurgie, toutes les cavités carious devraient être traitées et restaurées ou enlevées, le parodontum devrait être sain et l’hygiène buccodentaire devrait être très bonne. On croit que les dents infectées augmentent la charge inflammatoire systémique globale du corps en raison de la libération des métabolites bactériens oraux dans la circulation sanguine et par des réponses inflammatoires et immunologiques de l’hôte (OFFENBACHER et al, 2008). Le traitement des patients atteints de SA ne différencie aucun usal dans n’importe quelle procédure, à moins que le soin prophylactique d’antibiotique soit pris en charge (TORRES et al, 2006). Cela devrait être réalisé en partenariat avec le médecin, car il peut être nécessaire d’avoir besoin d’une prescription spécifique de médicaments (BERNICZEI-ROKYO et al., 2014). Ratifiant ces études, le traitement dentaire chirurgical du patient a été exécuté avec la prescription de prophylaxie antibiotique, aussi bien que des directives d’hygiène buccodentaire.
L’ajustement des conditions orales, avec l’ablation des foyers odontogenic avant la transplantation, peut réduire des complications pendant les procédures médicales nécessaires pour des destinataires solides d’organe (GULLEÇ et al, 2003). L’instruction d’hygiène buccodentaire est une stratégie efficace pour la réduction des micro-organismes parodontopathogènes, réduisant l’incidence des bactériémies et des complications suivantes pendant la période d’immunosuppression, aussi bien que l’enlèvement des foyers infectieux locaux, selon la performance dentaire exécutée dans le patient de cette étude.
CONCLUSION
Le traitement dentaire ambulatoire peut être exécuté dans les patients présentant la SA, à condition que les particularités du syndrome soient observées. Le rôle du dentiste dans la promotion de la santé buccodentaire est pertinent, afin d’éviter la présence de foyers infectieux, en particulier chez les patients immunodéprimés. Le dentiste doit également être conscient des problèmes cardio-vasculaires et hépatiques liés au syndrome ; traitement efficace, contribuant au bien-être global du patient.
RÉFÉRENCES
ALAGILLE, D. et al. Syndromic paucity of interlobular bile ducts (Alagille syndrome or arteriohepatic dysplasia): review of 80 cases. J Pediatr; v.110, p. 195-200, 1987.
AL-MUTAWA, S. et al. Oral findings in Alagille syndrome. Medical Principles and Practice, v.11, n. 3, p.161-163, 2002.
AMARAL TH, de Guerra CS, Bombonato-Prado KF, et al. Tooth pigmentation caused by bilirubin: a case report and histological evaluation. Spec Care Dentist., v. 28, n.6, p. 254–57, 2008.
BERNICZEI-ROYKO, A. et al. Medical and dental management of Alagille syndrome: a review. Med Sci Monit, v.20, p. 476-480, 2014.
CALLEA M, et al. Síndrome de Alagille: uma revisão. J Int Dent Med Research. v.6, n.1, p. 54–58, 2013.
CIOCCA, M.; ÀLVAREZ, F. Síndrome de Alagille. Arch Argent Pediatr, v. 110, n.6, p. 509-515, 2012.
CHATTERJEE, M.; MASON, C. Talon cusps presenting in a child with Alagille’s syndrome – a case report. J Clin Pediatr Dent., v. 32, n. 1, p. 61–64, 2007.
COZZANI, M.; FONTANA, M. Macrodontic maxillary incisor in alagille syndrome. Dent Res J., v. 9, n. 8, p. 251–254, 2014.
GILBERT, M. et al. Hum Mutat. 2019 Dec;40(12):2197-2220.
GUEGAN, K. et al. JAG1 mutations are found in approximately one third of patients presenting with only one or two clinical features of Alagille syndrome. Clin Genet., v. 82, p.33–40, 2012.
GULLEÇ, A.T. et al. Superficial fungical infections in 102 patients renal transplant recipients: a case control study. J Am Acad Dermatol.,v. 49, p.187-192, 2003.
HOSEY, M.T. et al. Oral findings in children with liver transplants. Int J Paediatr Dent., v. 5, n.1,p. 29-34, 1995.
LIN YT, LIN YT, CHEN CL. A survey of the oral status of children undergoing liver transplantation. Chang Gung Med J. v. 26, n.3, p. 184-188, 2003.
MITCHELL, E. et al. Alagille syndrome. Clin Liver Dis., v. 22, p.625–41, 2018.
OFFENBACHER, S. et al. Rethinking periodontal inflammation. J Periodontol, v. 79, p. 1577– 1584, 2008.
OLCZAK, B. et al. Oral candidiasis in immunosuppressed children and young adults after liver or kidney transplantation. Pediatr Dent. v. 32, n. 3, p.189-94, 2010.
PILLAI, A.A.; LEVITSKY J. Overview of immunosuppression in liver transplantation. World J Gastroenterol. v. 15, n.34, p. 4225-4233, 2009.
PRAVEEN P, et al. Cúspide de garra em um dente decíduo. J Dent Sci Res. v. 2, n.1, p. 34–40, 2011.
SAALMAN, R. et al. Long‐standing oral mucosal lesions in solid organ‐transplanted children‐a novel clinical entity. Transplantation 89: 606– 611. 2010.
SALEH, M. et al. Alagille syndrome: clinical perspectives. Appl Clin Genet., v.9, p.75-82, 2016.
SCULLY C. Oral Infectinos in the immunocompromised patient. Br Dent J. v.172, n.11, p. 401-407, 1992.
SEYMOUR, R.A. et al. Oral lesions in organ transplant patients. J Oral Pathol Med., v.26, n.7, p. 297-304, 1997.
SHEEHY EC, et al. Oral Health in children undergoing liver transplantation. Int J Pediatr Dent., v.10, n.2, p. 109-19, 2000.
SOUSA, A. C .M.; RESENDE, L. R. Síndrome de Alagille – relato de caso. Resid Pediatr. v.8, n.2, p.85-88, 2018.
TORRES, C.P. et al. Síndrome de Alagille: relato de caso. J. Health Sci. Inst., v. 24, n.2, p.149-153, 2006.
VIVAS, A. P. M. Avaliação de manifestações bucais em pacientes pediátricos submetidos ao transplante hepático.2012 Dissertação (Mestrado em Patologia Bucal) – Faculdade de Odontologia da Universidade de São Paulo, São Paulo, 2012.
WONDIMU, B.; NEMETH, A.; MODEER, T. Oral health in liver transplant children administered cyclosporin A or tacrolimus. International journal of paediatric dentistry, v. 11, n. 6, p. 424-429, 2001.
WRIGHT G., WELBURY RR., HOSEY MT. Cyclosporin‐induced gingival overgrowth in children. Int J Paediatr Dent., v.15, n.6, p. 403-411, 2005.
[1] Maître professeur à l’Université d’État d’Amazonas.
[2] Étudiant de premier cycle de l’Université d’État d’Amazonas.
[3] Professeur spécialiste à l’Université d’État d’Amazonas.
[4] Professeur de doctorat, Université d’État d’Amazonas.
[5] Professeur de doctorat, Université d’État d’Amazonas.
[6] Dentiste, spécialiste des patients ayant des besoins spéciaux.
Soumis : Février 2021.
Approuvé : Mars 2021.