DIAS, Amanda de Araújo [1]
HELMER, Jamille Lopes [2]
AZEVEDO, Sílvia Karinny Brito Calandrini de [3]
CALDATO, Cassio [4]
OLIVEIRA, Ciane Martins de [5]
MOREIRA, Rodrigo Canto [6]
DENDASCK, Carla Viana [7]
OLIVEIRA, Euzébio de [8]
DIAS, Amanda de Araújo; et. al. Facteurs de risque génétiques et environnementaux de cancer gastrique. Connaissances de base scientifique multidisciplinaire magazine, 1 an. Vol. 10, pp. 63-72. Novembre 2016 – ISSN. 2448-0959
RÉSUMÉ
Objectif : cette étude vise à aborder les principaux aspects concernant les facteurs de risque associés au cancer de l’estomac. Méthode : nous avons effectué une revue de la littérature dans des revues scientifiques, de livres et de sites Web qui traitent de ce sujet : Scielo, pubmed, bibliothèque virtuelle de la santé et l’Institut National du Cancer, recherché 30 articles. Résultats : À noter que les connaissances sur les facteurs de risque de Cancer de l’estomac sont d’une grande importance à la prévention et la lutte contre la cancérogenèse digestive
. Mots clés : facteurs de risque. Tumeurs gastriques.
1. INTRODUCTION
Cancer de l’estomac est l’un des plus comuns1.2 les cancers et est connue comme la deuxième cause de décès par cancer dans le monde entier. Chaque année, plus de 930 000 nouveaux cas de cancer de l’estomac ont été diagnostiqués dans le monde entier, suivi par 700 000 décès ².
Au Brésil, ces tumeurs apparaissent à la troisième place de l’incidence chez les hommes et à la cinquième place chez les femmes. Dans le pays les nouveaux cas estimés de 20 390, étant des hommes et des femmes ³ 7 520 12 870.
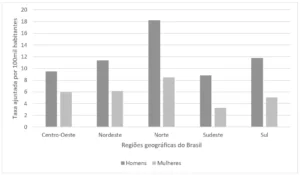
Dans le Pará, en 2014, les nouveaux cas estimés pour 100000 habitants était de 450 hommes et, chez les femmes, de 240. À Bethléem, les nouveaux cas estimés pour 100000 habitants était de 140 hommes et, chez les femmes, ³ 100.
Le tableau clinique des patients atteints de cancer gastrique est souvent caractérisée par la perte de poids en peu de temps, douleur locale, dyspepsie, nausées, vomissements, flatulences, sensation de plénitude qui contribuent à l’aggravation rapide de la maladie, de gêner les traitements proposés et, par conséquent, promouvoir la pire prognóstico4. Ces symptômes peuvent facilement être confondus avec ceux de gástrica5 de gastrite ou d’ulcère.
Le taux de survie à six mois est strictement lié à la phase de diagnostique et est environ 65 % de personnes ayant un diagnostic précoce et à moins de 15 % des personnes diagnostiquées à un stade avancé. Invasion métastatique survient dans 80 à 90 % de la pacientes5.
Le pronostic est situé de l’ampleur de l’invasion tumorale, présence ou absence de metástases6 et l’implication des ganglions lymphatiques, qui est considéré comme l’indicateur le plus fiable du pronostic dans le cancer gástrico5. La cancérogenèse gastrique, ainsi que d’autres organes est le processus en plusieurs étapes qui peuvent se manifester cliniquement comme l’atrophie gastrique, gastrite, métaplasie intestinale, dysplasie, ulcérations et, enfin, comme un néoplasme malin. Ces conditions ont tendance à être séquentiel et se produisent sur une période de plusieurs années, à la suite de l’exposition à une variété de facteurs endogènes et exógenos6.
Le fait que l’incidence de cette tumeur diffère considérablement selon la région géographique, indique que les facteurs de mode de vie modifiable, en particulier les facteurs alimentaires, ajoutés à des facteurs génétiques, peuvent influencer le développement de cette doença7.
Basé sur ce contexte, la présente étude vise à adresse les principaux aspects sur les facteurs de risque associés au cancer de l’estomac et contribuent à l’élaboration de mesures préventives efficaces pour lutter contre l’apparition de tumeurs gastriques.
2. MÉTHODOLOGIE
Ce travail a été mené à travers une revue de la littérature dans des revues scientifiques, de livres et de sites Web qui traitent de la question à l’étude : Scielo, pubmed, bibliothèque virtuelle de la santé et l’Institut National du Cancer. Les critères d’inclusion reposaient sur la période de temps entre 2003 et 2014 et en anglais, espagnol et portugais.
3. DISCUSSION ET ANALYSE DOCUMENTAIRE
facteurs génétiques 3,1
La classification de Lauren pour le cancer gastrique a été le plus utilisé dans l’Adénocarcinome gastrique, qui est divisé en intestinale et diffus. Par la suite, le type indéterminé a été inclus pour décrire une histologie rare. Il est prouvé que le type intestinal est associé à une métaplasie intestinale de muqueuse gastrique provoquée par des facteurs exogènes et le type diffus est plus lié à des anomalies genômicas8.9. Ce fait peut indiquer des voies de développement de tumeur intestinale et diffus adénocarcinome de l’estomac.
La cancérogenèse gastrique est un processus multifactoriel, où génétique et facteurs environnementaux interagissent pour activer plusieurs signaux intracellulaires, conduisant à la croissance incontrôlée et de la survie de cancer des cellules gástrico10. L’accumulation d’anomalies génétiques et moléculaires modifie l’expression de diverses sortes de gènes dont la fonction est importante pour la régulation celular11.
Le PAR-1 et PAR-2 sont exprimés dans les cellules de cancer de l’estomac et ses déclencheurs d’activation amplifient les voies biochimiques intracellulaires qui sous-tendent la cancérogenèse gastrique. Il semble également que l’expression des PAR-1 ou PAR-2 est en corrélation avec la profondeur d’invasion sur le mur et la dissémination métastatique et inversement avec la survie globale de la pacientes10.
En outre, l’amplification de la croissance épidermique factor receptor 2 (HER2) expression génique humaine et environ HER2 protéine est présente dans 15 % -20 % des patients atteints de jonction gastrique de cancer et gastresofágico. Le degré d’expression de HER2 et amplification varie avec la localisation du cancer, avec la plus haute expression dans gastresofágico et la partie proximale par rapport à la partie distale de l’estomac. Un grand nombre d’études semble indiquer que le HER2 est un facteur pronostique negativo12.
Parmi les plus répandues et communes des altérations génétiques dans le cancer gastrique sont des mutations dans le gène TP53 CDH1 et 13. En plus de mutations génétiques du gène CDH1 pour induire héréditaire diffus cancer de l’estomac (HDGC), des facteurs épigénétiques, tels que le hipermetilação de l’ADN contribuent également à la réduction de la E-cadhérine dans la cancérogenèse gastrique.
En outre, l’expression de la E-cadhérine peut être médiée par des agents infectieux, tels que h. pylori. Comme E-cadhérine est essentiel dans le processus de signalisation qui modulent la prolifération cellulaire, la survie, la migration et invasion, déréglementation de la E-cadhérine conduit à la dysfonction des cellules épithéliales gastriques et contribue au développement du cancer du gástrico14.
Dans la cancérogenèse gastrique, gènes suppresseurs de tumeur P53, P73 changent, Bcl-2 et APC. Gènes que la réparation des dommages à l’ADN sont chargés de détecter et réparent les variations d’autres gènes et ses déclencheurs de fonction une accumulation graduelle des mutations en outre, toute expression incontrôlée de p27 et Rb, CDC25B, P16, E2F entraîne une instabilité génomique, la prolifération cellulaire incontrôlée et la gástrico11 de développement de tumeur.
On peut observer que le niveau de génomique du cancer gastrique est une maladie hétérogène et que différents changements génétiques et moléculaires ont un impact sur la pratique médicale, puisqu’il peut être associé à des tableaux cliniques distinctes dans pacientes11.
Facteurs environnementaux
H. pylori
Helicobacter pylori est une bactérie à Gram négatif qui infecte la spirale plus de la moitié du mundial15 de la population. En plus de son rôle incontestable dans la gastrite chronique et de l’ulcère gastro-duodénal, l’association entre Helicobacter pylori et le cancer gastrique est également bien acceptée et études épidémiologiques estiment que le risque de cancer de l’estomac chez les individus infectés par h. pylori est augmenté à 20 vezes16. Actuellement, infection à Helicobacter pylori est réputée être le plus important facteur de risque d’apparition de cancer gástrico17.
H. pylori gastrite se caractérise par une inflammation grave et chronique qui peut durer des décennies si laissé non traité. L’inflammation persistante peut activer des neutrophiles, générer des espèces réactives de l’oxygène et d’azote, importants mutagènes et carcinogênicos18.
Le premier gène spécifique à la souche identifié à h. pylori a été le citotoxin antigène associé (merdes), qui est fortement associée au risque pour le développement du cancer de l’estomac. CagA + souches ont tendance à être plus virulent et induisent des niveaux plus élevés de l’expression des cytokines, telles que l’IL-1 b et IL-8, a montré que les patients infectés par des souches cette merde exprès sont probables trois fois plus élevés de développer un cancer gastrique que ceux infectés par des souches de cagA-19.
Composés N-nitroso et sel
Des études indiquent que la consommation d’aliments salés et composés N-nitroso et une faible consommation de fruits et légumes augmentent le risque de cancer de l’estomac. Des modèles animaux expérimentaux ont également soutenu l’hypothèse que le sel favorise la cancérogenèse gastrique induite par cancérogène N-nitroso, tels que N-methyl-N-nitro-N-nitrosoguanidina (MNNG) ou N-méthyl-N-nitrosoureia (MNU). Ainsi, l’association entre le NaCl saturé et la N-nitroso-cancérogène peut promouvoir cancérogenèse d’estomac chez les rats par inflammation, mutation et compensatória20 de la prolifération cellulaire.
Le NaCl peut agir en synergie avec l’infection à h. pylori, comme l’a montré dans des études cas-témoins et les animaux étudiés, par le biais de mécanismes qui comprennent le renforcement de l’expression du cagA, modifie la viscosité du mucus, avec perte subséquente de cellules parietais21.
En plus de causer une gastrite chronique, régimes riches en NaCl peuvent faciliter l’absorption des carcinogènes chimiques (hydrocarbures aromatiques polycycliques), agissant comme un promoteurs du développement de tumeurs chez les roedores22.
L’excès de chlorure de sodium conduit à la formation de malonodialdeído dans la muqueuse de la glandulaire de l’estomac et augmentent leur excrétion dans l’urine. Ainsi, la peroxydation des lipides se produit dans l’estomac glandulaire due aux dommages causés par le chlorure de sodium, ce qui conduit à la formation d’espèces réactives de l’oxygène (ROS), qui causent des dommages à l’ADN celular23. Ces molécules jouent un rôle crucial dans la carcinogenèse et peuvent être la cible des approches terapêuticas20.
Alcool
Compte tenu de la consommation d’alcool, certaines études ont montré un risque accru de cancer du estômago24.
L’alcool provoque plusieurs changements morphologiques et fonctionnels gastriques. En effet, l’éthanol nuit les mécanismes de défense muqueuses gastriques, en changeant la composition et la libération de mucus et de bicarbonate, en plus de s’immiscer dans le renouvellement de l’épithélium de le gástrico25.
L’augmentation des niveaux d’acétaldéhyde induite par une consommation excessive d’alcool peuvent causer des dommages de l’ADN et par la suite augmenter le risque de cancer du gástrico26. Induite par l’éthanol des ulcères gastriques dus à plusieurs mécanismes, y compris l’appauvrissement de la couche de mucus gastrique et l’audience Perméabilité muqueuse, qui conduit à une augmentation de la libération des ions d’hydrogène de la lumière et de diminue la différence de transluminal27 potentiel de membrane.
L’alcool brise la barrière des caustiques de dommages de la muqueuse gastrique, provoquant une rupture des vaisseaux sanguins, l’hémorragie et la nécrose de la muqueuse. Prédisposent à la formation de la gastrite et peut déclencher l’apparition d’un processus cancéreux. Les lésions de la muqueuse gastrique peuvent diminuer la production de facteur extrinsèque, causant l’individu à une carence en vitamine B12 absorption 28.
Usage du tabac
Environ 30 % des décès par cancer de l’estomac se produisent chez les fumeurs. Fumer a été systématiquement signalé comme le plus important facteur de risque comportementaux pour cancer gástrico7.
Les données épidémiologiques montrent que les cigarettes augmenter tant du taux de rechute de la maladie peptique accessoire, mais aussi ralentit la guérison des ulcères chez les humains. La mesure dans laquelle l’action est attribuable aux gènes Ucero la nicotine dans la fumée de cigarette est encore mal definido29.
inhibiteurs de la sécrétion gastrique 3,2
Médicaments qui inhibent la sécrétion acide de l’estomac tels que la cimétidine, la ranitidine et la loxtidina, qui bloque les récepteurs H2 de l’histamine sur les parietal cells de l’estomac et les bloqueurs de K +, H +-ATPase (pompe à protons), tels que l’oméprazole, réduire l’acidité gástrica22. L’état de l’hypochlorhydrie ou acloridria causés par ces médicaments ou pour d’autres raisons, causes le pH de l’estomac soit propice à la formation de colonies et la survie des microorganismes, qui favorise un processus inflammatoire chronique de la muqueuse, conduisant à la gastrite atrophique, résultat dans les foyers de métaplasie, dysplasie, évoluant sur des précédant l’apparition des neoplasias30.
4 – conclusion
Basé sur les résultats trouvés avec la réalisation de cette étude a conclu que les connaissances sur les facteurs de risque de Cancer de l’estomac sont d’une grande importance au développement de mesures préventives et efficaces au combat carcinogenèse digestive et sur l’amélioration du pronostic des personnes déjà touchées par cette pathologie. L’étude montre également que la prudence est indispensable dans l’utilisation clinique des médicaments antiacides parce que son utilisation aveugle peut entraîner l’initiation et la promotion des tumeurs.
RÉFÉRENCES
SOLEIL, Q., LI, Y. L’effet inhibiteur de l’acide Pseudolaric B sur résistance multidrogue GastricCancer et par la voie de Cox-2/PKC-a/P-gp, Plos One, c. 9, Sep/2014. Disponible à : < http://www.plosone.org/article/fetchobject.action?uri="info%3Adoi%2F10.1371%2Fjournal.pone.0107830&representation=PDF"> </>. Accessible au : 30/09/2014.
2. Taghızadeh-Kerman, a. et. Al. La signification pronostique du Ratio de ganglion métastatique chez les Patients atteints de Cancer gastrique : une évaluation dans le nord-est de l’Iran. Un Journal iranien de prévention du Cancer, c. 7, 2014. Disponible à : http://www.ncbi.nlm.nih.gov/pmc/articles/PMC4142944/. Accessible au : 30/09/2014.
3. GUIMARÃES, b., et al, l’incidence du cancer au Brésil.2014. disponible à : http://www2.inca.gov.br/wps/wcm/connect/tiposdecancer/site/home/estomago. Accessible au : 04/08/2014.
4. MAGALHÃES, l. p. et al., poids : Variation, degré d’éducation, assainissement de base, l’alcoolisme, tabagisme et manger des habitudes pregresso chez les patients avec estomac cancer, gastroentérologie, v. 45, no 2, Apr/jun/2008. Disponible à : < http://www.scielo.br/pdf/ag/v45n2/a04v45n2.pdf=""> </>. Consulté le 04/08/2014.
5. D’Angelo, g., Di Rienzo, t., OjettI, v., Microarray analysis dans le cancer gastrique : une revue, World Journal of Gastroenterology, c. 20, n. 34, Sep/2014. disponible à :<http: www.ncbi.nlm.nih.gov/pmc/articles/pmc4161784/="">. Accessible au : 01/08/2014.</http:>
6. CÉSAR, Ana., et al. génétique et les facteurs environnementaux impliqués dans la cancérogenèse gastrique, gastroentérologie, c. 39, no 4, décembre/2002. disponible à : <http: www.scielo.br/scielo.php?pid="S0004-28032002000400009&script=sci_arttext">.</http:> Accessible au : 04/08/2014.
7. XIE, f. et al. Consommation de café et risque de Cancer de l’estomac : une grande mise à jour de méta-analyse des études prospectives. Nutriments, v6, 2014. Disponible à :< http://www.mdpi.com/2072-6643/6/9/3734/htm="">. Accessible au : 25/07/2014.
8. Systèmes de classification de pathohistologiques BERLTH, F.et.al, dans le cancer gastrique : valeur diagnostique et pronostique de pertinence, Worl journal de Gastro-enterologie, c. 20, n. 19. mai / 2014Disponível à : http://www.ncbi.nlm.nih.gov/pubmed/24914328. Accessible au : 22/07/2014.
9. FORSTER, S.et.al, THBS4, une nouvelle molécule stromale des adénocarcinomes gastriques diffus-type, identifiés par l’expression à l’échelle du transcriptome, profilage, Mod Pathol, v. 24, n. 10, octobre 2011. disponible à :< http://www.ncbi.nlm.nih.gov/pubmed/21701537="">. Accessible au : 06/08/2014.
10. Sedda, s. et coll. récepteurs activés par la protéinase,-associated signaling dans le contrôle du cancer gastrique, monde du Journal Gastroenterology, c. 20, Sept. 2014. Disponiblesur < http://www.ncbi.nlm.nih.gov/pmc/articles/PMC4161785/pdf/WJG-20-11977.pdf >. Accéder au 30/09/2014.
TORRES-JASSO, j. h., SÁNCHEZ-LÓPEZ, j. y., Cancer de l’estomac : génétique, moléculaire y altérations Gaceta Mexico medical, c. 147, n1, 2011. Disponible à : < http://www.anmm.org.mx/GMM/2011/n1/73_GMM_Vol_147_-_1_2011.pdf >. Consulté le 01/08/2014
Jorgensen, j. t., rôle de récepteur de facteur de croissance épidermique humain 2 dans le cancer gastrique : question des aspects biologiques et pharmacologiques, monde du Journal Gastroenterology, v. 20, avr/2014. Disponible à : < http://www.ncbi.nlm.nih.gov/pmc/articles/PMC4000489/pdf/WJG-20-4526.pdf >. Consulté le 04/08/2014
PATEL, DD.et.al, Perspectives sur les nouveaux biomarqueurs dans le cancer gastrique : applications diagnostiques et pronostiques, World journal de Gastro-enterologie, c. 20, n. 33, Sep/2014. disponible à : < http://www.ncbi.nlm.nih.gov/pubmed/25206265 >. Accessible au : 04/08/2014.
14. LIU, x., KENT-MAN, c., E-cadhérine et Cancer de l’estomac : causes, conséquences et Applications, BioMed Research International, v. 2014, jul/2014. Disponibles dans <http: www.hindawi.com/journals/bmri/2014/637308/="">.</http:> Consulté le 03/08/2014.
15. SHIOTA, S.et.al, pylori, Cancer gastrique et duodénal ulcère montrent même phylogéographique origine dans la région des Andes en Colombie, Plos, v. 9, no 8, août 2014. disponible à : < http://www.plosone.org/article/info%3Adoi%2F10.1371%2Fjournal.pone.0105392 >. Consulté le : 02/08/2014
MARCHAND, S. J., LI, L. KIM. J., Racial et ethnique des disparités dans les résultats de cancer de l’estomac : plus importante que la technique chirurgicale ? Monde J Gastroenterol, c. 20, n. 33, Sep/2014. Disponible à : http://www.ncbi.nlm.nih.gov/pmc/articles/PMC4155347/. Accessible au 16/09/2014.
17. Pandey, A.et.al, cancérogène Helicobacter pylori dans le cancer de l’estomac et des lésions pré cancéreuses : Association avec tabac à chiquer, Worl journal de Gastro-enterologie, c. 20, n. 22, Juho/2014. disponible à : < http://www.ncbi.nlm.nih.gov/pubmed/24944476 >. Accessible au : 02/08/2014
18. SAAD, A.et.al, les facteurs génétiques de l’Helicobacter pylori et la cancérogenèse gastrique hôte, sciences de la vie, v. 3. disponible à : http://paulosantos.eu/media/Sampaio_Santos2008RPCB3.pdf. Accessible au : 29/07/2014.
19. HILL, M.et.al, Biopatologia de h. Pilory, Brazilian Journal of medicine laboratoire et pathologie, vol. 39, no 4, janvier/2013. disponible à :< http://www.scielo.br/scielo.php?script="sci_arttext&pid=S1676-24442003000400011">. Accessible au : 02/08/2014
20. SINTARA, K.et.al. Curcumine atténue gastrique Cancer induite par le N-méthyl-N-nitrosourée et saturée de chlorure de Sodium à des Rats, Journal de la biomédecine et de la biotechnologie, v. 2012, février 2012. disponible à : < http://www.hindawi.com/journals/bmri/2012/915380/ >. Consulté le : 22/07/2014.
21. LEE, Y.Y., Derakhshan, M.H., environnement et mode de vie facteurs de risque de gastrique Cancer-2013, Archives des iraniens Medicine, vol. 16, n° 6, juin 2013. disponible à : < http://www.ncbi.nlm.nih.gov/pubmed/23725070 >. Consulté le : 23 juillet 2014
22. AGNEAU, m., PINTO, l., PAUMGARTTEN, f., facteurs de risque dans la vision de la santé publique toxicologue, ordinateur portable, vol. 13, n. 1.2003
23. Agarwal, d., Smith, i., CRUZ, w., chimioprévention du cancer, Brazilian Journal of Oncology, c. 56, n. 3,2010.
24. Teixeira. Cancer de l’estomac, m. NOGUEIRA, le juge : facteurs de risque, Latin American Journal of nursing, v. 11, n ° 1, février/2013.
25. OLLY OLLY OXENFREE, f., FONSECA, f., FILS, j., les actions de l’alcool sur l’oesophage, estomac et des intestins, groupe d’édition Maurya, janvier/2005. disponible à : < http://www.moreirajr.com.br/revistas.asp?fase="r003&id_materia=2893"> </>. Consulté le : 04/08/2014.
26. Interactions de gène-régime JEONGSEON, K.et.al, du risque de cancer gastrique : un examen systématique, le World journal de Gastro-enterologie, c. 20, n28, juillet/2014. disponible à :< http://www.ncbi.nlm.nih.gov/pmc/articles/pmc4110595/="">. Consulté sur : 29 juillet 2014
27. HUANG, effet cytoprotecteur C.et.al of American Ginseng dans l’éthanol modèle ulcère gastrique de Rat, molécules, v. 19, no 1, décembre 2013. Disponible à : < http://www.mdpi.com/1420-3049/19/1/316 >. Consulté le : 03/08/2014
28. CHANSON, DU.et.al, gastroprotectrices effets de riz gluant extrait contre l’éthanol, l’indométhacine et ulcères provoqués par le Stress chez les Rats, Chonnam Medical Journal, vol. 50, n° 1, avril/2014.
29. WK, w., CHO, c., les actions pharmacologiques de la nicotine sur le système gastro-intestinal, Journal des Sciences pharmacologiques, v. 94, no 4, avril/2014.
Disponible à :< http://www.ncbi.nlm.nih.gov/pubmed/15107574="">. Accessible au : 02/08/2014
- MENDONÇA, R., GAGLIARDO, L. RIBEIRO, R. Cancer de l’estomac : l’importance de la thérapie nutritionnelle, santé Magazine, c. de l’environnement et 3, non 2, décembre 2008.
[1] Cours de premier cycle médical CESUPA-Centro Universitário l’état du Pará
[2] Cours de premier cycle médical CESUPA-Centro Universitário l’état du Pará
[3] Cours de premier cycle médical CESUPA-Centro Universitário l’état du Pará
[4] Cours de premier cycle médical CESUPA-Centro Universitário l’état du Pará
[5] Biologiste. Docteur en sciences-génétique biologique zone de Concentration. Professeur et chercheur à le Centro Universitário do Pará-CESUPA
[6] Maîtrise en neurosciences et comportement. Santé gestion spécialiste et affaires gestion thérapeute en réadaptation physique. Directeur marketing et directeur des ressources humaines.
[7] Doctorat en psychanalyse clinique, post doctorant en psychanalyse clinique et maîtrise en bioéthique, directeur du centre de recherche et études supérieures, entraîneur et professeur de cours de MBA en entreprise
[8] Biologiste, Master en biologie environnementale. Docteur en médecine tropicale maladies. Enseignant chercheur à l’Université fédérale du Pará – UFPA. Chercheur et développeur du Centre pour la médecine tropicale UFPA (NMT. UFPA).