ARTIGO DE REVISÃO
LIMA, Bruna Roberto de [1], LIMA, Douglas de [2], CORDEIRO, Maicon Luiz Borges [3], SILVA, Kleyson da [4], LIMA, Felipe Bueno [5], MAESTRI, Juliana Sousa [6]
LIMA, Bruna Roberto de. Et al. Efeito cardiovascular dos coxibes: revisão de literatura. Revista Científica Multidisciplinar Núcleo do Conhecimento. Ano 06, Ed. 04, Vol. 05, pp. 05-16. Abril. ISSN: 2448-0959, Link de acesso: https://www.nucleodoconhecimento.com.br/veterinaria/efeito-cardiovascular, DOI: 10.32749/nucleodoconhecimento.com.br/veterinaria/efeito-cardiovascular
RESUMO
Os anti-inflamatórios não esteróidais (AINEs), inibidores seletivos da ciclo-oxigenase-2 (COXIBEs), são os medicamentos de maior escolha atualmente. Eles são utilizados no tratamento da dor, hipertermia, artrite reumatoide, osteoartrite e edema. Enquanto os AINEs não seletivos são mais potentes na inibição da COX-1, os COXIBEs provocam menos efeitos colaterais gastrointestinais, porém não possuem ação antitrombótica por causar desequilíbrio na produção de prostaciclina e tromboxanos. Consequentemente, podem causar efeitos adversos, dentre os quais podemos destacar hipertensão arterial, injúria renal, e maior probabilidade de aglomeração plaquetária. Dessa forma, objetivou-se demonstrar através desse trabalho o mecanismo de ação dos COXIBEs no processo inflamatório e seus efeitos adversos. Para isso foi realizada uma revisão de literatura nas bases de dados do Google Acadêmico e Periódicos Capes por meio das expressões: processo inflamatório, mecanismo de ação e efeitos adversos dos COXIBEs. A partir das informações obtidas por meio da revisão de literatura pode-se concluir que, apesar dos efeitos adversos, os COXIBEs são medicamentos seguros, desde que sejam utilizados com cautela em pacientes com doenças pré-existentes.
Palavras-chave: AINEs, ciclo-oxigenase, COXIBEs, processo inflamatório, efeitos adversos.
1. INTRODUCÃO
Os anti-inflamatórios não-esteroides (AINES) são medicamentos de maior prescrição em todo mundo, sendo muito utilizados em tratamento de inflamações, controle de dor aguda e crônica, hipertermia, artrite reumatoide, osteoartrite e edema, em pacientes humanos e animais (KIM; GIORGI, 2013; BELUQUE, 2014).
Eles atuam inibindo a síntese de mediadores químicos e da enzima ciclooxigenase (COX), influenciando a ação de prostaglandina (PG), prostaciclina (PGI2) e tromboxano A2 (TxA2), componentes importantes na gênese da dor e inflamação (BORGES et al., 2012; KIM; GIORGI, 2013).
Atualmente os AINEs são classificados em não seletivos (convencionais ou clássicos), sendo esses os mais antigos e conhecidos, e os seletivos para COX-2 ou COXIBEs. Após diferenciação das duas isoformas de COX-1 e COX-2, em 1990, foi possível analisar o mecanismo de ação como os efeitos colaterais dos AINEs (BELUQUE, 2014). A COX-1 é uma enzima envolvida em processos fisiológicos, como proteção da mucosa gastrointestinal e vasodilatação renal, enquanto a COX-2 é uma enzima que se eleva em processos inflamatórios. Dessa maneira, foram desenvolvidos compostos seletivos para inibir a COX-2 (COXIBEs), com objetivo de melhorar a eficiência antiinflamatória com maior segurança para a musosa gástrica (BORGES et al., 2012).
Nos últimos tempos, vem sendo questionada a segurança do uso de AINEs na rotina clínica, principalmente dos inibidores seletivos da COX-2. Alguns estudos revelam a possível interação entre os inibidores COX-2 seletivos e seus efeitos adversos sobre o sistema cardiovascular, sendo frequentemente associados ao risco de trombose (BAUTLONI, 2010; BELUQUE, 2014).
2. REVISÃO DE LITERATURA
2.1 MECANISMO DE AÇÃO
O ácido araquidônico, classificado como um ácido graxo essencial, tem origem da conversão do ácido linoleico derivado da dieta alimentar. Este ácido graxo, precursor dos eicosanoides, é mantido em quantidade reduzida na célula. Sua liberação na membrana plasmática ocorre através da enzima fosfolipase A2, que ativa uma cascata metabólica que inicia com a ação da prostaglandina G/H sintaxe, conhecida como ciclooxigenase (COX). Tanto a COX-1 como a COX-2 originam a PGH2, um endoperóxido de prostaglandina instável formado a partir do ácido araquidônico (MENDES et al., 2012; TAVARES, 2012).
Através da prostaglandina (PG) H2, são produzidas várias prostaglandinas: PGI2, PGD2, PGE2 PGF2α-, e TxA2. De acordo com Batlouni (2009) e Mendes et al., (2012) as duas isoformas da ciclooxigenase possuem códigos genéticos diferentes. Enquanto a COX-1 apresenta-se constantemente em grande parte dos tecidos, a COX-2 é induzida em processos inflamatórios (Figura 1).
Figura 1: Esquema relacionado aos efeitos da ativação de COX-1 e COX-2
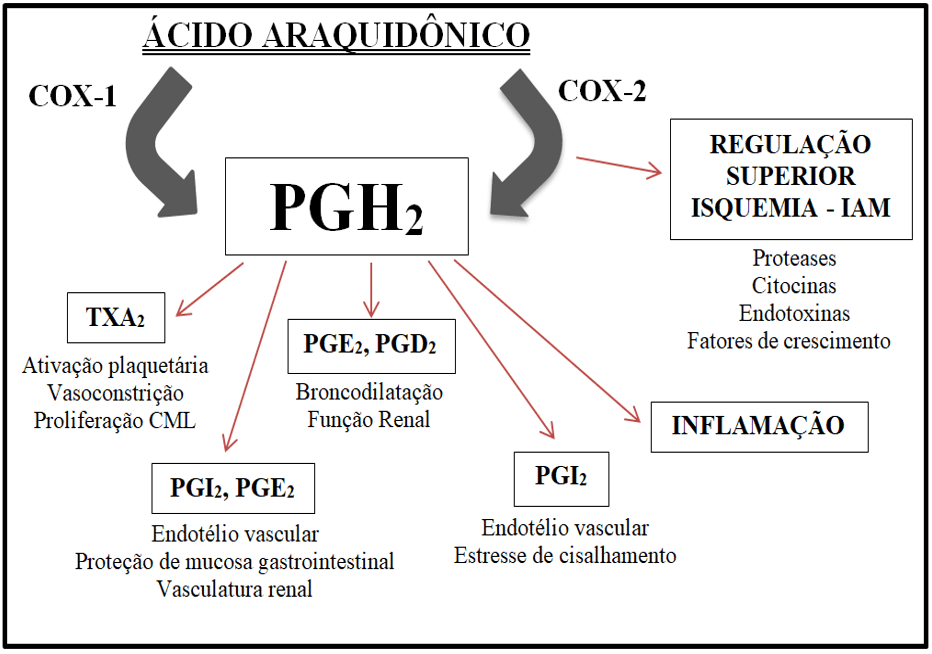
De modo geral, a COX-2 origina prostanoides (prostaglandinas indutoras) responsáveis pelos sinais característicos de inflamação: calor, rubor, edema e hiperalgesia. Também está presente nas células vasculares endoteliais como resposta ao estresse de cisalhamento, produzindo potente vasodilatação, inibição da agregação plaquetária e inibição da proliferação de células musculares lisas dos vasos. A ação dos prostanoides ocorre por meio de receptores acoplados a proteína G, provocando ativação de diferentes vias de sinalização no interior das células (ARAUJO et al., 2005; TAVARES, 2012; BELUQUE, 2014).
A inibição seletiva da COX-2 pode resultar em diminuição da quantidade de prostaciclina produzida no endotélio, sem alterar a produção plaquetária de TxA2, causando um desequilíbrio dos prostanoides hemostáticos que pode elevar ao risco de trombose e eventos cardiovasculares (BATLOUNI, 2009; BORGES et al., 2012; TAVARES, 2012). O estudo de Batlouni (2009) demonstrou efeitos cardioprotetores da COX-2 durante a fase tardia do pré-condicionamento do miocárdio.
Segundo Beluque (2014), as duas isoformas apresentam diferenças estruturais no local ativo. Somente a COX-2 forma pontes de hidrogênio em conjunto com os resíduos de arginina na posição 120, adjacente ao canal hidrofóbico, inibindo a ligação dos ácidos graxos do substrato ao local ativo. Assim, os COXIBEs realizam ação inibitória competitiva pelo local ativo da COX, sem interferência na função da peroxidase (TAVARES, 2012).
Alguns exemplos de COXIBEs que estão disponíveis para utilização em animais de companhia incluem o firocoxib (Previcox®; Meriel), robenacoxib (Onsior®, Novartis), cimicoxib (Cimalgex®; Vetoquinol) e mavacoxib (Trocoxil®; Pfizer) (CARMICHAEL, 2011; FANTONI, 2019).
2.2 AÇÕES FARMACOLÓGICAS
Segundo Borges et al. (2012) e Beluque (2014), é necessário o conhecimento da variabilidade da ação das duas isoformas da COX para entender sua toxicidade.
Sabe-se que a COX-1 é expressa constantemente na maioria dos tecidos, possuindo suma importância na manutenção do estado fisiológico normal, como o que ocorre na proteção da mucosa gastrointestinal, no controle do fluxo sanguíneo renal, nas funções pulmonares, reprodutivas, cardiovasculares e do sistema nervoso central. Desde a década de 60, os AINEs não seletivos foram introduzidos na prática clínica. Como representante desta classe, temos o ácido acetilsalicílico, o qual reduz à produção plaquetária de TXA2, devido ao bloqueio da COX-1, prevenindo desta forma a trombose arterial (BORGES et al., 2012; MENDES et al., 2012 BELUQUE, 2014).
Em contra partida, a indução da COX-2 é estimulada por citocinas, endotoxinas e por fatores de crescimento, originando as prostaglandinas indutoras de edema, rubor, febre e hiperalgesia. Sendo assim, os AINES seletivos da COX-2 aumentam o risco cardiovascular por não bloquear a formação de TXA2, não exercendo ação antiplaquetária. Isso eleva o risco de aterogênese focal nos locais de bifurcação vascular (BORGES et al., 2012; MENDES et al., 2012).
Nos estudos de Borges et al. (2012), correlacionando efeitos de COX-1 e COX-2, a potência inibitória de COX-1 pelo ácido acetilsalicílico é cerda de 166 vezes maior, justificando sua ação antitrombótica. Já os COXIBEs possuem menores efeitos colaterais gastrointestinais quando comparados aos AINEs não seletivos.
A prostaciclina, PGE2 e PGD2, geradas em várias regiões dos rins por ação da COX-1, diminuem a resistência vascular renal por seu efeito vasodilatador. Isso favorece a perfusão do órgão, levando à redistribuição do fluxo sanguíneo do córtex renal para os néfrons, prevenindo a deterioração funcional aguda dos rins (BORGES et al., 2012; MENDES et al., 2012).
Esta ação autorregulatória das prostaglandinas é de extrema importância principalmente em situações de redução da perfusão renal, como o que ocorre em casos de insuficiência cardíaca e de hipovolemia. Nestas situações, normalmente ocorre a ativação do sistema nervoso autônomo simpático (SNA simpático), que realiza o aumento do tônus vascular, e do sistema renina-angiotensina-aldosterona (SRAA), resultando em retenção de sódio e água, com o objetivo de aumentar o fluxo sanguíneo circulante e da pressão arterial sistêmica (BORGES et al., 2012). Porém, os AINEs diminuem estes efeitos natriuréticos e diuréticos, o que é deletério nestes casos de baixa perfusão renal (Figura 2).
Figura 2: Esquema relacionado aos efeitos da ativação de COX-1 e COX-2
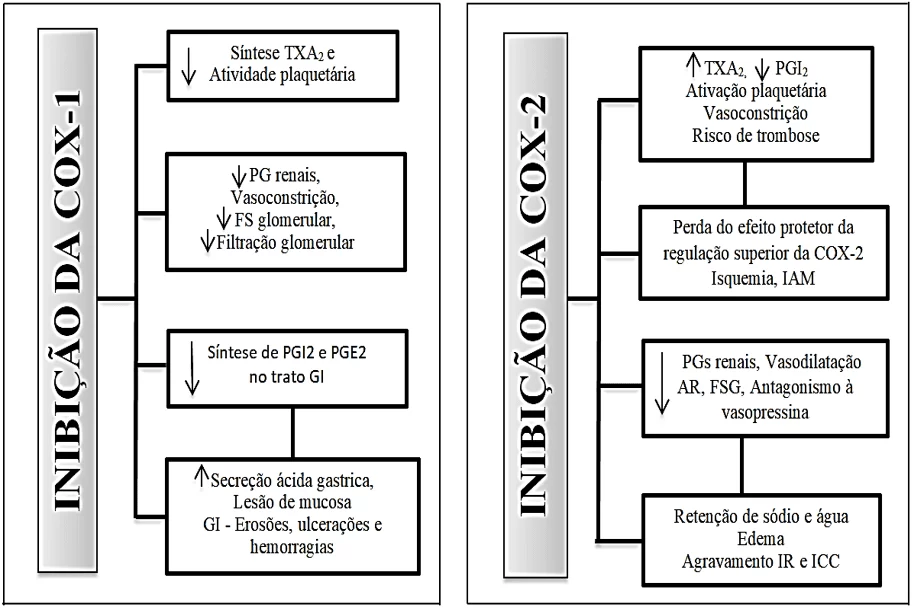
A dose recomendada para tratamento de doenças crônicas utilizando COXIBEs varia de acordo com o fármaco: firocoxib – 5 mg/kg SID; robenacoxib – 1 mg/kg SID; cimicoxib – 2 mg/kg; mavacoxib– 2mg/kg mensalmente (CARMICHAEL, 2011).
2.3 EFEITOS ADVERSOS
Os COXIBEs foram desenvolvidos inicialmente com a finalidade de reduzir os efeitos gastrointestinais indesejáveis dos AINEs não seletivos. No entanto, a inibição da COX-2 pode provocar diversos efeitos adversos, tanto no sistema cardiovascular como na função renal, entre outros com menor relevância clínica (BATLOUNI, 2010; TAVARES, 2012).
2.3.1 EFEITOS GASTROINTESTINAIS
Os AINEs não seletivos possuem vários efeitos adversos sobre o sistema gastrointestinal já comprovados cientificamente tais como: dor abdominal, náuseas, anorexia, úlceras gástricas, úlceras duodenais e hemorragia gastrointestinal. Verifica-se maior incidência de lesões gástricas do que duodenais (BORGES et al., 2012). Estes sinais se manifestam comumente em tratamentos crônicos, mas também podem ser constatados já na primeira administração do fármaco (SILVA; PERASSOLO; SUYENAGA, 2010).
As lesões gastrointestinais podem ser provocadas por ação tópica junto à mucosa ou devido aos efeitos sistêmicos relacionados a inibição da isoenzima COX-1 tais como: redução do fluxo sanguíneo local, aumento da secreção de ácido clorídrico, redução da síntese de glutation, muco e bicarbonato (HILÁRIO; TERRERI; LEN, 2006).
A nível tópico são as características ácidas dos AINES que provocam irritação de mucosas. Os AINEs podem agravar ainda situações de colite ulcerosa e Doença de Crohn (BATLOUNI, 2010; RIGATO, 2011).
Já os inibidores de COX-2 demonstram sintomas gastrointestinais moderados (dispepsia, náusea), mas potenciais efeitos adversos na função renal e prováveis consequências cardiovasculares e na fertilidade (TAVARES, 2012).
2.3.2 EFEITOS NA PRESSÃO ARTERIAL, EFEITOS RENAIS E RENOVASCULARES
Os AINEs comprometem a função renal, em especial nos pacientes que já apresentam redução de perfusão, pois ao bloquearem as prostaglandinas, ocorre redução dos mecanismos contra-regulatórios de reabsorção de sódio e água no túbulo renal. Isso ocorre devido a redução da produção de PGE2 e PGI2, causando aumento da tensão sobre a parede arterial e formação de edema, o que pode levar à insuficiência cardíaca e insuficiência renal aguda (RIGATO, 2011). Os COXIBEs podem também agravar a hipertensão arterial e interferir na ação de fármacos hipotensores (MENDES et al., 2012).
As complicações renais induzidas pelos AINEs são reversíveis com a supressão dos fármacos (BATLOUNI, 2010).
2.3.3 EFEITOS CARDIOVASCULARES
Em pacientes com doença renal pré-existente, o uso de COXIBEs aumenta o risco de desenvolvimento de doenças cardiovasculares. Estes fármacos estão associados ao aumento de risco de acidente vascular cerebral (AVC) (BALBINO, 2011). Isso ocorre devido a diminuição da produção endotelial de PGI2, enquanto a produção de TxA2 nas plaquetas se mantêm inalterada, o que reduz o efeito antitrombótico e aumenta a ativação, adesão e agregação plaquetária (MENDES et al., 2012).
Este desequilíbrio aumenta o risco de trombose e de lesões isquêmicas. Os pacientes medicados com COXIBEs são propensos a desenvolver hipertensão arterial e este é um fator de risco no desenvolvimento de trombose, bem como um fator de risco independente para a aterosclerose (CASTRO, 2012).
Um estudo realizado nos Estados Unidos, no ano de 2006, demonstrou que o rofecoxibe (Vioxx®), um potente inibidor da COX-2 apresentou significante aumento do risco de eventos cardiovasculares, motivo pelo qual foi retirado de circulação em 2004 (BRUEGGEMANN et al., 2010).
Em contrapartida, Schilling (2016) demonstrou em seu estudo que o celecoxibe (Celebrex® e Celebra®), não ocasiona o aumento de risco de insuficiência cardíaca mesmo que este medicamento iniba a enzima COX-2. Os efeitos cardiovasculares e renais dos COXIBEs dependem do tempo de exposição e da dose administrada, entre outros fatores (CASTRO, 2012).
2.3.4 OUTROS EFEITOS
Os COXIBES podem provocar outros efeitos adversos como tontura, cefaleia, sintomas de gripe, fadiga, ansiedade e insônia. Particularmente o celecoxib pode ser responsável por reações cutâneas, como a urticária, dermatite fotoalérgica, erupções cutâneas e em casos mais graves e possivelmente fatais, dermatite esfoliativa, síndrome de Steven Johnson e necrólise epidérmica tóxica (BATLOUNI, 2010; RIGATO, 2011).
3. CONSIDERAÇÕES FINAIS
Os inibidores seletivos da COX-2 são utilizados com frequência na rotina clínica devido sua eficácia antiinflamatória e seu menor efeito adverso sobre o trato gastrointestinal, quando comparado aos AINEs não seletivos. No entanto, em pacientes humanos que utilizaram os COXIBEs para tratamento de enfermidades inflamatórias crônicas, observou-se elevada taxa de distúrbios cardiovasculares.
Desta forma, podemos afirmar que o uso dos COXIBEs é seguro, desde que utilizado com cautela, principalmente em pacientes com histórico prévio de baixa perfusão renal e doenças cardiovasculares, pois seus efeitos podem levar à complicações clínicas como injúria renal e alterações tromboembólicas. O presente trabalho destaca a importância da realização de maiores estudos sobre os efeitos adversos destes fármacos em medicina veterinária.
REFERÊNCIAS
ARAUJO, Leila Fernandes.; SOEIRO, Alexandre de Matos.; FERNANDES, Juliano de Lara.; SERRANO JÚNIOR, Carlos Vicente. Eventos cardiovasculares: um efeito de classe dos inibidores de COX-2. Arquivos brasileiros de cardiologia, São Paulo, v.85, n.3, p.222-229, 2005. Disponível em: <http://www.scielo.br/scielo.php?script=sci_arttext&pid=S0066-782X2005001600016&lng=en&nrm=iso>. Acesso em: 17 mai. 2019.
BALBINO, Carlos Alberto. Anti-inflamatórios: uma compreensão total. Revista Pharmacia Brasileira, n.81, 2011. Disponível em:<http://www.cff.org.br/sistemas/geral/revista/pdf/131/030a045_entrevista_dr_balbino.pdf>. Acesso em: 2 jun. 2019.
BATLOUNI, Michel. Anti-inflamatórios não esteroides: Efeitos cardiovasculares, cérebro-vasculares e renais. Arquivo Brasileiro de Cardiologia, v.94, n.4, p.556-563, 2010. Disponível em: <http://www.scielo.br/scielo.php?script=sci_arttext&pid=S0066-782X2010000400019&lng=en&nrm=iso>. Acesso em: 17 mai. 2019.
BELUQUE, Tamyris. Efeitos da inibição da cox-2 no sistema cardiovascular de cães. 2014. 19 p. Trabalho Científico (Graduação) – Faculdade de Medicina Veterinária de Araçatuba, Universidade Estadual Paulista Júlio de Mesquita Filho, Araçatuba, 2014. Disponível em: <https://repositorio.unesp.br/handle/11449/124247>. Acesso em: 16 mai. 2019.
BORGES, Maria; MELCHERT, Alessandra; MARINI FILHO, Rivaldo; LAPOSY, Cecília Braga; ALEGRE, Beatriz Cristina Conceição Porto; SILVA, Karine Ramires. Função renal, hepática e cardíaca de cães hígidos sob terapia prolongada com celecoxibe. Ciência Rural, Santa Maria, v.42, n.10, 2012. Disponível em: <https://www.redalyc.org/html/331/33124570014/>. Acesso em: 18 mai. 2019.
BRUEGGEMANN, Lioubovi.I; MANI, Bharath K; MACKIE, Alexander R; CRIBBS, Leanne L; BYRON, Kenneth L. Novel Actions of Nonsteroidal Anti-Inflammatory Drugs on Vascular Ion Channels: Accounting for Cardiovascular Side Effects and Identifying New Therapeutic Applications. Molecular and Cellular Pharmacology, v.2, n.1, p.15, 2010. Disponível em: <https://www.ncbi.nlm.nih.gov/pmc/articles/PMC2915785/>. Acesso em: 1 jun. 2019.
CARMICHAEL, Stuart. Uso clínico de agentes anti-inflamatórios não esteróides (AINEs): a posição atual. European Journal of Companion Animal Practice, v.21, n.2, p.171-177, 2011. Disponível em: <https://www.zora.uzh.ch/id/eprint/123830/1/fecava_21.2.pdf#page=51>. Acesso em: 23 jul. 2020.
CASTRO, Sara Daniela Fonseca de. Hemorragia digestiva alta associada ao consumo de anti-inflamatórios não-esteróides e de ácido acetilsalicílico. 2012. 51p. Dissertação (Mestrado) – Faculdade de Ciências da Saúde, Universidade da Beira Interior, Covilhã, 2012. Disponível em: <https://ubithesis.ubi.pt/bitstream/10400.6/1075/1/Disserta%C3%A7%C3%A3o%20Sara%20Castro.pdf>. Acesso em: 2 jun. 2019.
FANTONI, Denise Tabacchi. Controle da dor em cães e gatos. Rev. Informativo Técnico Vetnil, n.4, 2019. Disponível em: <https://vetsmart-parsefiles.s3.amazonaws.com/f516c39b8cd0d651a4d04373485f2e08_vetsmart_admin_pdf_file.pdf>. Acesso em: 23 jul. 2020.
HILÁRIO, Maria Odete Esteves; TERRERI, Maria Teresa; LEN, Cláudio Arnaldo. Antiinflamatório não-hormonais: inibidores da ciclooxigenase 2. Jornal de Pediatria, Porto Alegre, v.82, n.5, nov. 2006. Disponível em: <hyyp://dx.doi.org/10.1590/S0021-75572006000700011>. Acesso em: 15 ago. 2020.
KIM, Tae-Wen; GIORGI, Mario. A brief overview of the coxib drugs in the veterinary field. American Journal of Animal and Veterinary Sciences, Pisa – Itália, v.8, n.2, p.89-97, 2013. Disponível em: <https://www.researchgate.net/publication/286342928_A_brief_overview_of_the_coxib_drugs_in_the_veterinary_field>. Acesso em: 1 jun. 2019.
MENDES, Regina Tainá; STANCZYK, Cassiano Pereira; SORDI, Regina; OTUKI, Michel Ffleith; SANTOS, Fábio André; FERNANDES, Daniel. Inibição seletiva da ciclo-oxigenase-2: riscos e benefícios. Revista Brasileira de Reumatologia, São Paulo, v.52, n.5, p.774-782, 2012. Disponível em: <http://www.scielo.br/scielo.php?script=sci_arttext&pid=S0482-50042012000500011&lng=en&nrm=iso>. Acesso em: 17 mai. 2019.
RIGATO, Hamilton Modesto. Determinação do perfil farmacocinético de anti-inflamatórios não hormonais aplicado a clínica. 2011. 95p. Tese (Doutorado) – Faculdade de Ciências Médicas, Universidade estadual de Campinas, Campinas, 2011. Disponível em:<http://repositorio.unicamp.br/bitstream/REPOSIP/311495/1/Rigato_HamiltonModesto_D.pdf>. Acesso em: 2 jun. 2019.
SCHILLING, Ray. Arthritis drugs can cause heart failure. Medical Articles by Dr. Ray, 2016. Disponível em: <http://www.askdrray.com/arthritis-drugs-can-cause-heart-failure/>. Acesso em: 2 jun. 2019.
SILVA, Carina Portillho; PERASSOLO, Magda Susana; SUYENAGA, Edina. Benefícios e riscos do uso de coxibes. Revista Eletrônica de Farmácia, v. VII (2), 14-33, 2010. Disponível em: <https://www.researchgate.net/publication/272852700_BENEFICIOS_E_RISCOS_DO_USO_DE_COXIBES>. Acesso em: 7 jun. 2019.
TAVARES, Tânia Isabel Almeida. Riscos e benefícios dos anti-inflamatórios não esteróides inibidores seletivos da ciclo-oxigenase 2. 2012. 61p. Monografia (Mestrado) – Faculdade de Ciências da Saúde, Universidade Fernando Pessoa, Porto, 2012. Disponível em: <http://bdigital.ufp.pt/handle/10284/3749>. Acesso em: 17 mai. 2019.
[1] Graduanda do curso de Medicina Veterinária.
[2] Graduando do curso de Medicina Veterinária.
[3] Graduando do curso de Medicina Veterinária.
[4] Graduando do curso de Medicina Veterinária.
[5] Graduando do curso de Medicina Veterinária.
[6] Mestre em Ciências Biológicas. Especialista em Clínica Médica e Cirúrgica de Pequenos Animais. Aperfeiçoamento nas Áreas de Eletrocardiografia (Grupo de Estudos Incor e Equalis), EcoDopplercardiografia (Profº James Andrade e Naya Cardiologia), Ultrassonografia Doppler (Bionóstic Interage) e Clínica Cardiológica Avançada (UFPR).
Enviado: Março, 2021.
Aprovado: Abril, 2021.

