ARTIGO DE REVISÃO
BUBA, Cibele Madsen [1], HAIDA, Kamila Satomi [2], TANNO, Gisela Andrea Yamashita [3], D’URSO, Francisco Pierozzi [4], MELO, Carlos Eduardo Fernandes Soares de [5]
BUBA, Cibele Madsen. Et al. Tratamento com corticoide intratimpânico na doença de Ménière e seu impacto na qualidade de vida. Revista Científica Multidisciplinar Núcleo do Conhecimento. Ano 04, Ed. 11, Vol. 02, pp. 110-129. Novembro de 2019. ISSN: 2448-0959, Link de acesso: https://www.nucleodoconhecimento.com.br/saude/corticoide-intratimpanico
RESUMO
A Doença de Ménière foi primeiramente relatada em 1861 por Prosper Ménière. A etiologia pode estar associada a processos infecciosos (virais ou bacterianos), anomalias do desenvolvimento do osso temporal, predisposição hereditária ou genética, trauma, doenças autoimunes, entre outras causas. O diagnóstico é primordialmente clínico. É caracterizada por episódios de vertigem, perda auditiva neurossensorial flutuante, plenitude aural e zumbido. O tratamento pode ser cirúrgico ou clínico. O tratamento clínico consiste no alívio dos sintomas através do uso de medicamentos, ainda em avaliação clínica, são eles: diuréticos, vasodilatadores, moduladores de fluxo sanguíneo, bloqueadores de canais de cálcio, antidepressivos, corticoides orais entre outros. Quando o tratamento clínico não apresenta a resolução esperada, o tratamento cirúrgico pode ser indicado como cirurgia do saco endolinfático. O tratamento com corticoide intratimpânico tem sido utilizado como terapia complementar ou adjuvante em pacientes que não responderam ao tratamento com medicação oral. Avalia-se a possibilidade de uma grande melhora na sintomatologia e na qualidade de vida dos pacientes com doença de Ménière, com remissão do cenário clínico e menor intervenção quando comparado ao tratamento cirúrgico. Este estudo tem como objetivo avaliar as implicações do tratamento com corticosteroide intratimpânico em um grupo de pacientes acompanhados no Serviço de Otorrinolaringologia de um hospital público de São Paulo. Utilizamos os questionários desenvolvidos especificamente para tonturas e zumbidos – o Dizziness Handicap Inventory (DHI) e o Tinnitus Handicap Inventory (THI), respectivamente.
Palavras-chave: Doença de Mèniére, Betaistina, Corticoide intratimpânico.
INTRODUÇÃO
A tríade sintomática da Doença de Ménière – perda auditiva, zumbido e vertigem, em episódios recorrentes – foi primeiramente relatada, em 1861, por Prosper Ménière. É uma das mais frequentes labirintopatias, com prevalência de 46 a 200 casos em cada 100 mil indivíduos1. Conforme evidenciado por Munhoz et al, não se nota diferença de distribuição entre os sexos e a manifestação ocorre preponderantemente a partir da quarta década de vida1.
A hidropsia endolinfática (HE) é o achado histopatológico da doença e é caracterizado pela distensão do espaço endolinfático1-3.
A etiologia da HE é variada, podendo estar associada a processos infecciosos (virais ou bacterianos), anomalias do desenvolvimento do osso temporal, predisposição hereditária ou genética, trauma, doenças autoimunes, entre outras causas1–5,10.
O diagnóstico da Doença de Ménière é clínico. Caracteriza-se por perda auditiva flutuante, do tipo neurossensorial, zumbido e plenitude aural e episódios recorrentes de vertigem1–11. Em 1972, foram definidos os parâmetros para o diagnóstico clínico da Doença de Ménière pelo Comitê de Audição e Equilíbrio da Academia Americana de Otorrinolaringologia e Cirurgia de Cabeça e Pescoço (AAO-HNS). Em 1995, esses critérios foram aprimorados1–11. De acordo com os novos critérios da AAO-HNS, indivíduos com dois ou mais episódios espontâneos de vertigem, que durem 20 minutos ou mais, com perda auditiva documentada em pelo menos um episódio e presença de zumbido ou plenitude aural são classificados clinicamente como portadores de Doença de Ménière definida1–11. O Comitê de Classificação da Sociedade Bárany, em 2015, instituiu alguns critérios para a Doença de Ménière definida e para a Doença de Ménière provável1,12. A doença definida foi caracterizada por dois ou mais episódios de vertigem, cada um com duração de 20 minutos até 12 horas; por avaliação audiológica evidenciando perda auditiva neurossensorial antes, durante ou após o episódio de vertigem e por sintomas auditivos flutuantes – hipoacusia, zumbido ou plenitude aural1,12. A doença provável foi determinada por dois ou mais episódios de vertigem ou tontura, que durem entre 20 minutos e 24 horas cada e sintomas auditivos flutuantes na orelha ipsilateral1,12. A certeza diagnóstica só será possível por meio do estudo do osso temporal após o óbito13.
As audiometrias sequenciais acabam por definir o diagnóstico, uma vez que evidenciam a flutuação da audição. A perda auditiva neurossensorial ocorre inicialmente nos sons mais graves e evolui gradativamente para o comprometimento das demais frequências6.
O tratamento pode ser clínico ou cirúrgico14. O tratamento clínico consiste no alívio dos sintomas através do uso de medicamentos, ainda em elucidação clínica, são eles: diuréticos, vasodilatadores, moduladores de fluxo sanguíneo, bloqueadores de canais de cálcio, antidepressivos, corticoides orais entre outros14.
O tratamento com corticoide intratimpânico (CI) vem sendo utilizado como terapia complementar ou adjuvante, em pacientes refratários ao tratamento com medicação via oral. Avalia-se a possibilidade de grande melhora da sintomatologia e da qualidade de vida dos pacientes com Doença de Ménière, com remissão do quadro clínico e menor intervenção quando comparado ao tratamento cirúrgico. A injeção intratimpânica de corticoide oferece potencial de uma terapia órgão especifica, administrada diretamente sobre a membrana da janela redonda evitando todos os efeitos adversos da terapia com corticoide sistêmico.
Em 1990, foi elaborado um questionário específico para tontura, o Dizziness Handicap Inventory (DHI) (quadro 1), visando avaliar a autopercepção dos efeitos incapacitantes, funcionais, emocionais e físicos, provocados pela tontura5,16. Já o Tinnitus Handicap Inventory (THI) (quadro 2), por sua vez, é um questionário que foi desenvolvido por Newman et al.5,17 em 1996, sendo constituído por 25 perguntas, com um escore que varia de 0 a 100 e quanto maior o escore, maior é a repercussão do zumbido na qualidade de vida do paciente. Ambos foram adaptados para a língua portuguesa e podem ser facilmente aplicados na prática clínica para a avaliação dos pacientes com tontura e zumbido, para a quantificação do incômodo relacionado a estes sintomas e para avaliar a resposta ao tratamento otoneurológico, seja ele medicamentoso, cirúrgico e/ou de reabilitação vestibular5.
A identificação dos aspectos mais afetados nos pacientes em acompanhamento pode auxiliar na escolha da terapia mais adequada.
Quadro 1. Dizziness Handicap Inventory (DHI) brasileiro
Quadro 2. Tinnitus Handicap Inventory (THI) brasileiro
MÉTODO
Trata-se de uma série de seis pacientes com diagnóstico definido da Doença de Ménière, conforme os critérios diagnósticos da Bárány Society, com refratariedade ao tratamento medicamentoso com betaistina (144 mg/dia) e submetidos à corticoterapia intratimpânica (Dexametasona) conforme protocolo de tratamento já utilizado neste serviço de otorrinolaringologia previamente (aplicação semanal, com intervalo de sete dias, durante três semanas consecutivas). Houve aprovação do estudo por comitê de ética em pesquisa (Parecer 2.798.783) e os participantes assinaram o termo de consentimento livre e esclarecido. Foram aplicados os questionários de referência (DHI e THI) anteriormente e posteriormente à aplicação do corticoide intratimpânico. O questionário inicial foi realizado antes da primeira aplicação do corticoide, quando o paciente já estava em tratamento com betaistina em dose plena por um período de no mínimo 60 dias. O questionário referente à avaliação da sintomatologia foi aplicado aproximadamente 30 dias após a última e terceira dose da Dexametasona intratimpânica (DI).
CRITÉRIOS DE INCLUSÃO
Foram incluídos neste estudo pacientes com Diagnóstico definido da Doença de Ménière, conforme os critérios diagnósticos da Bárány Society: apresentar 2 ou mais episódios de vertigem com duração de 20 minutos a 12 horas; ter exame audiológico com perda neurossensorial documentada em pelo menos um episódio de vertigem (antes, durante ou depois); apresentar sintomas auditivos flutuantes (zumbido, plenitude aural ou hipoacusia) e ter sintomas não explicados por outra patologia vestibular. Os pacientes que participaram do estudo deveriam ter registrados em prontuários exames de audiometria, tomografia computadorizada de alta resolução ou ressonância nuclear magnética, laboratoriais, eletrococlegrafia e avaliação otoneurológica. A realização de tratamento com três injeções de CI (Dexametasona), em semanas consecutivas também foi preponderante para a inclusão no presente estudo.
CRITÉRIOS DE EXCLUSÃO
Foram excluídos pacientes com diagnóstico de qualquer patologia cocleovestibular; que tenham cirurgia otológica prévia e/ou patologias de origem central e aqueles que se negaram a participar da pesquisa. Pacientes menores de 18 anos e/ou com incapacidade de compreender o termo de consentimento livre e esclarecido também foram excluídos deste estudo.
APRESENTAÇÃO DOS CASOS
1º Paciente: Sexo feminino, 56 anos, hipertensa e dislipidêmica. Histórico de tontura rotatória intensa, plenitude aural e zumbido bilateralmente, há 3 anos. Diagnóstico unilateral à esquerda definido da Doença de Ménière de acordo com o Comitê de Classificação da Sociedade Bárany.
2º Paciente: Sexo feminino, 60 anos, hipertensa e dislipidêmica, em acompanhamento no ambulatório de Otoneurologia do Hospital do Servidor Público Municipal de São Paulo. Previamente acompanhada em outro serviço, a paciente referia histórico de tontura rotatória e incapacitante, há aproximadamente 2 anos, com associação de zumbido e hipoacusia à direita. As crises tinham duração de horas com vômito intenso referido. Confirmado diagnóstico unilateral à direita definido da Doença de Ménière de acordo com o Comitê de Classificação da Sociedade Bárany.
3º Paciente: Sexo feminino, 48 anos, diabética do tipo II, em acompanhamento no ambulatório de Otoneurologia do Hospital do Servidor Público Municipal de São Paulo. História de tontura rotatória, zumbido e plenitude aural bilateralmente, há 3 anos, com sintomas intensificados à direita.
O diagnóstico foi definido da Doença de Ménière bilateralmente, conforme o Comitê de Classificação da Sociedade Bárany.
4º Paciente: Sexo feminino, 51 anos, hipertensa, em acompanhamento no ambulatório de Otoneurologia do Hospital do Servidor Público Municipal de São Paulo. Referia quadro clínico de hipoacusia e zumbido intenso referido à esquerda, há aproximadamente 2 anos. Não apresentava tontura importante, relatando ser do tipo rotatória e esporádica. O diagnóstico unilateral à esquerda definido da Doença de Ménière foi evidenciado conforme orientações do Comitê de Classificação da Sociedade Bárany.
5º Paciente: S.R.G.S., sexo feminino, 55 anos, previamente hígida. Histórico de vertigem esporádica com duração de segundos, há aproximadamente 3 anos, associada à plenitude aural e zumbido bilaterais. Realizado diagnóstico definido à direita da Doença de Ménière de acordo com o Comitê de Classificação da Sociedade Bárany.
6º Paciente: Sexo masculino, 55 anos, sem comorbidades. Referindo sintomatologia há 3 anos de vertigem com duração de horas, hipoacusia bilateral, zumbido bilateral – mais intenso à direita –, e plenitude aural intermitente – também mais evidente à direita. Classificado como diagnóstico definido unilateral à direita da Doença de Ménière de acordo com o Comitê de Classificação da Sociedade Bárany.
DISCUSSÃO
Na Doença de Ménière, os pacientes referem dificuldade de concentração mental e fadiga diretamente relacionados ao zumbido e à tontura. A insegurança física gerada pelos sintomas pode resultar no medo de sair sozinho, irritabilidade, temor do diagnóstico de uma doença séria, perda de autoconfiança, além de pânico, depressão e ansiedade5,18–20. As doenças que afetam o sistema vestibular implicam não apenas em problemas físicos e emocionais, mas também na incapacidade para o desempenho das atividades socias, profissionais e domésticas, resultando em piora importante da qualidade de vida (QV) e da saúde mental dos pacientes 21,22.
Os testes objetivos, tais como exames de imagem, audiometria, eletrococleografia, avaliação otoneurológica e laboratorial, são incapazes de avaliar os danos emocionais, psicológicos e o impacto sobre o cotidiano dos pacientes que enfrentam o diagnóstico de Ménière e é nesse contexto que os questionários são preponderantes no acompanhamento desses pacientes5,23.
A Organização Mundial de Saúde apresenta a definição de QV como “a percepção do indivíduo de sua posição na vida, no contexto de sua cultura e sistema de valores dos quais ele participa e em relação aos seus objetivos, expectativas e preocupações”24.
Foram desenvolvidos os questionários, primordialmente na língua inglesa, para avaliação da QV nos pacientes em tratamento para patologias que acometem o labirinto. Na década de 1990, Jacobson e Newman17 criaram um questionário específico para tontura, o DHI, tendo como meta avaliar a autopercepção dos efeitos incapacitantes impostos pela tontura25.
O DHI e o THI foram os questionários escolhidos para adaptação cultural para o Português Brasileiro, uma vez que mostraram-se instrumentos confiáveis e utilizados em vários estudos 5,25–33.
A identificação dos aspectos mais afetados nos pacientes com tontura é primordial na escolha da terapia mais adequada5,34. Além disso, o DHI e o THI vem sendo aplicados como métodos de avaliação dos efeitos e resultado do tratamento, seja ele cirúrgico, medicamentoso ou de reabilitação vestibular 5,26,28,35.
O presente estudo teve como objetivo comparar a QV dos pacientes, através do uso dos questionários THI e DHI, em tratamento prévio com dose plena de betaistina antes da aplicação de CI, em relação aos pacientes após a aplicação de CI.
Os questionários foram aplicados aos pacientes em dois diferentes momentos: em tratamento com dose plena de betaistina, anteriormente à aplicação de CI e após a aplicação das 3 doses.
Em comparação à literatura5,25, sobre a aplicação do questionário DHI em labirintopatias, pode-se afirmar que os resultados sobre aspectos físico, funcional e emocional foram bastante semelhantes, apesar do Diagnóstico definido da Doença de Ménière e do tratamento intensivo com altas doses medicamentosas.
Todos os pacientes deste estudo, em tratamento com betaistina e anteriormente à aplicação de CI, relataram em suas respostas ao DHI comprometimento do desempenho de atividades sociais. Estas atividades referem-se aos aspectos funcionais avaliados pelo DHI, já relatados no estudo conduzido por Ganança et al. (2004)5,25, em que se comprova que resultados da pesquisa então realizada vão ao encontro das afirmações de Yardley, Putman18, os quais referiram que muitos pacientes com tontura restringem conscientemente a prática de atividades físicas, viagens e interação social, visando à redução do risco de aparecimento destes sintomas diante de outras pessoas. Os aspectos funcionais segundo o DHI averiguaram a interferência da tontura na capacidade de desempenhar as atividades domésticas, profissionais, de lazer e sociais, e na independência ao se realizar determinadas tarefas como caminhar sem ajuda25.
Ainda segundo Ganança (2004)25, os aspectos emocionais avaliados pelo DHI também se mostraram afetados pela tontura, indicando acometimento da saúde mental dos pacientes na Doença de Ménière, que frequentemente apresentam ansiedade associada a ataques de pânico e sentimentos de despersonalização, ressaltando a relação entre as alterações vestibulares e os aspectos emocionais5,25,36–39.
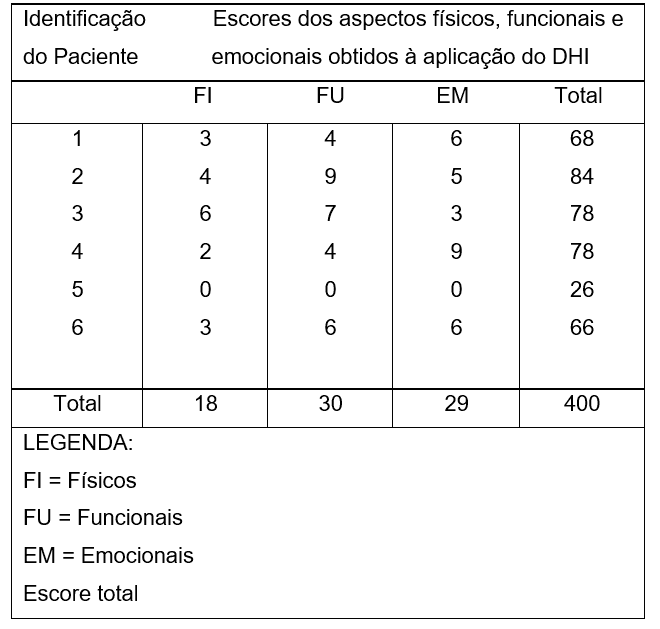
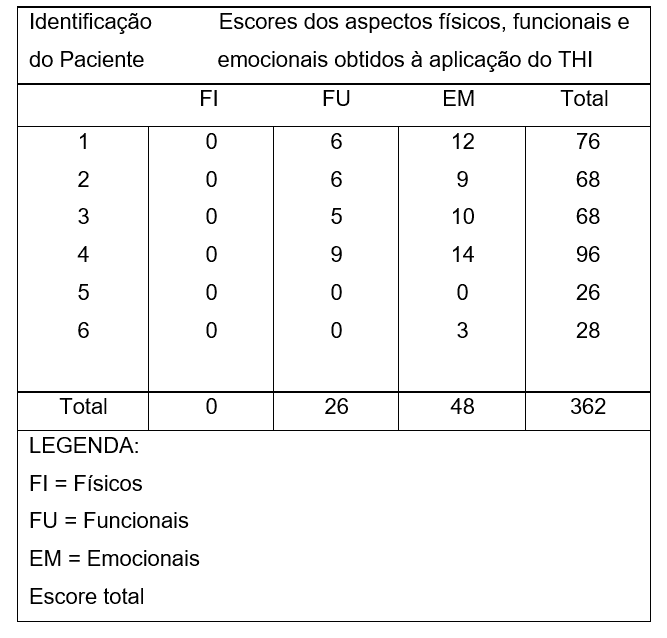
Os pacientes avaliados neste estudo em tratamento com dose plena de betaistina apresentaram, previamente à CI, grande comprometimento físico, funcional e emocional tanto no DHI quanto no THI (quadros 3 e 4).
Quadro 03. Resultados obtidos quanto aos aspectos físicos, emocionais e funcionais e escore total, na aplicação do DHI brasileiro nos pacientes com Doença de Ménière em tratamento com dose plena de Betaistina.
Quadro 04. Resultados obtidos quanto aos aspectos emocionais e funcionais e escore total, na aplicação do THI brasileiro nos pacientes com Doença de Ménière em tratamento com dose plena de Betaistina.
Previamente ao CI e já em tratamento com dose plena de betaistina, dos 6 pacientes acompanhados, 2 apresentaram comprometimento severo; 3, comprometimento catastrófico e somente 1 apresentou grau leve para o DHI. Para o THI, por sua vez, 3 pacientes apresentaram resultado severo, 1 resultado catastrófico e 2 apresentaram resultado leve.
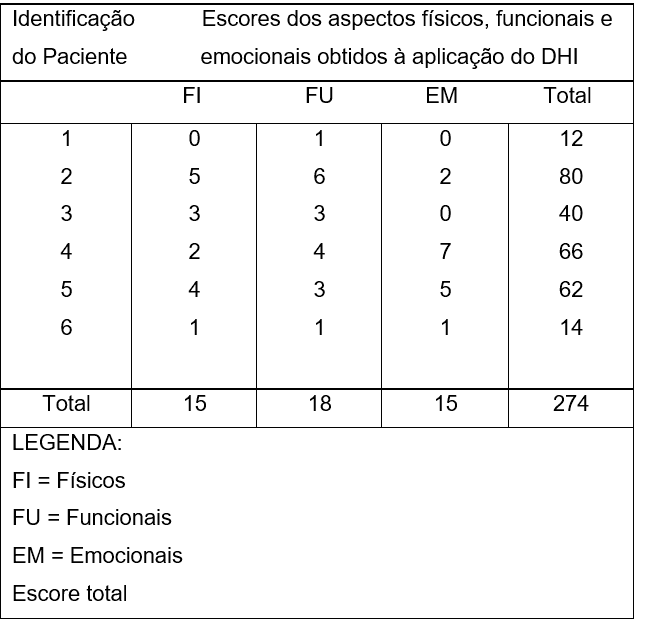
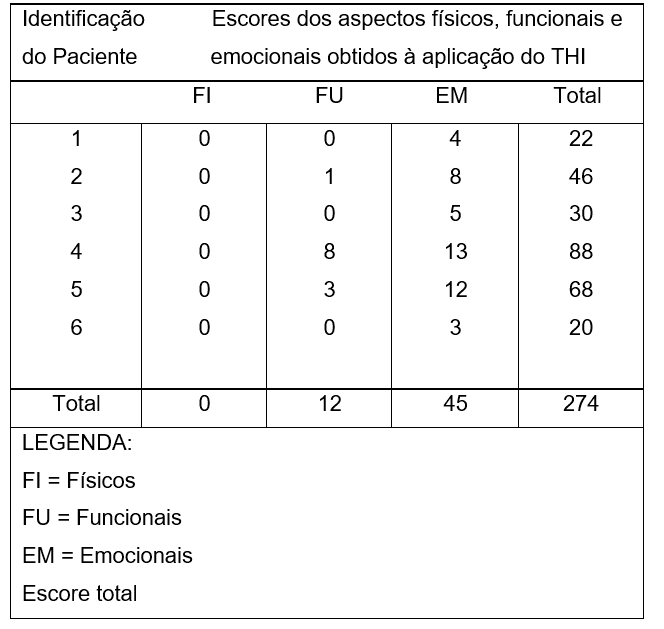
Os questionários foram novamente aplicados aos pacientes deste estudo, 30 dias após a última dose de DI (quadros 5 e 6).
Quadro 05. Resultados obtidos quanto aos aspectos físicos, emocionais e funcionais e escore total, na aplicação do DHI brasileiro nos pacientes com Doença de Ménière após 3 doses de Dexametasona intratimpânica.
Quadro 06. Resultados obtidos quanto aos aspectos emocionais e funcionais e escore total, na aplicação do THI brasileiro nos pacientes com Doença de Ménière após 3 doses de Dexametasona intratimpânica.
Após as 3 doses de CI, para o DHI, 2 pacientes apresentaram resultado desprezível, 1 resultado moderado, 2 apresentaram severo e 1 resultado catastrófico.
Para o THI, por sua vez, foram evidenciados 3 resultados leve, 1 resultado moderado, 1 resultado severo e 1 catastrófico.
Não existem estudos anteriores que possam ser comparados ao uso de CI e a aplicação do DHI e THI.
Apesar de alguns autores inferirem mínima e pouco significativa melhora nos testes objetivos – audiometria, eletrococleografia – para avaliação da Doença de Ménière, o que se pode evidenciar através deste estudo é que há uma melhora relatada por 5 dos 6 pacientes à aplicação do DHI e THI, sendo descrita piora por somente 1 paciente submetido ao tratamento com CI.
Deve-se levar em consideração o caráter subjetivo dos questionários aplicados, sendo as respostas oriundas dos sintomas relatados pelos pacientes.
Há, portanto, a necessidade de avaliar o estado emocional e psicológico dos pacientes, os possíveis ganhos secundários (tais como maior atenção e cuidados dos familiares, readaptação laboral em virtude dos sintomas).
O único caso avaliado em que houve piora dos testes subjetivos foi contraditório às provas objetivas (que evidenciaram melhora em todos os parâmetros) e o paciente mostrava-se visivelmente abalado psicologicamente após a aplicação das injeções de CI.
CONCLUSÃO
Os pacientes com diagnóstico definido da Doença de Ménière habitualmente relatam dificuldade de concentração mental, perda de memória e fadiga, oriundos do zumbido e da tontura. A insegurança física gerada pela tontura e pelo desequilíbrio pode conduzir à irritabilidade, perda de autoconfiança, medo de sair sozinho, receio do diagnóstico de uma doença séria, vergonha das manifestações e sintomas, além de ansiedade, depressão e pânico. Além de gerar problemas físicos e emocionais, a Doença de Ménière pode resultar na incapacidade para o desempenho das atividades profissionais, sociais e domésticas, piorando a qualidade de vida.
O presente estudo evidenciou majoritariamente melhora da sintomatologia e das queixas funcionais e emocionais dos pacientes após o uso de CI em comparação à alta dosagem de betaistina. Ressalta-se a possibilidade de aplicação dos questionários após um maior intervalo de tempo do tratamento com CI, a fim de constatar se tais melhoras persistem por um longo período ou se novas aplicações seriam necessárias.
Contudo, mais estudos são preponderantes para avaliação e elucidação da efetividade terapêutico no uso de DI na Doença de Ménière.
Propiciar melhora da qualidade de vida dos pacientes em tratamento é imprescindível, uma vez que a doença, quando em crises, pode ocasionar alterações emocionais e psicológicas de grande prejuízo.
REFERÊNCIAS
1. Chaves AG, Boari L, Munhoz MSL. Evolução clínica de pacientes com doença de Ménière. Rev. Bras. Otorrinolaringol. 2007, 73(3): 346-350. Disponível em: http://www.scielo.br/scielo.php?script=sci_arttext&pid=S0034-72992007000300009&lng=en. http://dx.doi.org/10.1590/S0034-72992007000300009.
2. Munhoz MSL, Silva MLG, Ganança MM, Caovilla HH, Frazza MM. Hydrops endolinfático e doença de Ménière. In: Silva MLG, Munhoz MSL, Ganança MM, Caovilla HH Quadros clínicos otoneurológicos mais comuns. São paulo: Atheneu; 2000. p. 21–35.
3. Thai-Van H, Bounaix M, Fraysse B. Ménières Disease – Pathophysiology and Treatment Drugs. Drugs. 2001;61(8):1089–102.
4. Paparella MM. Pathogenesis and pathophysiology of Meniere’s disease. Acta Otolaryngol (Stockh). 1991;111(sup485):26–35.
5. Castro ASO, Gazzola JM, Natour J, Ganança FF. Versão brasileira do Dizziness Handicap Inventory. Pró-Fono R. Atual. Cient. 2007; 19(1): 97-104. Disponível em: http://www.scielo.br/scielo.php?script=sci_arttext&pid=S0104-56872007000100011&lng=en. http://dx.doi.org/10.1590/S0104-56872007000100011.
6. Atherino CCT, Assunção ARM. Doença de Meniere no idoso. Revista Hospital Universitário Pedro Ernesto. 2015;14(1):66-70
7. Parker W. Meniere’s disease: etiologic considerations. Arch Otolaryngol Neck Surg. 1995;121(4):377–382.
8. Welling DB, Clarkson MW, Miles BA, Schmalbrock P, Williams PM, Chakeres DW, et al. Submillimeter magnetic resonance imaging of the temporal bone in Meniere’s disease. The Laryngoscope. 1996;106(11):1359–1364.
9. Atlas MD, Chai F, Boscato L. Meniere’s disease: evidence of an immune process. Am J Otol. 1998;19(5):628–631.
10. Ruckenstein MJ. Immunologic aspects of Meniere’s disease. Am J Otolaryngol. 1999;20(3):161–165.
11. Monsell E, Balkany T, Gates G, Goldenberg R, Meyerhoff W, House J. Committee on Hearing and Equilibrium Guidelines for the Diagnosis and Evaluation of Therapy in Ménière Disease. American Academy of Otolaryngology Head and Neck Foundation, Inc. Otolaryngol Neck Surg. 1995;113(3):181–185.
12. Lopez-Escamez JA, Carey J, Chung W-H, Goebel JA, Magnusson M ans, Mandalà M, et al. Diagnostic criteria for Menière’s disease. J Vestib Res. 2015;25(1):1–7.
13. Van de Heyning PH, Wuyts FL, Claes J, Koekelkoren E, Van Laer C, Valcke H. Definition, classification and reporting of Meniere’s disease and its symptoms. Acta Otolaryngol (Stockh). 1997;117(sup526):5–9.
14. Campos RAC, Fukujima MM. Vertigem de origem central. Associação Brasileira de Otorrinolaringologia e Cirurgia Cérvico-facial, Tratado de Otorrinolaringologia. Vol. 2. São Paulo: Rocca; 2011. 511–514 p.
15. Duracinsky M, Mosnier I, Bouccara D, Sterkers O, Chassany O, d’Oto-Rhino-Laryngologie (ORL) WG of the SF. Literature review of questionnaires assessing vertigo and dizziness, and their impact on patients’ quality of life. Value Health. 2007;10(4):273–284.
16. Castro ASO de, Gazzola JM, Natour J, Ganança FF. Versão brasileira do dizziness handicap inventory. Pró-Fono Rev Atualização Científica. 2007;
17. Newman CW, Jacobson GP, Spitzer JB. Development of the tinnitus handicap inventory. Arch Otolaryngol Neck Surg. 1996;122(2):143–148.
18. Yardley L, Putman J. Quantitative analysis of factors contributing to handicap and distress in vertiginous patients: a questionnaire study. Clin Otolaryngol Allied Sci. 1992;17(3):231–236.
19. Ganança MM, Caovilla HH. Desequilíbrio e reequilíbrio. In: Ganança MM Vertigem tem cura. São Paulo: Lemos Editorial; 1998. p. 13–9.
20. Ganança MM, Caovilla HH, Munhoz MSL, Silva MLG, Kuhn AMB, Ganança CF. Vertigem psicossomática. In: Silva MLG, Munhoz MSL, Ganança MM, Caovilla HH Quadros clínicos otoneurológicos mais comuns. São Paulo: Atheneu; 2000. p. 145–51.
21. Enloe LJ, Shields RK. Evaluation of health-related quality of life in individuals with vestibular disease using disease-specific and general outcome measures. Phys Ther. 1997;77(9):890–903.
22. Ganança FF, Perracini MR, Ganança CF. Reabilitação dos distúrbios do equilíbrio corporal. In: Ganança MM Vertigem: abordagens diagnósticas e terapêuticas. São Paulo: Lemos Editorial; 2002. p. 16.
23. Fielder H, Denholm SW, Lyons RA, Fielder CP. Measurement of health status in patients with vertigo. Clin Otolaryngol Allied Sci. 1996;21(2):124–126.
24. WHO. World Health Organization. International classification of impairments, disabilities, and handicaps: a manual of classification relating to the consequences of disease, published in accordance with resolution WHA29. 35 of the Twenty-ninth World Health Assembly, May 1976. 1980.
25. Ganança FF, Castro ASO, Branco FC, Natour J. Interferência da tontura na qualidade de vida de pacientes com síndrome vestibular periférica. Rev Bras Otorrinolaringol. 2004;70(1):94–101.
26. Jacobson GP, Newman CW, Hunter L, Balzer GK. Balance function test correlates of the Dizziness Handicap Inventory. J Am Acad Audiol. 1991;2(4):253–260.
27. Gámiz MJ, Lopez-Escamez JA. Health-related quality of life in patients over sixty years old with benign paroxysmal positional vertigo. Gerontology. 2004;50(2):82–86.
28. Perez N, Garmendia I, Martin E, Boleas MS, Garcia-Tapia R. Health measurement instruments in patients with vertigo. Acta Otorrinolaringol Esp. 2000;51(8):677–685.
29. Poon DMY, Chow LCK, Hui Y, Au DKK, Leung MCP. Translation of the dizziness handicap inventory into Chinese, validation of it, and evaluation of the quality of life of patients with chronic dizziness. Ann Otol Rhinol Laryngol. 2004;113(12):1006–1011.
30. Cunha F, Settanni FA, Ganança FF. What is the effect of dizziness on the quality of life for patients with Meniere’s disease? Rev Laryngol-Otol-Rhinol. 2005;126(3):155–158.
31. Handa PR, Kuhn AMB, Cunha F, Schaffleln R, Ganança FF. Qualidade de vida em pacientes com vertigem posicional paroxística benigna e/ou doença de Ménière. Braz J Otorhinolaryngol. 2005;71(6):776–83.
32. Segarra-Maegaki JA, Taguchi CK. Study about the benefits of vestibular rehabilitation in peripheral vestibular disorders. -Fono Rev Atualizacao Cient. 2005;17(1):3–10.
33. Gazzola JM, Rodrigues Perracini M, Malavasi Ganança M, Freitas Ganança F. Fatores associados ao equilíbrio funcional em idosos com disfunção vestibular crônica. Braz J Otorhinolaryngol. 2006;72(5).
34. Yardley L. Contribution of symptoms and beliefs to handicap in people with vertigo: a longitudinal study. Br J Clin Psychol. 1994;33(1):101–113.
35. Pérez N, Garmendia I, Martin E, García-Tapia R. Cultural adaptation of 2 questionnaires for health measurement in patients with vertigo. Acta Otorrinolaringol Esp. 2000;51(7):572–580.
36. Pratt RTC, Mckenzie W. Anxiety states following vestibular disorders. The Lancet. 1958;272(7042):347–349.
37. Leavy I, O’Leary JL. Incidence of vertigo in neurologic conditions. Trans Am Otol Soc. 1947;35:329–47.
38. Nobbs MB. Adjustment in Meniere’s disease. In: Kyle JG Adjustment to Acquired Hearing Loss: Analysis, Change and Learning. Bristol: Centre for Deaf Studies; 1988.
39. Grigsby JP, Johnston CL. Depersonalization, vertigo and Meniere’s disease. Psychol Rep. 1989;64(2):527–534.
[1] Otorrinolaringologista pelo Hospital do Servidor Público Municipal de São Paulo, HSPM, São Paulo, SP. Pós graduada em Atenção Básica em Saúde pela Universidade Federal de Santa Catarina, UFSC, Florianópolis, SC. Médica graduada pela Universidade Federal de Santa Maria, UFSM, RS.
[2] Otorrinolaringologista pelo Hospital do Servidor Público Municipal de São Paulo, HSPM, São Paulo, SP. Médica graduada pela Faculdade Evangélica do Paraná, FEPAR, Curitiba, PR.
[3] Mestre em Saúde da Comunicação pela Faculdade de Ciências Médicas da Santa Casa de Misericórdia de São Paulo, São Paulo, SP. Otorrinolaringologista pela Faculdade de Ciências Médicas da Santa Casa de Misericórdia de São Paulo, São Paulo, SP. Médica graduada pela Faculdade de Ciências Médicas da Santa Casa de Misericórdia de São Paulo, São Paulo, SP.
[4] Otorrinolaringologista pela Real e Benemérita Associação Portuguesa de Beneficência de São Paulo. Médico graduado pelo Centro Universitário de Volta Redonda, UniFOA, Volta Redonda, RJ.
[5] Pós graduado em Cirurgia Plástica da Face pelo Instituto Brasileiro de Pós Graduação, IBPG: Otorrinolaringologista pelo Hospital do Servidor Público Municipal de São Paulo, HSPM, São Paulo, SP. Médico graduado pela Universidade Federal de Pernambuco, UFPE, Recife, PE.
Enviado: Novembro, 2019.
Aprovado: Novembro, 2019.







Uma resposta
Uma luz no fim do tunel..