ARTICLE DE RÉVISION
SBRUZZI, Felipe Augusto [1], SILVA, Kelly Cristina da [2], TELLES, Sérgio Mazero [3], LIMA, Sirlene de Sousa [4], SANTANA, Claudinei Alves [5]
SBRUZZI, Felipe Augusto. Et al. Formulaire de suivi pour les patients adultes atteints de leucémie à l’aide d’Imatinib. Revista Científica Multidisciplinar Núcleo do Conhecimento. An 05, Ed. 10, vol. 02, p. 92 à 112. octobre 2020. ISSN: 2448-0959, Lien d’accès: https://www.nucleodoconhecimento.com.br/sante/laide-dimatinib
RÉSUMÉ
Introduction: La leucémie myéloïde chronique est un type de néoplasie sanguine maligne qui se caractérise principalement par la présence du chromosome Philadelphie à l’origine de l’oncoprotéine BCR-ABL. Il a augmenté l’activité de la tyrosine kinase, provoquant ainsi des changements dans les voies de signalisation intracellulaires et favorisant la prolifération incontrôlée, le dysfonctionnement cellulaire et l’absence d’apoptose. Malgré la faible incidence de la maladie, 1,5 cas pour 100000 habitants, le traitement par Imatinib, un puissant inhibiteur de la BCR-ABL, a changé le pronostic de la maladie et prolongé l’espérance de vie des patients, transformant une maladie mortelle en un état chronique. Objectif: Développer un formulaire de suivi régulier de ces patients par le pharmacien clinicien afin d’assurer une pharmacothérapie sûre et efficace. Méthodologie: Une revue de la littérature de type narratif a été initiée à partir de la question problématique: «Quelles données doivent être collectées par le pharmacien clinicien pendant l’assistance pharmaceutique pour évaluer et améliorer l’observance chez les patients adultes atteints de leucémie myéloïde chronique utilisant l’imatinib?» , suivi d’une recherche d’articles dans les bases de données PubMed et les sites Web gouvernementaux. Par la suite, la sélection du travail et l’analyse critique ont été effectuées pour construire un formulaire modèle à appliquer dans l’acte de distribution. Résultat et discussion. Onze articles ont été sélectionnés. La faible adhérence du patient au traitement de la leucémie myéloïde chronique peut entraîner un danger de mort potentiel. Par conséquent, le formulaire de suivi à appliquer par le pharmacien clinicien lors de la délivrance du mésylate d’imatinib est une stratégie viable et peu coûteuse pour améliorer l’observance de la pharmacothérapie et favoriser une meilleure réponse au traitement. Conclusion: La documentation systématique et standardisée de l’observance et des effets indésirables par le pharmacien clinicien permet la mise en place d’actions par l’équipe multidisciplinaire d’amélioration continue afin de maximiser la qualité des soins prodigués aux patients ainsi que la qualité de vie.
Mots clés : Leucémie, suivi pharmacothérapeutique, Imatinib.
INTRODUCTION
Le cancer est le nom donné à un ensemble de plus d’une centaine de pathologies, qui a des caractéristiques communes l’initiation par des dommages dans des gènes spécifiques de l’ADN et la croissance autonome et désordonnée des cellules qui acquièrent la capacité d’envahir les organes et les tissus adjacents entraînant des troubles fonctionnels (THAVAMANI et al., 2014).
Cette prolifération cellulaire anormale est connue sous le nom de néoplasie et dans la pratique il est appelé tumeur, et peut être classé comme malin ou bénin (INSTITUTO NACIONAL DO CÂNCER, 2019).
Un groupe spécial de néoplasmes malins sont des leucémies, qui sont caractérisées par une prolifération anormale des précurseurs des cellules de moelle osseuse de la lignée blanche (JULIUSSON et HOUGH, 2016; LIU et al., 2019). Les leucémies peuvent être classées selon le type de cellules, lymphocytiques ou myéloïdes affectés, et quant à la caractéristique, aiguë ou chronique (SAHDEVA et al., 2019).
La leucémie myéloïde chronique (LMC) est un type de trouble sanguin caractérisé par une augmentation du nombre de leucocytes avec déviation gauche, splenomegaly et la présence du chromosome de Philadelphie (Ph), qui résulte de la translocation réciproque entre les chromosomes (9;22) (q34;q11), donnant lieu à la protéine bcr-abl, avec une activité accrue de tyrosine kinase (FLIS et CHOJNACKI, 2019).
La protéine BCR-ABL est présente chez plus de 90 % des patients atteints de LMC, et son hyperactivité stimule la libération d’effecteurs de prolifération cellulaire et d’inhibiteurs de l’apoptose, et son activité est responsable du processus de formation du cancer dans la LMC (DI FELICE et al., 2018).
La découverte de cette altération moléculaire en plus de l’optimisation du diagnostic de la LMC a également fourni le développement de thérapies visant à cette altération moléculaire, et des méthodes de surveillance des maladies résiduelles minimales, fournissant une amélioration du traitement (BORTOLHEIRO et CHIATTONE, 2008).
La LMC présente trois phases cliniques distinctes qui surviennent tout au long de la maladie, étant classées comme phase chronique, phase de transformation et phase finale ou de souffle (HEFNER et al., 2016).
Traditionnellement, le traitement du cancer peut être effectué par la chirurgie, la chimiothérapie et les modalités de radiothérapie, et la combinaison est commune pour obtenir un meilleur résultat clinique (NATIONAL CANCER INSTITUO, 2019).
La chimiothérapie classique vise à la destruction des cellules dans la réplication rapide qui suggèrent des mutations et/ou des changements importants dans l’ADN, cependant, les cellules normales de tissu qui ont également la réplication rapide sont détruites fournissant ainsi de nombreux effets indésirables aux patients (BAGNYKOVA et al., 2010).
Dans les cellules cancéreuses, telles que la LMC, les voies de signalisation intracellulaire sont modifiées, favorisant la prolifération incontrôlée, le dysfonctionnement cellulaire et l’absence d’apoptose (ANDERSON et al., 2015). Sur la base d’une meilleure compréhension de ces processus, lancés dans les années 1980, les médicaments appelés inhibiteurs de la tyrosine kinase (ITQ) ont commencé à être étudiés (CHABNER et ROBERTS, 2005).
En CML en raison de sa caractéristique pathognomonica, le BCR-ABL oncogène, est devenu le candidat idéal pour la « balle magique » conçu par Paul Ehrlich (Chabner et Roberts, 2005). Ainsi, la « thérapie de cible » avec ITQ cherche à inhiber sélectivement les voies de signalisation dérégulées des cellules néoplastiques des patients présentant CML, ayant comme premier médicament utilisé le mesyate d’imatinib, un inhibiteur puissant de BCR-ABL (DREWS, 2006 ; MOULIN et coll., 2017).
En raison du vieillissement et de la croissance démographique, l’incidence et la mortalité du cancer ont augmenté dans le monde entier (BRAY et al., 2018). Au Brésil, l’Institut national du cancer (INCA) estime que pour chaque année de l’exercice biennal 2018/2019 600 000 nouveaux cas de cancer sont diagnostiqués, parmi ces leucémies apparaissent à la 9ème place chez les hommes avec 5 940 nouveaux cas et 10e chez les femmes avec 4 860 nouveaux cas (INSTITUTO NACIONAL DE CÂNCER, 2017).
La LMC représente environ 15 % des nouveaux cas de leucémie, avec un risque estimé de 1,5 cas pour 100 000 personnes (RYCHTER et al., 2017). Malgré la faible incidence par rapport à d’autres types de cancer (poumon, prostate, sein), due à la thérapie de mesilate d’imatinib, les patients présentant LMC ont montré une amélioration considérable du taux de survie de cinq ans et ont modifié le pronostic de la maladie (TRIVEDI et al., 2014; SAUSSELE et al., 2018; TAN et al., 2019; LATREMOUILLE-VIAU et al., 2017).
Pour les patients diagnostiqués au milieu des années 1970, le taux de survie à cinq ans était de 22 %, de 2008 à 2014, de 69 %, et actuellement la plupart des patients recevant un IQT ont une espérance de vie compatible avec les personnes normales, ce qui rend la LMC actuellement considérée comme une maladie chronique qui nécessite un suivi régulier par l’équipe de santé (SIEGEL et al. , 2019).
Le traitement de la LMC nécessite l’action intégrée de l’équipe multidisciplinaire, et le professionnel pharmaceutique est indispensable dans le suivi pharmacothérapeutique (SP) du traitement du cancer afin d’assurer une pharmacothérapie sûre et efficace (SOUZA et al., 2018).
L’AP est une pratique personnalisée dans laquelle le pharmacien clinicien a la responsabilité d’orienter, de détecter, de prévenir et de résoudre les problèmes liés aux médicaments, couvrant les effets indésirables de la chimiothérapie et de la thérapie utilisée, ainsi que les techniques d’administration, d’observance du traitement et des interactions médicamenteuses (CALADO et al., 2019).
Compte tenu de la complexité de la LMC, le suivi effectué par le professionnel pharmaceutique clinique est essentiel pour l’efficacité du traitement.
OBJECTIF
Construisez un modèle de formulaire de suivi pharmacothérapeutique pour les patients adultes atteints de leucémie myéloïde chronique BCL-ABR positive à l’aide d’Imatinib Mesiduct.
MÉTHODOLOGIE
L’œuvre est une revue littéraire du type narratif. Ainsi, à partir de la question du problème: « Quelles données devraient être recueillies par le pharmacien clinique au cours de l’aide pharmaceutique pour évaluer et améliorer l’observance des patients adultes atteints de leucémie myéloïde chronique à l’aide d’Imatinib? » une recherche a été effectuée sur la plate-forme PubMed basée sur la stratégie PICO et les descripteurs ont été utilisés: « leucémie, myélogéne, chronique, bcr-abl positif » ET « médicament d’observance ». Les articles des 5 dernières années ont été examinés et la recherche a été effectuée dans la base de données de juin à décembre 2019.
Les critères d’inclusion étaient les suivants : articles disponibles en ligne complet, en anglais, qui avaient des patients adultes de la population, et avec le thème de l’évaluation de l’observance des médicaments dans la LMC. Comme critères d’exclusion étaient: articles qui ont évalué exclusivement un autre médicament autre que le mesysrate d’imatinib, qui n’a pas utilisé un formulaire.
De plus, pour constituer le formulaire, on a consulté les sites gouvernementaux.
RÉSULTATS ET DISCUSSION
La recherche sur le site Web de Pubmed avec les descripteurs a donné lieu à 52 articles et de ceux-ci, sur la base des critères d’inclusion et d’exclusion, 11 ont été sélectionnés pour faire l’examen de la littérature dans la préparation du formulaire.
Ces articles sont présentés au tableau 1 dans l’ordre de date décroissante de publication.
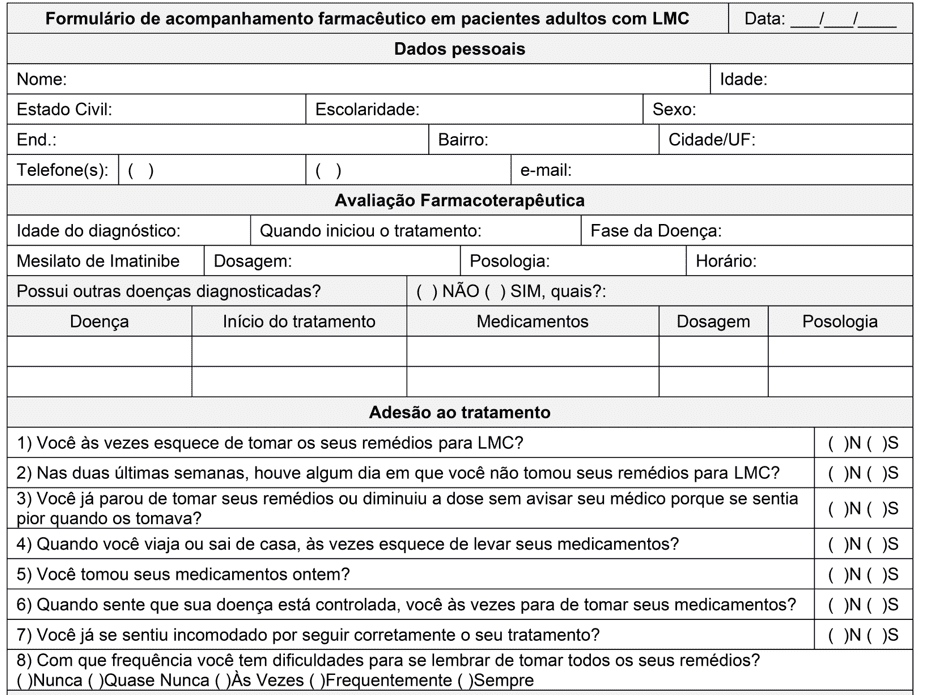
Selon ce qui a été observé par Moulin et coll., l’inclusion du pharmacien clinique pendant le traitement des patients atteints de LMC a non seulement amélioré l’observance du traitement et a diminué les effets indésirables des médicaments (EIM) signalés par les patients, mais a également amélioré les paramètres cytogénétiques (MOULIN et al., 2017). Dans cette étude, après 4 mois de suivi, les auteurs ont trouvé une expression inférieure du chromosome de Philadelphie dans le groupe surveillé par rapport au contrôle non surveillé. Dans le groupe suivi, la réponse cytogénétique complète observée est passée de 87,0 % à 95,6 % des patients tandis que dans le groupe non surveillé, elle est restée dans 61,5 %. Ainsi, l’application d’un formulaire au moment de la dispensation est une stratégie efficace pour accompagner le patient et améliorer l’observance du traitement. Pour atteindre cet objectif, un formulaire de suivi pharmaceutique a été élaboré chez les patients adultes atteints de LMC (annexe I).
La première partie du formulaire vise à recueillir les données personnelles des patients afin d’identifier et de faciliter le contact avec le patient. C’est parce que certaines des études sélectionnées montrent que dans certaines populations les ades peuvent être favorisées par certaines caractéristiques socio-économiques, mais les études diffèrent quant à laquelle sont plus présents dans la population. Tsai et al. (2018) ont constaté dans la population étudiée que les patients plus âgés et les patients mariés ont une meilleure observance. Selon Rychter et al (2017), la présence d’au moins 1 comorbidité et d’âge de plus de 65 ans sont des caractéristiques favorables à l’adering. En revanche, Unnikrishnan et al. (2016) et Hefner et al. (2016) n’ont trouvé aucune corrélation entre les caractéristiques socioéconomiques de la population étudiée et le traitement adhérant. Ainsi, on observe que la corrélation entre les données socio-économiques et l’observance varie selon la population étudiée, n’étant pas un paramètre prédictif pour l’observance ou la non-observance du patient.
Tableau 1.A – Articles sélectionnés sur la base de critères d’inclusion et d’exclusion, ordre décroissant de l’année de publication.
| Auteur/Année | Titre | Objectifs | Forme d’Adecin | N(1) | Pays | Médicaments |
| MULU FENTIE et al., 2019 | Prevalence and determinants of non-adherence to Imatinib in the first 3-months treatment among newly diagnosed Ethiopian’s with chronic myeloid leukemia. | Évaluer la prévalence et les raisons de ne pas adhérer à l’Imatinib chez les patients atteints de LMC(2) qui ont été récemment diagnostiqués au cours des 3 premiers mois de traitement. | MMAS-8(3) | 147 | Ethiopie | Imatinib |
| TSAI et al., 2018 | Side effects and medication adherence of tyrosine kinase inhibitors for patients with chronic myeloid leukemia in Taiwan. | Clarifier l’influence des effets indésirables sur l’observance chez les patients taïwanais atteints de LMC(2). | MMAS-8(3) | 58 | Taiwan | Imatinibe
Dasatinibe Nilotinibe |
| HEFNER et al., 2017 | Adherence and Coping Strategies in Outpatients With Chronic Myeloid Leukemia Receiving Oral Tyrosine Kinase Inhibitors. | Évaluer les stratégies d’observance et d’adaptation chez les patients en dehors de l’environnement hospitalier avec la LMC(2). | BAASIS(4) | 35 | Allemagne | Inhibiteurs de la tyrosine kinase |
(1) N = Nombre de participants; (2) LMC = Leucémie myéloïde chronique; (3) MMAS-8 = Échelle d’adhérence thérapeutique Morisky de 8 points; (4)BAASIS = Échelle de Bâle pour l’évaluation immunosuppressive de l’observance des médicaments; (5) MMAS-4 = Échelle d’adhérence thérapeutique Morisky à 4 points.
Tableau 1.B – Articles sélectionnés sur la base de critères d’inclusion et d’exclusion, ordre décroissant de l’année de publication.
| Auteur/Année | Titre | Objectifs | Forme d’Adecin | N(1) | Pays | Médicaments |
| RYCHTER et al., 2017 | Treatment adherence in chronic myeloid leukaemia patients receiving tyrosine kinase inhibitors. | Évaluer le traitement adhérant aux patients polonais adultes atteints de LMC(2) | Formulaire développé pour l’étude. | 140 | Pologne | Imatinib
Dasatinib Nilotinib |
| GEISSLEr et al., 2017 | Factors influencing adherence in CML and ways to improvement: Results of a patient-driven survey of 2546 patients in 63 countries. | Évaluer l’étendue de l’observance sous-optimale et étudier les raisons et les modèles de comportement d’adhérence des patients atteints de LMC(2) dans le monde entier. | MMAS-8(3) | 2546 | 63 pays | Imatinib
Dasatinib Nilotinib Autres traitements |
| MULUNEH et al., 2016 | Patient perspectives on the barriers associated with medication adherence to oral chemotherapy. | Analyser à l’aide d’un questionnaire l’utilisation de la chimiothérapie orale et identifier les possibilités d’amélioration dans les éléments suivants. | Questionnaire adapté avec 30 questions | 93 | États-Unis | Chimiothérapie orale |
(1) N = Nombre de participants; (2) LMC = Leucémie myéloïde chronique; (3) MMAS-8 = Échelle d’adhérence thérapeutique Morisky de 8 points; (4) BAASIS = Échelle de Bâle pour l’évaluation immunosuppressive de l’observance des médicaments; (5) MMAS-4 = Échelle d’adhérence thérapeutique Morisky à 4 points
Tableau 1.C – Articles choisis en fonction de critères d’inclusion et d’exclusion, ordre décroissant de l’année de publication.
| Auteur/Année | Titre | Objectifs | Forme d’Adecin | N(1) | Pays | Médicaments |
| MOULIN et coll.
Novembre/201614 |
The role of clinical pharmacists in treatment adherence: fast impact in suppression of chronic myeloid leukemia development and symptoms | Évaluer le rôle du pharmacien clinique dans le traitement des patients atteints de LMC(2), ainsi que la participation du pharmacien clinicien. | MMAS-4(5) | 23 | Brésil | Inhibiteurs de la tyrosine kinase |
| KEKÄLE et al., 2016 | Impact of tailored patient education on adherence of patients with chronic myeloid leukaemia to tyrosine kinase inhibitors: a randomized multicentre intervention study. | Évaluer l’influence de l’éducation personnalisée au patient sur l’adhésion à l’ITQ chez les patients atteints de LMC(2). | MMAS-8(3) | 86 | Finlande | Inhibiteurs de la tyrosine kinase |
| UNNIKRISHNAN et al., 2016 | Comprehensive Evaluation of Adherence to Therapy, Its Associations, and Its Implications in Patients With Chronic Myeloid Leukemia Receiving Imatinib. | Évaluer l’adforebation et la qualité de vie chez les patients atteints de LMC(2) recevant l’Imatinib pendant une longue période de temps. | MMAS-8(3) | 221 | Inde | Imatinib |
(1) N = Nombre de participants; (2) LMC = Leucémie myéloïde chronique; (3) MMAS-8 = Échelle d’adhérence thérapeutique Morisky de 8 points; (4) BAASIS = Échelle de Bâle pour l’évaluation immunosuppressive de l’observance des médicaments; (5) MMAS-4 = Échelle d’adhérence thérapeutique Morisky à 4 points
Tableau 1.D – Articles choisis en fonction des critères d’inclusion et d’exclusion, ordre décroissant de l’année de publication.
| Auteur/Année | Titre | Objectifs | Forme d’Adecin | N(1) | Pays | Médicaments |
| HOSOYA et al., 2015 | Failure mode and effects analysis of medication adherence in patients with chronic myeloid leukemia | Identifiez la faible observance chez les patients atteints de LMC(2) à l’aide du mode échec et de l’analyse des effets. | Formulaire développé pour l’étude | 54 | Japon | Imatinibe
Dasatinibe Nilotinibe |
| BRECCIA et al., 2015 | Adherence and future discontinuation of tyrosine kinase inhibitors in chronic phase chronic myeloid leukemia. A patient-based survey on 1133 patients. | Étudier l’observance et les avantages potentiels en matière de qualité de vie, de satisfaction à l’égard du traitement et de la vie sociale chez les patients atteints de LMC(2) | Formulaire développé pour l’étude. | 1133 | Italie | Inhibiteurs de la tyrosine kinase |
(1) N = Nombre de participants; (2) LMC = Leucémie myéloïde chronique; (3) MMAS–8 = Échelle d’adhérence thérapeutique Morisky de 8 points; (4) BAASIS = Échelle de Bâle pour l’évaluation immunosuppressive de l’observance des médicaments; (5) MMAS-4 = Échelle d’adhérence thérapeutique Morisky à 4 points
L’une des attributions du pharmacien clinicien est l’évaluation de la pharmacothérapie, afin que le patient puisse utiliser en toute sécurité les médicaments dont il a besoin, aux doses, à la fréquence et aux horaires appropriés, atteignant ainsi les objectifs thérapeutiques. Pour cela, des domaines spécifiques ont été réservés pour recueillir l’âge du diagnostic, le début du traitement, la phase de la maladie et les paramètres liés à la pharmacothérapie d’imatinib.
Au Brésil, l’ordonnance no 1 219 du 4 novembre 2013 établit le protocole clinique et les lignes directrices thérapeutiques pour la LMC chez les adultes et est une référence pour l’évaluation pharmacothérapeutique de ces patients. En cela, il est recommandé d’utiliser l’imatinib comme traitement de première intention et ce qu’est la pharmacothérapie pour les phases chroniques (PC) et de transformation ou accélérée (TA) (BRASIL, 2013).
Aux PC, il est recommandé une dose unique de 400 mg/jour par jour par voie orale après le repas le plus important de la journée, et peut augmenter en deux doses de 300 mg, l’une le matin et l’autre le soir, si après trois mois une réponse inadéquate, la perte de réponse précédente ou la progression de la maladie. En ce qui concerne l’TA, la dose recommandée est de 600 mg/jour et peut être élevée jusqu’à 800 mg/jour dans les crises d’explosion (BRASIL, 2013).
En plus d’avoir un rôle fondamental dans l’adhésion au traitement des patients, le pharmacien clinicien devrait également identifier, évaluer et intervenir dans les interactions médicamenteuses. Pour évaluer les interactions médicamenteuses possibles lors de l’utilisation de l’imatinib, la présence d’autres maladies et pharmacothérapies de ces maladies est évaluée sous la forme. Dans le cas des interactions médicamenteuses, le pharmacien doit être au courant des médicaments qui ont la métabolisation hépatique, parce que l’imatinib est métabolisé dans cette voie par l’enzyme CYP3A4 (GLIVEC, 2020). Le maintien d’une concentration sanguine supérieure à 300 mg est extrêmement important pour le succès de la réponse moléculaire/cytogénétique et de la survie accrue sans progression de la maladie (BRASIL, 2013). Par conséquent, les inducteurs de cette enzyme tels que la dtethasone et l’Hypericum perfortum, qui peuvent réduire la concentration plasmatique d’Imatinib, devraient être évités. Ainsi que des inhibiteurs comme le ketoconazole, la clarithromycine qui pourrait diminuer le métabolisme et augmenter les concentrations d’imatinib menant il y a une augmentation de l’EIM (GLIVEC, 2020).
La deuxième partie de l’article vise à évaluer le traitement du patient. Selon la définition de l’Organisation mondiale de la santé (OMS), l’observance des maladies chroniques est la mesure dans laquelle le comportement d’une personne est d’accord avec les recommandations d’un professionnel de la santé, et le comportement peut être représenté par la prise de médicaments, le suivi de l’alimentation ou les changements de mode de vie (OMS, 2003)
Dans les articles sélectionnés, les articles suivants ont été mesurés à l’aide de questionnaires qui évaluent ce comportement par des actions pertinentes au traitement de la LMC, telles que : oubli d’une ou de plusieurs doses, changement de dose sans prévenir le prescripteur, ne pas prendre de médicaments parce qu’il se sent bien ou parce qu’il a une réaction indésirable. Le modèle de questionnaire le plus utilisé dans les articles (six sur onze sélectionnés) pour évaluer l’observance était l’échelle d’adhérence thérapeutique Morisky, avec 8 articles (MMAS-8) étant les plus fréquents. En face de cela, le MMAS-8 a été choisi pour la composition de la forme d’accompagnement.
Un autre facteur important pour le choix était le temps requis pour l’application et la facilité de classer le patient. Le MMAS-8 se compose de sept questions avec des alternatives « Oui» ou « non », et un élément (le dernier) qui comporte une échelle likert de 5 points (allant de 0 points à « oujour » à 1 point à « amais »). Chaque élément assing un comportement spécifique de l’utilisation de médicaments et n’est pas un déterminant du comportement des médicaments. Les scores de MMAS peuvent varier de 0 à 8 et les patients sont classés en trois niveaux de soutien : haute résistance (score 8); adéposition moyenne (score 6 à 7,75); et adtake faible (<6).
Un questionnaire modifié de l’échelle de Bâle pour l’évaluation immunosuppressive de l’adepitus (BAASIS) a été utilisé par Hefner et coll. (2016). Cela comporte quatre questions « oui » ou « non » et une seule réponse affirmative est nécessaire pour considérer le patient comme « non adhérent », ce qui peut provoquer une réponse négative chez le patient par rapport à la classification du MMAS-8 (soutien élevé, moyen et faible). Un autre facteur considéré pour le choix a été l’absence dans BAASIS des questions liées au comportement « d’arrêter de prendre des médicaments lorsque vous sentez que la maladie est contrôlée ». C’est parce que dans certaines études, il a été détecté que les patients ont tendance à être plus adhérents dans la première et la deuxième année après le diagnostic, probablement en raison des symptômes diminués et les EIM deviennent plus évidents que la maladie elle-même (GEISSLER et al, 2017).
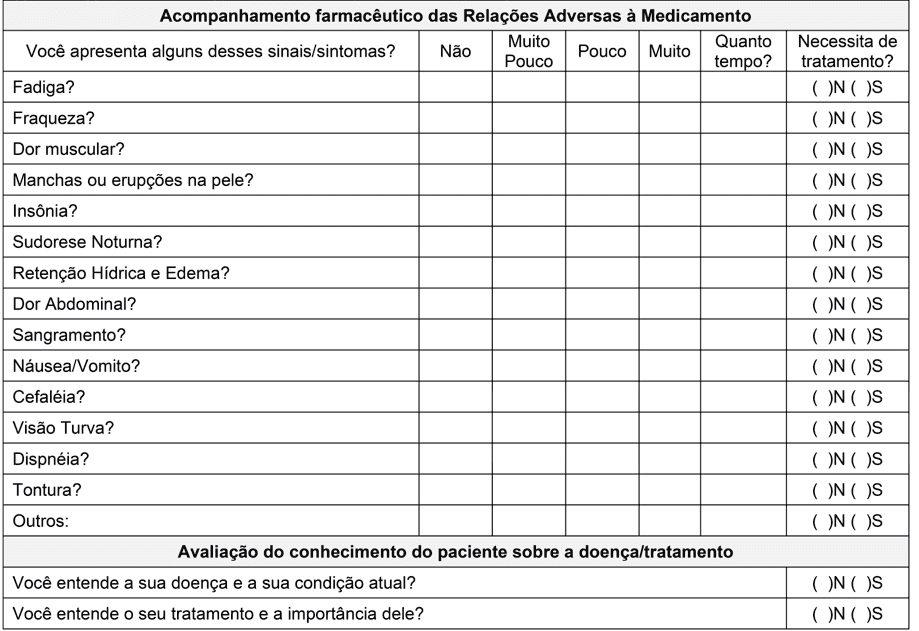
Pour évaluer EIM et ses conséquences sur l’annonce, une troisième partie a été incluse dans le formulaire avec des questions sur les réactions les plus courantes.
Selon une étude de cohorte menée en Éthiopie par Mulu Fentie et al. (2019), il a été identifié que la principale raison du soutien non-traitement était les événements indésirables liés à l’Imatinib, aux médicaments qui étaient 68,8%. Et la plainte principale environ 68% étaient liées aux effets gastro-intestinaux. L’étude montre également que les patients qui n’ont pas connu de EIM étaient six fois plus susceptibles d’adhérer au traitement.
Comme mentionné ci-dessus, Moulin et al. (2017) ont démontré que l’action du pharmacien clinicien par le suivi pharmacologique améliorait l’observance et réduisait les effets indésirables. Au cours des quatre mois de suivi, les chercheurs ont réduit le nombre de non-adhérents de huit à zéro, en utilisant l’échelle d’adhérence thérapeutique Morisky en 4 points. En outre, le nombre de patients se plaignant de la EIM est passé de 35% à 7%.
Bien que la durée des études et le nombre de personnes évaluées aient été relativement faibles, les résultats sont prometteurs. En outre, il est nécessaire d’une étude plus précise par rapport au nombre de personnes et de suivi pour de plus longues périodes.
En contre-match, une étude portant sur 63 pays et 2546 patients a révélé que ce n’est pas le fait que le patient éprouve EIM qui influence l’observance, mais plutôt la façon dont la gestion de ceux-ci est effectuée par l’équipe multidisciplinaire (GEISSLER et al., 2017).
Compte tenu de ces résultats, nous avons trouvé des preuves que la meilleure façon de promouvoir le traitement adeforego est de contourner les événements indésirables ou même si possible d’éviter d’éventuels événements indésirables futurs pour promouvoir un meilleur traitement. Ce sont les raisons pour lesquelles nous insérons dans la forme des questions sur les principaux ADR décrits pour le Mesysate d’Imatinib, l’intensité et le temps que le patient les éprouve et ressent le besoin de traitement. Ainsi, nous espérons identifier et contourner les principaux effets indésirables liés aux médicaments, afin de promouvoir une plus grande sécurité, de soutenir et d’améliorer la qualité de vie des patients.
Bien que la stratégie choisie pour évaluer et améliorer l’observance et réduire les ADR des patients soit la forme, Geissler et al. (2017) ont constaté qu’un facteur important qui affecte l’observance et peut être influencé par les professionnels de la santé est l’information des patients au sujet de la LMC. Dans cette étude, les patients qui se sentaient mieux informés au sujet de la maladie étaient sensiblement plus adhérents. Ainsi, deux questions ont été insérées dans notre forme pour évaluer la connaissance du patient de la maladie/traitement et ainsi, avec la participation de l’équipe multidisciplinaire, pour planifier des stratégies complémentaires. Toujours avec cette information, il est prévu d’intégrer le patient plus activement dans le traitement en mettant l’accent sur l’information et pas seulement dans l’instruction qu’il devrait suivre.
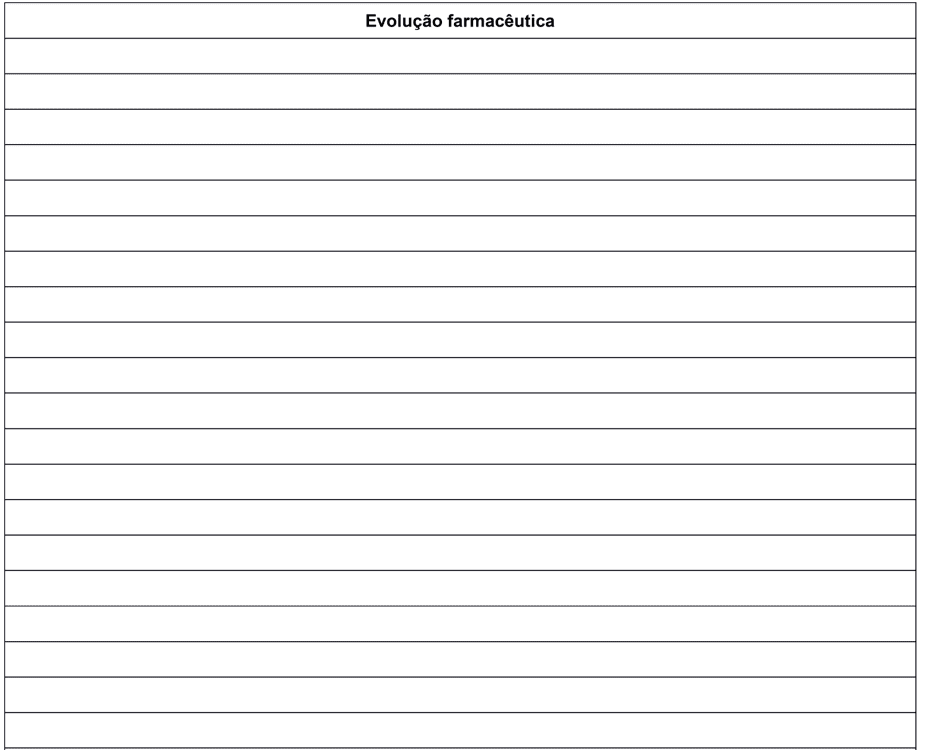
Pendant la préparation du formulaire, il n’a pas été possible d’anticiper les situations ou la D’EIM que les patients pouvaient signaler. Cela dit, le dos du formulaire a été utilisé pour le domaine « Pharmaceutical Evolution » où ils peuvent être notés par exemple: données subjectives, données objectives, évaluation et planification spécifique pour le patient évalué.
La proposition de construire le modèle de formulaire pour l’application chez les patients atteints de LMC vise à améliorer la réponse au traitement avec Imatinib Mesitate et la qualité de vie. Ainsi, à ce jour, il n’est pas prévu d’intégrer les résultats de cette activité dans un projet de recherche. Par conséquent, aucune modification et consentement n’ont été produits pour se conformer à la résolution no 510 du 7 avril 2016 du ministère de la Santé. Cette résolution prévoit des recherches dont les procédures méthodologiques impliquent l’utilisation de données directement obtenues auprès des participants ou d’informations identifiables (BRASIL, 2016). Toutefois, un texte à signer par le patient ou son représentant est placé au verso du formulaire indiquant qu’il est au courant que les données fournies seront utilisées pour le suivi pharmacothérapeutique du traitement de la leucémie myéloïde chronique.
Annexe I – Formulaire de suivi pharmaceutique chez les patients adultes atteints de LMC.
CONCLUSION
On sait que plusieurs facteurs servent d’obstacles au non-traitement au traitement pharmacologique, tels que : les événements indésirables, la routine quotidienne des médicaments, le sentiment de bien-être sans traitement, l’insuffisance de l’information sur le médicament. Cependant, en particulier dans la leucémie myéloïde chronique, le non-traitement avec le Mesilate d’Imatinib peut avoir comme conséquence le traitement mortel potentiel, puisque l’issue de cette maladie est bien connue et documentée. Par conséquent, il est essentiel de suivre fréquemment par le pharmacien clinique pour identifier les facteurs précoces qui peuvent contribuer négativement, facilitant la planification des interventions afin de promouvoir une meilleure observance et, par conséquent, d’atteindre des objectifs thérapeutiques.
À cette fin, une stratégie viable et peu coûteuse est la mise en œuvre d’un formulaire de suivi qui sera appliqué par le pharmacien au moment de la dispense. Ainsi, la documentation normalisée des soins dispensés servira non seulement à optimiser la pharmacothérapie, mais aussi à accroître la sécurité des patients, contribuant au développement d’actions visant à l’évolution du patient, à une communication plus efficace entre les équipes multidisciplinaires et à l’aide à la mise en œuvre d’améliorations continues afin de maximiser la qualité des soins prodigués aux patients.
RÉFÉRENCES
ANDERSON, Kristin R. et al. Medication adherence among adults prescribed imatinib, dasatinib, or nilotinib for the treatment of chronic myeloid leukemia. Journal of Oncology Pharmacy Practice, v. 21, n. 1, p. 19-25, 2015.
BAGNYUKOVA, Tetyana V. et al. Chemotherapy and signaling: How can targeted therapies supercharge cytotoxic agents?. Cancer biology & therapy, v. 10, n. 9, p. 839-853, 2010.
BORTOLHEIRO, Teresa C; CHIATTONE, Carlos S. Leucemia mielóide crônica: história natural e classificação. Revista Brasileira de Hematologia e Hemoterapia, v. 30, p. 3-7, 2008.
BRASIL. Ministério da Saúde (MS). Resolução nº 510, de 7 de abril de 2016. Disponível em: http://bvsms.saude.gov.br/bvs/saudelegis/cns/2016/res0510_07_04_2016.html. Acessado em: 23 de maio de 2020.
BRASIL. Ministério da Saúde (MS). Portaria nº 1.219, de 4 de novembro de 2013. Disponível em: http://bvsms.saude.gov.br/bvs/saudelegis/sas/2013/prt1219_04_11_2013.html. Acessado em: 23 de maio de 2020.
BRAY, Freddie et al. Global cancer statistics 2018: GLOBOCAN estimates of incidence and mortality worldwide for 36 cancers in 185 countries. CA: a cancer journal for clinicians, v. 68, n. 6, p. 394-424, 2018.
BRECCIA, Massimo et al. Adherence and future discontinuation of tyrosine kinase inhibitors in chronic phase chronic myeloid leukemia. A patient-based survey on 1133 patients. Leukemia research, v. 39, n. 10, p. 1055-1059, 2015.
CALADO, Deysiane Santos; TAVARES, Diego de Hollanda Cavalcanti; BEZERRA, Grasiela Costa. O papel da atenção farmacêutica na redução das reações adversas associados ao tratamento de pacientes oncológicos. Revista Brasileira de Educação e Saúde, v. 9, n. 3, p. 94-99, 2019.
CHABNER BA, ROBERTS TG Jr. Timeline: chemotherapy and the war on cancer. Nat Rev Cancer, v. 5, p. 65-72, 2005.
DI FELICE, Enza et al. The impact of introducing tyrosine kinase inhibitors on chronic myeloid leukemia survival: a population-based study. BMC cancer, v. 18, n. 1, p. 1069, 2018.
DREWS, Jürgen. Case histories, magic bullets and the state of drug discovery. Nature Reviews Drug Discovery, v. 5, n. 8, p. 635-640, 2006.
FLIS, Sylwia; CHOJNACKI, Tomasz. Chronic myelogenous leukemia, a still unsolved problem: pitfalls and new therapeutic possibilities. Drug design, development and therapy, v. 13, p. 825, 2019.
GEISSLER, Jan et al. Factors influencing adherence in CML and ways to improvement: Results of a patient-driven survey of 2546 patients in 63 countries. Journal of Cancer Research and Clinical Oncology, v. 143, n. 7, p. 1167-1176, 2017.
HEFNER J, CSEF EJ, KUNZMANN V. Fear of progression in outpatients with chronic myeloid leukemia on oral tyrosine kinase inhibitors. In: Oncology Nursing Forum. Oncology Nursing Society, 2016. p. 190.
HOSOYA, Kazuhisa et al. Failure mode and effects analysis of medication adherence in patients with chronic myeloid leukemia. International journal of clinical oncology, v. 20, n. 6, p. 1203-1210, 2015.
Instituto Nacional de Câncer Jose Alencar Gomes da Silva. ABC do câncer: abordagens básicas para o controle do câncer, 5. ed. Rio de Janeiro: INCA, 2019.
Instituto Nacional de Câncer Jose Alencar Gomes da Silva. Estimativa 2018: incidência de câncer no Brasil. Rio de Janeiro, 2017. Disponível em: https://www.inca.gov.br/sites/ufu.sti.inca.local/files//media/document//estimativa-incidencia-de-cancer-no-brasil-2018.pdf. Acesso em: 08 out. 2019.
JULIUSSON, G.; HOUGH, R. Leukemia. Prog Tumor Res 2016; 43: 87–100. Google Scholar| Crossref| Medline.
KEKÄLE, Meri et al. Impact of tailored patient education on adherence of patients with chronic myeloid leukaemia to tyrosine kinase inhibitors: a randomized multicentre intervention study. Journal of advanced nursing, v. 72, n. 9, p. 2196-2206, 2016.
LATREMOUILLE-VIAU, Dominick et al. Health care resource utilization and costs in patients with chronic myeloid leukemia with better adherence to tyrosine kinase inhibitors and increased molecular monitoring frequency. Journal of Managed Care & Specialty Pharmacy, v. 23, n. 2, p. 214-224, 2017.
LIU, Tao; PENG, Xing-Chun; LI, Bin. The Metabolic Profiles in Hematological Malignancies. Indian Journal of Hematology and Blood Transfusion, p. 1-10, 2019.
MOULIN, Silmara Mendes Martins et al. The role of clinical pharmacists in treatment adherence: fast impact in suppression of chronic myeloid leukemia development and symptoms. Supportive Care in Cancer, v. 25, n. 3, p. 951-955, 2017.
MULU FENTIE, Atalay et al. Prevalence and determinants of non-adherence to Imatinib in the first 3-months treatment among newly diagnosed Ethiopian’s with chronic myeloid leukemia. PloS one, v. 14, n. 3, p. e0213557, 2019.
MULUNEH, Benyam et al. Patient perspectives on the barriers associated with medication adherence to oral chemotherapy. Journal of Oncology Pharmacy Practice, v. 24, n. 2, p. 98-109, 2018.
Novartis Biociências S.A. Bula do medicamento Glivec®. Disponível em: https://portal.novartis.com.br/UPLOAD/ImgConteudos/1821.pdf. Acessado em: 20 de agosto de 2020.
RYCHTER, Anna et al. Treatment adherence in chronic myeloid leukaemia patients receiving tyrosine kinase inhibitors. Medical Oncology, v. 34, n. 6, p. 104, 2017.
SACHDEVA, Ashwani et al. Association of leukemia and mitochondrial diseases—A review. Journal of family medicine and primary care, v. 8, n. 10, p. 3120, 2019.
SAUSSELE, Susanne et al. Defining therapy goals for major molecular remission in chronic myeloid leukemia: results of the randomized CML Study IV. Leukemia, v. 32, n. 5, p. 1222-1228, 2018.
SIEGEL, Rebecca L.; MILLER, Kimberly D.; JEMAL, Ahmedin. Cancer statistics, 2019. CA: a cancer journal for clinicians, v. 69, n. 1, p. 7-34, 2019.
SOUZA, Jessica de O. et al. Adherence to TKI in CML patients: more than reports. Supportive Care in Cancer, v. 26, n. 2, p. 325-326, 2018.
TAN, Bee Kim et al. Efficacy of a medication management service in improving adherence to tyrosine kinase inhibitors and clinical outcomes of patients with chronic myeloid leukaemia: a randomised controlled trial. Supportive Care in Cancer, p. 1-11, 2019.
THAVAMANI B. Samuel; MATHEW, Molly; DHANABAL, S. P. Anticancer activity of cissampelos pareira against dalton’s lymphoma ascites bearing mice. Pharmacognosy magazine, v. 10, n. 39, p. 200, 2014.
TRIVEDI, Digisha et al. Adherence and persistence among chronic myeloid leukemia patients during second-line tyrosine kinase inhibitor treatment. Journal of Managed Care Pharmacy, v. 20, n. 10, p. 1006-1015, 2014.
TSAI, Yu-Fen et al. Side effects and medication adherence of tyrosine kinase inhibitors for patients with chronic myeloid leukemia in Taiwan. Medicine, v. 97, n. 26, 2018.
UNNIKRISHNAN, Radhika et al. Comprehensive evaluation of adherence to therapy, its associations, and its implications in patients with chronic myeloid leukemia receiving imatinib. Clinical Lymphoma Myeloma and Leukemia, v. 16, n. 6, p. 366-371. e3, 2016.
WORLD HEALTH ORGANIZATION et al. Adherence to long-term therapies: evidence for action. World Health Organization, 2003.
[1] Pharmacien. Spécialiste en pharmacie clinique et hospitalière, Senac. Spécialiste multiprofessionnel en oncologie (HIAE).
[2] Pharmaceutique. Spécialiste en pharmacie clinique et hospitalière, Senac.
[3] Pharmacien. Spécialiste en pharmacie clinique et hospitalière, Senac.
[4] Pharmaceutique. Spécialiste en pharmacie clinique et hospitalière, Senac.
[5] Pharmacien. Maîtrise en sciences médicales, FMUSP. Spécialiste multiprofessionnel en oncologie (LSH). Spécialiste en pharmacie hospitalière (FOC).
Soumis : août 2020.
Approuvé : octobre 2020.