ÜBERPRÜFUNG ARTIKEL
SBRUZZI, Felipe Augusto [1], SILVA, Kelly Cristina da [2], TELLES, Sérgio Mazero [3], LIMA, Sirlene de Sousa [4], SANTANA, Claudinei Alves [5]
SBRUZZI, Felipe Augusto. Et al. Nachsorgeformular für erwachsene Patienten mit Leukämie mit Imatinib. Revista Científica Multidisciplinar Núcleo do Conhecimento. Jahrgang 05, Ed. 10, Vol. 02, S. 92-112. Oktober 2020. ISSN: 2448-0959, Zugriffsverbindung: https://www.nucleodoconhecimento.com.br/gesundheit/imatinib
ZUSAMMENFASSUNG
Einleitung: Chronische myeloische Leukämie ist eine Art von maligner Blutneoplasie, die hauptsächlich durch das Vorhandensein des Philadelphia-Chromosoms gekennzeichnet ist, aus dem das Onkoprotein BCR-ABL stammt. Es hat die Tyrosinkinaseaktivität erhöht, wodurch Veränderungen in den intrazellulären Signalwegen verursacht und unkontrollierte Proliferation, zelluläre Dysfunktion und Abwesenheit von Apoptose gefördert werden. Trotz der geringen Inzidenz der Krankheit, 1,5 Fälle pro 100.000 Einwohner, veränderte die Therapie mit Imatinib, einem wirksamen Inhibitor von BCR-ABL, die Prognose der Krankheit und verlängerte die Lebenserwartung der Patienten, wodurch eine tödliche Krankheit in eine Krankheit umgewandelt wurde chronische Erkrankung. Ziel: Entwicklung eines Formulars zur regelmäßigen Überwachung dieser Patienten durch den klinischen Apotheker, um eine sichere und wirksame Pharmakotherapie zu gewährleisten. Methodik: Aus der Problemfrage wurde eine Literaturrecherche vom narrativen Typ eingeleitet: “Welche Daten sollte der klinische Apotheker während der pharmazeutischen Unterstützung sammeln, um die Adhärenz bei erwachsenen Patienten mit chronischer myeloischer Leukämie unter Verwendung von Imatinib zu bewerten und zu verbessern?” , gefolgt von der Suche nach Artikeln in PubMed-Datenbanken und Regierungswebsites. Anschließend wurden Arbeitsauswahl und kritische Analyse durchgeführt, um ein Modellformular zu erstellen, das beim Abgeben angewendet werden kann. Ergebnis und Diskussion. Elf Artikel wurden ausgewählt. Die geringe Einhaltung der Behandlung der chronischen myeloischen Leukämie durch den Patienten kann möglicherweise lebensbedrohlich sein. Daher ist das Follow-up-Formular, das der klinische Apotheker bei der Abgabe von Imatinibmesylat anwenden muss, eine praktikable und kostengünstige Strategie, um die Einhaltung der Pharmakotherapie zu verbessern und ein besseres Ansprechen auf die Behandlung zu fördern. Schlussfolgerung: Die systematische und standardisierte Dokumentation der Einhaltung und der Nebenwirkungen durch den klinischen Apotheker ermöglicht die Umsetzung von Maßnahmen des multidisziplinären Teams zur kontinuierlichen Verbesserung, um die Qualität der Patientenversorgung sowie die Lebensqualität zu maximieren.
Schlagworte: Leukämie, pharmakotherapeutische Nachsorge, Imatinib.
EINFÜHRUNG
Krebs ist der Name einer Reihe von mehr als hundert Pathologien, die als gemeinsame Merkmale die Einleitung durch Schädigung bestimmter DNA-Gene und das autonome und ungeordnete Wachstum von Zellen hat, die die Fähigkeit erwerben, in benachbarte Organe und Gewebe einzudringen, was zu Funktionsstörungen führt (THAVAMANI et al., 2014).
Diese abnorme Zellproliferation ist als Neoplasie bekannt und in der Praxis wird sie Tumor genannt und kann als bösartig oder gutartig eingestuft werden (INSTITUTO NACIONAL DO CÂNCER, 2019).
Eine besondere Gruppe bösartiger Neoplasmen sind Leukämien, die durch eine abnormale Proliferation von Knochenmarkzellen-Vorläufern der weißen Abstammung gekennzeichnet sind (JULIUSSON And HOUGH, 2016; LIU et al., 2019). Leukämien können nach der Art der betroffenen Zelle, lymphozytischen oder myeloischen, und in Bezug auf die charakteristische, akute oder chronische (SACHDEVA et al., 2019).
Chronische myeloische Leukämie (CML) ist eine Art von Blutkrankheit, die durch eine Zunahme der Anzahl von Leukozyten mit linker Abweichung, Splenomegalie und dem Vorhandensein des Philadelphia-Chromosoms (Ph) gekennzeichnet ist, die sich aus der wechselseitigen Translokation zwischen Chromosomen (9;22) (q34;q11) ergibt, was zu bcr-abl Protein, mit erhöhter Tyrosinkinase-Aktivität (FLIS UND CHOJNACKI, 2019) führt.
Das BCR-ABL-Protein ist bei mehr als 90% der Patienten mit CML vorhanden, und seine Hyperaktivität stimuliert die Freisetzung von Zellproliferationseffektoren und Apoptose-Inhibitoren, und seine Aktivität ist verantwortlich für den Prozess der Krebsbildung in CML (DI FELICE et al., 2018).
Die Entdeckung dieser molekularen Veränderung zusätzlich zur Optimierung der Diagnose von CML lieferte auch die Entwicklung von Therapien, die auf diese molekulare Veränderung abzielen, und Methoden zur Überwachung minimaler Resterkrankungen, die eine Verbesserung der Behandlung bieten (BORTOLHEIRO AND CHIATTONE, 2008).
CML präsentiert 3 verschiedene klinische Phasen, die im Verlauf der Krankheit entstehen und als chronische Phase, Transformationsphase und End- oder Explosionsphase klassifiziert werden (HEFNER et al., 2016).
Traditionell kann die Krebsbehandlung durch Operation, Chemotherapie und Strahlentherapie-Modalitäten durchgeführt werden, und die Kombination ist üblich, um ein besseres klinisches Ergebnis zu erzielen (INSTITUO NACIONAL DE CÂNCER, 2019).
Die klassische Chemotherapie zielt auf die Zerstörung von Zellen in der schnellen Replikation ab, die auf Mutationen und/oder wichtige Veränderungen in der DNA hindeuten, jedoch werden normale Gewebezellen, die ebenfalls eine schnelle Replikation haben, zerstört, wodurch zahlreiche nebenwirkungende Wirkungen für Patienten auftreten (BAGNYKOVA et al., 2010).
In Krebszellen, wie CML, werden intrazelluläre Signalwege verändert, die unkontrollierte Proliferation, zelluläre Dysfunktion und das Fehlen von Apoptose fördern (ANDERSON et al., 2015). Basierend auf einem besseren Verständnis dieser Prozesse, die in den 1980er Jahren initiiert wurden, begannen Medikamente, die als Tyrosinkinase-Inhibitoren (ITQ) bezeichnet werden, untersucht zu werden (CHABNER And ROBERTS, 2005).
Bei LMC wurde das Onkogen BCR-ABL aufgrund seiner pathognomonischen Eigenschaften zum idealen Kandidaten für das von Paul Ehrlich idealisierte “Wundermittel” (Chabner und Roberts, 2005). Daher versucht die “Zieltherapie” mit ITQ, die deregulierten Signalwege der neoplastischen Zellen von Patienten mit CML selektiv zu hemmen, wobei als erstes Medikament Imatinibmesylat verwendet wird, ein wirksamer Inhibitor von BCR-ABL (DREWS, 2006; MOULIN et al ., 2017).
Aufgrund der Alterung und des Bevölkerungswachstums hat die Inzidenz und Mortalität von Krebs weltweit zugenommen (BRAY et al., 2018). In Brasilien schätzt das National Cancer Institute (INCA), dass für jedes Jahr der Zweijahresperiode 2018/2019 600.000 neue Krebsfälle diagnostiziert werden, von denen Leukämien bei Männern mit 5.940 Neuerkrankungen auf Platz 9 und bei Frauen auf Platz 10 liegen 4.860 neue Fälle (INSTITUTO NACIONAL DE CÂNCER, 2017).
AUF CML entfallen etwa 15 % der neuen Leukämiefälle mit einem geschätzten Risiko von 1,5 Fällen pro 100.000 Personen (RYCHTER et al., 2017). Trotz der geringen Inzidenz im Vergleich zu anderen Krebsarten (Lunge, Prostata, Brust), aufgrund der Imatinib-Mesiat-Therapie, zeigten Patienten mit CML eine erhebliche Verbesserung der 5-Jahres-Überlebensrate und modifizierten die Prognose der Krankheit (TRIVEDI et al., 2014; SAUSSELE et al., 2018; TAN et al., 2019; LATREMOUILLE-VIAU et al., 2017).
Bei Patienten, die Mitte der 1970er Jahre diagnostiziert wurden, betrug die 5-Jahres-Überlebensrate 22 %, von 2008 bis 2014, 69 %, und derzeit haben die meisten Patienten, die TQI erhalten, eine Lebenserwartung, die mit normalen Menschen kompatibel ist, was CML derzeit als chronische Erkrankung betrachtet, die eine regelmäßige Nachbeobachtung durch das Gesundheitsteam erfordert (SIEGEL et al. , 2019).
Die Behandlung von CML erfordert das integrierte Handeln des multidisziplinären Teams, und der Pharmafachmann ist bei der pharmakotherapeutischen Nachbeobachtung (PN) der Krebsbehandlung unverzichtbar, um eine sichere und wirksame Pharmakotherapie zu gewährleisten (SOUZA et al., 2018).
PN ist eine personalisierte Praxis, in der der klinische Apotheker die Verantwortung für Dieführung, Erkennung, Prävention und Lösung von arzneimittelbedingten Problemen hat, die die nebenwirkungen der Chemotherapie und der verwendeten Therapie sowie die Verabreichungstechniken, die Einhaltung der Behandlung und arzneimitteler Wechselwirkungen abdecken (CALADO et al., 2019).
Angesichts der Komplexität von CML ist die Nachsorge des klinischen Pharmafachs für die Wirksamkeit der Behandlung von entscheidender Bedeutung.
ZIELSETZUNG
Erstellen Sie ein pharmakotherapeutisches Follow-up-Formularmodell für erwachsene Patienten mit positiver BCL-ABR chronischer myeloischer Leukämie mit Imatinib Mesiduct.
METHODIK
Das Werk ist eine Literaturrezension des Erzähltyps. So aus der Problemfrage: “Welche Daten sollte der Klinische Apotheker während der pharmazeutischen Unterstützung sammeln, um die Adhärenz von erwachsenen Patienten mit chronischer myeloischer Leukämie mit Imatinib zu bewerten und zu verbessern?” Eine Suche wurde auf der PubMed-Plattform auf basis der PICO-Strategie durchgeführt und die Deskriptoren wurden verwendet: “leukemia, myelogenous, chronic, bcr-abl positive” AND “medication adherence”. Die Artikel der letzten 5 Jahre wurden berücksichtigt und die Suche wurde in der Datenbank von Juni bis Dezember 2019 durchgeführt.
Die Inklusionskriterien waren: Artikel in voller Online-Version, in englischer Sprache, die als erwachsene Patienten der Bevölkerung verfügbar waren, und mit dem Thema der Bewertung der Arzneimitteltreue in CML. Als Ausschlusskriterien waren: Artikel, die ausschließlich ein anderes Medikament als Imatinib-Mesysirate bewerteten, das kein Formular verwendet.
Auch, um das Formular zu bilden wurden konsultiert Regierungswebsites.
ERGEBNIS UND DISKUSSION
Die Recherche auf der Pubmed-Website mit den Deskriptoren führte zu 52 Artikeln, von dem auf der Grundlage der Aufnahme- und Ausschlusskriterien 11 ausgewählt wurden, um die Literaturrecherche bei der Erstellung des Formulars zu bilden.
Diese Artikel sind in Tabelle 1 in der Reihenfolge des absteigenden Datums der Veröffentlichung dargestellt.
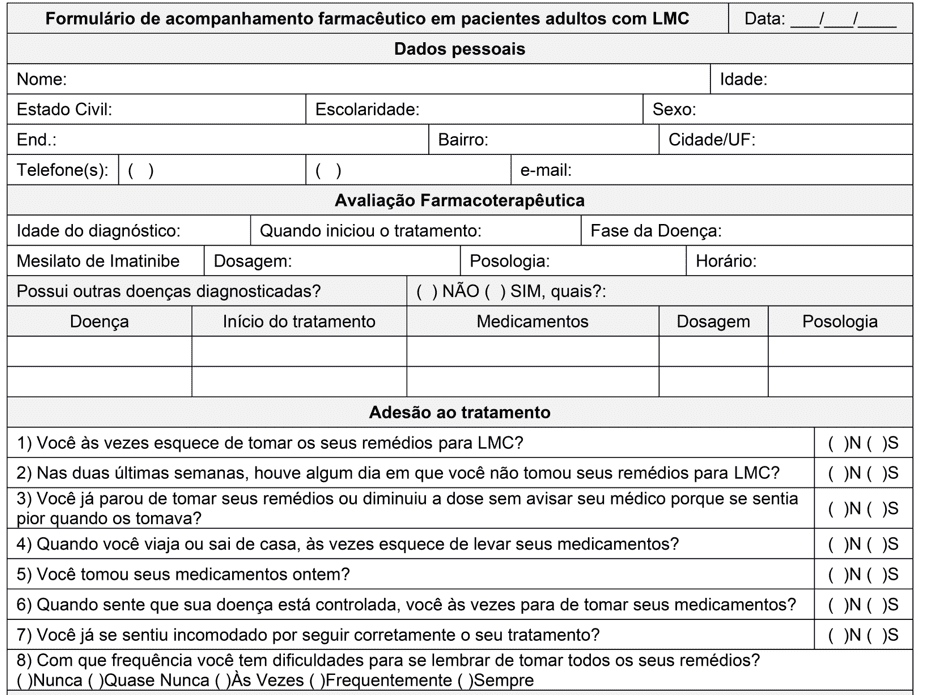
Nach dem, was von Moulin et al. beobachtet wurde, verbesserte die Einbeziehung des Klinischen Apothekers während der Behandlung von Patienten mit CML nicht nur die Adhärenz der Behandlung und verringerte die von den Patienten berichteten unerwünschten Arzneimittelwirkungen (UA), sondern verbesserte auch die zytogenetischen Parameter (MOULIN et al., 2017). In dieser Studie fanden die Autoren nach 4 Monaten Follow-up eine geringere Expression des Philadelphia-Chromosoms in der überwachten Gruppe in Bezug auf die nicht überwachte Kontrolle. In der überwachten Gruppe stieg das gesamte beobachtete zytogenetische Ansprechen von 87,0 % auf 95,6 % der Patienten, während es in der nicht überwachten Gruppe bei 61,5 % blieb. Somit ist die Anwendung eines Formulars zum Zeitpunkt der Dispensation eine effektive Strategie, um den Patienten zu begleiten und die Behandlungstreue zu verbessern. Um dieses Ziel zu erreichen, wurde bei erwachsenen Patienten mit CML (Anhang I) ein pharmazeutisches Nachsorgeformular erstellt.
Der erste Teil des Formulars dient dazu, die persönlichen Daten der Patienten zu sammeln, um den Kontakt mit dem Patienten zu identifizieren und zu erleichtern. Dies liegt daran, dass einige der ausgewählten Studien zeigen, dass in einigen Populationen die Ades durch einige sozioökonomische Merkmale begünstigt werden können, aber die Studien unterscheiden sich darüber, welche in der Bevölkerung präsenter sind. Tsai et al (2018) fanden in der Studienpopulation heraus, dass ältere Patienten und verheiratete Patienten eine bessere Adhärenz haben. Nach Rychter et al (2017) sind das Vorhandensein von mindestens 1 Komorbidität und Alter über 65 Jahre günstige Eigenschaften für die Beweigung. Im Gegensatz dazu fanden Unnikrishnan et al (2016) und Hefner et al (2016) keinen Zusammenhang zwischen den sozioökonomischen Merkmalen der untersuchten Bevölkerung und der anhaftenden Behandlung. So wird beobachtet, dass die Korrelation zwischen sozioökonomischen Daten und DerBindung je nach untersuchter Bevölkerung variiert, da es sich nicht um einen prädiktiven Parameter für die Patientenbindung oder Nicht-Adhärenz handelt.
Tabelle 1.A – Artikel, die auf der Grundlage von Inklusions- und Ausschlusskriterien ausgewählt wurden, absteigende Reihenfolge des Jahres der Veröffentlichung.
| Autor/Jahr | Titel | Ziele | Form von Adecin | N(1) | Land | Medikamente |
| MULU FENTIE et al., 2019 | Prevalence and determinants of non-adherence to Imatinib in the first 3-months treatment among newly diagnosed Ethiopian’s with chronic myeloid leukemia. | Bewertung der Prävalenz und der Gründe für die Nichteinhaltung von Imatinib bei Patienten mit CML(2), die kürzlich in den ersten 3 Monaten der Behandlung diagnostiziert wurden. | MMAS-8(3) | 147 | Äthiopien | Imatinib |
| TSAI et al., 2018 | Side effects and medication adherence of tyrosine kinase inhibitors for patients with chronic myeloid leukemia in Taiwan. | Klärung des Einflusses nachteiliger Auswirkungen auf die Adhärenz bei taiwanesischen Patienten mit CML(2). | MMAS-8(3) | 58 | Taiwan | Imatinibe
Dasatinibe Nilotinibe |
| HEFNER et al., 2017 | Adherence and Coping Strategies in Outpatients With Chronic Myeloid Leukemia Receiving Oral Tyrosine Kinase Inhibitors. | Bewertung von Haft- und Bewältigungsstrategien bei Patienten außerhalb des Krankenhausumfelds mit CML(2). | BAASIS(4) | 35 | Deutschland | Tyrosinkinase-Inhibitoren |
(1)N = Anzahl der Teilnehmer; (2)CML = Chronische myeloische Leukämie; (3)MMAS-8 = 8-item Morisky Therapeutic Adherence Scale;(4)BAASIS = Basel Scale for Immunosuppressive Drug Adherence Assessment; (5)MMAS-4 = 4-teilige Morisky Therapeutic Adherence Scale.
Tabelle 1.B – Artikel, die auf der Grundlage von Inklusions- und Ausschlusskriterien ausgewählt wurden, absteigende Reihenfolge des Jahres der Veröffentlichung.
| Autor/Jahr | Titel | Ziele | Form von Adecin | N(1) | Land | Medikamente |
| RYCHTER et al., 2017 | Treatment adherence in chronic myeloid leukaemia patients receiving tyrosine kinase inhibitors. | Bewertung der Behandlung mit cmL-Patienten mit CML(2) | Form für die Studie entwickelt. | 140 | Polen | Imatinib
Dasatinib Nilotinib |
| GEISSLEr et al., 2017 | Factors influencing adherence in CML and ways to improvement: Results of a patient-driven survey of 2546 patients in 63 countries. | Bewertung des Ausmaßes der suboptimalen Adhärenz und Untersuchung der Gründe und Muster des Adhärenverhaltens von Patienten mit CML(2) auf der ganzen Welt. | MMAS-8(3) | 2546 | 63 Länder | Imatinib
Dasatinib Nilotinib Andere Behandlung |
| MULUNEH et al., 2016 | Patient perspectives on the barriers associated with medication adherence to oral chemotherapy. | Analysieren Sie durch einen Fragebogen die Anwendung einer oralen Chemotherapie und identifizieren Sie Verbesserungsmöglichkeiten im Folgenden. | Fragebogen mit 30 Fragen angepasst | 93 | USA | Orale Chemotherapie |
(1) N = Anzahl der Teilnehmer; (2) CML = Chronische myeloische Leukämie; (3) MMAS-8 = 8-item Morisky Therapeutic Adherence Scale; (4)BAASIS = Basel Scale for Immunosuppressive Drug Adherence Assessment; (5)MMAS-4 = 4-teilige Morisky Therapeutic Adherence Scale
Tabelle 1.C – Artikel, die auf der Grundlage von Aufnahme- und Ausschlusskriterien ausgewählt wurden, absteigende Reihenfolge des Jahres der Veröffentlichung.
| Autor/Jahr | Titel | Ziele | Form von Adecin | N(1) | Land | Medikamente |
| MOULIN et al.
Nov/201614 |
The role of clinical pharmacists in treatment adherence: fast impact in suppression of chronic myeloid leukemia development and symptoms | Bewertung der Rolle des klinischen Apothekers bei der Behandlung von Patienten mit CML(2) sowie der Beteiligung des klinischen Apothekers. | MMAS-4(5) | 23 | Brazilien | Tyrosinkinase-Inhibitoren |
| KEKÄLE et al., 2016 | Impact of tailored patient education on adherence of patients with chronic myeloid leukaemia to tyrosine kinase inhibitors: a randomized multicentre intervention study. | Bewertung des Einflusses der personalisierten Ausbildung an den Patienten auf die Einhaltung von ITQ bei Patienten mit CML(2). | MMAS-8(3) | 86 | Finnland | Tyrosinkinase-Inhibitoren |
| UNNIKRISHNAN et al., 2016 | Comprehensive Evaluation of Adherence to Therapy, Its Associations, and Its Implications in Patients With Chronic Myeloid Leukemia Receiving Imatinib. | Bewerten Sie Dievortung und Lebensqualität bei Patienten mit CML(2), die Imatinib für einen langen Zeitraum erhalten. | MMAS-8(3) | 221 | Indien | Imatinib |
(1) N = Anzahl der Teilnehmer; (2) CML = Chronische myeloische Leukämie; (3) MMAS-8 = 8-item Morisky Therapeutic Adherence Scale;(4)BAASIS = Basel Scale for Immunosuppressive Drug Adherence Assessment; (5) MMAS-4 = 4-teilige Morisky Therapeutic Adherence Scale
Tabelle 1.D – Artikel, die auf der Grundlage von Aufnahme- und Ausschlusskriterien ausgewählt wurden, absteigende Reihenfolge des Jahres der Veröffentlichung.
| Autor/Jahr | Titel | Ziele | Form von Adecin | N(1) | Land | Medikamente |
| HOSOYA et al., 2015 | Failure mode and effects analysis of medication adherence in patients with chronic myeloid leukemia | Identifizieren Sie anhand des Fehlermodus und der Effektanalyse, wie niedrige Adhärenz bei Patienten mit CML(2) auftritt. | Form für die Studie entwickelt | 54 | Japan | Imatinibe
Dasatinibe Nilotinibe |
| BRECCIA et al., 2015 | Adherence and future discontinuation of tyrosine kinase inhibitors in chronic phase chronic myeloid leukemia. A patient-based survey on 1133 patients. | Untersuchung der Einhaltung und des potenziellen Nutzens bei der Lebensqualität, der Zufriedenheit mit der Behandlung und des sozialen Lebens bei Patienten mit CML(2) | Form für die Studie entwickelt. | 1133 | Italien | Tyrosinkinase-Inhibitoren |
(1) N = Anzahl der Teilnehmer; (2) CML = Chronische myeloische Leukämie; (3) MMAS-8 = 8-item Morisky Therapeutic Adherence Scale;(4)BAASIS = Basel Scale for Immunosuppressive Drug Adherence Assessment; (5)MMAS-4 = 4-teilige Morisky Therapeutic Adherence Scale
Eine der Zuschreibungen des klinischen Apothekers ist die Bewertung der Pharmakotherapie, so dass der Patient die Medikamente, die er benötigt, sicher verwenden kann, in den entsprechenden Dosen, Häufigkeit und Zeitplänen, um so die therapeutischen Ziele zu erreichen. Dazu wurden bestimmte Bereiche vorbehalten, um das Alter der Diagnose, den Beginn der Behandlung, die Krankheitsphase und die Parameter im Zusammenhang mit der Imatinib-Pharmakotherapie zu erfassen.
In Brasilien legt die Verordnung Nr. 1.219 vom 4. November 2013 das klinische Protokoll und die therapeutischen Richtlinien für CML bei Erwachsenen fest und ist eine Referenz für die pharmakotherapeutische Bewertung dieser Patienten. Hierbei wird die Verwendung von Imatinib als Erstlinientherapie empfohlen und welche Pharmakotherapie für chronische Phasen (CP) und Transformation oder Beschleunigung (TB) (BRASIL, 2013).
In CP wird eine Einzeldosis 400 mg/Tag oral nach der größten Mahlzeit des Tages empfohlen, und kann in zwei Dosen von 300 mg eskalieren, eine am Morgen und die andere am Abend, wenn nach drei Monaten eine unzureichende Reaktion, Verlust der vorherigen Reaktion oder Progression der Krankheit. In Bezug auf TB beträgt die empfohlene Dosis 600mg/Tag und kann bei Explosionskrisen bis zu 800 mg/Tag erhöht werden (BRASIL, 2013).
Der klinische Apotheker sollte nicht nur eine grundlegende Rolle bei der Patientenbehandlung spielen, sondern auch Arzneimittelwechselwirkungen identifizieren, bewerten und eingreifen. Um mögliche Wechselwirkungen mit Arzneimitteln während der Anwendung von Imatinib zu bewerten, wird das Vorhandensein anderer Krankheiten und Pharmakotherapien dieser Krankheiten in der Form bewertet. Im Falle von Arzneimittelwechselwirkungen sollte der Apotheker sich der Medikamente bewusst sein, die eine Lebermetabolisierung haben, da Imatinib auf diesem Weg durch das Enzym CYP3A4 metabolisiert wird (GLIVEC, 2020). Die Aufrechterhaltung einer Blutkonzentration von mehr als 300mg ist extrem wichtig für den Erfolg der molekularen/zytogenetischen Reaktion und ein erhöhtes Überleben ohne Krankheitsprogression (BRASIL, 2013). Daher sollten Induktoren dieses Enzyms wie Dtethason und Hypericum perforatum, die Plasmakonzentration von Imatinib reduzieren können, vermieden werden. Neben Inhibitoren wie Ketoconazol, Clarithromycin, die den Stoffwechsel verringern und die Konzentrationen von Imatinib führenkönnte, gibt es einen Anstieg der UA (GLIVEC, 2020).
Der zweite Teil des Artikels zielt darauf ab, die Behandlung des Patienten zu bewerten. Nach der Definition der Weltgesundheitsorganisation (WHO) ist die Einhaltung chronischer Krankheiten der Grad, in dem das Verhalten einer Person mit den Empfehlungen eines Arztes übereinstimmt und das Verhalten durch Medikamenteneinnahme, Diät-Follow-up oder Lebensstiländerungen dargestellt werden kann (WHO, 2003)
In den ausgewählten Artikeln wurden die folgenden Artikel durch Fragebögen gemessen, die dieses Verhalten durch Maßnahmen bewerten, die für die Behandlung von CML relevant sind, wie z. B.: Vergessen einer oder mehrerer Dosen, Dosisänderung ohne Benachrichtigung des Verschreibenden, nichtdie Einnahme von Medikamenten, weil er sich gut fühlt oder weil er eine Unerwünschte Wirkung hat. Das am häufigsten verwendete Fragebogenmodell in den Artikeln (sechs von elf ausgewählten) zur Beurteilung der Einhaltung war die Morisky Therapeutic Adherence Scale, wobei 8 Positionen (MMAS-8) am häufigsten waren. Zuvor wurde der MMAS-8 für die Zusammensetzung der begleite Form ausgewählt.
Ein weiterer wichtiger Faktor für die Wahl war die Zeit, die für die Anwendung benötigt wurde, und die Leichtigkeit, den Patienten zu klassifizieren. Das MMAS-8 besteht aus sieben Fragen mit “Ja” oder “Nein” Alternativen und einem Element (dem letzten), das eine Likert-Skala von 5 Punkten aufweist (von 0 Punkten bis “immer” bis 1 Punkt bis “nie”). Jedes Element Assing ein bestimmtes Verhalten der Medikamentenkonsum und ist nicht eine Determinante des Verhaltens von Medikamenten. MMAS-Scores können zwischen 0 und 8 liegen, und die Patienten werden in drei Unterstützungsstufen eingeteilt: hohe Festigkeit (Score 8); mittlere Abscheidung (Score 6 bis 7.75); geringe Aufnahme (<6).
Ein modifizierter Fragebogen der Baseler Skala für immunsuppressive Sdrug Adepitus Assessment (BAASIS) wurde von Hefner et al (2016) verwendet. Dies hat vier “Ja” oder “Nein” Fragen und nur eine positive Antwort ist erforderlich, um den Patienten als “nicht-anhänger”, die eine negative Antwort beim Patienten im Vergleich zu der Klassifizierung von MMAS-8 (hohe, mittlere und niedrige Unterstützung) provozieren kann. Ein weiterer Faktor, der zur Wahl in Betracht gezogen wurde, war das Fehlen von Problemen im Zusammenhang mit dem Verhalten in BAASIS, “um die Einnahme von Medikamenten zu beenden, wenn Sie das Gefühl haben, dass die Krankheit kontrolliert wird”. Dies liegt daran, dass in einigen Studien festgestellt wurde, dass Patienten im ersten und zweiten Jahr nach der Diagnose tendenziell stärker haften, wahrscheinlich aufgrund verminderter Symptome und UA deutlicher werden als die Krankheit selbst (GEISSLER et al., 2017).
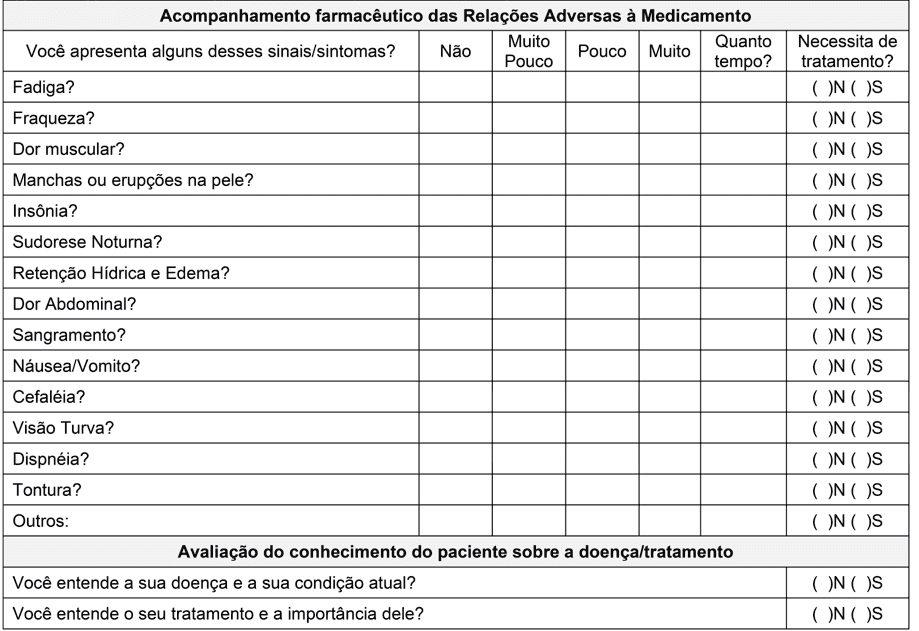
Um UA und seine Auswirkungen auf die Anzeige zu bewerten, wurde ein dritter Teil mit Fragen zu den häufigsten Reaktionen in das Formular aufgenommen.
Laut einer Kohortenstudie, die in Äthiopien von Mulu Fentie et al.(2019) durchgeführt wurde, wurde festgestellt, dass der Hauptgrund für die Nichtbehandlung Nebenwirkungen im Zusammenhang mit Imatinib waren, mit Medikamenten, die 68,8% betrugen. Und die Hauptbeschwerde über 68% waren im Zusammenhang mit magenintestinalen Wirkungen. Die Studie zeigt auch, dass Patienten, die keine UA erlebten, sechsmal häufiger an der Behandlung festhielten.
Wie bereits erwähnt, zeigten Moulin et al (2017), dass die Wirkung des Klinischen Apothekers durch pharmakologische Nachbeobachtung die Adhärenz verbesserte und Nebenwirkungen reduzierte. Während der vier Monate der Nachbeobachtung reduzierten die Forscher die Anzahl der Nicht-Anhänger von acht auf Null, indem sie die 4-Punkte-Morisky Therapeutic Adherence Scale nutzten. Darüber hinaus ging die Zahl der Patienten, die sich über UA beschwerten, von 35 % auf 7 % zurück.
Andererseits ergab eine Studie mit 63 Ländern und 2546 von durchgeführten Patienten, dass nicht die Tatsache, dass bei dem Patienten UA auftreten, die Einhaltung beeinflusst, sondern vielmehr, wie gut das multiprofessionelle Team sein Management durchführt (GEISSLER et al., 2017).
Im Gegenspiel ergab eine Studie mit 63 Ländern und 2546 Patienten, dass es nicht die Tatsache ist, dass der Patient eine UA erlebt, die die Einhaltung beeinflusst, sondern wie gut das Management dieser Probleme vom multidisziplinären Team durchgeführt wird (GEISSLER et al., 2017).
Angesichts dieser Ergebnisse haben wir Beweise dafür gefunden, dass der beste Weg zur Förderung der Behandlung adeforego darin besteht, unerwünschte Ereignisse zu umgehen oder sogar, wenn möglich, mögliche zukünftige unerwünschte Ereignisse zu vermeiden, um eine bessere Behandlung zu fördern. Dies sind die Gründe, warum wir in der Form Fragen über die wichtigsten UA für Imatinib Sysysate beschrieben, die Intensität und Zeit, die der Patient erlebt sie und fühlt die Notwendigkeit für eine Behandlung. So hoffen wir, die wichtigsten unerwünschten Wirkungen im Zusammenhang mit Medikamenten zu identifizieren und zu umgehen, um mehr Sicherheit, Unterstützung und die Lebensqualität der Patienten zu fördern.
Obwohl die gewählte Strategie zur Bewertung und Verbesserung der UA von Patienten die Form ist, fanden Geissler et al (2017) heraus, dass ein wichtiger Faktor, der die Adhärenz beeinflusst und von gesundheitsmedizinischen Fachkräften beeinflusst werden kann, Patienteninformationen über CML sind. In dieser Studie waren Patienten, die sich besser über die Krankheit informiert fühlten, deutlich stärker anhaftend. So wurden zwei Fragen in unsere Form eingefügt, um das Wissen des Patienten über die Krankheit/Behandlung zu bewerten und so unter Beteiligung des multidisziplinären Teams ergänzende Strategien zu planen. Noch mit diesen Informationen, es wird erwartet, dass der Patient aktiver in die Behandlung zu integrieren, die Betonung der Informationen und nicht nur in der Anweisung, dass es folgen sollte.
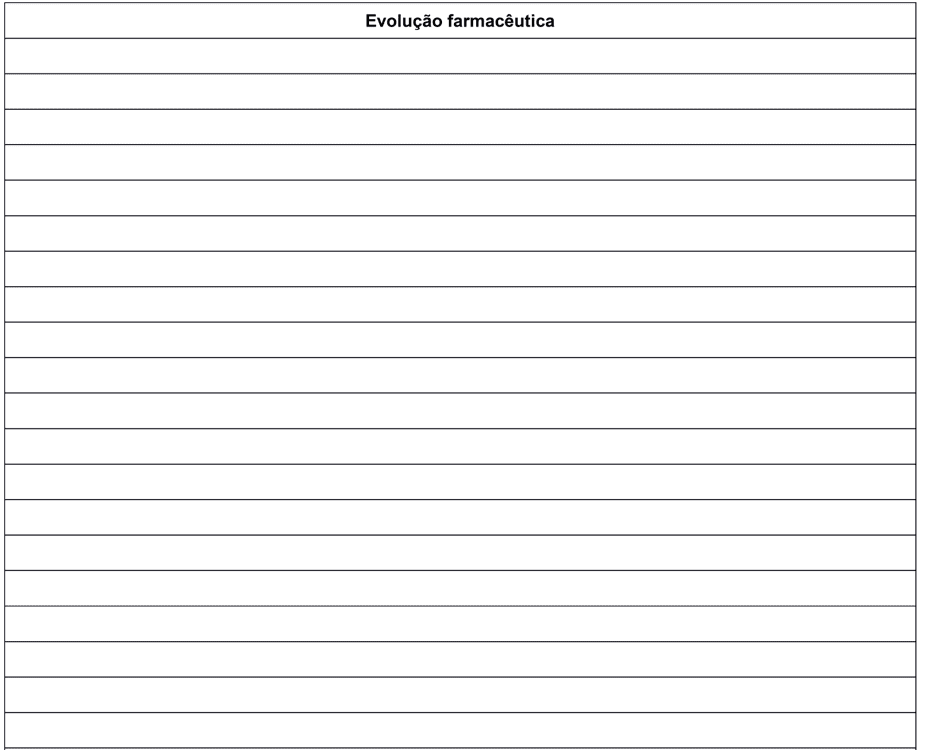
Während der Vorbereitung des Formulars war es nicht möglich, Situationen oder UA vorherzusehen, die Patienten melden konnten. Allerdings wurde die Rückseite des Formulars für das Feld “Pharmaceutical Evolution” verwendet, wo sie beispielsweise notiert werden können: subjektive Daten, objektive Daten, Auswertung und spezifische Planung für den evaluierten Patienten.
Der Vorschlag, das Formularmodell für die Anwendung bei Patienten mit CML zu konstruieren, zielt darauf ab, das Ansprechen auf die Behandlung mit Imatinib Mesirate und die Lebensqualität zu verbessern. Daher ist bisher nicht beabsichtigt, die Ergebnisse dieser Tätigkeit in ein Forschungsprojekt zu integrieren. Daher wurden keine Bedingungen der Klarstellung und Zustimmung oder ein anderes Dokument erstellt, um der Resolution Nr. 510 vom 7. April 2016 des Gesundheitsministeriums zu entsprechen. Diese Entschließung sieht Forschung vor, deren methodische Verfahren die Verwendung von Daten beinhalten, die direkt von Teilnehmern erhalten wurden, oder identifizierbare Informationen (BRASIL, 2016). Auf der Rückseite des Formulars wird jedoch ein vom Patienten oder seinem Vertreter zu unterzeichnender Text mit der Angabe versehen, dass er sich bewusst ist, dass die zur Verfügung gestellten Daten für die pharmakotherapeutische Nachbeobachtung der Behandlung von chronischer myeloischer Leukämie verwendet werden.
Anhang I – Pharmazeutisches Nachsorgeformular bei erwachsenen Patienten mit CML.
FAZIT
Es ist bekannt, dass mehrere Faktoren als Hindernisse für die Nichtbehandlung der pharmakologischen Behandlung dienen, wie: unerwünschte Ereignisse, tägliche Routine der Medikamente, Wohlbefinden ohne Behandlung, unzureichende Informationen über das Medikament. Jedoch, insbesondere bei chronischer myeloischer Leukämie, Nichtbehandlung mit Imatinib Mesilate kann zu einer potenziellen lebensbedrohlichen Behandlung führen, da der Ausgang dieser Krankheit gut bekannt und dokumentiert ist. Daher ist es wichtig, dass der klinische Apotheker häufig nachverfolgt wird, um frühe Faktoren zu identifizieren, die negativ beitragen können, was die Planung von Interventionen erleichtert, um eine bessere Adhärenz zu fördern und damit therapeutische Ziele zu erreichen.
Zu diesem Zweck ist eine tragfähige und kostengünstige Strategie die Umsetzung eines Folgeformulars, das der Apotheker zum Zeitpunkt der Abgabe anwenden muss. So dient die standardisierte Dokumentation der angebotenen Versorgung nicht nur der Optimierung der Pharmakotherapie, sondern auch der Erhöhung der Patientensicherheit, die zur Entwicklung von Maßnahmen zur Entwicklung des Patienten beiträgt, eine effektivere Kommunikation zwischen multidisziplinären Teams ermöglicht und bei der Umsetzung kontinuierlicher Verbesserungen hilft, um die Qualität der Versorgung der Patienten zu maximieren.
REFERENZEN
ANDERSON, Kristin R. et al. Medication adherence among adults prescribed imatinib, dasatinib, or nilotinib for the treatment of chronic myeloid leukemia. Journal of Oncology Pharmacy Practice, v. 21, n. 1, p. 19-25, 2015.
BAGNYUKOVA, Tetyana V. et al. Chemotherapy and signaling: How can targeted therapies supercharge cytotoxic agents?. Cancer biology & therapy, v. 10, n. 9, p. 839-853, 2010.
BORTOLHEIRO, Teresa C; CHIATTONE, Carlos S. Leucemia mielóide crônica: história natural e classificação. Revista Brasileira de Hematologia e Hemoterapia, v. 30, p. 3-7, 2008.
BRASIL. Ministério da Saúde (MS). Resolução nº 510, de 7 de abril de 2016. Disponível em: http://bvsms.saude.gov.br/bvs/saudelegis/cns/2016/res0510_07_04_2016.html. Acessado em: 23 de maio de 2020.
BRASIL. Ministério da Saúde (MS). Portaria nº 1.219, de 4 de novembro de 2013. Disponível em: http://bvsms.saude.gov.br/bvs/saudelegis/sas/2013/prt1219_04_11_2013.html. Acessado em: 23 de maio de 2020.
BRAY, Freddie et al. Global cancer statistics 2018: GLOBOCAN estimates of incidence and mortality worldwide for 36 cancers in 185 countries. CA: a cancer journal for clinicians, v. 68, n. 6, p. 394-424, 2018.
BRECCIA, Massimo et al. Adherence and future discontinuation of tyrosine kinase inhibitors in chronic phase chronic myeloid leukemia. A patient-based survey on 1133 patients. Leukemia research, v. 39, n. 10, p. 1055-1059, 2015.
CALADO, Deysiane Santos; TAVARES, Diego de Hollanda Cavalcanti; BEZERRA, Grasiela Costa. O papel da atenção farmacêutica na redução das reações adversas associados ao tratamento de pacientes oncológicos. Revista Brasileira de Educação e Saúde, v. 9, n. 3, p. 94-99, 2019.
CHABNER BA, ROBERTS TG Jr. Timeline: chemotherapy and the war on cancer. Nat Rev Cancer, v. 5, p. 65-72, 2005.
DI FELICE, Enza et al. The impact of introducing tyrosine kinase inhibitors on chronic myeloid leukemia survival: a population-based study. BMC cancer, v. 18, n. 1, p. 1069, 2018.
DREWS, Jürgen. Case histories, magic bullets and the state of drug discovery. Nature Reviews Drug Discovery, v. 5, n. 8, p. 635-640, 2006.
FLIS, Sylwia; CHOJNACKI, Tomasz. Chronic myelogenous leukemia, a still unsolved problem: pitfalls and new therapeutic possibilities. Drug design, development and therapy, v. 13, p. 825, 2019.
GEISSLER, Jan et al. Factors influencing adherence in CML and ways to improvement: Results of a patient-driven survey of 2546 patients in 63 countries. Journal of Cancer Research and Clinical Oncology, v. 143, n. 7, p. 1167-1176, 2017.
HEFNER J, CSEF EJ, KUNZMANN V. Fear of progression in outpatients with chronic myeloid leukemia on oral tyrosine kinase inhibitors. In: Oncology Nursing Forum. Oncology Nursing Society, 2016. p. 190.
HOSOYA, Kazuhisa et al. Failure mode and effects analysis of medication adherence in patients with chronic myeloid leukemia. International journal of clinical oncology, v. 20, n. 6, p. 1203-1210, 2015.
Instituto Nacional de Câncer Jose Alencar Gomes da Silva. ABC do câncer: abordagens básicas para o controle do câncer, 5. ed. Rio de Janeiro: INCA, 2019.
Instituto Nacional de Câncer Jose Alencar Gomes da Silva. Estimativa 2018: incidência de câncer no Brasil. Rio de Janeiro, 2017. Disponível em: https://www.inca.gov.br/sites/ufu.sti.inca.local/files//media/document//estimativa-incidencia-de-cancer-no-brasil-2018.pdf. Acesso em: 08 out. 2019.
JULIUSSON, G.; HOUGH, R. Leukemia. Prog Tumor Res 2016; 43: 87–100. Google Scholar| Crossref| Medline.
KEKÄLE, Meri et al. Impact of tailored patient education on adherence of patients with chronic myeloid leukaemia to tyrosine kinase inhibitors: a randomized multicentre intervention study. Journal of advanced nursing, v. 72, n. 9, p. 2196-2206, 2016.
LATREMOUILLE-VIAU, Dominick et al. Health care resource utilization and costs in patients with chronic myeloid leukemia with better adherence to tyrosine kinase inhibitors and increased molecular monitoring frequency. Journal of Managed Care & Specialty Pharmacy, v. 23, n. 2, p. 214-224, 2017.
LIU, Tao; PENG, Xing-Chun; LI, Bin. The Metabolic Profiles in Hematological Malignancies. Indian Journal of Hematology and Blood Transfusion, p. 1-10, 2019.
MOULIN, Silmara Mendes Martins et al. The role of clinical pharmacists in treatment adherence: fast impact in suppression of chronic myeloid leukemia development and symptoms. Supportive Care in Cancer, v. 25, n. 3, p. 951-955, 2017.
MULU FENTIE, Atalay et al. Prevalence and determinants of non-adherence to Imatinib in the first 3-months treatment among newly diagnosed Ethiopian’s with chronic myeloid leukemia. PloS one, v. 14, n. 3, p. e0213557, 2019.
MULUNEH, Benyam et al. Patient perspectives on the barriers associated with medication adherence to oral chemotherapy. Journal of Oncology Pharmacy Practice, v. 24, n. 2, p. 98-109, 2018.
Novartis Biociências S.A. Bula do medicamento Glivec®. Disponível em: https://portal.novartis.com.br/UPLOAD/ImgConteudos/1821.pdf. Acessado em: 20 de agosto de 2020.
RYCHTER, Anna et al. Treatment adherence in chronic myeloid leukaemia patients receiving tyrosine kinase inhibitors. Medical Oncology, v. 34, n. 6, p. 104, 2017.
SACHDEVA, Ashwani et al. Association of leukemia and mitochondrial diseases—A review. Journal of family medicine and primary care, v. 8, n. 10, p. 3120, 2019.
SAUSSELE, Susanne et al. Defining therapy goals for major molecular remission in chronic myeloid leukemia: results of the randomized CML Study IV. Leukemia, v. 32, n. 5, p. 1222-1228, 2018.
SIEGEL, Rebecca L.; MILLER, Kimberly D.; JEMAL, Ahmedin. Cancer statistics, 2019. CA: a cancer journal for clinicians, v. 69, n. 1, p. 7-34, 2019.
SOUZA, Jessica de O. et al. Adherence to TKI in CML patients: more than reports. Supportive Care in Cancer, v. 26, n. 2, p. 325-326, 2018.
TAN, Bee Kim et al. Efficacy of a medication management service in improving adherence to tyrosine kinase inhibitors and clinical outcomes of patients with chronic myeloid leukaemia: a randomised controlled trial. Supportive Care in Cancer, p. 1-11, 2019.
THAVAMANI B. Samuel; MATHEW, Molly; DHANABAL, S. P. Anticancer activity of cissampelos pareira against dalton’s lymphoma ascites bearing mice. Pharmacognosy magazine, v. 10, n. 39, p. 200, 2014.
TRIVEDI, Digisha et al. Adherence and persistence among chronic myeloid leukemia patients during second-line tyrosine kinase inhibitor treatment. Journal of Managed Care Pharmacy, v. 20, n. 10, p. 1006-1015, 2014.
TSAI, Yu-Fen et al. Side effects and medication adherence of tyrosine kinase inhibitors for patients with chronic myeloid leukemia in Taiwan. Medicine, v. 97, n. 26, 2018.
UNNIKRISHNAN, Radhika et al. Comprehensive evaluation of adherence to therapy, its associations, and its implications in patients with chronic myeloid leukemia receiving imatinib. Clinical Lymphoma Myeloma and Leukemia, v. 16, n. 6, p. 366-371. e3, 2016.
WORLD HEALTH ORGANIZATION et al. Adherence to long-term therapies: evidence for action. World Health Organization, 2003.
[1] Apotheker. Facharzt für Klinische und Krankenhausapotheke, Senac. Multiprofessioneller Onkologie-Spezialist (HIAE).
[2] Pharmazeutische. Facharzt für Klinische und Krankenhausapotheke, Senac.
[3] Apotheker. Facharzt für Klinische und Krankenhausapotheke, Senac.
[4] Pharmazeutische. Facharzt für Klinische und Krankenhausapotheke, Senac.
[5] Apotheker. Master in Medical Sciences, FMUSP. Multiprofessioneller Onkologie-Spezialist (HSL). Facharzt für Krankenhausapotheke (FOC).
Eingereicht: August 2020.
Genehmigt: Oktober 2020.