ARTÍCULO DE REVISIÓN
SBRUZZI, Felipe Augusto [1], SILVA, Kelly Cristina da [2], TELLES, Sérgio Mazero [3], LIMA, Sirlene de Sousa [4], SANTANA, Claudinei Alves [5]
SBRUZZI, Felipe Augusto. Et al. Forma de seguimiento para pacientes adultos con leucemia con Imatinib. Revista Científica Multidisciplinar Núcleo do Conhecimento. Año 05, Ed. 10, Vol. 02, páginas 92-112. Octubre de 2020. ISSN: 2448-0959, Enlace de acceso: https://www.nucleodoconhecimento.com.br/salud/leucemia-con-imatinib
RESUMEN
Introducción: La leucemia mieloide crónica es un tipo de neoplasia maligna de la sangre que se caracteriza principalmente por la presencia del cromosoma Filadelfia que origina la oncoproteína BCR-ABL. Ha aumentado la actividad de la tirosina quinasa, lo que provoca cambios en las vías de señalización intracelular y promueve la proliferación descontrolada, la disfunción celular y la ausencia de apoptosis. A pesar de la baja incidencia de la enfermedad, 1,5 casos por 100.000 habitantes, la terapia con Imatinib, un potente inhibidor de BCR-ABL, cambió el pronóstico de la enfermedad y alargó la esperanza de vida de los pacientes, transformando una enfermedad mortal en una condicion cronica. Objetivo: Desarrollar un formulario para el seguimiento regular de estos pacientes por parte del farmacéutico clínico para garantizar una farmacoterapia segura y eficaz. Metodología: La revisión de la literatura de tipo narrativo se inició a partir de la pregunta del problema: “¿Qué datos debe recopilar el farmacéutico clínico durante la asistencia farmacéutica para evaluar y mejorar la adherencia en pacientes adultos con leucemia mieloide crónica que usan Imatinib?” , seguido de la búsqueda de artículos en bases de datos PubMed y sitios web gubernamentales. Posteriormente, se llevó a cabo la selección del trabajo y el análisis crítico para construir una forma modelo a aplicar en el acto de dispensación. Resultado y discusión. Se seleccionaron once artículos. La baja adherencia del paciente al tratamiento de la leucemia mieloide crónica puede resultar potencialmente mortal. Por tanto, el formulario de seguimiento que debe aplicar el farmacéutico clínico al dispensar mesilato de imatinib es una estrategia viable y de bajo coste para mejorar la adherencia a la farmacoterapia y promover una mejor respuesta al tratamiento. Conclusión: La documentación sistemática y estandarizada de adherencia y efectos adversos por parte del farmacéutico clínico permite la implementación de acciones por parte del equipo multidisciplinario de mejoras continuas con el fin de maximizar la calidad de la atención brindada a los pacientes así como la calidad de vida.
Palabras clave: Leucemia, seguimiento farmacoterapéutico, Imatinib.
INTRODUCCIÓN
Cáncer es el nombre dado a un conjunto de más de cien patologías, que tiene como características comunes la iniciación por daño en genes específicos del ADN y el crecimiento autónomo y desordenado de células que adquieren la capacidad de invadir órganos y tejidos adyacentes que resultan en trastornos funcionales (THAVAMANI et al., 2014).
Esta proliferación celular anormal se conoce como neoplasia y en la práctica se llama tumor, y puede clasificarse como maligna o benigna (INSTITUTO NACIONAL DO CÂNCER, 2019).
Un grupo especial de neoplasias malignas son las leucemias, que se caracterizan por la proliferación anormal de precursores de células de médula ósea del linaje blanco (JULIUSSON y HOUGH, 2016; LIU et al., 2019). Las leucemias pueden clasificarse según el tipo de célula afectada, linfocítica o mieloide, y en cuanto a la característica, aguda o crónica (SACHDEVA et al., 2019).
La leucemia mieloide crónica (LMC) es un tipo de trastorno sanguíneo caracterizado por un aumento en el número de leucocitos con desviación izquierda, esplenomegalia y la presencia del cromosoma Filadelfia (Ph), que resulta de la translocación recíproca entre cromosomas (9;22) (q34;q11), dando lugar a proteína bcr-abl, con aumento de la actividad de la tirosina quinasa (FLIS Y CHOJNACKI, 2019).
La proteína BCR-ABL está presente en más del 90% de los pacientes con LMC, y su hiperactividad estimula la liberación de efectos de proliferación celular e inhibidores de la apoptosis, y su actividad es responsable del proceso de formación del cáncer en LMC (DI FELICE et al., 2018).
El descubrimiento de esta alteración molecular además de optimizar el diagnóstico de LMC también proporcionó el desarrollo de terapias dirigidas a esta alteración molecular, y métodos de seguimiento de enfermedades residuales mínimas, proporcionando una mejora en el tratamiento (BORTOLHEIRO Y CHIATTONE, 2008).
CML presenta 3 fases clínicas distintas que surgen a lo largo del curso de la enfermedad, siendo clasificadas como fase crónica, fase de transformación y fase final o explosiva (HEFNER et al., 2016).
Tradicionalmente, el tratamiento del cáncer se puede realizar a través de las modalidades de cirugía, quimioterapia y radioterapia, y la combinación es común para obtener un mejor resultado clínico (NATIONAL CANCER INSTITUO, 2019).
La quimioterapia clásica tiene como objetivo la destrucción de células en replicación rápida que sugieran mutaciones y/o cambios importantes en el ADN, sin embargo, las células tisulares normales que también tienen replicación rápida se destruyen proporcionando así numerosos efectos adversos a los pacientes (BAGNYKOVA et al., 2010).
En las células cancerosas, como la LMC, se alteran las vías de señalización intracelular, promoviendo la proliferación incontrolada, la disfunción celular y la ausencia de apoptosis (ANDERSON et al., 2015). Sobre la base de una mejor comprensión de estos procesos, iniciado en la década de 1980, se comenzaron a estudiarse fármacos llamados inhibidores de la tirosina quinasa (ITQ) (CHABNER y ROBERTS, 2005).
En CML debido a su característica de pathognomonica, el BCR-ABL oncogene, se ha convertido en el candidato ideal para la “bala mágica” concebida por Paul Ehrlich (Chabner y Roberts, 2005). Por lo tanto, la “Terapia de destino” con ITQ busca inhibir selectivamente las vías de señalización desreguladas de las células neoplásicas de los pacientes con LMC, teniendo como primer fármaco utilizado imatinib mesyate, un potente INHIBIDOR de BCR-ABL (DREWS, 2006; MOULIN et al., 2017).
Debido al envejecimiento y el crecimiento de la población, la incidencia y mortalidad del cáncer ha ido creciendo en todo el mundo (BRAY et al., 2018). En Brasil, el Instituto Nacional del Cáncer (INCA) estima que para cada año del bienio 2018/2019 se diagnostican 600.000 nuevos casos de cáncer, entre estas leucemias aparecen en el noveno lugar entre los hombres con 5.940 nuevos casos y el décimo en mujeres con 4.860 nuevos casos (INSTITUTO DE NACIONAL CNCER, 2017).
La LML representa aproximadamente el 15% de los nuevos casos de leucemia, con un riesgo estimado de 1,5 casos por cada 100.000 personas (RYCHTER et al., 2017). A pesar de la baja incidencia en comparación con otros tipos de cáncer (pulmón, próstata, mama), debido al tratamiento con mesilato de imatinib, los pacientes con LMC mostraron una mejora considerable en la tasa de supervivencia de cinco años y modificaron el pronóstico de la enfermedad (TRIVEDI et al., 2014; SAUSSELE et al., 2018; TAN et al., 2019; LATREMOUILLE-VIAU et al., 2017).
Para los pacientes diagnosticados a mediados de la década de 1970, la tasa de supervivencia a cinco años fue del 22%, de 2008 a 2014, del 69%, y actualmente la mayoría de los pacientes que reciben TQI tienen una esperanza de vida compatible con las personas normales, lo que actualmente se considera la LMC como una condición crónica que requiere un seguimiento regular por parte del equipo de salud (SIEGEL et al. , 2019).
El tratamiento de la LMC requiere la acción integrada del equipo multidisciplinario, y el profesional farmacéutico es indispensable en el seguimiento farmacoterapéutico (SF) del tratamiento oncológico para garantizar una farmacoterapia segura y eficaz (SOUZA et al., 2018).
SF es una práctica personalizada en la que el farmacéutico clínico tiene la responsabilidad de orientación, detección, prevención y resolución de problemas relacionados con fármacos, cubriendo los efectos adversos de la quimioterapia y la terapia utilizada, así como las técnicas de administración, adherencia al tratamiento e interacciones farmacológicas (CALADO et al., 2019).
Dada la complejidad de la LMC, el seguimiento realizado por el profesional farmacéutico clínico es esencial para la eficacia del tratamiento.
OBJETIVO
Construir un modelo de formulario de seguimiento farmacoterapéutico para pacientes adultos con leucemia mieloide crónica BCL-ABR positiva utilizando Imatinib Mesiduct.
METODOLOGÍA
La obra es una revisión bibliográfica del tipo narrativo. Así, a partir de la pregunta problemática: “¿Qué datos debe recopilar el Farmacéutico Clínico durante la asistencia farmacéutica para evaluar y mejorar la adherencia de pacientes adultos con Leucemia mieloide crónica utilizando Imatinib?” se llevó a cabo una búsqueda en la plataforma PubMed basada en la estrategia PICO y se utilizaron los descriptores: “leukemia, myelogenous, chronic, bcr-abl positive” AND “medication adherence”. Se consideraron los artículos de los últimos 5 años y la búsqueda se llevó a cabo en la base de datos de junio a diciembre de 2019.
Los criterios de inclusión fueron: artículos disponibles en línea en línea, en inglés, que tenían como población de pacientes adultos, y con el tema de la evaluación de la adherencia a los medicamentos en LMC. Como criterios de exclusión eran: artículos que evaluaron exclusivamente otro medicamento distinto del mesysirate de imatinib, que no utilizaba un formulario.
Además, para componer el formulario se consultaron sitios gubernamentales.
RESULTADO Y DISCUSIÓN
La búsqueda en el sitio web de Pubmed con los descriptores dio lugar a 52 artículos y de estos, basados en los criterios de inclusión y exclusión, 11 fueron seleccionados para componer la revisión de la literatura en la preparación del formulario.
Estos artículos se presentan en el Cuadro 1 en orden de descendente de la publicación.
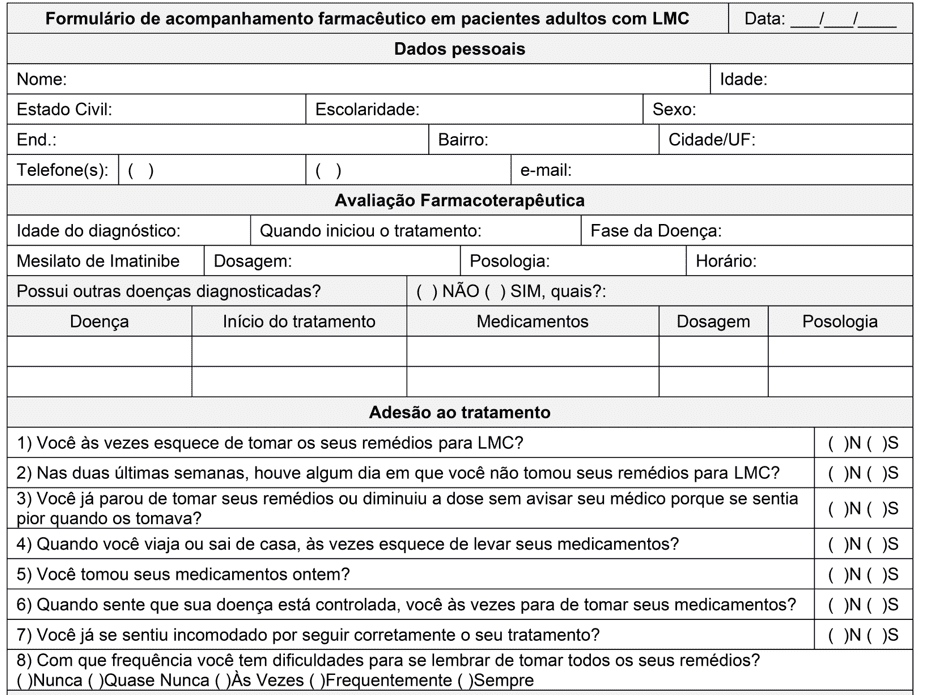
Según lo observado por Moulin et al., la inclusión del Farmacéutico Clínico durante el tratamiento de pacientes con LMC no sólo mejoró la adherencia al tratamiento y disminuyó las reacciones adversas a los medicamentos (RAM) notificadas por los pacientes, sino que también mejoró los parámetros citogenéticos (MOULIN et al., 2017). En este estudio, después de 4 meses de seguimiento, los autores encontraron una expresión más baja del cromosoma Filadelfia en el grupo monitoreado en relación con el control no supervisado. En el grupo supervisado, la respuesta citogenética completa observada aumentó del 87,0% al 95,6% de los pacientes, mientras que en el grupo no supervisado se mantuvo en el 61,5%. Por lo tanto, la aplicación de una forma en el momento de la dispensación es una estrategia eficaz para acompañar al paciente y mejorar la adherencia al tratamiento. Para lograr este objetivo, se elaboró un formulario de seguimiento farmacéutico en pacientes adultos con LMC (Anexo I).
La primera parte del formulario está destinada a recopilar los datos personales de los pacientes para identificar y facilitar el contacto con el paciente. Esto se debe a que algunos de los estudios seleccionados muestran que en algunas poblaciones las ades pueden ser favorecidas por algunas características socioeconómicas, pero los estudios difieren en cuanto a cuáles están más presentes en la población. Tsai et al (2018) encontraron en la población del estudio que los pacientes mayores y los pacientes casados tienen mejor adherencia. Según Rychter et al (2017) la presencia de al menos 1 comorbilidad y edad mayor de 65 años son características favorables para adering. Por el contrario, Unnikrishnan et al (2016) y Hefner et al (2016) no encontraron correlación entre las características socioeconómicas de la población estudiada y el tratamiento adherido. Así, se observa que la correlación entre los datos socioeconómicos y la adherencia varía según la población estudiada, no siendo un parámetro predictivo para la adherencia o no adherencia del paciente.
Tabla 1.A – Artículos seleccionados en función de criterios de inclusión y exclusión, orden descendente del año de publicación.
| Autor/Año | Título | Metas | Forma de Adecin | N(1) | País | Medicamentos |
| MULU FENTIE et al., 2019 | Prevalence and determinants of non-adherence to Imatinib in the first 3-months treatment among newly diagnosed Ethiopian’s with chronic myeloid leukemia. | Evaluar la prevalencia y las razones de no adherencia a Imatinib en pacientes con LMC(2) que fueron diagnosticados recientemente en los primeros 3 meses de tratamiento. | MMAS-8(3) | 147 | Etiopía | Imatinib |
| TSAI et al., 2018 | Side effects and medication adherence of tyrosine kinase inhibitors for patients with chronic myeloid leukemia in Taiwan. | Aclarar la influencia de los efectos adversos sobre la adherencia en pacientes taiwaneses con LMC(2). | MMAS-8(3) | 58 | Taiwán | Imatinibe
Dasatinibe Nilotinibe |
| HEFNER et al., 2017 | Adherence and Coping Strategies in Outpatients With Chronic Myeloid Leukemia Receiving Oral Tyrosine Kinase Inhibitors. | Evaluar las estrategias de adherencia y afrontamiento en pacientes fuera del entorno hospitalario con LMC(2). | BAASIS(4) | 35 | Alemania | Inhibidores de la tirosina quinasa |
(1) N – Número de participantes; (2) LMC – Leucemia mieloide crónica; (3) MMAS-8 – Escala de adherencia terapéutica Morisky de 8 elementos; (4)BAASIS – Escala de Basilea para la evaluación de la adherencia a fármacos inmunosupresores; (5) MMAS-4 – Escala de adherencia Terapéutica Morisky de 4 elementos.
Tabla 1.B – Artículos seleccionados en función de criterios de inclusión y exclusión, orden descendente del año de publicación.
| Autor/Año | Título | Metas | Forma de Adecin | N(1) | País | Medicamentos |
| RYCHTER et al., 2017 | Treatment adherence in chronic myeloid leukaemia patients receiving tyrosine kinase inhibitors. | Evaluar el tratamiento adherido a pacientes polacos adultos con LMC(2) | Forma desarrollada para el estudio. | 140 | Polonia | Imatinib
Dasatinib Nilotinib |
| GEISSLEr et al., 2017 | Factors influencing adherence in CML and ways to improvement: Results of a patient-driven survey of 2546 patients in 63 countries. | Evaluar el alcance de la adherencia subóptima e investigar las razones y patrones de comportamiento de adherencia de los pacientes con LMC(2) en todo el mundo. | MMAS-8(3) | 2546 | 63 países | Imatinib
Dasatinib Nilotinib Otro tratamiento |
| MULUNEH et al., 2016 | Patient perspectives on the barriers associated with medication adherence to oral chemotherapy. | Analizar a través de un cuestionario el uso de quimioterapia oral e identificar oportunidades de mejora en lo siguiente. | Cuestionario adaptado con 30 preguntas | 93 | Estados Unidos | Quimioterapia oral |
(1) N – Número de participantes; (2) LMC – Leucemia mieloide crónica; (3) MMAS-8 – Escala de adherencia terapéutica Morisky de 8 elementos; (4) BAASIS – Escala de Basilea para la evaluación de la adherencia a fármacos inmunosupresores; (5) MMAS-4 – Escala de adherencia terapéutica Morisky de 4 artículos
Tabla 1.C – Artículos seleccionados en función de criterios de inclusión y exclusión, orden descendente del año de publicación.
| Autor/Año | Título | Metas | Forma de Adecin | N(1) | País | Medicamentos |
| MOULIN et al.
Nov/201614 |
The role of clinical pharmacists in treatment adherence: fast impact in suppression of chronic myeloid leukemia development and symptoms | Evaluar el papel del farmacéutico clínico en el tratamiento de pacientes con LMC(2), así como la participación del farmacéutico clínico. | MMAS-4(5) | 23 | Brasil | Inhibidores de la tirosina quinasa |
| KEKÄLE et al., 2016 | Impact of tailored patient education on adherence of patients with chronic myeloid leukaemia to tyrosine kinase inhibitors: a randomized multicentre intervention study. | Evaluar la influencia de la educación personalizada para el paciente en la adherencia a ITQ en pacientes con LMC(2). | MMAS-8(3) | 86 | Finlandia | Inhibidores de la tirosina quinasa |
| UNNIKRISHNAN et al., 2016 | Comprehensive Evaluation of Adherence to Therapy, Its Associations, and Its Implications in Patients With Chronic Myeloid Leukemia Receiving Imatinib. | Evaluar la adforebación y la calidad de vida en pacientes con LMC(2) que reciben Imatinib durante un largo período de tiempo. | MMAS-8(3) | 221 | India | Imatinib |
(1) N – Número de participantes; (2) LMC – Leucemia mieloide crónica; (3) MMAS-8 – Escala de adherencia terapéutica Morisky de 8 elementos; (4) BAASIS – Escala de Basilea para la evaluación de la adherencia a fármacos inmunosupresores; (5) MMAS-4 – Escala de adherencia terapéutica Morisky de 4 artículos
Tabla 1.D – Artículos seleccionados en función de criterios de inclusión y exclusión, orden descendente del año de publicación.
| Autor/Año | Título | Metas | Forma de Adecin | N(1) | País | Medicamentos |
| HOSOYA et al., 2015 | Failure mode and effects analysis of medication adherence in patients with chronic myeloid leukemia | Identifique la baja adherencia en pacientes con LMC(2) utilizando el modo de fallo y el análisis de efectos. | Formulario desarrollado para el estudio | 54 | Japón | Imatinibe
Dasatinibe Nilotinibe |
| BRECCIA et al., 2015 | Adherence and future discontinuation of tyrosine kinase inhibitors in chronic phase chronic myeloid leukemia. A patient-based survey on 1133 patients. | Investigar la adherencia y el beneficio potencial en la calidad de vida, la satisfacción con el tratamiento y la vida social en pacientes con LMC(2) | Forma desarrollada para el estudio. | 1133 | Italia | Inhibidores de la tirosina quinasa |
(1) N – Número de participantes; (2) LMC – Leucemia mieloide crónica; (3) MMAS-8 – Escala de adherencia terapéutica Morisky de 8 elementos; (4) BAASIS – Escala de Basilea para la evaluación de la adherencia a fármacos inmunosupresores; (5) MMAS-4 – Escala de adherencia terapéutica Morisky de 4 artículos
Una de las atribuciones del farmacéutico clínico es la evaluación de la farmacoterapia, para que el paciente pueda utilizar con seguridad los medicamentos que necesita, a las dosis, frecuencias y horarios adecuados, logrando así los objetivos terapéuticos. Para ello, se reservaron campos específicos para recoger la edad de diagnóstico, el inicio del tratamiento, la fase de la enfermedad y los parámetros relacionados con la farmacoterapia de imatinib.
En Brasil, la Ordenanza No 1.219 de 4 de noviembre de 2013 establece el protocolo clínico y las pautas terapéuticas para la LMC en adultos y es una referencia para la evaluación farmacoterapéutica de estos pacientes. En esto, se recomienda utilizar Imatinib como tratamiento de primera línea y qué es la farmacoterapia para las fases crónica (FC) y de transformación o acelerada (TA) (BRASIL, 2013).
En FC se recomienda una dosis única 400 mg/día por vía oral después de la comida más grande del día, y puede aumentar en dos dosis de 300 mg, uno por la mañana y el otro por la noche, si después de tres meses una respuesta inadecuada, pérdida de la respuesta previa o progresión de la enfermedad. En relación con TA, la dosis recomendada es de 600mg/día y puede elevarse hasta 800 mg/día en crisis de explosión (BRASIL, 2013).
Además de desempeñar un papel fundamental en la adhesión al tratamiento del paciente, el farmacéutico clínico también debe identificar, evaluar e intervenir en las interacciones farmacológicas. Para evaluar posibles interacciones farmacológicas durante el uso de imatinib, se evalúa en forma la presencia de otras enfermedades y farmacoterapias de estas enfermedades. En el caso de las interacciones farmacológicas, el farmacéutico debe tener en cuenta los medicamentos que tienen metabolización hepática, ya que imatinib se metaboliza en esta vía mediante la enzima CYP3A4 (GLIVEC, 2020). El mantenimiento de una concentración sanguínea superior a 300mg es extremadamente importante para el éxito de la respuesta molecular/citogenética y el aumento de la supervivencia sin progresión de la enfermedad (BRASIL, 2013). Por lo tanto, se deben evitar los inductores de esta enzima como la dtethasona y el Hypericum perforatum, que pueden reducir la concentración plasmática de Imatinib. Así como inhibidores como el ketoconazol, claritromicina que podría disminuir el metabolismo y aumentar las concentraciones de imatinib liderando hay un aumento en RAM (GLIVEC, 2020).
La segunda parte del artículo tiene como objetivo evaluar el tratamiento del paciente. Según la definición de la Organización Mundial de la Salud (OMS), la adherencia en las enfermedades crónicas es el grado en que el comportamiento de una persona está de acuerdo con las recomendaciones de un profesional de la salud, y el comportamiento puede estar representado por la ingesta de medicamentos, el seguimiento de la dieta o los cambios en el estilo de vida (OMS, 2003)
En los artículos seleccionados, se midieron a través de cuestionarios que evalúan este comportamiento a través de acciones relevantes para el tratamiento de la LMC, tales como: olvidar una o más dosis, cambiar la dosis sin notificar al prescriptor, no tomar medicamentos porque se siente bien o porque tiene una reacción adversa. El modelo de cuestionario más utilizado en los artículos (seis de once seleccionados) para evaluar la adherencia fue la Escala de Adherencia Terapéutica Morisky, con 8 elementos (MMAS-8) siendo el más frecuente. Frente a esto, el MMAS-8 fue elegido para la composición de la forma adjunta.
Otro factor importante para la elección fue el tiempo necesario para la aplicación y la facilidad para clasificar al paciente. El MMAS-8 consta de siete preguntas con alternativas “sí” o “no”, y un elemento (el último) que cuenta con una escala similar de 5 puntos (que van desde 0 puntos a “siempre” a 1 punto a “nunca”). Cada elemento que se aplica a un comportamiento específico del uso de medicamentos y no es un determinante del comportamiento de los medicamentos. Las puntuaciones de MMAS pueden variar de 0 a 8 y los pacientes se clasifican en tres niveles de apoyo: alta resistencia (puntuación 8); adeposición media (puntuación 6 a 7,75); y baja adtake (<6).
Hefner et al (2016) utilizaron un cuestionario modificado de la Escala de Basilea para la Evaluación de los Adeptos de Medicamentos Inmunosupresores (BAASIS). Esto tiene cuatro preguntas “sí” o “no” y sólo se necesita una respuesta afirmativa para considerar al paciente como “no adherente”, lo que puede provocar una respuesta negativa en el paciente en comparación con la Clasificación de MMAS-8 (soporte alto, medio y bajo). Otro factor considerado para la elección fue la ausencia en BAASIS de problemas relacionados con el comportamiento “para dejar de tomar medicamentos cuando se siente que la enfermedad está controlada”. Esto se debe a que en algunos estudios, se ha detectado que los pacientes tienden a ser más adherentes en el primer y segundo año después del diagnóstico, probablemente debido a la disminución de los síntomas y LAS RAM se hacen más evidentes que la enfermedad en sí (GEISSLER et al, 2017).
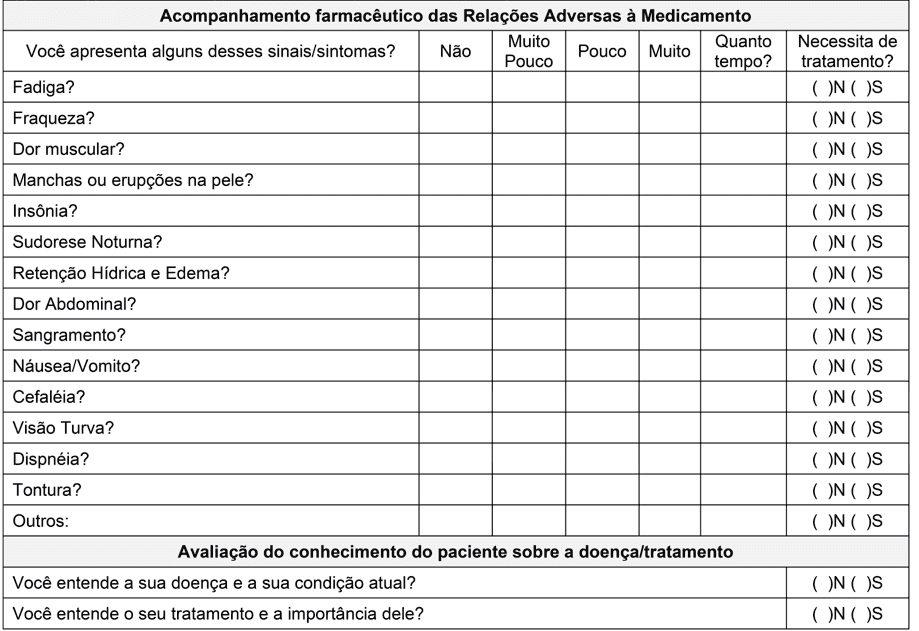
Para evaluar RAM y sus consecuencias sobre el anuncio, se incluyó una tercera parte en el formulario con preguntas sobre las reacciones más comunes.
Según un estudio de cohortes realizado en Etiopía por Mulu Fentie et al (2019), se identificó que la razón principal del apoyo no a tratarse fue de los acontecimientos adversos relacionados con Imatinib, a fármacos del 68,8%. Y la queja principal alrededor del 68% estaban relacionadas con efectos gastrointestinales. El estudio también muestra que los pacientes que no experimentaron ningún RAM tenían seis veces más probabilidades de adherirse al tratamiento.
Como se mencionó anteriormente, Moulin et al (2017) demostraron que la acción del farmacéutico clínico a través del seguimiento farmacológico mejoró la adherencia y redujo los efectos adversos. Durante los cuatro meses de seguimiento, los investigadores redujeron el número de no adherentes de ocho a cero, utilizando la Escala de Adherencia Terapéutica Morisky de 4 elementos. Además, el número de pacientes que se quejándose de la RAM disminuyó del 35% al 7%.
Aunque la duración de los estudios y el número de individuos evaluados fueron relativamente pequeños, los resultados son prometedores. Además, es necesario un estudio más preciso en relación con el número de personas y el seguimiento durante períodos más largos.
En contra-partido, un estudio que cubre 63 países y 2546 pacientes encontró que no es el hecho de que el paciente experimenta RAM lo que influye en la adherencia, sino más bien el manejo de estos es realizado por el equipo multidisciplinario (GEISSLER et al., 2017).
En vista de estos resultados, encontramos evidencia de que la mejor manera de promover el tratamiento adeforego es eludir los eventos adversos o incluso si es posible para evitar posibles eventos adversos futuros para promover un mejor tratamiento. Estas son las razones por las que insertamos en la forma preguntas sobre las principales HAM descritas para Mesysate de Imatinib, la intensidad y el tiempo que el paciente experimenta y siente la necesidad de tratamiento. Por lo tanto, esperamos identificar y eludir los principales efectos indeseables relacionados con la medicación, para promover una mayor seguridad, apoyar y aumentar la calidad de vida de los pacientes.
Aunque la estrategia elegida para evaluar y mejorar la adherencia y reducir las ADR de los pacientes es la forma, Geissler et al (2017) encontraron que un factor importante que afecta a la adherencia y puede ser influenciado por los profesionales de la salud es la información del paciente sobre la LMC. En este estudio, los pacientes que se sintieron mejor informados sobre la enfermedad eran significativamente más adherentes. Así, se insertaron dos preguntas en nuestra forma para evaluar el conocimiento del paciente sobre la enfermedad/tratamiento y así, con la participación del equipo multidisciplinar, para planificar estrategias complementarias. Todavía con esta información, se espera integrar al paciente más activamente en el tratamiento haciendo hincapié en la información y no sólo en las instrucciones que debe seguir.
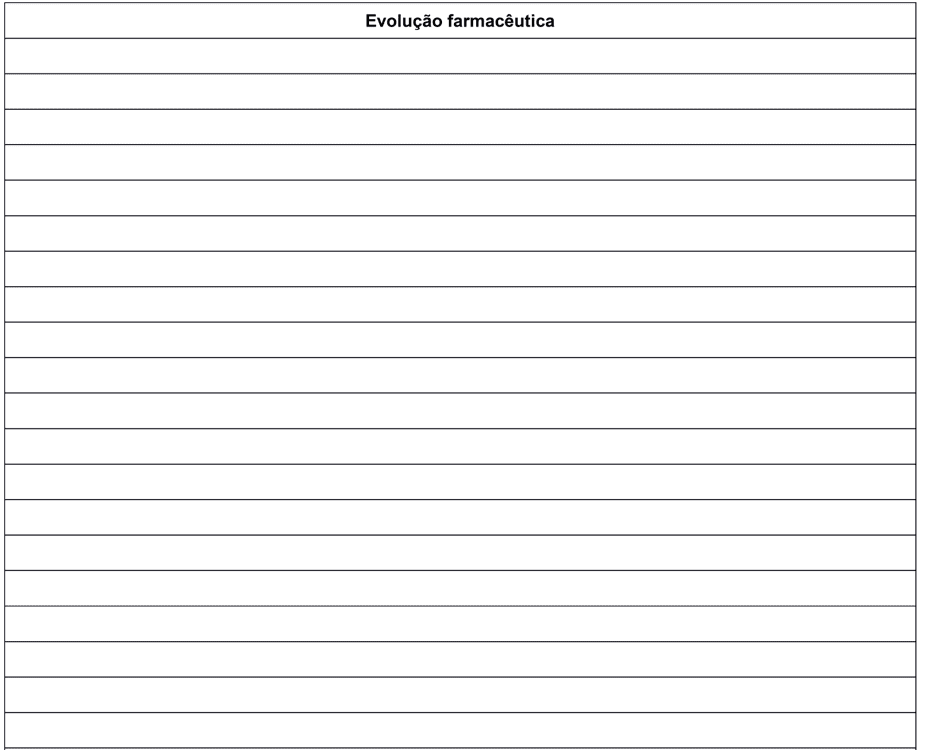
Durante la preparación del formulario no fue posible anticipar cualquier situación o RAM que los pacientes pudieran reportar. Dicho esto, la parte posterior del formulario se utilizó para el campo “Evolución farmacéutica” donde se pueden señalar, por ejemplo: datos subjetivos, datos objetivos, evaluación y planificación específica para el paciente evaluado.
La propuesta de construir el modelo de forma para su aplicación en pacientes con LMC tiene como objetivo mejorar la respuesta al tratamiento con Imatinib Mesirate y la calidad de vida. Por lo tanto, hasta la fecha, no hay intención de incorporar los resultados de esta actividad en un proyecto de investigación. Por lo tanto, no se produjeron Términos de Aclaración y Consentimiento ni ningún otro documento para cumplir con la Resolución No 510 del 7 de abril de 2016 del Ministerio de Salud. Esta resolución prevé investigaciones cuyos procedimientos metodológicos implican el uso de datos obtenidos directamente de los participantes o información identificable (BRASIL, 2016). Sin embargo, un texto que deberá firmar el paciente o su representante se coloca en el reverso del formulario indicando que es consciente de que los datos proporcionados se utilizarán para el seguimiento farmacoterapéutico del tratamiento de la leucemia mieloide crónica.
Anexo I – Forma de seguimiento farmacéutico en pacientes adultos con LMC.
CONCLUSIÓN
Se sabe que varios factores sirven como barreras para el no tratamiento para el tratamiento farmacológico, tales como: eventos adversos, rutina diaria de la medicación, sentirse bien sin tratamiento, información inadecuada sobre el medicamento. Sin embargo, en particular en la leucemia mieloide crónica, el no tratamiento con Imatinib Mesilato puede dar lugar a un tratamiento potencial para la vida, ya que el resultado de esta enfermedad es bien conocido y documentado. Por lo tanto, es esencial a menudofollow up por el farmacéutico clínico para identificar los primeros factores que pueden contribuir negativamente, facilitando la planificación de las intervenciones con el fin de promover una mejor adherencia y en consecuencia alcanzar objetivos terapéuticos.
Con este fin, una estrategia viable y de bajo costo es la implementación de un formulario de seguimiento que debe aplicar el farmacéutico en el momento de la dispensación. Así, la documentación estandarizada de la atención prestada servirá no sólo para optimizar la farmacoterapia, sino también para aumentar la seguridad del paciente, contribuyendo al desarrollo de acciones dirigidas a la evolución del paciente, haciendo una comunicación más eficaz entre los equipos multidisciplinares y ayudando en la implementación de mejoras continuas con el fin de maximizar la calidad de la atención prestada a los pacientes.
REFERENCIAS
ANDERSON, Kristin R. et al. Medication adherence among adults prescribed imatinib, dasatinib, or nilotinib for the treatment of chronic myeloid leukemia. Journal of Oncology Pharmacy Practice, v. 21, n. 1, p. 19-25, 2015.
BAGNYUKOVA, Tetyana V. et al. Chemotherapy and signaling: How can targeted therapies supercharge cytotoxic agents?. Cancer biology & therapy, v. 10, n. 9, p. 839-853, 2010.
BORTOLHEIRO, Teresa C; CHIATTONE, Carlos S. Leucemia mielóide crônica: história natural e classificação. Revista Brasileira de Hematologia e Hemoterapia, v. 30, p. 3-7, 2008.
BRASIL. Ministério da Saúde (MS). Resolução nº 510, de 7 de abril de 2016. Disponível em: http://bvsms.saude.gov.br/bvs/saudelegis/cns/2016/res0510_07_04_2016.html. Acessado em: 23 de maio de 2020.
BRASIL. Ministério da Saúde (MS). Portaria nº 1.219, de 4 de novembro de 2013. Disponível em: http://bvsms.saude.gov.br/bvs/saudelegis/sas/2013/prt1219_04_11_2013.html. Acessado em: 23 de maio de 2020.
BRAY, Freddie et al. Global cancer statistics 2018: GLOBOCAN estimates of incidence and mortality worldwide for 36 cancers in 185 countries. CA: a cancer journal for clinicians, v. 68, n. 6, p. 394-424, 2018.
BRECCIA, Massimo et al. Adherence and future discontinuation of tyrosine kinase inhibitors in chronic phase chronic myeloid leukemia. A patient-based survey on 1133 patients. Leukemia research, v. 39, n. 10, p. 1055-1059, 2015.
CALADO, Deysiane Santos; TAVARES, Diego de Hollanda Cavalcanti; BEZERRA, Grasiela Costa. O papel da atenção farmacêutica na redução das reações adversas associados ao tratamento de pacientes oncológicos. Revista Brasileira de Educação e Saúde, v. 9, n. 3, p. 94-99, 2019.
CHABNER BA, ROBERTS TG Jr. Timeline: chemotherapy and the war on cancer. Nat Rev Cancer, v. 5, p. 65-72, 2005.
DI FELICE, Enza et al. The impact of introducing tyrosine kinase inhibitors on chronic myeloid leukemia survival: a population-based study. BMC cancer, v. 18, n. 1, p. 1069, 2018.
DREWS, Jürgen. Case histories, magic bullets and the state of drug discovery. Nature Reviews Drug Discovery, v. 5, n. 8, p. 635-640, 2006.
FLIS, Sylwia; CHOJNACKI, Tomasz. Chronic myelogenous leukemia, a still unsolved problem: pitfalls and new therapeutic possibilities. Drug design, development and therapy, v. 13, p. 825, 2019.
GEISSLER, Jan et al. Factors influencing adherence in CML and ways to improvement: Results of a patient-driven survey of 2546 patients in 63 countries. Journal of Cancer Research and Clinical Oncology, v. 143, n. 7, p. 1167-1176, 2017.
HEFNER J, CSEF EJ, KUNZMANN V. Fear of progression in outpatients with chronic myeloid leukemia on oral tyrosine kinase inhibitors. In: Oncology Nursing Forum. Oncology Nursing Society, 2016. p. 190.
HOSOYA, Kazuhisa et al. Failure mode and effects analysis of medication adherence in patients with chronic myeloid leukemia. International journal of clinical oncology, v. 20, n. 6, p. 1203-1210, 2015.
Instituto Nacional de Câncer Jose Alencar Gomes da Silva. ABC do câncer: abordagens básicas para o controle do câncer, 5. ed. Rio de Janeiro: INCA, 2019.
Instituto Nacional de Câncer Jose Alencar Gomes da Silva. Estimativa 2018: incidência de câncer no Brasil. Rio de Janeiro, 2017. Disponível em: https://www.inca.gov.br/sites/ufu.sti.inca.local/files//media/document//estimativa-incidencia-de-cancer-no-brasil-2018.pdf. Acesso em: 08 out. 2019.
JULIUSSON, G.; HOUGH, R. Leukemia. Prog Tumor Res 2016; 43: 87–100. Google Scholar| Crossref| Medline.
KEKÄLE, Meri et al. Impact of tailored patient education on adherence of patients with chronic myeloid leukaemia to tyrosine kinase inhibitors: a randomized multicentre intervention study. Journal of advanced nursing, v. 72, n. 9, p. 2196-2206, 2016.
LATREMOUILLE-VIAU, Dominick et al. Health care resource utilization and costs in patients with chronic myeloid leukemia with better adherence to tyrosine kinase inhibitors and increased molecular monitoring frequency. Journal of Managed Care & Specialty Pharmacy, v. 23, n. 2, p. 214-224, 2017.
LIU, Tao; PENG, Xing-Chun; LI, Bin. The Metabolic Profiles in Hematological Malignancies. Indian Journal of Hematology and Blood Transfusion, p. 1-10, 2019.
MOULIN, Silmara Mendes Martins et al. The role of clinical pharmacists in treatment adherence: fast impact in suppression of chronic myeloid leukemia development and symptoms. Supportive Care in Cancer, v. 25, n. 3, p. 951-955, 2017.
MULU FENTIE, Atalay et al. Prevalence and determinants of non-adherence to Imatinib in the first 3-months treatment among newly diagnosed Ethiopian’s with chronic myeloid leukemia. PloS one, v. 14, n. 3, p. e0213557, 2019.
MULUNEH, Benyam et al. Patient perspectives on the barriers associated with medication adherence to oral chemotherapy. Journal of Oncology Pharmacy Practice, v. 24, n. 2, p. 98-109, 2018.
Novartis Biociências S.A. Bula do medicamento Glivec®. Disponível em: https://portal.novartis.com.br/UPLOAD/ImgConteudos/1821.pdf. Acessado em: 20 de agosto de 2020.
RYCHTER, Anna et al. Treatment adherence in chronic myeloid leukaemia patients receiving tyrosine kinase inhibitors. Medical Oncology, v. 34, n. 6, p. 104, 2017.
SACHDEVA, Ashwani et al. Association of leukemia and mitochondrial diseases—A review. Journal of family medicine and primary care, v. 8, n. 10, p. 3120, 2019.
SAUSSELE, Susanne et al. Defining therapy goals for major molecular remission in chronic myeloid leukemia: results of the randomized CML Study IV. Leukemia, v. 32, n. 5, p. 1222-1228, 2018.
SIEGEL, Rebecca L.; MILLER, Kimberly D.; JEMAL, Ahmedin. Cancer statistics, 2019. CA: a cancer journal for clinicians, v. 69, n. 1, p. 7-34, 2019.
SOUZA, Jessica de O. et al. Adherence to TKI in CML patients: more than reports. Supportive Care in Cancer, v. 26, n. 2, p. 325-326, 2018.
TAN, Bee Kim et al. Efficacy of a medication management service in improving adherence to tyrosine kinase inhibitors and clinical outcomes of patients with chronic myeloid leukaemia: a randomised controlled trial. Supportive Care in Cancer, p. 1-11, 2019.
THAVAMANI B. Samuel; MATHEW, Molly; DHANABAL, S. P. Anticancer activity of cissampelos pareira against dalton’s lymphoma ascites bearing mice. Pharmacognosy magazine, v. 10, n. 39, p. 200, 2014.
TRIVEDI, Digisha et al. Adherence and persistence among chronic myeloid leukemia patients during second-line tyrosine kinase inhibitor treatment. Journal of Managed Care Pharmacy, v. 20, n. 10, p. 1006-1015, 2014.
TSAI, Yu-Fen et al. Side effects and medication adherence of tyrosine kinase inhibitors for patients with chronic myeloid leukemia in Taiwan. Medicine, v. 97, n. 26, 2018.
UNNIKRISHNAN, Radhika et al. Comprehensive evaluation of adherence to therapy, its associations, and its implications in patients with chronic myeloid leukemia receiving imatinib. Clinical Lymphoma Myeloma and Leukemia, v. 16, n. 6, p. 366-371. e3, 2016.
WORLD HEALTH ORGANIZATION et al. Adherence to long-term therapies: evidence for action. World Health Organization, 2003.
[1] Farmacéutico. Especialista en Farmacia Clínica y Hospitalaria, Senac. Especialista en Oncología Multiprofesional (HIAE).
[2] Farmacéutica. Especialista en Farmacia Clínica y Hospitalaria, Senac.
[3] Farmacéutico. Especialista en Farmacia Clínica y Hospitalaria, Senac.
[4] Farmacéutica. Especialista en Farmacia Clínica y Hospitalaria, Senac.
[5] Farmacéutico. Máster en Ciencias Médicas, FMUSP. Especialista en Oncología Multiprofesional (HSL). Especialista en Farmacia Hospitalaria (FOC).
Enviado: Agosto, 2020.
Aprobado: Octubre de 2020.