ОБЗОР СТАТЬИ
TAVARES, Marcela Marçolla [1]
TAVARES, Marcela Marçolla. Использование коллоидов и кристаллоидов в периоперационный период тяжелых пациентов: Споры. Междисциплинарный научный журнал Core знаний. 05-й год, Эд. 01, Vol. 01, стр. 05-21. Январь 2020 года. ISSN: 2448-0959, ссылка для доступа: https://www.nucleodoconhecimento.com.br/здравоохранение/коллоидно-кристаллоиды
РЕЗЮМЕ
Поскольку управление заменой жидкости влияет на прогноз пациента, основные и клинические исследования рассматриваются различные аспекты, которые способствуют администрированию жидкостей и объема в периоперационный период. До сих пор нет единого мнения о том, когда и в ком указывать периоперационную гемодинамическую оптимизацию. Дополнительные вопросы, такие как относительная роль оптимизации кристаллоидного и коллоидного соотношения, не были решены. Эта работа состоит из литературного обзора, проведенного в период с февраля по октябрь 2019 года, в котором была проведена консультация с различными научными публикациями, присутствующими в Интернете, путем консультаций в базах данных: ScienceDirect, UptoDate, Medline/PubMed, Lilacs, sciELO, с терминами Периоперационная жидкая терапия, Гемодинамика, Объем Изменения, Кристаллоид, Коллоид. Из этого, было отмечено, что жидкости должны применяться, как и любые другие лекарства, уважая их индивидуальные указания и ограничения, что является основой концепции Цели управляемой терапии – новая концепция, которая поощряет пациента разработки критериев включения для оптимизации жидкости. Ссылаясь на это, выгодные аспекты периоперационной замены объема изонотическими решениями понятны, хотя необходимы дополнительные рандомизированные контролируемые испытания, чтобы доказать его отношение к результату.
Ключевые слова: Периоперационная текучесть терапии, Гемодинамика, Объем замены.
1. ВВЕДЕНИЕ
Поскольку управление заменой жидкости влияет на прогноз пациента, основные и клинические исследования были рассмотрены различные аспекты, которые способствуют администрированию жидкостей и объема в периоперационный период. Фундаментальные исследования улучшили знания о функции эндотелиального сосудистого барьера и его функциональных изменениях, ответственных за экстравазацию сосудов. Клинические исследования, провозглашающие различные подходы к контролю жидкости, показали противоречивые результаты и, в большинстве случаев, не относятся к физиологической основе сосудистого барьера. На основе мета-анализа последних 30 лет был проведен ряд исследований, проведенных для снижения смертности и хирургической заболеваемости путем преднамеренных и профилактических манипуляций периоперационной гемодинамики, что говорит о тенденции научного сообщества выяснить, действительно ли полезна гемодинамическая оптимизаци[2]я.
Он отвечает за исследования, которые сосредоточены главным образом на клинических целях для руководства объемной терапии в периоперационный период. Однако, рассуждения, как правило, должны быть выведены из физиологических фактов и значительных и сопоставимых исследований. Таким образом, в этом обзоре кратко излагаются соответствующие знания о воздействии различных внутривенных жидкостей и на гемодинамический мониторинг. Поскольку до сих пор нет консенсуса по этому вопросу, представляющим большой интерес для всех анестезиологов, цель этой статьи заключается в том, чтобы прояснить некоторые преимущества и недостатки основных жидкостей, используемых в замене периферийного объема.
Относительная роль оптимизации кристаллоидных и коллоидных отношений, хотя и не решена, есть доказательства того, что способствует сбалансированным решениям с концентрацией электролита, аналогичной той, что находится в плазме, и больших объемов солевой раствор следует избегать, так как они вызывают гиперхлорический ацидо[3]з.
2. МАТЕРИАЛ И МЕТОДИС
Эта работа состоит из литературного обзора, проведенного в период с февраля по октябрь 2019 года, в котором была проведена консультация с различными научными публикациями, присутствующими в Интернете, через поиск, из баз данных ScienceDirect, UptoDate, Medline/PubMed, Lilacs, sciELO, в основном с терминами Периоперационная текучесть терапии, Гемодинамика, Волемичная Репозиция, Кристаллоид, Коллоид.
Критериями для включения в это исследование были научные статьи, описывающие основные различия между коллоидами и кристаллоидами, а также их основные показания в периоперационном периоде. Были рассмотрены некоторые методы исследований в период с 1980 по 2019 год, включая рандомизированные и многоцентровых перспективные исследования, мета-анализы, ретроспективные наблюдательные исследования и обзоры литературы.
3. Отзыв
3.1 ФИЗИОЛОГИЯ ФКУД ФКУПЛЕТИЯ
Общая вода в организме для человека 75 кг составляет примерно 45 л (60%). Две трети этой (30 л) является внутриклеточной водой. Оставшаяся треть (15 л) во внеклеточном отсеке делится между внутрисосудистыми (3 л) и внесосудистыми (12 л) отсеками (рис. 1)[4]. Общий внутрисосудистый объем составляет около 5 л и имеет клеточные компоненты (красные и белые кровяные тельца и тромбоциты: [2 L]40%) и неклеточные (плазма: 60%[3 L]). Плазма является aqueous решениеней неорганических ионов (преимущественно хлорид натрия), простых молекул, таких как мочевина, и крупных органических молекул, таких как альбумин и глобулины.
FIGURE 01: Пояснительная модель распределения жидкости в организме

Как показано на рисунке 01, отмечается, что большая часть жидкого объема сконцентрирована во внутриклеточной среде, состоящей из гликозатного раствора.
Повышенная проницаемость сосудов из-за воспалительной активации с нарушением функции эндотелиальных клеток может произойти по целому ряду причин во время более крупных хирургических процедур[5]. В частности, хирургическая травма тканей, гипоперфузия тканей из-за недостаточной жидкостной терапии, травма ишемии/реперфузии, сепсис (местный или кровный) и использование сердечно-легочного шунтирования (например, сердечно-легочного шунтирования) признаются воспалительными стимулами, которые могут скомпрометировать сосудистую функцию[6].
3.2 ЗАМЕНА ТОМА
Объемзамены должны быть указаны всякий раз, когда есть необходимость: 1) Заменить кровопотерю во время операции, 2) Заменить потери с потоотделением и производство мочи 3) Предоперационные операции кишечника и 4) обслуживание третьего пространства потерь[7].
Это понимается третьим пространством, чтобы быть термин, предложенный Рэндалл в 1952 году, чтобы описать ситуацию, в которой внеклеточной жидкости теряется или похищается в области тела, где он не участвует в обмене, и, следовательно, не отвечает потребностям пациента воды[8].
3.3 PERIOPERATIVE HEMODYNAMICALLY OPTIMIZED STRATEGY
Пациенты, которые могли бы извлечь выгоду из этой терапии являются те, на высокий риск в соответствии с пересмотренным индексом сердечного риска и предоперационной сердечно-легочной тренировки тес[6]т[9],,[10]
Согласно систематическому обзору литературы по периоперационной оптимизации у пациентов с высоким хирургическим риском, были найдены важные факторы, которые помогли бы выявить пациентов, которые больше всего выиграют от оптимизации периопараторной жидкости[11]. Результаты описаны в таблице 01, основанной на исследованиях Mangano et al. (1996), Poldermans и др. (1999) и Shoemaker и др. (1988).
TABLE 01 – Критерии включения для периоперационной оптимизации
| Histórico de enfermidade cardíaca ou pulmonar severa, como por exemplo DPOC, infarto agudo do miocárdio, e insuficiência cardíaca. |
| Cirurgias extensas que envolvam anastomoses do trato gastrointestinal (por exemplo, esofagectomia). |
| Perda massiva e abrupta de sangue (>2,5L) |
| Idade maior ou igual a 70 anos com reserve fisiológica limitada em um ou mais órgãos vitais. |
| Septicemia |
| Insuficiência Respiratória (PaO2 <60 mmHg e FIO2 >0.4) |
| Acometimento abdominal agudo como pancreatite, perfuração de vísceras ou sangramentos do TGI. |
| Insuficiência Renal Aguda |
| Doença vascular em estágio avançado |
Источник: Tote; Основания (2006)
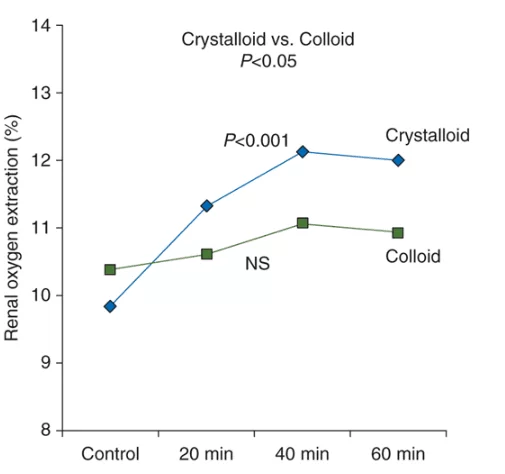
На основе исследования с участием 30 тяжелых пациентов, которые прошли операции на сердце, было продемонстрировано, что, несмотря на увеличение сердечного индекса и почечного кровотока с обеих жидкостей, ни одна из жидкостей улучшение почечной оксигенации, потому что оба индуцированной геморазбавения. GFR увеличился в кристаллоида (28%), но не в коллоидной группе, как показано на рисунке 02[12].
То же исследование показало, что использование кристаллоидов увеличило скорость фильтрации (24%) а также экстракции почечного кислорода (23%), даже без увеличения сосудистого питания компонента, предполагая, что увеличение ГФР – основного определяющего фактора потребления кислорода – не сопровождалось пропорциональным увеличением доли кислорода, поставляемого в почки. Другими словами, их результаты суммируют сяобирают в графике (рисунок 02), что кристаллоидная повышенная экстракция почечного кислорода (P 0.001) 20, 40 и 60 мин после болуса, в отличие от коллоида (NS), предполагая нарушение оксигенации почек во втором случае. Изменение в извлечении почечного кислорода было значительно (P 0.05) более выраженным в кристаллоидной группе по сравнению с коллоидной группой[11].
FIGURE 02: Влияние кристаллоида (10 мл/кг) и коллоидного инфузии (20 мл/кг) на экстракцию почечного кислорода после кардиохирургии
3.4 ТИП ЖИДКОСТИ ДЛЯ СТРАТЕГИИ ГЕМОДИНАМИЧЕСКОЙ ОПТИМИЗАЦИИ
Многочисленные презентации растворов доступны для замены объема, они различаются в зависимости от состава ионов и наличия или отсутствия органических соединений. Таким образом, у нас есть присутствие коллоидов и кристаллоидов.
Коллоиды считаются плазменными расширителями, потому что они вызывают меньше потери капилляров и меньше отеков легких, чем кристаллоиды. Они уменьшают экспрессию воспалительных посредников, улучшают микроциркуляцию тканей и оксигенацию и способствуют более высокой реанительности громкости, чем кристаллоиды. Тем не менее, побочные эффекты (CS) уже наблюдались[5].
Кристаллоиды, с другой стороны, оставляют внутрисосудистое отделение раньше и в большем количестве, чем коллоиды, и, следовательно, для пополнения дефицита необходимо большее количество (в 3-4 раза больше объема кристаллоидов[6]). Некоторые из основных характеристик кристаллоидов представлены в таблицах 02 и коллоидах в таблице 03[3].
TABLE 2 – Основные кристаллоиды и их осмоляритность и концентрации натрия (Наз) и калия (КЗ)
| Cristaloide | Osmolaridade (mOsm/L) | Na+ | K+ |
| Glucose 5% | 252 | — | — |
| Glucose 25% | 1260 | — | — |
| Glucose 50% | 2520 | — | — |
| Sodium chloride 0.9% | 308 | 154.0 | 154.0 |
| Sodium chloride and glucose | 264 | 31.0 | 31.0 |
| Ringer’s solution | 309 | 147.0 | 156.0 |
| Compound sodium lactatea | 278 | 131.0 | 111.0 |
| Plasmalyte B | 298.5 | 140 | 98 |
| Normasol | 280 | 140 | 98 |
Источник: Адаптировано из Грокотта. Эт др. (2005)
В проспективном, слепом исследовании у факультативных пациентов, перенесших несердечную хирургию, внутриоперационная реанимация жидкости с использованием коллоидов (6% HES), снижение частоты послеоперационной тошноты и рвоты, сильной боли, периорбитального отека и двойного зрени[13]я.
У пациентов, перенесших серьезную операцию на брюшной полости, когда они получали кристаллоиды в одиночку, они привели к накоплению кишечной жидкости по сравнению с теми, кто также получил коллоиды (6% HES[14]). Это приводит к увеличению отеков тканей. Связь отеков тканей с нарушением перфузии и оксигенации является спорным[15]
TABLE 3: Основные коллоиды и их соответствующие значения средневзвешенного молекулярного веса (PMMP), средневзвешенного молекулярного числа (NMMP) и натрия (Наз) и Хлора (Cl-) концентрации
| Solução | Coloide | PMMP(Da) | NMMP (Da) | Na+(mmol/L) | Cl- (mmol/L) |
| Gelofusine (4%) | Succinylated gelatin | 30,000 | 22,600 | 154 | 125 |
| Haemaccel (3.5%) | Polygeline | 35,000 | 24,300 | 145 | 145 |
| Voluven | Tetrastarch | 130,000 | 60,000 | 154 | 154 |
| Pentaspan | Pentastarch | 264,000 | 63,000 | 154 | 154 |
| HAES-steril 6% or 10% | Pentastarch | 200,000 | 60,000 | 154 | 154 |
| EloHase 6% | Hexastarch | 200,000 | 60,000 | 154 | 154 |
| Hespan 6% | Hetastarch | 450,000 | 70,000 | 150 | 150 |
| Hextend | Hetastarch | 670,000 | 70,000 | 143 | 124 |
| Gentran 40 | Dextran 40 | 40,000 | 25,000 | 154 | 154 |
| Gentran 70 | Dextran 70 | 70,000 | 39,000 | 154 | 154 |
| Rheomacrodex | Dextran 40 | 40,000 | 25,000 | 154 | 154 |
| Macrodex | Dextran 70 | 70,000 | 39,000 | 154 | 154 |
Адаптировано из Грокотта; Mythen, mythen, mythen. ГАН (2005)
С другой стороны, большое количество соленового раствора приводит к гиперхлоремич[16]ескому ацидозу и состояние гиперко[17]агулобилити еще больше, чем это обычно наблюдается при настое других кристаллоидов[18].
3.5 RATIONAL USE OF FLUIDS В ПЕРИОПЕРИСИЯ ПЕРИОД
Больше, чем тип используемой жидкости, существует все более явная озабоченность по выявлению реальных признаков замены жидкости в периоперационном периоде.
Одной из наиболее распространенных стратегий является Целевая терапия (GOT), которая неоднократно использовалась для существенного улучшения результатов гемодинамической оптимизации, как в краткосрочной, так и в долгосрочной [19]п[20]ерспективе, подход TGO ориентирован на максимизацию (оптимизацию) сердечного выброса (CO) путем поэтапного введения жидкост[21]и.
Национальный консенсус, проведенный в 2016 году, пришел к выводу, что успех в целевой терапии (GOT) и других ограничительных стратегий жидкости предполагает, что периоперационное планирование жидкости должно подчеркивать, что жидкая терапия проводится только тогда, когда есть четкое ука[22]зание с использованием критериев включения, представленных в таблице 01.
Кроме того, что касается целевой терапевтической стратегии, Есть 9 исследований, в которых терапевтическая стратегия, направленная на цель была также использована для максимизации гемодинамических переменных, связанных с потоком хирургических, внутриоперационных и послеоперационных пациенто[23]в. Исследования показали, что стратегия лечения снижает желудочно-кишечные осложнения и продолжительность пребывания в больн[24]ице, как в палате, так и в отделениях интенсивной терапии[25].
Одновременно с началом терапии, важно подчеркнуть, что, после начала, оценка отзывчивости до введения жидкости может не только помочь в выявлении пациентов, нуждающихся в жидкостях, но и избежать ненужных и вредных перегрузок жидкости. Эта оценка состоит, например, в наблюдении функциональных динамических параметров, таких как изменения в сердечном выходе во время преднагрузочных маневров – таких как пассивное повышение нижних конечностей[20].
У пациентов с высоким риском хирургического вмешательства использование гемодинамического протокола для поддержания перфузии тканей снижает послеоперационную смертность и отка[26]з. Мониторинг сердечного выброса путем расчета переноса кислорода и потребления также помог направлять терапию[18].
4. ЗАКЛЮЧИТЕЛЬНЫЕ СООБРАЖЕНИЯ
Идеальным режимом замены является режим, который снизит смертность и улучшит качество жизни, снизит множественную органную недостаточность и использование крови и будет недорогим. Эта схема, очевидно, еще не достигнута. Поскольку на практике не существует основанного на фактических данных руководящих принципов, на практике используется сочетание кристаллоидов и коллоидов, и более важно знать, как заменить, чем знать, что заменить.
Как правило, жидкости должны применяться, как и любые другие лекарства, уважая их индивидуальные показания и ограничения. Ссылаясь на это, выгодные аспекты периоперационной замены объема изонотическими решениями понятны, хотя необходимы дополнительные рандомизированные контролируемые испытания, чтобы доказать его отношение к результату. Подводя итоги приведенных выше аргументов, рациональной стратегией введения жидкости может быть лечение пациентов, перенесающих операцию с низким риском, с незначительной внутрисосудистой потерей объема с кристаллоидным вливанием и использование сочетания кристаллоидного и коллоидного введения, тщательно оцениваемого на основе гемодинамических измерений.
Наконец, мы пришли к выводу, что целенаправленная терапия в периоперационный период связана со снижением осложнений и длительности госпитализации. Благотворное воздействие ОТ может быть достигнуто, таким образом, избегая трудностей с госпитализацией в отделения интенсивной терапии.
5. ССЫЛКИ
BRANDSTRUP, B.; SVENDSEN, P. E.; RASMUSSEN, M.; et al. Which goal for fluid therapy during colorectal surgery is followed by the best outcome: near-maximal stroke volume or zero fluid balance? British Journal of Anaesthesia. United Kingdom, v. 109, n.2 , p. 191–199, 17 jun. 2012. Disponível em: <https://ac-els-cdn.ez3.periodicos.capes.gov.br/S000709121732888X/1-s2.0-S000709121732888X-main.pdf?_tid=bde7ae63-beb3-46c9-9adc-e0f04482d0cf&acdnat=1539636094_9a27cfa1829cc5679acd68973a0e7357>. Acesso em: 15 out. 2019.
BUNDGAARD-NIELSEN, M.; HOLTE, K.; SECHER, N. H.; KEHLET, H. Monitoring of peri-operative fluid administration by individualized goal-directed therapy. Acta Anaesthesiologica Scandinavica. USA v. 51, n. 3, p. 331–340, mar. 2007. Wiley/Blackwell (10.1111). Disponível em: <http://doi.wiley.com/10.1111/j.1399-6576.2006.01221.x>. Acesso em: 16 out. 2019.
GOW, K. W.; PHANG, P. T.; TEBBUTT-SPEIRS, S. M.; et al. Effect of crystalloid administration on oxygen extraction in endotoxemic pigs. Journal of Applied Physiology. USA, v. 85, n. 5, p. 1667–1675, nov. 1998. American Physiological SocietyBethesda, MD . Disponível em: <http://www.physiology.org/doi/10.1152/jappl.1998.85.5.1667>. Acesso em: 15 out. 2019.
GROCOTT, M. P. W.; MYTHEN, M. G.; GAN, T. J. Perioperative Fluid Management and Clinical Outcomes in Adults. Anesthesia & Analgesia. USA, v. 100, n. 4, p. 1093–1106, 2005. Disponível em: <https://insights.ovid.com/crossref?an=00000539-200504000-00032>. Acesso em: 15 out. 2019..
GURGEL, S. T.; DO NASCIMENTO, P. Maintaining Tissue Perfusion in High-Risk Surgical Patients. Anesthesia & Analgesia. USA, v. 112, n. 6, p. 1384–1391, 2011. Disponível em: <http://www.ncbi.nlm.nih.gov/pubmed/21156979>. Acesso em: 16 out. 2019..
HAMILTON, M. A.; CECCONI, M.; RHODES, A. A Systematic Review and Meta-Analysis on the Use of Preemptive Hemodynamic Intervention to Improve Postoperative Outcomes in Moderate and High-Risk Surgical Patients. Anesthesia & Analgesia. USA, v. 112, n. 6, p. 1392–1402, 2011. Disponível em: <http://www.ncbi.nlm.nih.gov/pubmed/20966436>. Acesso em: 16 out. 2019.
HOLTE, K.; SHARROCK, N. E.; KEHLET, H. Pathophysiology and clinical implications of perioperative fluid excess. British Journal of Anaesthesia. United Kingdom, v. 84, n. 4, p. 622-632, oct. 2002. Disponível em: <https://www.ncbi.nlm.nih.gov/pubmed/12393365>. Acesso em: 16 out. 2019.
KELLUM, J. A. Saline-induced hyperchloremic metabolic acidosis. Critical care medicine. New York, v. 30, n. 1, p. 259–61, 2002. Disponível em: <http://www.ncbi.nlm.nih.gov/pubmed/11902280>. Acesso em: 15 out. 2019.
LEE, T. H.; MARCANTONIO, E. R.; MANGIONE, C. M.; et al. Derivation and Prospective Validation of a Simple Index for Prediction of Cardiac Risk of Major Noncardiac Surgery. Circulation. Dallas, v. 100, n. 10, sep. 1999. Disponível em: < https://www.ncbi.nlm.nih.gov/pubmed/10477528>. Acesso em: 15 out. 2019.
LORENTZ, M. N. Reposição volêmica perioperatória. Rev Med Minas Gerais. Minas Gerais, v. 20, n. 4, p. 47–56, 2018. Disponível em: <http://rmmg.org/artigo/detalhes/1025>. Acesso em: 15 out. 2019.
MANGANO, D. T.; LAYUG, E. L.; WALLACE, A.; TATEO, I. Effect of Atenolol on Mortality and Cardiovascular Morbidity after Noncardiac Surgery. New England Journal of Medicine. Canada, v. 335, n. 23, p. 1713–1721, 1996. Massachusetts Medical Society . Disponível em: <http://www.nejm.org/doi/abs/10.1056/NEJM199612053352301>. Acesso em: 15 out. 2019.
MORETTI, E. W.; ROBERTSON, K. M.; EL-MOALEM, H.; GAN, T. J. Intraoperative Colloid Administration Reduces Postoperative Nausea and Vomiting and Improves Postoperative Outcomes Compared with Crystalloid Administration. Anesthesia & Analgesia. USA, v. 96, n. 2, p. 611–617, 2003. Disponível em: <https://insights.ovid.com/crossref?an=00000539-200302000-00056>. Acesso em: 15 out. 2019.
MYTHEN, M. G.; WEBB, A. R. Perioperative plasma volume expansion reduces the incidence of gut mucosal hypoperfusion during cardiac surgery. Archives of surgery. Chicago, v. 130, n. 4, p. 423–9, 1995. Disponível em: <http://www.ncbi.nlm.nih.gov/pubmed/7535996>. Acesso em: 16 out. 2019.
ØSTGAARD, G.; REED, R. K. Interstitial fluid accumulation does not influence oxygen uptake in the rabbit small intestine. Acta Anaesthesiologica Scandinavica. USA, v. 39, n. 2, p. 167–173, 1995. Wiley/Blackwell (10.1111). Disponível em: <http://doi.wiley.com/10.1111/j.1399-6576.1995.tb04037.x>. Acesso em: 15 out. 2019.
PEARSE, R.; DAWSON, D.; FAWCETT, J.; et al. Early goal-directed therapy after major surgery reduces complications and duration of hospital stay. A randomised, controlled trial [ISRCTN38797445]. Critical Care. New York, v. 9, n. 6, p. R687, 2005. Disponível em: <http://www.ncbi.nlm.nih.gov/pubmed/16356219>. Acesso em: 16 out. 2019.
PEREL, A.; HABICHER, M.; SANDER, M. Bench-to-bedside review: Functional hemodynamics during surgery – should it be used for all high-risk cases? Critical Care. New York, v. 17, n. 1, p. 203, 2013. BioMed Central. Disponível em: <http://ccforum.biomedcentral.com/articles/10.1186/cc11448>. Acesso em: 15 out. 2019.
POLDERMANS, D.; BOERSMA, E.; BAX, J. J.; et al. The Effect of Bisoprolol on Perioperative Mortality and Myocardial Infarction in High-Risk Patients Undergoing Vascular Surgery. New England Journal of Medicine. Canada, v. 341, n. 24, p. 1789–1794, 1999. Massachusetts Medical Society. Disponível em: <http://www.nejm.org/doi/abs/10.1056/NEJM199912093412402>. Acesso em: 15 out. 2019.
RAOBAIKADY, R.; DINESH, S.; HACKING, M.; WIGMORE, T. Cardiopulmonary exercise testing as a screening test for perioperative management of major cancer surgery: a pilot study. Critical Care. New York, v. 11, n. Suppl 2, p. 250, 2007. BioMed Central. Disponível em: <http://ccforum.biomedcentral.com/articles/10.1186/cc5410>. Acesso em: 15 out. 2019.
RIELLA MC, RIELLA CV, PACHALY MA, RIELLA LV. Metabolismo da água. In: Riella MC, org. Princípios de nefrologia e distúrbios hidroeletrolíticos. 5ª ed. Rio de Janeiro, Brasil: Guanabara Koogan; 2010. p. 105-38.
RUTTMANN, T. G.; JAMES, M. F.; VILJOEN, J. F. Haemodilution induces a hypercoagulable state. British Journal of Anaesthesia. United Kingdom, v. 76, n. 3, p. 412–414, 1996. Oxford University Press. Disponível em: <http://linkinghub.elsevier.com/retrieve/pii/S0007091217435483>. Acesso em: 16 out. 2019.
SHOEMAKER, W. C.; APPEL, P. L.; KRAM, H. B.; WAXMAN, K.; LEE, T. S. Prospective trial of supranormal values of survivors as therapeutic goals in high-risk surgical patients. Chest. Glenview, v. 94, n. 6, p. 1176–86, 1988. Disponível em: <http://www.ncbi.nlm.nih.gov/pubmed/3191758>. Acesso em: 16 out. 2019.
SILVA, E. D.; PERRINO, A. C.; TERUYA, A.; et al. Brazilian Consensus on perioperative hemodynamic therapy goal guided in patients undergoing noncardiac surgery: fluid management strategy – produced by the São Paulo State Society of Anesthesiology (Sociedade de Anestesiologia do Estado de São Paulo – SAESP). Brazilian Journal of Anesthesiology (English Edition). São Paulo v. 66, n. 6, p. 557–571, 2016. Sociedade Brasileira de Anestesiologia. Disponível em: <https://linkinghub.elsevier.com/retrieve/pii/S0104001416301750>. Acesso em: 15 out. 2019.
SINCLAIR, S.; JAMES, S.; SINGER, M. Intraoperative intravascular volume optimisation and length of hospital stay after repair of proximal femoral fracture: randomised controlled trial. BMJ (Clinical research ed.). London, v. 315, n. 7113, p. 909–12, 1997. Disponível em: <http://www.ncbi.nlm.nih.gov/pubmed/9361539>. Acesso em: 16 out. 2019.
SKYTTE LARSSON, J.; BRAGADOTTIR, G.; KRUMBHOLZ, V.; et al. Effects of acute plasma volume expansion on renal perfusion, filtration, and oxygenation after cardiac surgery: a randomized study on crystalloid vs colloid. British Journal of Anaesthesia. United Kingdom, v. 115, n. 5, p. 736–742, 2015. Oxford University Press. Disponível em: <https://linkinghub.elsevier.com/retrieve/pii/S0007091217310759>. Acesso em: 15 out. 2019.
SUBRAMANIAM, B.; SUBRAMANIAM, K.; PARK, K. W. Volume Replacement Strategies and Outcome. International Anesthesiology Clinics. USA, v. 48, n. 1, p. 115–125, 2010. Disponível em: <https://insights.ovid.com/crossref?an=00004311-201004810-00009>. Acesso em: 16 out. 2019.
TOCANTINS, L. M.; CARROLL, R. T.; HOLBURN, R. H. The Clot Accelerating Effect of Dilution on Blood and Plasma. Relation to the Mechanism of Coagulation of Normal and Hemophilic Blood. Blood. Washington, v. 6, n. 8, 1951. Disponível em: <http://www.bloodjournal.org/content/6/8/720.short?sso-checked=true>. Acesso em: 15 out. 2019.
TOTE, S. P.; GROUNDS, R. M. Performing perioperative optimization of the high-risk surgical patient. British Journal of Anaesthesia. United Kingdom, v. 97, n. 1, p. 4–11, 2006. Oxford University Press. Disponível em: <http://linkinghub.elsevier.com/retrieve/pii/S0007091217351772>. Acesso em: 15 out. 2019.
APPENDIX – СПРАВКИ В ФУТНОТЕ
2. Hamilton, 2011.
3. Holte, 2002.
4. Grocott, 2005.
5. Brandstrup, 2012.
6. Lorentz, 2018.
7. Subramaniam, 2010.
8. Riella, 2010.
9. Lee, 1999.
10. Raobaikady, 2007.
11. Tote, 2006.
12. Skytte Larsson, 2015.
13. Moretti, 2003.
14. ØStgaard, 1995.
15. Gow, 1998.
16. Kellum, John.
17. Ruttmann, 1996.
18. Tocantins et al. 1951
19. Gurgel; Nascimento, 2011.
20. Hamilton, Cecconi, Rhodes, 2011.
21. Perel, Habicher, Sander, 2003.
22. Silva, Et al. 2016.
23. Bundgaard-Nielsen, 2007.
24. Mythen, 1995.
25. Sinclair, Stephen. James, Sally. Singer, Merrill, 1997.
26. Pearse, Ruppert, 2005.
[1] Медицинских. Аспирант в области интенсивной терапии для взрослых.
Отправлено: декабрь 2019 года.
Утверждено: январь 2020 года.