ARTICOLO ORIGINALE
DIOCESANO, Kamila Bezerra Fernandes [1], COSTA, Aurélio Antonio Ribeiro [2], LEITÃO, Glauber Moreira [3]
DIOCESANO, Kamila Bezerra Fernandes. COSTA, Aurélio Antonio Ribeiro. LEITÃO, Glauber Moreira. Cancro al seno multifocale/multicentro: profilo clinico/epidemiologico e modelli immunohistochimici tra i foci: studio trasversale. Revista Científica Multidisciplinar Núcleo do Conhecimento. Anno 05, Ed. 06, Vol. 04, pp. 73-94. giugno 2020. ISSN: 2448-0959. Collegamento di accesso: https://www.nucleodoconhecimento.com.br/salute/multifocale-multicentrico, DOI: 10.32749/nucleodoconhecimento.com.br/salute/multifocale-multicentrico
RIEPILOGO
Il cancro al seno multifocale/multicentro (MF/MC) è una malattia che comprende molti paradigmi nell’attuale pratica del cancro al seno. Per combattere la morbilità e la mortalità di questo l’opzione migliore è una strategia terapeutica razionale, che dovrebbe iniziare con una chiara comprensione biologica della multicentricità e della multifocalità, poiché questo è noto, il trattamento corretto può essere seguito. Il nostro obiettivo era quello di definire il profilo dei pazienti con cancro al seno multifocale e multicentro e valutare se c’è disaccordo tra i foci tumorali per quanto riguarda il recettore ormonale e Her-2. Abbiamo analizzato retrospettivamente 89 pazienti con carcinoma mammario invasivo multifocale e multicentrico in due istituzioni terziarie nel nord-est del Brasile, valutando il recettore ormonale, Her-2 e ki67 in ogni focus tumorale di 25 di questi pazienti, evidenziando il disaccordo o meno tra di loro, e il tipo e il grado istologico, la metastasi dei linfonodi e la distanza e l’età. Di questi pazienti, il 9% presentava eterogeneità tra i foci tumorali. La percentuale di metastasi nel linfonodo ascellare era del 42% e solo del 10% per metastasi distanti. Il 45% delle donne nello studio aveva un grado istologico II o III. Abbiamo trovato una prevalenza di 40.5% di Her-2 negativo e 45% del recettore estrogeno positivo. Non c’era alcuna differenza statisticamente significativa tra il cancro multifocale e quello multicentrico. Concludiamo che il cancro al seno MF/MC mostra eterogeneità tra i foci tumorali in relazione ai parametri biologici, che svolge un ruolo cruciale nel prendere decisioni sul trattamento e di conseguenza sulla ricorrenza del tumore, la prognosi e la metastasi lontana.
Parole chiave: cancro al seno, eterogeneità, multifocale, multicentro.
INTRODUZIONE
Il cancro al seno è il neolasma maligno che colpisce maggiormente le donne in tutto il mondo. È la seconda causa di morte per cancro nei paesi sviluppati, dietro solo il cancro ai polmoni, e la principale causa di morte per cancro nei paesi in via di sviluppo. Nel 2013 ci sono stati circa 1,8 milioni di nuovi casi in tutto il mondo e 471.000 decessi[1]. Per il Brasile, la stima è di circa 60.000 nuovi casi di cancro al seno all’anno, con un rischio stimato di 56,20 casi ogni 100.000 donne. Nello stato di Pernambuco è 2.450 nuovi casi, con un tasso di incidenza lordo di 90.25 casi per 100.000 abitanti solo per Recife, la capitale[2].
Il cancro al seno è classificato come multicentro (MC) e/o multifocale (MF) quando presenta più di un fuoco tumorale e sincrono nello stesso seno. La differenza tra loro si basa sulla posizione, se si trovano in diversi quadranti del seno o in esso, rispettivamente[3,4].
L’incidenza di tumori MF e/o MC varia tra il 6% e il 60[5,6]%. Le caratteristiche clinica-patologiche e prognostiche del cancro al seno multifocale e multicentrico del cancro al seno multifocale non sono ancora ben consolidate.
Sulla base del ragionamento che le lesioni con istologia e laurea simili dovrebbero essere biologicamente simili, l’American College of Pathology raccomanda di caratterizzare tutti i foci di MF/MC con immunohistochimica solo quando l’istoologia e o il grado istologico differiscono l’uno dall’altr[7]o. Pertanto, l’immunohistochimica viene richiesta solo per il tumore più grande e gli altri foci non vengono valutat[8]i.
Uno studio che includeva 113 pazienti, in cui è stata valutata l’immunosofochimica di tutti i foci tumorali, ha scoperto che il disaccordo tra i foci era presente nel 4,4% – 18,6% dei casi, essendo indicato trattamenti diversi rispetto a quanto sarebbe stato prescritto se avessero preso in considerazione solo l’immunosofia di un singolo obiettivo, il più grand[9]e.
La decisione di scegliere la migliore opzione terapeutica per il cancro al seno MC/MF dovrebbe iniziare con una chiara comprensione biologica ed epidemiologica della multicentricità e multifocus, poiché questi sono noti, il trattamento corretto può essere seguito. La valutazione immunoistochimica dei tumori svolge un ruolo cruciale nel processo decisionale nel trattamento del cancro al seno e quando espressa con discordante nei vari foci può fornire ai pazienti l’opportunità di diverse terapie.
Secondo quanto studiato, l’obiettivo di questo studio è stato quello di descrivere il profilo clinico ed epidemiologico delle donne con cancro al seno MF/MC e i modelli immunohistochimici dei vari foci di cancro al seno in ogni donna in due ospedali terziari nel nord-est del Brasile.
Metodi
Lo studio trasversale descrittivo è stato condotto presso l’Instituto de Medicina Integral Prof. Fernando Figueira (IMIP) e l’Ospedale Baro de Lucena (HBL), istituzioni nello stato di Pernambuco, si sono concentrate sull’assistenza medica in varie specialità e impegnate nell’insegnamento, nella ricerca e nell’ampliamento.
Il campione è stato convenzionalmente costituito da donne identificate retroattivamente con il cancro al seno MF o MC assistito nell’IMIP da gennaio 2013 a giugno 2016 e in HBL nel periodo da gennaio 2012 a giugno 2016 che soddisfano i criteri di ammissibilità della ricerca, che sono: avere due o più foci tumorali diagnosticati nello stesso seno contemporaneamente , tranne nei casi di recidiva di un tumore precedente, essendo vivo e con lo stesso tipo e grado istologico tra i foci.
Sono state effettuate visite settimanali al laboratorio di anatomia patologica HBL e al centro mammario IMIP e sono stati selezionati i risultati della biopsia istopatologica o chirurgica dei tumori al seno di pazienti con un profilo compatibile con i criteri di ammissibilità dello studio.
Il tessuto tumorale ottenuto dalla biopsia del nucleo o al momento della chirurgia definitiva viene conservato e confezionato in formalina (10% di formaldeide) memorizzati nel buffer ed elaborati in blocchi di paraffina. Questi blocchi vengono conservati a temperatura ambiente fino a ulteriori analisi, sia per l’esame istopatologico che immunohistochimico.
Dopo aver identificato questi pazienti, il ricercatore ha contattato i pazienti che sono stati presentati alla ricerca e invitati a partecipare firmando il modulo di consenso gratuito e informato.
È stata richiesta l’immunoistochimica di ogni tumore. Questo è stato ottenuto attraverso i blocchi di paraffina già immagazzinati, o, retrospettivamente, dai record esistenti del focus del tumore studiato.
L’immunohistochimica è uno strumento vitale nello studio delle lesioni mammarie. Uso di anticorpi specifici contro le proteine intracellulari presenti in una piccola quantità nel nucleo, nel citoplasma e/o nella membrana cellular[10]e. La tecnica immunohistochimica identifica nel tumore i recettori estrogeno e progesterone, l’indice di proliferazione delle cellule tumorali e l’espressione della proteina della membrana HER-2. È stato richiesto per tutti i tumori multipli presenti contemporaneamente nello stesso seno ed è stato eseguito in un laboratorio con un professionista specializzato in patologia mammaria, in cui utilizza il metodo di streptavidin-biotina marcato attraverso la macchina PT-link di DAKO.
I pazienti che non hanno autorizzato la richiesta di immunoistochimica hanno accettato di partecipare allo studio solo con le informazioni contenute nelle cartelle cliniche e i dati istopatologici e immunohistochimici esistenti.
Recettore ormonale, Her-2 e ki67 sono stati valutati in ogni messa a fuoco del tumore, evidenziando disaccordo o non tra di loro; tipo e grado istologico; metastasi e distanza dei linfonodi; l’invasione linfovascolare e l’età del paziente.
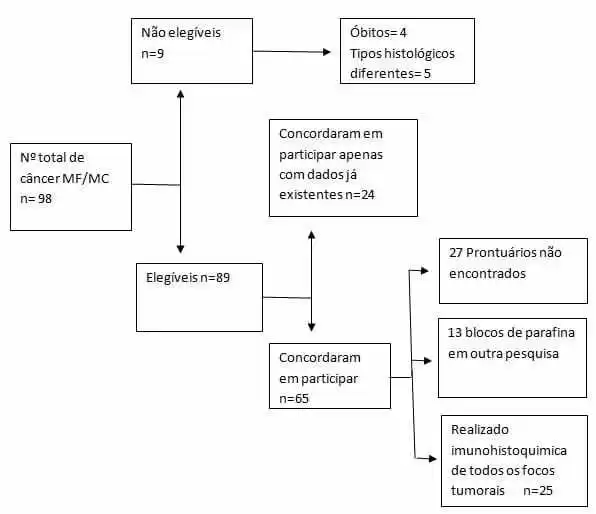
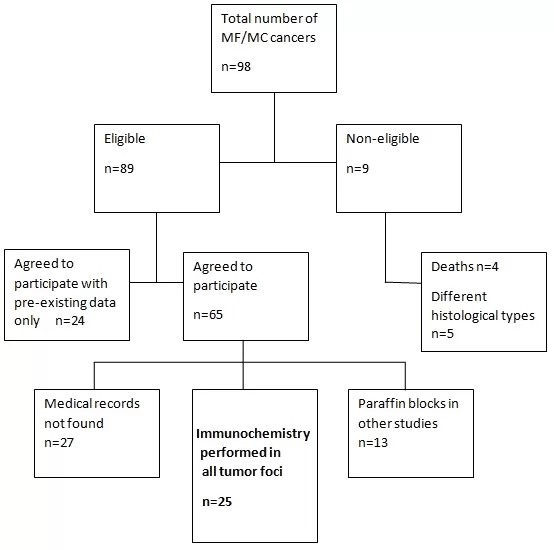
come illustrato nella Figura 1. Diagramma di flusso dell’acquisizione dei partecipanti
Le informazioni raccolte sono state inserite in doppia voce (il ricercatore e un collaboratore), in tempi diversi, in una scheda dati (software Microsoft Office Excel – 2010), creata con lo scopo di convalidare la digitazione. Il database è stato sottoposto a test di correzione e patch per rilevare errori o incoerenze nei dati. Solo dopo aver confrontato le banche ed eseguito i test di coerenza e pulizia è stato utilizzato il database definitivo per l’analisi statistica.
Il Software SPSS 13.0 (Pacchetto statistico per le scienze sociali) per Windows ed Excel 2010 sono stati utilizzati per l’analisi dei dati. Per analizzare il comportamento delle variabili di studio, sono state eseguite misure di tendenza centrale e le loro dispersioni, il test Quiquadrado delle tendenze e Fisher’s Exact, a un livello di significatività del 5%, quando rilevante. Tutti i test sono stati applicati con il 95% di confidenza. I risultati sono presentati in forma tabella con le rispettive frequenze assolute e relative.
Risultati
L’incidenza di tumori MF/MC nel nostro studio è stata del 4% nel 2013 e del 5% nel 2015. I dati Imip per il 2012 e il 2014 non sono disponibili (tabella 1). Il 64% delle donne con cancro MF/MC aveva più di 50 anni. Con l’eccezione che molti dati non erano disponibili, abbiamo riscontrato una frequenza del 33% delle donne brune, del 24% con una scuola elementare incompleta e del 13% delle donne sposate (tabella 2).
TABELLA 1 – Incidenza di cancro al seno non ifocale, multifocale e multicentro presso l’Ospedale Baro de Lucena, HBL, e Instituto Materno Infantil Prof. Fernando Figueira, IMIP. Recife, Pernambuco
| CA de Mama | n (HBL/IMIP) | % (HBL/IMIP) |
| 2012 | ||
| Unifocal | (195/-) | (92,4/-) |
| MC/MF | (16/-) | (7,6/-) |
| 2013 | ||
| Unifocal | 477 (184/293) | 95,9 (93,4/97,7) |
| MC/MF | 20 (13/ 7) | 4,0 (6,6/2,3) |
| 2014 | ||
| Unifocal | (150/-) | (92,6/-) |
| MC/MF | (12/12) | (7,4/-) |
| 2015 | ||
| Unifocal | 523 (162/361) | 94,9 (89,5/97,6) |
| MC/MF | 28 (19/9) | 5,0 (10,5/2,4) |
I dati IMIP per il 2012 e il 2014 non sono disponibili.
Fonte: Ricerca IMIP/HBL
TABELLA 2 – Caratteristiche dei pazienti con cancro al seno multifocale e multicentro operati presso l’Ospedale Barào de Lucena, HBL, e l’Instituto Materno Infantil Prof. Fernando Figueira, IMIP. Recife, Pernambuco
| Variabili | n | % |
| Età | ||
| < 50 | 26 | 29,2 |
| ≥ 50 | 57 | 64,1 |
| Cor | ||
| Branca | 16 | 18,0 |
| Nero | 2 | 2,2 |
| Marrone | 30 | 33,7 |
| Scuola | ||
| Analfabeta | 6 | 6,7 |
| Scuola elementare incompleta | 22 | 24,7 |
| Completa la scuola elementare | 6 | 6,7 |
| Scuola superiore incompleta | 1 | 1,1 |
| Scuola superiore completa | 12 | 13,5 |
| Stato civile | ||
| Unione stabile | 1 | 1,1 |
| Singolo | 8 | 9,0 |
| Sposato | 13 | 14,6 |
| Divorziato | 3 | 3,4 |
| Vedova | 9 | 10,1 |
I dati non informati per ogni variabile sono stati omessi dalla tabella.
Fonte: Ricerca IMIP/HBL
Tipo istologico duttale è stato trovato in 82% delle donne nel nostro studio. La percentuale di metastasi nel linfonodo ascellare era del 42% e solo del 10% per metastasi distanti. Il 45% delle donne nello studio aveva un grado istologico II o III. Abbiamo trovato una prevalenza di 40.5% di Her-2 negativo e 45% del recettore estrogeno positivo. Per quanto riguarda Ki67, abbiamo trovato 41% con un alto tasso di proliferazione cellulare. La percentuale di eterogeneità tra i foci era del 9% e abbiamo trovato il 65% di MF e il 17% di MC (tabella 3).
TABELLA 3 – Caratteristiche cliniche e tumorali dei pazienti affetti da cancro al seno multifocale e multicentro operati presso l’Ospedale Baro de Lucena, HBL e l’Instituto Materno Infantil Prof. Fernando Figueira, IMIP. Recife, Pernambuco
| Variabili | n | % |
| Re (Re) | ||
| Positivo | 40 | 44,9 |
| Negativo | 20 | 22,5 |
| RP | ||
| Positivo | 35 | 39,3 |
| Negativo | 25 | 28,1 |
| Her-2 | ||
| Positivo | 18 | 20,2 |
| Negativo | 36 | 40,5 |
| Ki67 | ||
| <14% | 16 | 18,0 |
| >14% | 37 | 41,6 |
| Linfonodi compromessi | ||
| Cambio | 23 | 25,8 |
| 1 a 3 | 18 | 20,2 |
| 4 più | 20 | 22,5 |
| Grado istologico | ||
| I | 9 | 10,1 |
| II | 27 | 30,4 |
| III | 13 | 14,6 |
| Tipo istologico | ||
| Ductal | 73 | 82,0 |
| Lobular | 1 | 1,1 |
| Altro | 4 | 4,5 |
| Dimensioni del tumore più grande | ||
| <2 cm | 24 | 27,0 |
| 2-5 cm | 32 | 36,0 |
| >5 cm | 5 | 5,6 |
| Metastasi distante | ||
| sì | 9 | 10,1 |
| No | 48 | 53,9 |
| Invasione linfovascolare linfovasculara | ||
| sì | 20 | 22,5 |
| No | 24 | 27,0 |
| Eterogeneità tra foci | ||
| sì | 8 | 9,0 |
| No | 17 | 19,1 |
| Distanza tra i foci | ||
| 4 cm (multifocale) | 58 | 65,2 |
| > 4 cm (multicentro) | 15 | 16,9 |
I dati non informati per ogni variabile sono stati omessi dalla tabella.
Fonte: Ricerca IMIP/HBL
Non sono state osservate differenze significative nel confronto delle variabili tra donne con o senza eterogeneità tra i foci tumorali (tabella 4) e tra MF e MC (tabella 5).
TABELLA 4 – Caratteristiche cliniche e tumorali dei pazienti con carceri mammario multifocale/multicentro operati presso l’Ospedale Baro de Lucena, HBL e L’Instituto Materno Infantil Prof. Fernando Figueira, IMIP, in relazione all’eterogeneità tra foci. Recife, Pernambuco
| Eterogeneità tra foci | |||
| Variabili | sì | No | valore p |
| n (%) | n (%) | ||
| Linfonodi compromessi | |||
| Cambio | 2 (40,0) | 3 (60,0) | 1,000 * |
| 1 a 3 | 2 (33,3) | 4 (66,7) | |
| 4 più | 3 (50,0) | 3 (50,0) | |
| Grado istologico | |||
| I | 2 (66,7) | 1 (33,3) | 0,748 * |
| II | 2 (25,0) | 6 (75,0) | |
| III | 1 (33,3) | 2 (66,7) | |
| Dimensioni del tumore più grande | |||
| <2 cm | 4 (57,1) | 3 (42,9) | 0,510 * |
| 2-5 cm | 3 (33,3) | 6 (66,7) | |
| >5 cm | 0 (0,0) | 2 (100,0) | |
| Metastasi distante | |||
| sì | 1 (20,0) | 4 (80,0) | 0,588 * |
| No | 5 (45,5) | 6 (54,5) | |
| Invasione linfovascolare linfovasculara | |||
| sì | 4 (57,1) | 3 (42,9) | 0,592 * |
| No | 2 (28,6) | 5 (71,4) | |
(*) Test esatto di Fisher
Fonte: Ricerca IMIP/HBL
TABELLA 5 – Caratteristiche cliniche e tumorali dei pazienti con cancro al seno multifocale e multicentro operati presso l’Ospedale Baro de Lucena, HBL e L’Instituto Materno Infantil Prof. Fernando Figueira, IMIP. Recife, Pernambuco
| Distanza tra i foci | |||
| Variabili | 4 cm (multifocale) | >4cm (multicentro) | valore p |
| n (%) | n (%) | ||
| Re (Re) | |||
| Positivo | 29 (80,6) | 7 (19,4) | 1,000 * |
| Negativo | 12 (80,0) | 3 (20,0) | |
| Rp | |||
| Positivo | 26 (81,3) | 6 (18,7) | 1,000 * |
| Negativo | 15 (78,9) | 4 (21,1) | |
| Her-2 | |||
| Positivo | 14 (82,4) | 3 (17,6) | 0,723 * |
| Negativo | 22 (75,9) | 7 (24,1) | |
| Ki67 | |||
| <14% | 13 (86,7) | 2 (13,3) | 0,695 * |
| >14% | 22 (75,9) | 7 (24,1) | |
| Linfonodi compromessi | |||
| Cambio | 16 (84,2) | 3 (15,8) | 0,839 * |
| Da 1 a 3 | 11 (73,3) | 4 (26,7) | |
| 4 più | 16 (80,0) | 4 (20,0) | |
| Grado istologico | |||
| Ho | 6 (66,7) | 3 (33,3) | 0,440 * |
| Ⅱ | 20 (87,0) | 3 (13,0) | |
| Iii | 9 (81,8) | 2 (18,2) | |
| Tipo istologico | |||
| Ductal | 49 (80,3) | 12 (19,7) | 0,370 * |
| Lobular | 1 (100,0) | 0 (0,0) | |
| Altro | 2 (50,0) | 2 (50,0) | |
| Dimensioni del tumore più grande | |||
| <a0>2 cm</a0> | 19 (79,2) | 5 (20,8) | 0,884 * |
| 2-5 cm | 20 (76,9) | 6 (23,1) | |
| >5 cm | 2 (66,7) | 1 (33,3) | |
| Metastasi distante | |||
| sì | 5 (62,5) | 3 (37,5) | 0,331 * |
| No | 35 (83,3) | 7 (16,7) | |
| Invasione linfovascolare linfovasculara | |||
| sì | 13 (72,2) | 5 (27,8) | 0,256 * |
| No | 21 (87,5) | 3 (12,5) | |
(*) Fisher Esatta fonte di test: Ricerca IMIP/HBL
Discussione
L’incidenza dei tumori MF/MC è stata di circa il 5%, essendo del 65% MF e 17% MC, leggermente inferiore a quella riscontrata n[5,6,9]ella letteratura, che molto probabilmente deriva dal fatto che questo tasso varia a seconda dell’entità del campionamento del tessuto mammario analizzato dal patologo sulla macroscopia, poiché è stato dimostrato che un campionamento più completo ha portato all’identificazione di ulteriori lesioni; con la mancanza di una definiz[5]ione standard MF/MC; e con le diverse sensibilità dei metodi di imaging utilizzati preoperatoriamente per rilevare più foci malign[3,4,11-13]i. Uno studio american[5]o ha valutato 3.924 donne con cancro al seno e ha trovato il 24% di MF/MC utilizzando solo criteri patologici nella loro selezione, 79% MF e 20% MC. Una meta-analisi comprendente 22 studi e 67557 donne hanno trovato MF/MC nel 9,5% dei casi, ma alcuni studi hanno usato metodi di imaging preoperatorio come criterio diagnostico[14].
Abbiamo trovato un campione più ampio di donne marroni/nere e sposate. Il basso livello di scuola osservato in questo studio riflette il grado di conoscenza del paziente, che aumenta con l’aumentare della scolarità. Uno studio brasiliano [15]ha mostrato un’associazione tra la conoscenza dei fattori di rischio per il cancro al seno e anni di studio, e non c’era alcuna relazione tra il colore della pelle delle variabili e lo stato civile. Uno studio american[16]o ha associato donne afro-discendenti e non si è mai sposata, con uno stadio avanzato della malattia, forse perché queste donne mancavano del sostegno finanziario e sociale fornito dal coniuge e da fattori culturali e socioeconomici legati al colore. Nel nostro studio, anche se abbiamo avuto una prevalenza di donne con bassa scolarità, marrone e nero, non abbiamo osservato un aumento dello stadio avanzato.
La maggior parte dei pazienti nello studio aveva 50 anni o più (64%). È noto che il cancro al seno è più frequente in questa fascia di età, e questa è una possibile spiegazione per questo campione. Alcune relazioni in letteratura associano MF/MC a giovani donne sotto i 50 anni, al tipo istologi[3,12]co lobulare e a un maggiore[17] coinvolgimento dei linfonodi, so[3,4,8,12,17]stenendo l’ipotesi che MF/MC siano biologicamente più aggressivi, abbiano una maggiore propensione alla diffusione metastatica e siano correlati a un risultato peggior[12]e.
La percentuale di linfonodi ascellari interessati nel nostro studio era del 42% e solo del 10% per metastasi distanti. I pazienti con carcinomi invasivi multipli sono ad alto rischio di metastasi nei linfonodi ascellari, tuttavia, non è stato dimostrato aumentare il rischio di metastasi distante per i pazienti con malattia negativa del ganglio[4]. Uno studio australiano [18]con 848 donne con cancro al seno unifocale e MF/MC ha eseguito analisi multivariate confrontando diverse variabili con la misurazione della dimensione del più grande focus tumorale e con la misurazione della somma dei vari foci tumorali, e ha concluso che la tendenza della metastasi dei tumori al seno è un riflesso del carico tumorale totale invece della dimensione del più grande fuoco e che l’uso della dimensione cumulativa dei foci nei tumori multifocali dimostra un linfonodo di positività identica a quella della dimensione equivalente dei tumori unifocali. Utilizzando la dimensione del fuoco dominante, c’è una maggiore probabilità di positività del linfonodo e forse una prognosi peggiore rispetto ai tumori unifocali della stessa dimensione.
Il tipo istologico più frequente era quello duttale (82%), simile a quello trovato da diversi autor[3,9,17,19]i. Lynch et al[5] descrivono un aumento del tasso di metastasi ai linfonodi regionali in relazione ai tumori non ifocali. Questa associazione solleva la questione se MF/MC sono sottovalutati con l’attuale sistema di staging, che tiene conto solo del più grande focus tumorale, o se hanno semplicemente una biologia intrinseca più aggressiva.
Grado istologico è un fattore prognostico noto nel cancro al seno. Numerosi studi hanno dimostrato la sua significativa associazione con la sopravvivenza. Allo stesso tempo, è una componente importante della decisione terapeutica e ha un ruolo predittivo nella risposta terapeutic[20]a. Gli studi mostrano una forte associazione tra MF/MC e grado istologico II/II[11,17,19]I. Il 45% delle donne nello studio aveva un grado istologico II o III.
Abbiamo trovato una prevalenza del 40,5% di Her-2 negativo e del 45% del recettore estrogeno positivo, contro i dati nella letteratura che mostrano una correlazione tra MF/MC e fattori clinici patologici che suggeriscono tumori più aggressivi, con notevole associazione di Her2 positivo e assenza di recettore estrogeno ormonal[12]e. Crediamo che la causa di questa differenza possa essere dovuta alla piccola dimensione del campione, caratterizzando così un errore statistico di tipo II. Per quanto riguarda Ki67, il 41% corrispondeva ad un’elevata proliferazione cellulare. Infatti, alcuni casi di tumori ormonali-responsive saranno condotti alla chemioterapia a causa di questo fatto.
L’American College of Pathology [7]ritiene sufficiente che la caratterizzazione immunohistochimica delle lesioni multifocali con grado e istologia simili si basi solo sulla più grande lesione. Tuttavia, studi recenti mettono[9,21,22] in discussione questa raccomandazione, come hanno dimostrato che, nonostante la somiglianza delle caratteristiche patologiche, le lesioni possono essere diverse in termini di stato del recettore dell’estrogeno e Her-2, potenzialmente influenzando il loro trattamento. Nel nostro studio, abbiamo trovato il 9% di eterogeneità tra i foci, inclusa l’analisi ki67. Buggi et a[9]l ha riscontrato discrepanza tra i foci rispetto a Ki67 nel 15% dei casi.
I recettori ormonali erano discrepanti tra i foci nell’8% del campione e Her-2 nel 4%, ma l’analisi di questi elementi è stata compromessa a causa del fatto che in oltre il 50% dei casi l’immunoistochimica è stata ottenuta solo dal più alto obiettivo tumorale. Buggi et a[9]l descritto un tasso di disaccordo tra i risultati del recettore ormonale per gli estrogeni di 4.4% e Her-2 di 9.7% tra i foci. Pekar[22] e Choi [21]hanno osservato tassi di discrepanza tra il 3-4% per il recettore degli estrogeni e il 6% per Her-2. Secondo Pekar[22], i pazienti che hanno dimostrato eterogeneità avevano una prognosi peggiore rispetto ai pazienti che non hanno dimostrato eterogeneità, che non è stata trovata nel nostro studio, in cui non sono state osservate differenze significative tra l’eterogeneità e i gruppi omogenei, ma abbiamo avuto limitazioni dovute al piccolo campione e alle perdite nell’analisi, che potrebbero cambiare questo scenario.
Non vi era alcuna rilevanza statistica nel confronto delle variabili tra MF e MC a causa di un campione di piccole dimensioni. Nella letteratura, non abbiamo osservato grandi differenze tra MF/MC in relazione al tipo e al grado istologico, alla metastasi dei linfonodi e alla distanza e dimensione del tumor[5,13]e.
Le decisioni cliniche nella terapia adiuvante sistemica nel cancro al seno si basano su criteri istologici e sul profilo immunohistochimico della maggiore attenzione al tumore, ignorando i foci simultanei più piccoli.
La presenza di foci aggiuntivi non è presa in considerazione nella decisione di terapie adiuvioni. Se esaminiamo solo il tumore più grande in questi casi, potremmo perdere pazienti che avevano bisogno di una terapia specifica. Le conseguenze dell’eterogeneità tra i foci tumorali per il processo decisionale terapeutico e, pertanto, per una maggiore sopravvivenza del paziente sono raramente affrontate nella letteratura.
Pertanto, si dovrebbe prestare maggiore attenzione ai tumori MF/MC e la possibilità di avere come routine la richiesta di immunohistochimica per tutti i foci tumorali dovrebbe essere valutata regolarmente, poiché dall’approccio standard i pazienti con disaccordo tra i foci avrebbero smesso di ricevere un trattamento ormonale e anti-Her-2 per il cancro al seno.
Ci sono alcune limitazioni alla nostra analisi. In primo luogo, il nostro lavoro è stato retrospettivo, anche se alcuni degli approcci dei dati estratti sono stati richiesti durante lo studio, i dati sul tumore istopatologico non potevano essere dettagliati, quando non sono stati fatti al momento della preparazione del risultato istopatologico; oltre al fatto che alcuni blocchi di paraffina erano disponibili per ulteriori ricerche, rendendo impossibile eseguire l’immunoistochimica e, di conseguenza, una piccola dimensione del campione. Questo fatto potrebbe non riuscire a evidenziare alcune associazioni che potrebbero esistere, caratterizzando così un errore statistico di tipo II. Questo fatto compromette la convalida esterna dei nostri risultati.
CONCLUSIONE
La maggior parte dei tumori MF/MC hanno omogeneità tra i foci tumorali, e la valutazione di più di un focus può avere conseguenze terapeutiche solo in una minoranza di casi, oltre ad aumentare i costi e il tempo. Tuttavia, poiché la prognosi e il trattamento dei pazienti affetti da cancro al seno possono variare a seconda della caratterizzazione molecolare del tumore, si può sostenere, dal punto di vista biologico, che l’analisi di un solo obiettivo, come indicato nelle attuali raccomandazioni, non sarebbe appropriato. Ci sono prove emergenti che questa raccomandazione potrebbe non essere sostenibile nel tempo e potrebbe essere necessario adattarsi per essere compatibile con l’evoluzione dei paradigmi del cancro al seno.
Concludiamo che il cancro al seno MF/MC mostra una piccola percentuale di eterogeneità tra i foci in relazione ai parametri biologici, tuttavia, questo svolge un ruolo cruciale nel prendere decisioni sul trattamento adiuvante e di conseguenza sul tasso di prognosi, recidiva tumorale e metastasi distante per le donne con tale scoperta. Sarebbe estremamente interessante richiedere regolarmente l’immunohistochimica per tutti i foci tumorali nei casi di MF/MC. Tuttavia, considerando il potenziale onere finanziario aggiuntivo per i laboratori all’avvio di questa raccomandazione, i laboratori di patologia potrebbero dover sviluppare ulteriori strategie per affrontare questa nuova proposta.
ETHICAL ASPECTS
Questo progetto è conforme alle leggi vigenti del paese e ai postulati della Dichiarazione di Helsinki, [23]approvati dal Comitato locale per l’etica e la ricerca (CEP).
RIFERIMENTI
- Global Burden of Disease Cancer Collaboration. “The Global Burden of Cancer 2013.” JAMA oncology4 (2015): 505–527.
- MS/INCA. Estimativa 2016: Incidência de Câncer no Brasil/ Instituto Nacional de Câncer José Alencar Gomes da Silva, Coordenação de prevenção e vigilância. Rio de Janeiro: INCA, 2015. ISBN 978-85-7318-283-5, acessado em inca.gov.br/estimativa/2016/estimativa-2016-v11.pdf
- Zhou M, Tang Z, Li J, Fan J H, Pang Y, et al; Clinical and Pathologic Features of Multifocal and Multicentric Breast Cancer in Chinese Women: A Retrospective Cohort Study. Journal of Breast Cancer. 2013;16(1):77-83.
- Salgado R, Aftimos P, Sotiriou C, Desmedt C; Evolving paradigms in multifocal breast cancer. Semin Cancer Biol. 2015 Apr; 31:111-8.
- Lynch S P, Lei X, Chavez-MacGregor M, Hsu L, Meric-Bernstam F, et al; Multifocality and multicentricity in breast cancer and survival outcomes. Annals of Oncology 2012, 23: 3063–3069
- Lynch S P, Lei X, Hsu L, Meric-Bernstam F, Buchholz T A, et al; Breast Cancer Multifocality and Multicentricity and Locoregional Recurrence. The Oncologist 2013, 18:1167-1173.
- Fitzgibbons P L, Bose S, Chen Y, Connolly J L, Baca M E et al. Protocol for the examination of specimens from patients with invasive carcinoma of the breast. Version Invasivebreast 4.0.0.0 June 2017 cap.org/cancerprotocols 2017 College of American Pathologists (CAP)
- Weissenbacher T M, Zschage M, Janni W, Jeschke U, Dimpfl T, et al; Multicentric and multifocal versus unifocal breast cancer: is the tumor-node-metastasis classification justified? Breast Cancer Res Treat (2010) 122:27–34
- Buggi F, Folli S, Curcio A, Casadei-Giunchi D, Rocca A, et al; Multicentric/multifocal breast cancer with a single histotype: is the biological characterization of all individual foci justified? Annals of Oncology 2012 23: 2042–2046
- Chagas C R, et al. Tratado de Mastologia da SBM – Rio de Janeiro : Revinter, 2011. ISBN 978853720346-0
- Boros M, Podoleanu C, Georgescu R, Moldovan C, Molna C, et al; Multifocal/multicentric breast carcinomas showing intertumoral heterogeneity: a comparison of histological tumor and lymph node metastasis. Pol J Pathol 2015; (2): 125-132.
- Neri A, Marrelli D, Megha T, Bettarini F, Tacchini D, et al. “Clinical significance of multifocal and multicentric breast cancers and choice of surgical treatment: a retrospective study on a series of 1158 cases.” BMC Surgery. 2015;15(1):1.
- Kadioğlu H, Özbaş S, Akcan A, Soyder A, Soylu L, et al. Comparison of the histopathology and prognosis of bilateral versus unilateral multifocal multicentric breast cancers. World Journal of Surgical Oncology. 2014; 12:266.
- Vera-Badillo F E, Napoleone M, Ocana A, Templeton A J, Seruga B, et al.; Effect of multifocality and multicentricity on outcome in early stage breast cancer: a systematic review and meta-analysis. BreastCancer Res Treat 2014; 146: 235-244.
- Batiston A P, Tamaki E M, Souza L A, Santos M L M. ; Conhecimento e prática sobre os fatores de risco para o câncer de mama entre mulheres de 40 a 69 anos. RevBras Saúde MaternInfant, Recife; 2011; 11 (2): 163-171.
- Lannin D R, Mathews H F, Mitchell J; Influence of socioeconomic and cultural factors on racial differences in late stage presentation of breast cancer. JAMA. 1998; 279 (22): 1801-1807.
- Yerushalmi R, Kennecke H, Woods R, Olivotto I A, Speers C, et al. Does multicentric/multifocal breast cancer differ from unifocal breast cancer? An analysis of survival and contralateral breast cancer incidence. Breast Cancer Res Treat (2009) 117: 365.
- Coombs J, Boyages J; Multifocal and multicentric breast cancer: does each focus matter? J ClinOncol 2005; 23: 7497-7502.
- M, Marian. C, Moldovan. C, Stolnicu. S, Morphological heterogeneity of the simultaneous ipsilateral invasive tumor foci in breast carcinoma: A retrospective study of 418 cases of carcinomas, In Pathology – Research and Practice, 2012, (208): 604-609, ISSN 0344-0338.
- Curigliano G, Burstein H J, Winer E, Gnant M, Dubsky P, et al. De-escalating and escalating treatments for early-stage breast cancer: the St. Gallen International Expert Consensus Conference on the Primary Therapy of Early Breast Cancer 2017. Ann Oncol.2017 Aug 1;28(8):1700-1712.
- Choi Y, Kim E J, Seol H, Lee H E, Jang M J, et al. The hormone receptor, human epidermal growth factor receptor 2, and molecular subtype status of individual tumor foci in multifocal/multicentric invasive ductal carcinoma of breast. Hum Pathol.2012 Jan;43(1):48-55.
- Pekar, G., Gere, M., Tarjan, M., Hellberg, D. and Tot, T., Molecular phenotype of the foci in multifocal invasive breast carcinomas: Intertumoral heterogeneity is related to shorter survival and may influence the choice of therapy. Cancer, 2014 Jan 1; 120 (1): 26–34.
- Review C, Communication S, Principles G. World Medical Association Declaration of Helsinki: ethical principles for medical research involving human subjects. JAMA. 2013;310:2191-2194.
APPENDIX – FIGURE E TABELLE IN ITALIANO
Fig. 1 Diagramma di flusso della selezione dei partecipanti
TABELLA 1 – Incidenza di cancro al seno non ifocale, multifocale e multicentrico presso l’Ospedale Baron de Lucena (HBL) e il Prof. Fernando Figueira Madre e Bambino Istituto (IMIP). Recife
| Cancro al seno | n (HBL/IMIP) | % (HBL/IMIP) |
| 2012 | ||
| Unifocal | (195/-) | (92.4/-) |
| MC/MF | (16/-) | (7.6/-) |
| 2013 | ||
| Unifocal | 477 (184/293) | 95.9 (93.4/ 97.7) |
| MC/MF | 20 (13/7) | 4.0 (6.6/ 2.3) |
| 2014 | ||
| Unifocal | (150/-) | (92.6/-) |
| MC/MF | (12/ 12) | (7.4/-) |
| 2015 | ||
| Unifocal | 523 (162/361) | 94.9 (89.5/ 97.6) |
| MC/MF | 28 (19/ 9) | 5.0 (10.5/ 2.4) |
IMIP data for 2012 and 2014 are not available. Source: IMIP/HBL research
TABLE 2 – Characteristics of patients with multifocal and multicentric breast cancer operated at the Barão de Lucena Hospital (HBL) and Prof. Fernando Figueira Mother and Child Institute (IMIP). Recife, Pernambuco
| Variables | n | % |
| Age | ||
| <50 | 26 | 29.2 |
| ≥50 | 57 | 64.1 |
| Skin color | ||
| White | 16 | 18.0 |
| Black | 2 | 2.2 |
| Mixed race black | 30 | 33.7 |
| Schooling | ||
| Illiterate | 6 | 6.7 |
| Incomplete elementary school | 22 | 24.7 |
| Complete elementary school | 6 | 6.7 |
| Incomplete high school | 1 | 1.1 |
| Complete high school | 12 | 13.5 |
| Stato civile | ||
| Unione civile | 1 | 1.1 |
| Singolo | 8 | 9.0 |
| Sposato, Capodanno | 13 | 14.6 |
| Divorced | 3 | 3.4 |
| Widowed | 9 | 10.1 |
Data not reported for each variable were omitted from the table. Source: IMIP/HBL research
TABLE 3 – Clinical and tumor characteristics of patients with multifocal and multicentric breast cancer operated at the Barão de Lucena Hospital (HBL) and Prof. Fernando Figueira Mother and Child Institute (IMIP). Recife, Pernambuco
| Variables | n | % |
| ER | ||
| Positive | 40 | 44.9 |
| Negative | 20 | 22.5 |
| PR | ||
| Positive | 35 | 39.3 |
| Negative | 25 | 28.1 |
| HER2 | ||
| Positive | 18 | 20.2 |
| Negative | 36 | 40.5 |
| Ki67 | ||
| <14% | 16 | 18.0 |
| >14% | 37 | 41.6 |
| Compromised lymph nodes | ||
| Absent | 23 | 25.8 |
| 1 to 3 | 18 | 20.2 |
| 4 or more | 20 | 22.5 |
| Histological grade | ||
| I | 9 | 10.1 |
| II | 27 | 30.4 |
| III | 13 | 14.6 |
| Histological type | ||
| Ductal | 73 | 82.0 |
| Lobular | 1 | 1.1 |
| Others | 4 | 4.5 |
| Size of the largest tumor | ||
| <2 cm | 24 | 27.0 |
| 2-5 cm | 32 | 36.0 |
| >5 cm | 5 | 5.6 |
| Distant metastasis | ||
| Yes | 9 | 10.1 |
| No | 48 | 53.9 |
| Lymphovascular invasion | ||
| Yes | 20 | 22.5 |
| No | 24 | 27.0 |
| Heterogeneity between foci | ||
| Yes | 8 | 9.0 |
| No | 17 | 19.1 |
| Distance between foci | ||
| ≤ 4 cm (multifocal) | 58 | 65.2 |
| > 4 cm (multicentric) | 15 | 16.9 |
Data not reported for each variable were omitted from the table. ER: Estrogen receptor PR: Progesterone receptor. Source: IMIP/HBL research
TABLE 4 – Clinical and tumor characteristics of patients with multifocal/multicentric breast cancer operated at the Barão de Lucena Hospital (HBL) and Prof. Fernando Figueira Mother and Child Institute (IMIP), in relation to heterogeneity between foci. Recife, Pernambuco
| Heterogeneity between foci | |||
| Variables | Yes | No | p-value |
| n (%) | n (%) | ||
| Compromised lymph nodes | |||
| Absent | 2 (40.0) | 3 (60.0) | 1.000 * |
| 1 to 3 | 2 (33.3) | 4 (66.7) | |
| 4 or more | 3 (50.0) | 3 (50.0) | |
| Histological grade | |||
| I | 2 (66.7) | 1 (33.3) | 0.748 * |
| II | 2 (25.0) | 6 (75.0) | |
| III | 1 (33.3) | 2 (66.7) | |
| Size of the largest tumor | |||
| <2 cm | 4 (57.1) | 3 (42.9) | 0.510 * |
| 2-5 cm | 3 (33.3) | 6 (66.7) | |
| >5 cm | 0 (0.0) | 2 (100.0) | |
| Distant metastasis | |||
| Yes | 1 (20.0) | 4 (80.0) | 0.588 * |
| No | 5 (45.5) | 6 (54.5) | |
| Lymphovascular invasion | |||
| Yes | 4 (57.1) | 3 (42.9) | 0.592 * |
| No | 2 (28.6) | 5 (71.4) | |
(*) Fisher’s Exact Test. Source: IMIP/HBL research
TABLE 5 – Clinical and tumor characteristics of patients with multifocal and multicentric breast cancer operated at the Barão de Lucena Hospital (HBL) and Prof. Fernando Figueira Mother and Child Institute (IMIP). Recife, Pernambuco
| Distance between foci | |||
| Variables | ≤4 cm (multifocal) | >4 cm (multicentric) | p-value |
| n (%) | n (%) | ||
| ER | |||
| Positive | 29 (80.6) | 7 (19.4) | 1.000 * |
| Negative | 12 (80.0) | 3 (20.0) | |
| PR | |||
| Positive | 26 (81.3) | 6 (18.7) | 1.000 * |
| Negative | 15 (78.9) | 4 (21.1) | |
| HER2 | |||
| Positive | 14 (82.4) | 3 (17.6) | 0.723 * |
| Negative | 22 (75.9) | 7 (24.1) | |
| Ki67 | |||
| <14% | 13 (86.7) | 2 (13.3) | 0.695 * |
| >14% | 22 (75.9) | 7 (24.1) | |
| Compromised lymph nodes | |||
| Absent | 16 (84.2) | 3 (15.8) | 0.839 * |
| 1 to 3 | 11 (73.3) | 4 (26.7) | |
| 4 or more | 16 (80.0) | 4 (20.0) | |
| Histological grade | |||
| I | 6 (66.7) | 3 (33.3) | 0.440 * |
| II | 20 (87.0) | 3 (13.0) | |
| III | 9 (81.8) | 2 (18.2) | |
| Histological type | |||
| Ductal | 49 (80.3) | 12 (19.7) | 0.370 * |
| Lobular | 1 (100.0) | 0 (0.0) | |
| Others | 2 (50.0) | 2 (50.0) | |
| Size of the largest tumor | |||
| <2 cm | 19 (79.2) | 5 (20.8) | 0.884 * |
| 2-5 cm | 20 (76.9) | 6 (23.1) | |
| >5 cm | 2 (66.7) | 1 (33.3) | |
| Distant metastasis | |||
| Yes | 5 (62.5) | 3 (37.5) | 0.331 * |
| No | 35 (83.3) | 7 (16.7) | |
| Lymphovascular invasion | |||
| Yes | 13 (72.2) | 5 (27.8) | 0.256 * |
| No | 21 (87.5) | 3 (12.5) | |
(*) Fisher’s Exact Test. Source: IMIP/HBL research
[1] Master in salute materna e infantile da parte del programma di laurea stricto sensu dell’Instituto de Medicina Integral Professor Fernando Figueira – IMIP, Pernambuco.
[2] Dottorato di ricerca in Tocoginecologia presso l’Università Statale di Campinas, Brasile.
[3] Laurea magistrale in Oncologia presso l’Università di San Paolo, Brasile.
Inviato: Febbraio 2020.
Approvato: giugno 2020.