ОРИГИНАЛ СТАТЬИ
RIBEIRO, Fernando de Sá [1], JESUS, Jéssica Barbosa de [2], SOUZA, Alessandra Mendonça Teles de [3]
RIBEIRO, Fernando de Sá. JESUS, Jéssica Barbosa de. SOUZA, Alessandra Mendonça Teles de. Анализ и характеристика перспективной терапевтической цели, выявленной в Leishmania spp. Revista Científica Multidisciplinar Núcleo do Conhecimento. Ano 05, Ed. 05, Vol. 09, pp. 99-132. Maio de 2020. ISSN: 2448-0959, ссылка для доступа: https://www.nucleodoconhecimento.com.br/здравоохранение/целевой-терапевтический
РЕЗЮМЕ
Лейшманиоз является запущенным заболеванием, вызванным простейшей формой рода Leishmania spp., которая поражает около 1,6 миллиона особей каждый год и 500 000 представлены в висцеральной форме. В Бразилии ежегодно происходит около 30 000 новых случаев заболевания. Кроме того, на страну приходится 90% зарегистрированных случаев висцерального лейшманиоза, и это более тяжелая форма заболевания. В совмещенный к этим фактам, в настоящее время обработка неэффективна, способствуя к установке резистентных напряжений. В настоящее время лечение имеет несколько побочных эффектов и необратимый ущерб здоровью пациентов, этот факт способствовал поиску новых препаратов против лейшманиоза. Фермент олигопептидаза B (OPB) был изучен в качестве возможной терапевтической цели в развитии антипаразитарных агентов. Таким образом, целью этой работы является построение трехмерной модели фермента Oligopeptidase B различных видов Leishmania spp. и сравнить их друг с другом. Для этого был использован метод сравнительного моделирования. В этом методе модели видов L. brasiliensis, L. donovani, L. infantum, L. mexicana и L. panamensis были построены по программе MODELLER. Как только модели были готовы, процесс проверки был проведен и впоследствии охарактеризован, что позволило проверить многообещающую степень сходства между моделями. Наконец, эти модели были представлены методу анализа обычными режимами, которые получили аналогичную схему движения, таким образом, можно было проверить движение в определенном регионе альфа-селикса, что, следовательно, приводит к триаде фермента подвергается, что может свидетельствовать о механизме действия. Наконец, ожидается, что он будет использовать модели, построенные для оказания помощи в разработке перспективных новой терапии для лечения лейшманиоза.
Ключевые слова: Лейшманиаз, олигопептидаза B, молекулярное моделирование, нормальные режимы.
ВВЕДЕНИЕ
Лейшманиоз, вызванный лейшманией spp., это заболевание, характеризующееся несколькими типами проявлений, от легкой, в которой есть сообщения о небольших поражениях, что даже без должного лечения регресс к самым тяжелым из них, таких как Висцеральный лейшманиоз (VL). В Бразилии наиболее тяжелая форма этого заболевания представляет тревожные данные по сравнению с другими странами, что делает страну крупнейшим держателем случаев VL во всей Америке (ALVARENGA, 2010; ВОЗ, 2019).
Это заболевание относится к группе забытых заболеваний, которые являются частью всех тех заболеваний, которые в основном затрагивают слаборазвитые страны и более бедные регионы, так что оно не вызывает интереса к разработке лекарственных средств. Поэтому необходимо, чтобы эффективные и недорогие методы выжили, чтобы преодолеть отсутствие финансовых стимулов для изучения этого заболевания. Таким образом, вычислительные методы могут быть использованы для того, чтобы сократить время разработки перспективной новой терапии и, следовательно, затраты по сравнению с более традиционными методами разработки лекарственных средств (BAILEY et al., 2017; ВОЗ, 2017).
Несмотря на небольшие инвестиции в этой области, есть лечение для таких заболеваний, как противоминные пентас валентес (препарат первого выбора) или амфотерицин В (препарат второго выбора). Тем не менее, такие методы лечения имеют ряд недостатков, таких как высокая частота резистентности и широкий спектр побочных эффектов, начиная от морской болезни до возможных проблем, вызванных третьей (третьей) парой черепного нерва, что приводит к затруднениям двигателя (MACEDO-SILVA et al., 2014).
С учетом возникшей проблемы и эпидемиологической важности лейшманиоза, необходимость исследования новых конкретных терапевтических целей против этой болезни является печально известной. В качестве одной из новых терапевтических целей, у нас есть Oligopeptidase B (OPB) (рисунок 1), который является протеазой серина, принадлежащих к подсемейства S9A, имея в качестве характеристики каталитическая триада состоит из остатков аминокислот serine (Ser), асаптической кислоты (Asp) и гистидин (Его), которые расположены между двумя доменами. Этот фермент имеет столь же характерную способность расщеплять остатки белковых структур. Кроме того, он описывается в литературе как ключевой компонент для иммунного механизма побега паразита, расщепление энолазы, белок, который будет opsonisar простейшие, так что при признании макрофага он разрушается. Однако, в то время как паразит находится внутри макрофагов, OPB является супер выраженным, в результате чего паразит не будет признан в клетке, поэтому он будет размножаться, пока он не будет сглажен (SODERO et al., 2016; SWENERTON et al., 2011; ОВЧИННИКОВА и др. 2018).
Рисунок 1: Трехмерная структура L. major OPB (КОД PDB 2XE4) (MCLUSKEY et al., 2010), показывающая каталитические домены и домены. Вторичные структуры, такие как суглюк, листья и ручки, показаны красным, желтым и зеленым цветом соответственно. В частности, показаны остатки (Ser557, Asp662 и His697) каталитического триады.
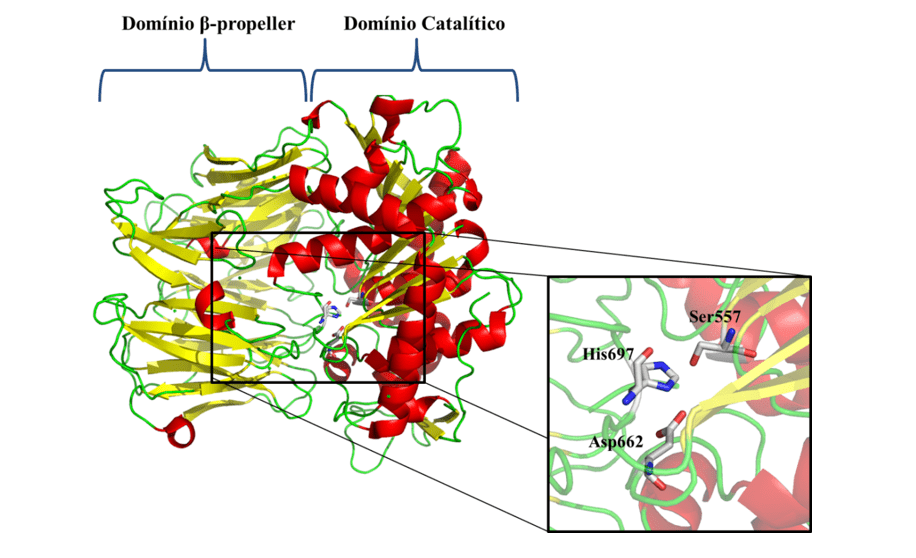
Поэтому исследование, о котором идет речь, было направлено на изучение и характеристику ОПБ и их активных мест, видов L. brasiliensis, L, donovani, L. infantum, L. mexicana и L. panamensis. Наконец, ожидается выявление возможных сходств между белками, с тем чтобы это позволило в будущем разработать многообещающую новую терапию с широким спектром действий на ферменты всех видов в исследовании.
ОБЩАЯ ЦЕЛЬ
Ввиду необходимости разработки новых химических образований для лечения лейшманиоза, эта работа была основной целью построить и охарактеризовать фермент олигопептидаза B Лейшмании spp. с использованием вычислительных методов обучения.
КОНКРЕТНЫЕ ЦЕЛИ
- Для построения и проверки моделей олигопептидазаs B ферментов вида Лейшмания;
- Выполните характеристику ферментов;
- Выполняйте симуляционные исследования в обычных режимах.
МАТЕРИАЛ И МЕТОДИС
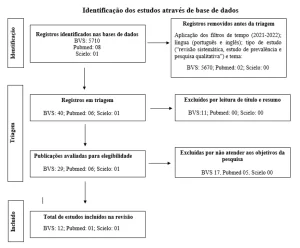
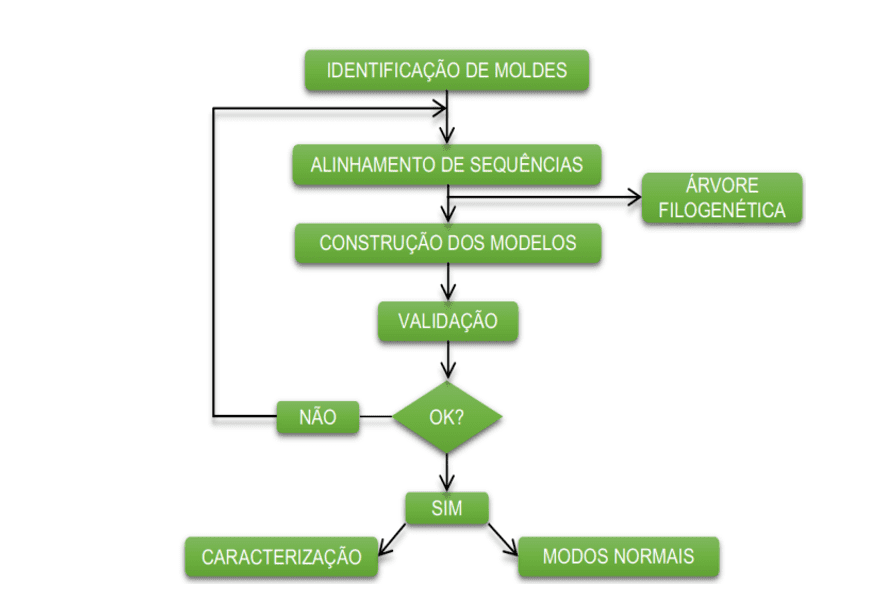
На приведенной ниже диаграмме (диаграмма 1) упрощенно показаны шаги, используемые при разработке этой работы.
Схема 1: Упрощенная схема материальных шагов и методов.
ПОЛУЧЕНИЕ ПЕРВИЧНОЙ СТРУКТУРЫ
Основные структуры Leishmanias OPBs были получены из базы данных Uniprot (The Universal Protein Resource) (WANG et al., 2012).
MOLD ID
Затем, поиск белков плесени был выполнен из выравнивания между аминокислотной последовательности целевого белка и аминокислотных последовательностей белков, отложенных в банке данных о белках (PDB) сервером BLAST (Basic Local Alignment Search Tool) (ATLSCHUL et al., 1997) на основе идентичности между аминокислотными последовательностями.
РАССТАНОвКА СЕКВЕНС
После того, как плесень, которая будет использоваться была определена, плесень последовательность была приведена в соответствие с их соответствующих OPBs, в программе ClustalOmega (ClustaO) (SIEVERS и др., 2011).
КОНСТРУКЦИЯ МОДЕЛИ
После получения выравнивания эта информация была использована в программе MODELLER v9.20 для построения 3D-структур моделей (WEBB и SALI, 2016).
ПРОВЕРКА ПОСТРОЕННЫХ МОДЕЛЕЙ
Для проверки моделей использовался график Ramachandran, генерируемый PDFBsum, Verify 3D и ProSA-web-сервером, полученный с сервера Saves.
При анализе графика Рамачандрана допустимо визуализировать дигелраальные углы (фи (я) и пси (я)) аминокислотных остатков в структуре белка. Угол phi является результатом связи между группой NH и альфа-углеродом, в то время как угол пси (я) происходит от связи между альфа-углеродом и группой углерода (RAMACHANDRAN et al., 1963).
График обеспечивает простой способ визуализации распределения торм углы структуры белка. Кроме того, он предоставляет обзор разрешенных и не разрешенных областей значений угла torm, служа важным фактором в оценке качества 3D белковых структур. При этом он определяет остатки, которые находятся в регионах, которые являются энергетически более благоприятными и неблагоприятными и направляет оценку качества теоретических или экспериментальных моделей белков. Этот график делится на регионы, так что наиболее благоприятные регионы в красном, дополнительные регионы более разрешительные в коричневых, разрешительных регионах в желтых и неразрешительных регионах в белом. Согласно этой проверке прогнозируемой модели, которая должна рассматриваться как отличная качественная, она должна иметь более 90% аминокислотных остатков в наиболее благоприятном регионе (SANTOS-FILHO и ALENCASTRO, 2003).
Кроме того, он должен иметь большинство своих остатков в наиболее благоприятных регионах, а также не иметь остатков в неразрешительных регионах, за исключением аминокислот глицин (Gly) и proline (Pro), которые являются исключениями для этой области. Эти два остатка представляют собой вариации в боковой цепи, которые придают большую жесткость, в случае Pro, и большую гибкость, в случае Gly, таким образом, может взять на себя неожиданные ангуляции. По этой причине они принимаются в неразрешительных регионах диаграммы. Существование недопускаемых регионов связано с тем, что между остатками (боковыми цепями) аминокислот имеются стерические эффекты. (MORRIS et al., 1992).
Verify 3D анализирует совместимость атомной (3D) модели с собственной аминокислотной (1D) последовательностью. Каждый остаток получает структурный класс, основанный на его местоположении и окружающей среде (альфа, бета, петля, полярный, аполярный и т.д.). Вскоре после этого, база данных, генерируемых из хороших структур используется, чтобы получить балл для каждого из 20 аминокислот в этом структурном классе. Вертикальная ось на графике представляет собой средний балл профиля 3D-1D для каждого остаточного в раздвижном окне из 21 остаточного, а результаты в виде баллов варьируются от -1 (плохой балл) до 1 (хороший балл) (EISENBERG et al., 1997).
ProSa-web вычисляет общий балл качества для конкретной структуры ввода. Если оценка этого находится за пределами диапазона, характерного для местных белков, структура, вероятно, содержит ошибки. Много местных показателей качества указывают на проблемные части модели, которые также выделены в 3D молекулы зрителя для легкого обнаружения (WIEDERSTEIN и SIPPL, 2007).
АНАЛИЗ ВТОРИЧНОЙ СТРУКТУРЫ
После стадии проверки третичные структуры моделей были сопоставлены с распределением вторичной структуры, предсказанной quick2D, доступной на сервере Bioinformatics Toolkit (https://toolkit.tuebingen.mpg.de/), выбрав таким образом модели (ALVA et al., 2016).
ХАРАКТЕРЦИЯ ОЛИГОПЕПТИДАС (OPBS) ЛЕЙШМАНИАС
ЭЛЕКТРОСТАКТАЦИЯ POTENTIAL MAP (MEP)
Для получения евродепутатами поверхностей и мест подключения ОПБ было использовано расширение программы PyMOL, apb-инструментов (BAKER et al., 2001). Перед анализом в PyMOL ферменты были подготовлены в СЕРВЕРе PDB2P-R (http://nbcr-222.ucsd.edu/pdb2pqr_2.0.0/) с использованием стандартного параметра сервера (DOLINSKY et al., 2004).
ХАРАКТЕРИСТИКА сайтов и ПОДSITES ОПБ
Модели и плесень были представлены в белков плюс платформы с использованием опции Dogsitescorer (VOLKAMER et al., 2012), в которой полости были предсказаны в 3D структурах моделей. Это привело к результатам в отношении возможных связывающих участков и ферментных подсайтов для прогнозирования этих полостей. Программа использует трехмерную сетку, край которой может быть отрегулирован между 0,2 и 1,0 евро, а также гауссианский фильтр, который используется для идентификации полостей на поверхности белка, которые подходят для размещения атомов лиганда. Кроме того, DoGSiteScorer также прогнозирует лекарственность для каждой предсказанной полости. Таким образом, для каждого взаимодействия между белком и возможным препаратом назначается оценка, относящаяся к лекарственности полости, называемая drugscore. Для прогнозирования стоимости препарата программа использует векторной аппарат поддержки (SVM), в которой используются следующие дескрипторы: объем, доля неполярных остатков и глубина (VOLKAMER et al., 2012).
ФИЛОГЕНЕТИКИ ТРИ
Наконец, степень эволюционного родства между видами Лейшманий была проанализирована с помощью программы MEGA (Molecular evulutionary genetics analysis), используя методы присоединения к соседам, что позволяет строить филогенетическое дерево для определения эволюционной вероятности между популяциями последовательностей, ранее определенных пользователем (KUMAR et al., 2004).
NORMAL MODES
Для выполнения обычных режимов использовались файлы, генерируемые на стадиях энергетических минимизов, созданных версией GROMACs 5.1.2. Были выполнены первые 4 шага, связанных с процессом молекулярной динамики. Первым было поколение топологических файлов, с добавлением водорода в белок. Во втором был создан водяной ящик, и это очень важный шаг для расчета взаимодействия между белком и растворителем. В третьем, ионы были добавлены для создания нейтральной системы. Наконец, на четвертом этапе были проведены минимизации энергии, в которые было вставлено силовое поле AMBER99SB. С этого момента, нормальные режимы моделей были выполнены с помощью ANM (Anisotropic Network Model) (http://anm.csb.pitt.edu/) сервер для анализа движения ферментов вида лейшмании, а также для наблюдения за некоторыми важными характеристиками фермента, таких как возможные движения, связанные с механизмом действия (EYAL et al., 2015).
РЕЗУЛЬТАТЫ И ОБСУЖДЕНИЯ
SELECTION OF MOLD PROTEINS AND ALIGNMENT BETWEEN SEQUENCES
Мы получили 100 первичных структур ОПБ лейшмании spp. с помощью сервера UniProt, с 5 видами Leishmanias выбран. Пересмотренные аминокислотные последовательности, отобранные из фермента OPB, были L.brasiliensis, Л. доновани, Л. инфантум, Л. Мексика на 4Х5-8, C9EF60, A4HT8, E9AMS8 и A0A088RJA7, соответственно, эти виды были отобраны, в связи с их высокой заболеваемостью в южной Америке и их устойчивостью к текущему лечению лейшманиаза (GHORHOUI.
Для построения 3D-моделей программа BLAST использовалась для сравнения аминокислотных последовательностей целевых последовательностей с белковыми последовательностями экспериментально выясненной трехмерных структур. Основываясь на идентичности между последовательностями и количеством пробелов, ENZYME OPB L. major (код PDB 2XE4) был выбран в качестве белка плесени (MCLUSKEY et al., 2010). Идентичность между целевыми ферментами и их соответствующей плесенью представляла значения между 86% и 96% (таблица 1). Процент идентичности между двумя последовательностями относится к присутствию одной и той же аминокислоты в одном и том же положении между выровненных последовательностями. Для построения модели белка с более чем 80 аминокислотными остатками процент идентичности между первичными структурами плесени и моделью должен быть выше 25%. Кроме того, процент разрывов должен быть низким в 20%, чтобы считаться хорошим выравниванием (SANTOS-FILHO и ALENCASTRO, 2003). Таким образом, высока вероятность сходства трехмерных структур белков.
Таблица 1: Процент идентичности между моделями олигопептии B видов лейшмании и их соответствующей плесени.
| Proteína molde (código PDB) | Modelos de OPB
(código uniprot) |
Identidade (%) | Gaps (%) |
| OPB
L. major (código PDB 2XE4) |
L.brasiliensis
(A4H5Q8) |
86 | 0 |
| L. donovani
(C9EF60) |
96 | 0 | |
| L. infantum
(A4HTZ8) |
96 | 0 | |
| L. Mexicana
(E9AMS8) |
90 | 0 | |
| L. panamensis
(A0A088RJA7) |
86 | 0 |
Источник: Автор.
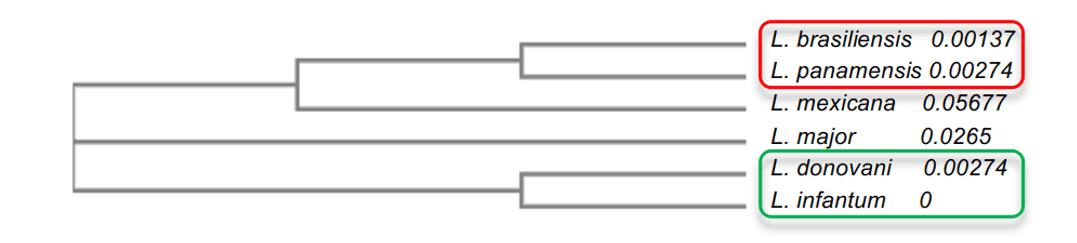
При анализе филогенетического дерева можно было объяснить степень идентичности среди видов лейшмании. Было отмечено, что виды с более высокой степенью идентичности, такие как L. infantum и L. donovani, оба с 96%, представили близость друг к другу, помимо того, что ближе к L.major. Другие виды представили более низкие значения, такие как L.mexicana (90%), который был в медиане по отношению к другим моделям. Наконец, модели с самым низким процентом идентичности, L. brasiliensis и L. panamensis, оба с 86%, были более далеки эволюционно от формы, но были очень близки друг к другу (рисунок 2). Этот анализ позволил понять разницу между степенью идентичности между видами и пониманиеней некоторых важных характеристик фермента среди видов.
Рисунок 2: Филогенетическая схема дерева Leishmania spp. OpBs ферментов. В этом представлении показаны группы с наибольшим сходством друг с другом, где группа 1 выделена красным цветом, а группа 2 – зеленым цветом.
ТРИ-МЕРЕМЕР МОЕСТЬ ЕЭНСЕЭНЦИЯ ЛЕИШМАНИЯ ВИДИ
3D-модели вида были построены по программе Modeller (WEBB и SALI, 2016) из выравнивания первичных структур (рисунок 3 и 4).
Рисунок 3: Результат выравнивания между первичными последовательностями ОПБ, выбранных в UNIPROT (Часть 1/2).

Рисунок 4: Результат выравнивания между первичными последовательностями ОПБ, выбранных в UNIPROT (Часть 2/2).

При наблюдении за результатом выравнивания структур (рисунки 3 и 4) наблюдалась более высокая степень сходства между L. donovani и L. infantum (группа 2), а также большая соответствие между L. brasiliensis и L. panamensis (группа 1). Эти результаты подтверждают то, что было представлено филогенетическим деревом на рисунке 2, где предполагается близость между видами, L. donovani и L. infantum и другая близость между видами L. brasiliensis и L. panamensis. С другой стороны, обе упомянутые группы представляли большую эволюционную дистанцию по сравнению друг с другом. Этот факт печально известен, когда в анализе выравнивания проводится сравнение, где первичные структуры показали большую разницу между остатками, по сравнению с двумя группами. Кроме того, результат выравнивания L. mexicana оказался весьма многообещающим, что относится к поддержке этой предлагаемой дискуссии, поскольку наблюдаемые различия по сравнению с другими видами были эквивалентны, иногда к первой упомянутой группе, иногда ко второй. В некоторых частях проанализированных последовательностей, конкретные мутации, которые характерны только для L. mexicana были также отмечены в некоторых частях проанализированных последовательности. Таким образом, этот факт может быть засвидетельствован своим положением в медиане в филогенетическом дереве, по отношению к другим видам.
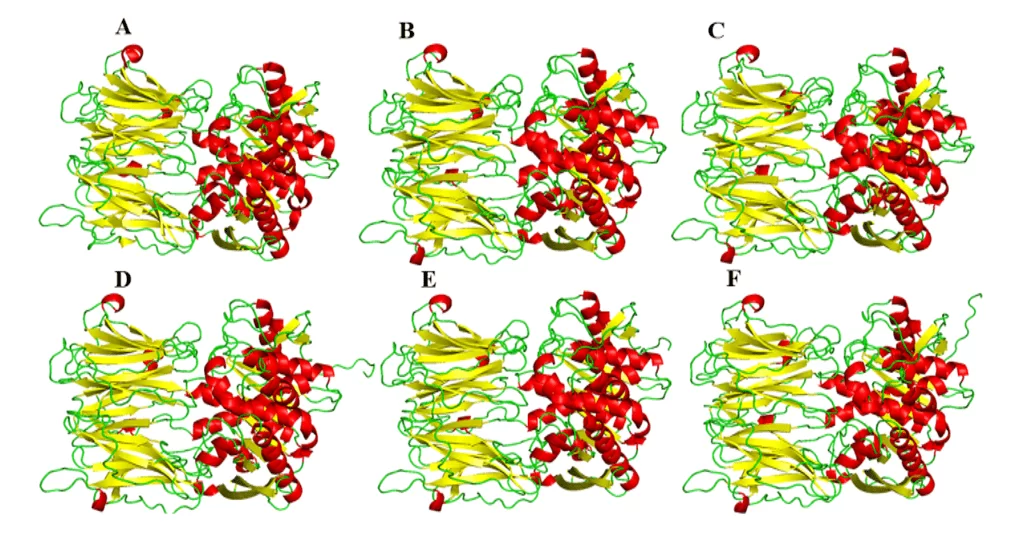
В результате сравнительного моделирования были получены модели настоящего исследования, что свидетельствует о большом визуальном сходстве в трехмерной форме по отношению к плесени (рисунок 5). Что касается сравнения между моделями, они представили различные суммы в секурс и лист-я структур между собой. Это различие можно объяснить специфическими различиями в составе остатков белка, но таких различий в важных регионах этих ферментов, таких как переплет. Таким образом, эти различия не так важны, чтобы изменить структуры или профиль взаимодействия с возможным препаратом на сайте связывания.
Рисунок 5: Модели и плесень OPBs лейшмании spp., будучи показаны в красном селерки, зеленый ручки и желтый листья-я. Para OPB, (A) L.major (molde) e modelos: (B) L. brasiliensis, (C) L. donovani, (D) L. infantum, (E) L. mexicana e (F) L. panamensis.
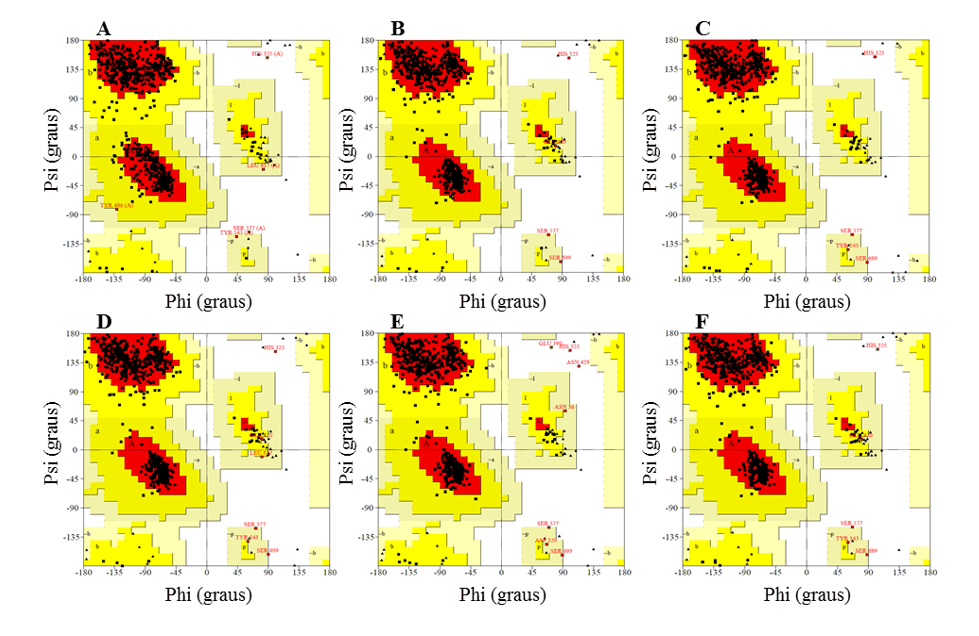
На стадии проверки они были проанализированы на основе анализа графиков ramachandran (предоставлены сервером PDBsum), 3D-1D баллов (предоставленных программой verify-3D) и оценка-Я (предоставлена ProSA-веб-сервер). Значения, полученные для моделей, сравнивались с значениями, полученными для формы.
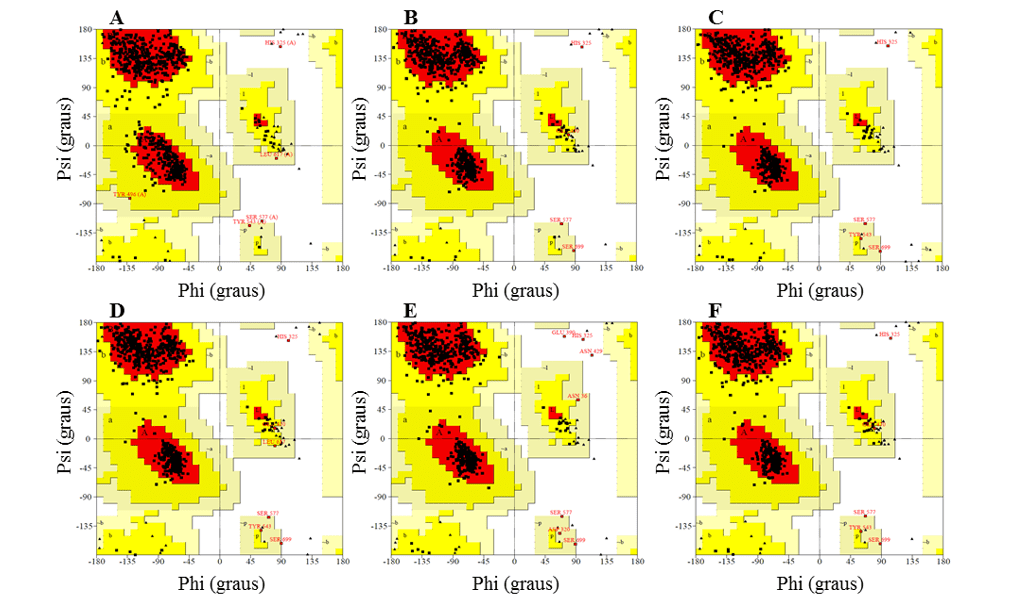
В рамачандранской графе модели представили большинство остатков в благоприятных регионах, варьируясь от 91,2 до 92,3%, в то время как доля остатков в неблагоприятных регионах составляла максимум 0,5%, а лучшими моделями были L.infantum и L.brasilienses. Эти модели представляли наибольшее количество остатков в благоприятных регионах с 92,3% и 92,2% и самый низкий процент остатков в неблагоприятных регионах с 0,3% и 0,2%, соответственно (рисунок 6).
Во всех моделях можно было заметить, что остатки Ser, которые являются частью каталитическая триада, находились в неблагоприятных регионах. Однако этот факт не влияет на действительность моделей, так как при сравнении плесень представляла тот же результат. Таким образом, этот результат не настраивает низкую надежность моделей.
Рисунок 6: Результаты рамачандранских графиков, полученных программой PROCHECK, структуры генерируемых моделей ОПБ и плесень.
| Структуры | % отходов в регионах | ||||
| Благоприятные | Разрешены | Неблагоприятных | |||
| OLIGOPEPTIDASE B | L. major (A)
(PDB 2XE4) |
90,2 | 9,5 | 0,3 | |
| L.brasilienses (B) | 92,2 | 7,7 | 0,2 | ||
| L. donovani (C) | 91,9 | 8,0 | 0,2 | ||
| L. infantum (D) | 92,3 | 7,3 | 0,3 | ||
| L. Mexicana (E) | 91,2 | 8,3 | 0,5 | ||
| L. panamensis (F) | 91,4 | 8,3 | 0,3 | ||
Источник: Подготовлено автором на основе результатов procheck.
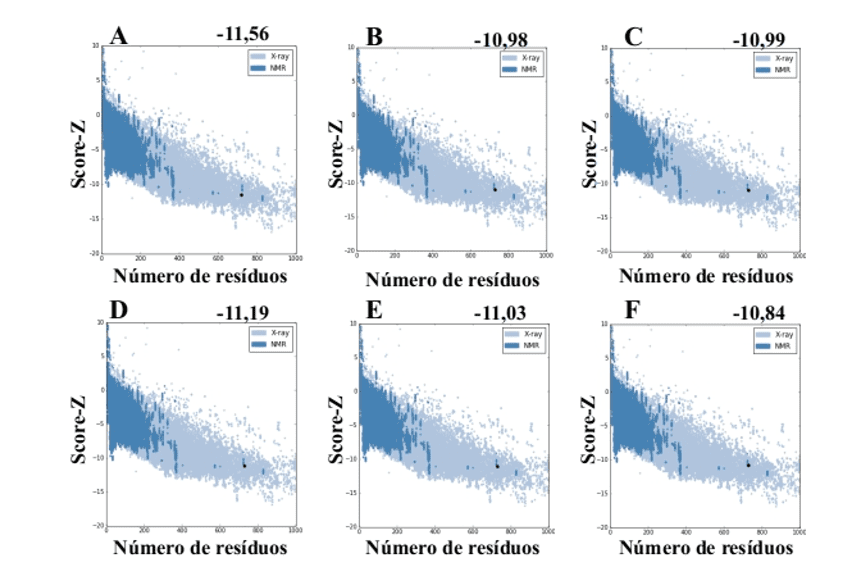
При использовании сервера ProSA-Web из моделей, генерируемых MODELLER, они представили значения оценки -10,84 до -11.19, и эти значения совместимы со структурами PDB (рисунок 7).
Рисунок 7: Результаты оценки, рассчитанные на сервере ProSA-web структур формы (для сравнения). (A) L .major (molde) e modelos: (B) L. brasilienses (C) L. donovani (D) L. infantum (E) L. mexicana (F) L. panamensis. Область в темно-синем цвете указывает на счет белков, полученных ЯМР, и в светло-голубом цвете белков, полученных рентгеновской дифракцией.
3D-программа Verify использовалась для оценки совместимости между 1D и 3D-структурами. Полученные модели представили 95,28% до 98,34% аминокислот с совместимостью 3D-1D 0.2, а модели L. donovani и L.brasilienses получили лучшие результаты. Согласно идеальным параметрам программы, большинство остатков должны представлять значения выше нуля, так как значения ниже нуля указывают на области молекулы с проблемами. Процент аминокислот с совместимостью 3D-1D 0,2 должен быть выше 80% (EISENBERG et al., 1997). Таким образом, эти результаты показывают, что модели представили 1D-3D совместимость, и остатки, которые представили несовместимость не являются частью активного сайта ферментов (таблица 2).
Таблица 2: Результаты проверки 3D, показывающие процент остатков с баллом 0,2.
| Estruturas | % de resíduos com score > 0,2 | |
| OLIGOPEPTIDASE B | L.major
(PDB 2XE4) |
93,20 |
| L.brasilienses | 95,62 | |
| L.donovani | 97,12 | |
| L.infantum | 94,93 | |
| L.mexicana | 95,62 | |
| L.panamensis | 94,93 |
Источник: Автор.
VALIDATION OF THE CATALYTIC TRIAD OF THE ENZYME OF THE MODELS
Благодаря механизму ПБ, необходимо проанализировать расстояние и ориентацию между аминокислотными остатками и каталитической триадой (Ser, Asp и His) генерируемых моделей с целью повышения надежности моделей.
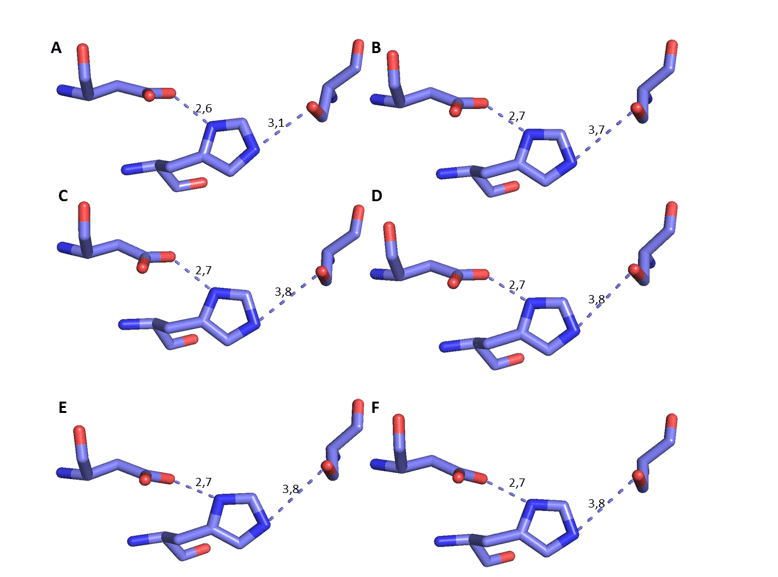
Можно наблюдать сравнение этих конкретных остатков моделей OPB с плесенью, о котором идет речь на рисунке 17. Кроме того, можно было измерить расстояние между остатками каталитической триады, основываясь на механизме взаимодействия между участком и субстратом, с Его в качестве эталона (DEREWENDA et al. , 1994). Поэтому должно быть определенное расстояние до механизма действия. Это расстояние должно быть около 3,5 “между его кислорода и сер азота, в дополнение к расстоянию около 2,6” между аспартатом кислорода и другого азота, как описано в литературе (DEREWENDA и др.. , 1994). В этом анализе удалось убедиться в том, что данное расстояние претерпело небольшое изменение и по-прежнему соответствует тому, что уже было описано. Это расстояние важно, потому что протеазы серино требуют, чтобы его для расщепления субстрата произошло (HEDSTROM, 2002) (рисунок 8). На основе этих достоверных результатов была продолжена дальнейшая характеристика моделей.
Рисунок 8: 3D-представление каталитическая триады ОПБ, соответственно, Ser, His и Asp. Темно-синий цвет представляет собой атом азота, красный кислород и сиреневый углерод. Para OPB, (A) L.major (molde)e modelos: (B) L. brasilienses (C) L. donovani (D) L. infantum (E) L. mexicana (F) L. panamensis.
КОНЦИЦИЯ ОЛИГОПЕПТИДАСЕС ЛЕИШМАНИАС
ВТОРОСТЕПЕННАЯ СТРУКТУРА ПРОГНОЗИРОВАНИЯ
Из предсказания вторичной структуры ферментов OPBs было выявлено количество и положение вторичных структур моделей. PSISPRED представлены между 15 и 16 сепликов структур и все представлены 38 пар листьев (таблица 3). По результатам, полученным PSIPRED, было проведено визуальное сравнение этой прогнозируемой вторичной структуры с трехмерными структурами 5 моделей с использованием программы Pymol. Модели L.brasilienses и L. panamensis представили наилучшее сходство по отношению к вторичным и третичным предсказанным структурам (2D-3D), представляя 15 спилежки и 38 листьев. Из 15 пропеллеров, представленных в трехмерной структуре модели 8 из пропеллеров, были в том же положении, что и предсказано PSIPRED. Эти суликсы соответствуют аминокислотной последовательности: от 59 до 74, 78 до 93, 535 до 540, 545 до 563, 631 до 640, 703 до 721 и 727 до 730.
В общем анализе не было никаких обострений в количествах листьев сhelix и q между предсказаниями и полученными моделями (таблица 3).
Таблица 3: Сравнение вторичных структур, предсказанных psipred и которые найдены через Pymol.
| Modelos | α-Hélices | Folhas β | PSIPRED
α-Hélices |
PSIPRED
Folhas β |
| L.brasiliensis | 15 | 38 | 11 | 36 |
| L. donovani | 16 | 38 | 11 | 36 |
| L. infantum | 16 | 38 | 11 | 36 |
| L. mexicana | 15 | 38 | 10 | 36 |
| L. panamensis | 15 | 38 | 11 | 36 |
Источник: Автор.
Кроме того, можно было заметить, что количество 15 к-Пропеллеров было одинаковым для L.brasilienses, L. Mexicana и L. panamensis. Так же, как L.infantum и L.donovani, они получили номер 16 хеликс. Согласно филогенетическому дереву, эти две упомянутые группы находятся в одном внутреннем узло и считаются монофилетические (рисунок 2).
Затем, RMSD (корень среднего квадратного отклонения) было выполнено между моделями и плесенью. Значения были многообещающими, как видно из таблицы 4, потому что RMSD не превышали значение 0,19 Евро. Этот вывод может быть оправдан высокой степенью идентичности между плесенью и соответствующими моделями. В целом, ожидается, что белки с идентичностью более 30%, имеют отличное перекрытие основных цепей, тем самым получая RMSD порядка 2 “(BENNER и др., 1997 ; CHOTHIA et al., 1986).
Таблица 4: RMSDs OPBs, генерируемые Модельером, имеющие с ориентацией альфа-углероды формы OPB L. major.
| Molde | Modelos | RMSD (Å) |
| L. major
(2XE4) |
L.brasiliensis | 0,15 |
| L. donovani | 0,15 | |
| L. infantum | 0,16 | |
| L. Mexicana | 0,19 | |
| L. panamensis | 0,14 |
Источник: Автор.
MAP OF MOLECULAR ELECTROSTATIC POTENTIAL (MEP) OF THE SURFACE OF ENZYMES AND RECEPTIVE SITES
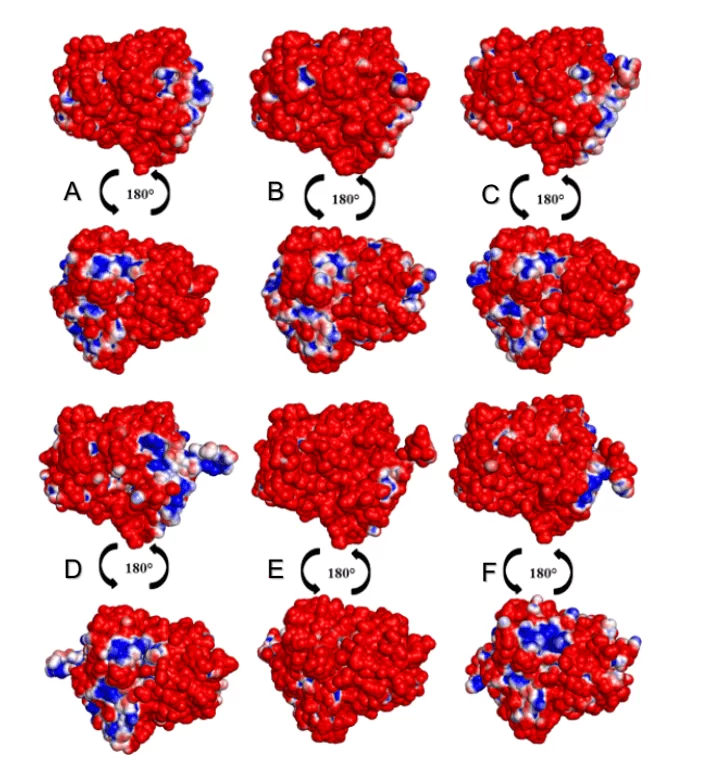
При анализе мпевров поверхностей ОПБ можно было заметить, что все виды лейшмании представляют собой более высокий процент отрицательных, чем положительных регионов, как показано на рисунке 15. Вид L. donovani и L. infantum (зеленая группа) предложил отрицательную область (в синем цвете) в том же регионе. Вид L.brasilienses и L. panamensis (красная группа) представил аналогичный отрицательный регион, в аналогичном colorimetric картины. Оба результата могут быть оправданы тем, что виды по сравнению друг с другом принадлежат к одному и тому же монофилетической (рисунок 2).
Рисунок 9: Карта электростатического потенциала 3D-моделей Leishmania spp OPBs и их плесени. Para OPB, (A) L.major (molde) e modelos: (B) L. brasilienses (C) L. donovani, (D) L. infantum, (E) L. mexicana (F) L. panamensis. В синем цвете он представляет положительную область и в красном цвете, отрицательную область.
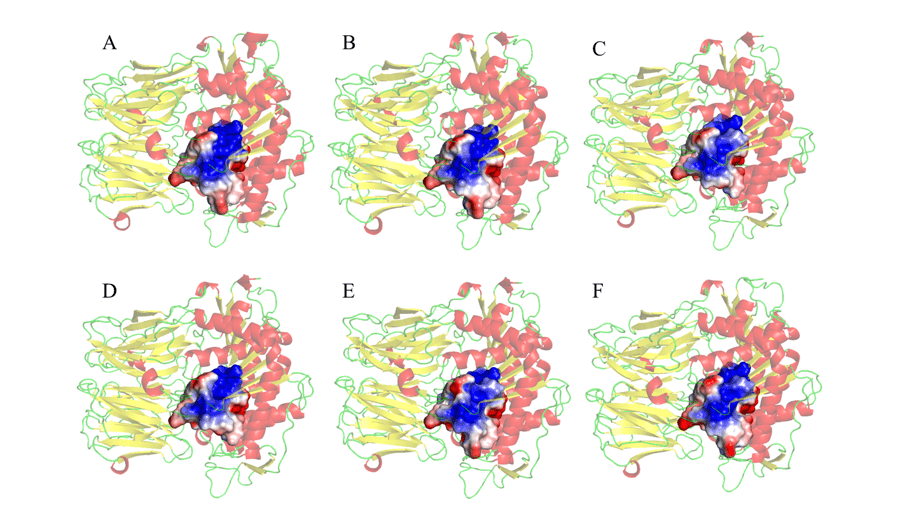
Наконец, евродепутат остатков был также исполнен в радиусе 5 евро вокруг каталитического триады, как показано на рисунке 10. Выбор наблюдать за Евродепутатом региона вокруг каталитического триады состоял в том, что это второй регион взаимодействия между ферментом и субстратом, в котором будет размещение (ANDERSSON et al., 2010). Таким образом, с учетом одной из целей исследования удалось проверить значительное сходство и соответствие между плесенью и проверенными моделями. Эти результаты, как показано на рисунке 10, показали в основном большую электропозитивную часть (синим цветом) в центральной области участков соединения. Отрицательные области (красным цветом) наблюдались в периферийных районах изучаемых евродепутатов. Эти результаты являются многообещающими, так как было установлено, что эти регионы полностью схожи во всех моделях, и может помочь в разработке препарата, который имеет возможность действовать конкретно во всех исследуемых моделях.
Рисунок 10: Представление потенциальной карты электростатической поверхности аминокислотных остатков, 5 “вокруг каталитической триады, которые составляют активное место фермента. (A) L.major (molde) e modelos: (B) L. brasilienses (C) L. donovani (D) L. infantum (E) L. mexicana (F) L. panamensis. В красном цвете находятся суглики, зеленые ручки и желтые листья- я. В золотистом цвете переплету. В синем цвете он представляет положительную область и в красном цвете, отрицательную область.
DOGSITESCORER, КАЛИФОРНИЯ
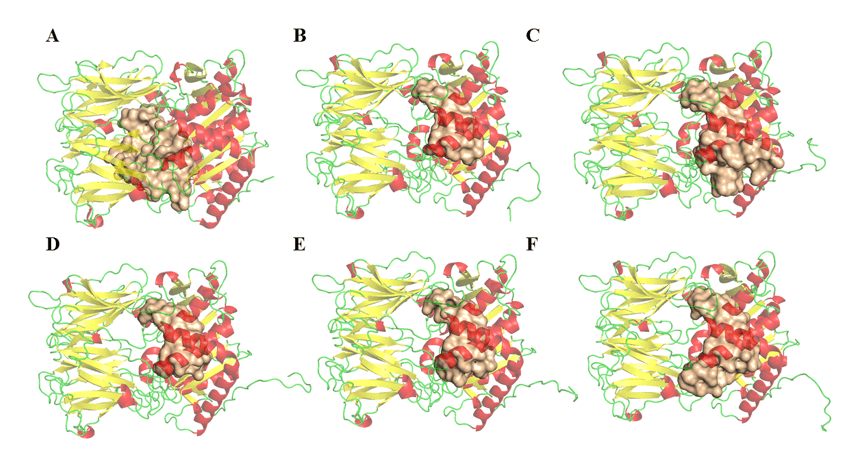
Определение объема, площади и глубины параметров возможных связывающих участков опбовых ферментов видов Лейшмании было выполнено в программе DoGSiteScorer (http://poseview.zbh.uni-hamburg.de/) ProteinsPlus – Structure-based Modeling Support Server (VOLKAMER et al., 2012). Программа указывает на три ссылки сайтов, как описано в литературе. На рисунке 11 показано сравнение возможного региона активного сайта и его различий. Эти переменные среди ОПБ могут быть связаны с остатками, которые не описаны как важные для их ингибирования, но были рассмотрены в ходе этого анализа. Таким образом, этот результат не исключает возможности антипейна или любой другой молекулы, имеющей широкий спектр ингибирования фермента, в связи с тем, что результаты, связанные с drugscore были очень похожи и положительны во всех регионах. В таблице 5 наблюдается относительное расхождение между объемом и результатами области полостей, найденных в моделях. Этот результат не предполагает предвзятого отношения к ингибирующей потенциалу одного препарата в соответствующих ферментах. Тем не менее, он обращает внимание на тот факт, что некоторые белки имеют большие полости, чем другие. Тем не менее, эти же полости имеют точки общего, и это остатки, которые составляют каталитическое место, как можно увидеть на рисунке 11 и могут быть изучены.
Таблица 5: Значения, относящиеся к возможным регионам соединения OPBs (полученные сервером).
| Estruturas | DogSiteScoore | |||
| Volume | Área | Drug Score | ||
| OLIGOPEPTIDASE B | L. major
(PDB 2XE4) |
1690,62 | 1818,41 | 0,80 |
| L.brasiliensis | 1527,84 | 1766,63 | 0,80 | |
| L. donovani | 1074,57 | 1428,55 | 0,79 | |
| L. infantum | 1309,97 | 1572,19 | 0,80 | |
| L. mexicana | 800,92 | 799,38 | 0,85 | |
| L. panamensis | 971,96 | 1083,40 | 0,81 | |
Источник: Автор.
Рисунок 11: структуры OPBs и возможные области соединения (получено сервером DogSite). (A) L .major (molde)e modelos: (B) L. brasilienses, (C), L. donovani, (D) L. infantum, (E) L. mexicana e (F) L. panamensis. В красном цвете находятся суглики, зеленые ручки и желтые листья- я. В золотистом цвете переплету.
NORMAL MODES
После характеристики фермента в структурных, поверхностных и связывающих участках, нормальные режимы для ферментов каждого вида были выполнены с целью их соответствующих движений.
После релаксации и энергии минимиза, выполняемых молекулярной динамикой в GROMACS, эти структуры были представлены на нормальный анализ для того, чтобы наблюдать возможные совместимые движения.
Можно было наблюдать во всех моделях изучаемые выразительные движения определенной селикса, и при анализе этого региона в ее аминокислотном составе можно заметить, что она высоко сохраняется. Таким образом, схема движения повторялась во всех рассматриваемых моделях. Этот регион предложил линейное движение, отодвигаемый от центра к периферии, обнажая каталитическую триаду. Это может свидетельствовать о движении, выполняемом белком для размещения субстрата.
При наблюдении фигуры 12 и 13, один и тот же цвет картина может наблюдаться во всех моделях исследования. Эти данные представляют способность данного региона двигаться в определенном направлении. Синие цвета представляют более неизменные области во время моделирования в обычных режимах, при этом, шаблон жесткости в белках заметно, соответствующие главным образом к й-листья домена к-пропеллер и некоторые сhelixes, которые составляют каталитический домен. Цвета, близкие к зеленому цвету, представляют промежуточные области по отношению к емкости и диапазону движения. Основываясь на этой информации, можно воспринимать это окрашивание в петлях на концах моделей, а также в некоторых селигах каталитического домена. Наконец, есть те регионы, которые представили оранжево-красную окраску, в которой представлен огромный потенциал движения. Таким образом, можно увидеть, что на концах каталитической областей есть небольшие области петель с таким потенциалом движения, а также спирали, расположенные в части каталитического домена, а точнее перед каталитическим триадой ОПБ, в которой она получила наиболее выразительное движение исследования.
Все модели получили одинаковую конфигурацию движения, где суглюк (оранжевый) оказался регионом с самой высокой пропускной способностью движения. Таким образом, ОПБ Л. Бразилиленсис, Л. доновани, Л. инфантум, Л. Мексика на и Л. Панаменсис в их наибольшем диапазоне движения, полученных, соответственно, 9,8, 11,3 “, 11,9” и 11,6 “(рисунок 12 и 13).
Рисунок 12: Результат анализа нормальными режимами в представлении по pymol программы, в изображении движения моделей проявляются, в их расслабленной форме (справа) по сравнению с движением большей амплитуды (слева). Также представлены наиболее жесткие регионы (Темно-синий), регионы с небольшим движением (Light Blue), промежуточные области (зеленый), регионы с хорошим потенциалом движения (оранжевый) и чрезвычайно податливые области (красный) (Part1/2).
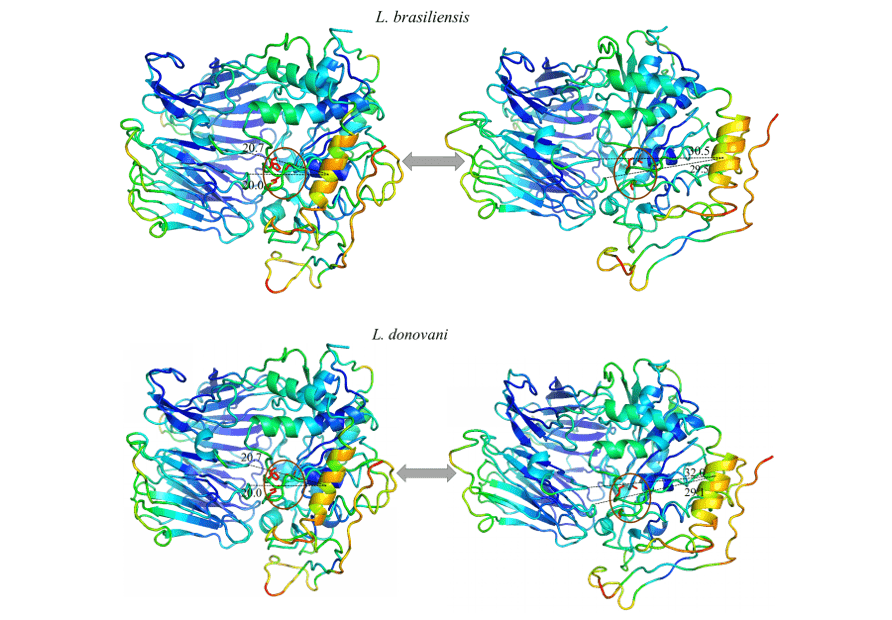
Рисунок 13: Результат анализа нормальными режимами в представлении по pymol программы, в изображении движения моделей проявляются, в их расслабленной форме (справа) по сравнению с движением большей амплитуды (слева). Также представлены наиболее жесткие регионы (Темно-синий), регионы с небольшим движением (Light Blue), промежуточные области (зеленый), регионы с хорошим потенциалом движения (оранжевый) и чрезвычайно податливые регионы (красный). (Часть 2/2)
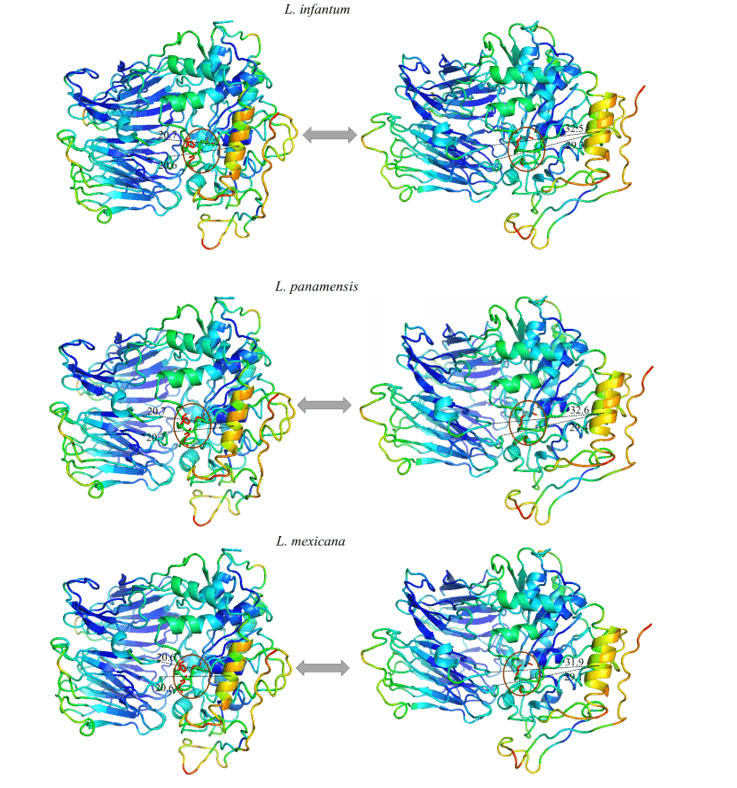
В связи с этим, нормальные исследования одобряют возможный механизм OPBs еще не описаны для Leishmania spp видов. до настоящего исследования.
ЗАКЛЮЧЕНИЕ
В этом исследовании были получены трехмерные модели опбного фермента L.brasiliensis, L. donovani, L. infantum, L. mexicana и L. panamensis. Проверка моделей предоставила надежные результаты для всех полученных трехмерных моделей. При характеристике фермента поверхностная электростатическая потенциальная карта показала, что большинство остатков представляли отрицательный заряд. При характеристике региона вокруг каталитическая триада она продемонстрировала сходство между объемом, площадью и соответствием между положительными и отрицательными остатками. Таким образом, удалось проверить, что результаты анализа в нормальных режимах предполагали выразительное движение в одной из конкретных супор, происходят на линейном расстоянии от центра к периферии, тем самым обнажая каталитическую триаду. Описание этих движений, выполняемых этим ферментом, имеет большое значение для понимания его функционирования.
Наконец, результаты настоящего исследования могут добавить знаний в научное сообщество, в результате чего разъяснения и новые вопросы, связанные с этой темой, служа основой для возможных исследований в области здравоохранения.
ССЫЛКИ
A. Benner S, Cannarozzi G, Gerloff D, Turcotte M, Chelvanayagam G. Bona Fide Predictions of Protein Secondary Structure Using Transparent Analyses of Multiple Sequence Alignments. Chem Rev. 1997;97(8):2725-2844. doi:10.1021/cr940469a.
Alva, V., Nam, S. Z., Söding, J., & Lupas, A. N. (2016). The MPI bioinformatics Toolkit as an integrative platform for advanced protein sequence and structure analysis. Nucleic Acids Research, 44(W1), W410–W415. doi.org/10.1093/nar/gkw348.
Alvarenga DG, Escalda PMF, da Costa ASV, Monreal MTFD. Leishmaniose visceral: Estudo retrospectivo de fatores associados à letalidade. Rev Soc Bras Med Trop. 2010;43(2):194-197.
Altschul SF, Madden TL, Schäffer AA, et al. Gapped BLAST and PSI-BLAST: a new generation of protein database search programs. Nucleic Acids Res. 1997;25(17):3389‐3402. doi:10.1093/nar/25.17.3389.
Andersson CD, Chen BY, Linusson A. Mapping of ligand-binding cavities in proteins [published correction appears in Proteins. 2011 Apr;79(4):1363]. Proteins. 2010;78(6):1408–1422. doi:10.1002/prot.22655.
Bailey F, Mondragon-Shem K, Hotez P, et al. A new perspective on cutaneous leishmaniasis-Implications for global prevalence and burden of disease estimates. PLoS Negl Trop Dis. 2017;11(8):e0005739. Published 2017 Aug 10. doi:10.1371/journal.pntd.0005739.
Carmo RF, Luz ZMP da, Bevilacqua PD. Percepções da população e de profissionais de saúde sobre a leishmaniose visceral. Cien Saude Colet. 2016;21(2):621-628. doi:10.1590/1413-81232015212.10422015.
Chothia C, Lesk AM. The relation between the divergence of sequence and structure in proteins. EMBO J. 1986;5(4):823‐826.
Derewenda ZS, Derewenda U, Kobos PM. (His)Cε-H···O=C< Hydrogen Bond in the Active Sites of Serine Hydrolases. J Mol Biol. 1994;241(1):83-93. doi:10.1006/JMBI.1994.1475.
Dolinsky TJ, Nielsen JE, McCammon JA, Baker NA. PDB2PQR: an automated pipeline for the setup of Poisson-Boltzmann electrostatics calculations. Nucleic Acids Res. 2004;32(Web Server issue):W665–W667. doi:10.1093/nar/gkh381.
Eisenberg, D., Lüthy, R., & Bowie, J. U. (1997). [20]VERIFY3D: Assessment of protein models with three-dimensional profiles. Methods in Enzymology, 277, 396–404. https://doi.org/10.1016/S0076-6879(97)77022-8.
Eyal E, Lum G, Bahar I. The anisotropic network model web server at 2015 (ANM 2.0). Bioinformatics. 2015;31(9):1487–1489. doi:10.1093/bioinformatics/btu847.
Ghorbani Masoud, Farhoudi Ramin. Leishmaniasis in humans: drug or vaccine therapy? Drug Des Devel Ther. 2018;12:25-40. doi:10.2147/DDDT.S146521.
Hedstrom L. Serine Protease Mechanism and Specificity. Chem Rev. 2002;102(12):4501-4524. doi:10.1021/cr000033x.
Katsila T, Spyroulias GA, Patrinos GP, Matsoukas MT. Computational approaches in target identification and drug discovery. Comput Struct Biotechnol J. 2016;14:177–184. Published 2016 May 7. doi:10.1016/j.csbj.2016.04.004.
Kumar S, Tamura K, Nei M. MEGA3: Integrated software for molecular evolutionary genetics analysis and sequence alignment. Brief Bioinform. 2004;5(2):150-163.
Macedo-Silva RM, dos Santos C de LP, Diniz VA, De Carvalho JJ, Guerra C, Côrte-Real S. Peripheral blood fibrocytes: New information to explain the dynamics of Leishmania infection. Mem Inst Oswaldo Cruz. 2014;109(1):61-69. doi:10.1590/0074-0276130247
Machado P de A, Carneiro MPD, Sousa-Batista A de J, et al. Leishmanicidal therapy targeted to parasite proteases. Life Sci. 2019;219:163-181. doi:10.1016/J.LFS.2019.01.015.
Morris, A. L., MacArthur, M. W., Hutchinson, E. G., & Thornton, J. M. (1992). Stereochemical quality of protein structure coordinates. Proteins: Structure, Function, and Bioinformatics, 12(4), 345–364. https://doi.org/10.1002/prot.340120407.
Ovchinnikova M V., Mikhailova AG, Karlinsky DM, Gorlenko VA, Rumsh LD. Reversible cyclic thermal inactivation of oligopeptidase B from Serratia proteamaculans. Acta Naturae. 2018;10(2):65-70.
Ramachandran, G. N., Ramakrishnan, C., & Sasisekharan, V. (1963). Stereochemistry of polypeptide chain configurations. Journal of Molecular Biology, 7(1), 95–99. https://doi.org/10.1016/S0022-2836(63)80023-6.
Santos Filho, O. A., & Alencastro, R. B. de. (2003). Modelagem de proteínas por homologia. Química Nova, 26(2), 253–259. https://doi.org/10.1590/S0100-40422003000200019
Sievers F, Wilm A, Dineen D, et al. Fast, scalable generation of high-quality protein multiple sequence alignments using Clustal Omega. Mol Syst Biol. 2011;7:539. Published 2011 Oct 11. doi:10.1038/msb.2011.75.
SODERO ACR, DOS SANTOS ACGO, MELLO JFRE, et al. Oligopeptidase B and B2: comparative modelling and virtual screening as searching tools for new antileishmanial compounds. Parasitology. 2017;144(4):536-545. doi:10.1017/s0031182016002237.
Swenerton RK, Zhang S, Sajid M, et al. The oligopeptidase B of Leishmania regulates parasite enolase and immune evasion. J Biol Chem. 2011;286(1):429-440. doi:10.1074/jbc.M110.138313.
Volkamer, A., Kuhn, D., Rippmann, F., & Rarey, M. (2012). Dogsitescorer: A web server for automatic binding site prediction, analysis and druggability assessment. Bioinformatics, 28(15), 2074–2075. https://doi.org/10.1093/bioinformatics/bts310.
Wang Q, Arighi CN, King BL, et al. Community annotation and bioinformatics workforce development in concert–Little Skate Genome Annotation Workshops and Jamborees. Database (Oxford). 2012;2012:bar064. Published 2012 Mar 20. doi:10.1093/database/bar064
Webb B, Sali A. Comparative Protein Structure Modeling Using MODELLER. Curr Protoc Bioinformatics. 2016;54:5.6.1–5.6.37. Published 2016 Jun 20. doi:10.1002/cpbi.3.
Wiederstein, M., & Sippl, M. J. (2007). ProSA-web: Interactive web service for the recognition of errors in three-dimensional structures of proteins. Nucleic Acids Research, 35(SUPPL.2), 407–410. https://doi.org/10.1093/nar/gkm290.
WHO. Integrating Neglected Tropical Diseases into Global Health and Development: Fourth WHO Report on Neglected Tropical Diseases.; 2017. http://apps.who.int/iris/bitstream/10665/255011/1/9789241565448-eng.pdf?ua=1.
WHO. (2019). Leishmanioses – Informe Epidemiológico das Américas No 7 – Março, 2019. Retrieved from http://iris.paho.org/xmlui/bitstream/handle/123456789/50505/ 2019-cde-leish-informe-epi-das-americas.pdf?sequence=2&isAllowed=y.
ПРИЛОЖЕНИЕ – ЦИФРЫ И ТАБЛИЦЫ НА АНГЛИЙСКОМ ЯЗЫКЕ
Схема 1: Упрощенная схема материальных шагов и методов.
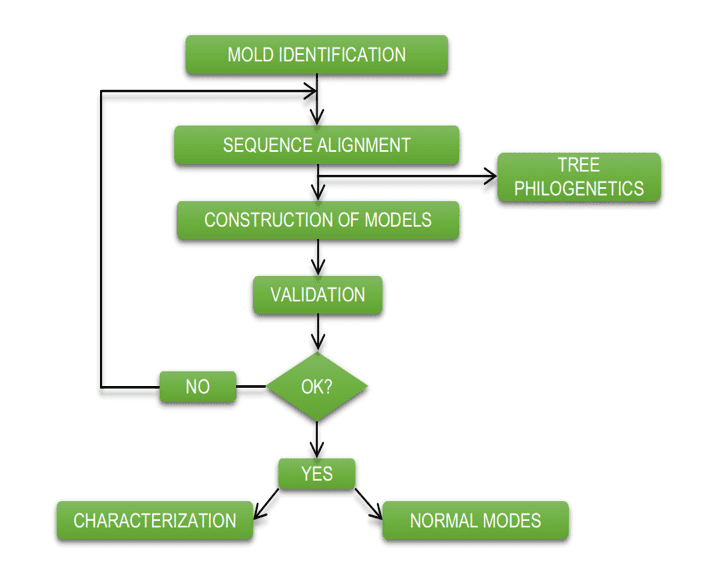
Таблица 1: Процент идентичности между моделями олигопептии B видов лейшмании и их соответствующей плесени.
| Mold protein (code PDB) | Models OPB
(código uniprot) |
Identity (%) | Gaps (%) |
| OPB
L. major (code PDB 2XE4) |
L.brasiliensis
(A4H5Q8) |
86 | 0 |
| L. donovani
(C9EF60) |
96 | 0 | |
| L. infantum
(A4HTZ8) |
96 | 0 | |
| L. Mexicana
(E9AMS8) |
90 | 0 | |
| L. panamensis
(A0A088RJA7) |
86 | 0 |
Fonte: Autoral.
Рисунок 6: Результаты рамачандранских графиков, полученных программой PROCHECK, структуры генерируемых моделей ОПБ и плесень.
| Structures | % waste in the regions | ||||
| Favorable | Allowed | Unfavorable | |||
| OLIGOPEPTIDASE B | L. major (A)
(PDB 2XE4) |
90,2 | 9,5 | 0,3 | |
| L.brasilienses (B) | 92,2 | 7,7 | 0,2 | ||
| L. donovani (C) | 91,9 | 8,0 | 0,2 | ||
| L. infantum (D) | 92,3 | 7,3 | 0,3 | ||
| L. Mexicana (E) | 91,2 | 8,3 | 0,5 | ||
| L. panamensis (F) | 91,4 | 8,3 | 0,3 | ||
Источник: Подготовлено автором на основе результатов procheck.
Рисунок 7: Результаты оценки, рассчитанные на сервере ProSA-web структур формы (для сравнения). (A) L .major (molde) e modelos: (B) L. brasilienses (C) L. donovani (D) L. infantum (E) L. mexicana (F) L. panamensis. Область в темно-синем цвете указывает на счет белков, полученных ЯМР, и в светло-голубом цвете белков, полученных рентгеновской дифракцией
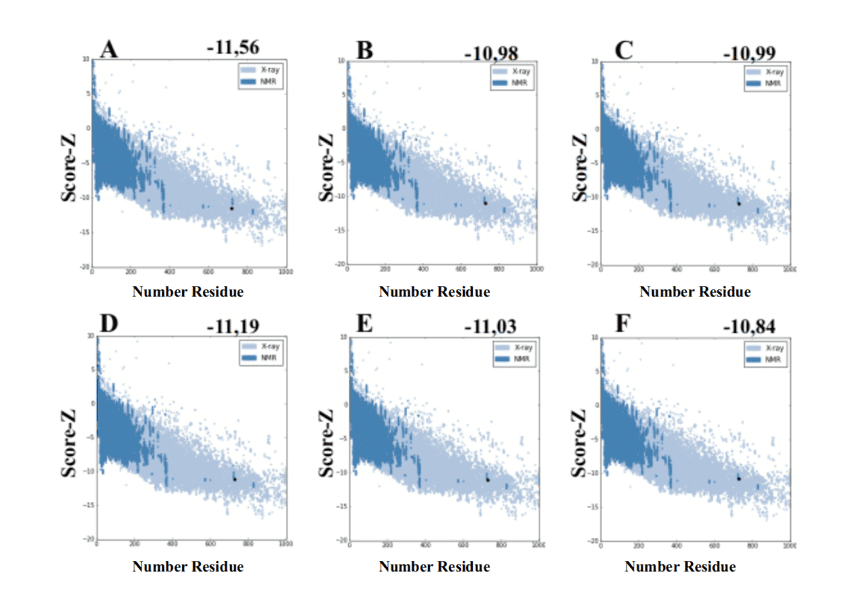
Таблица 2: Результаты проверки 3D, показывающие процент остатков с баллом 0,2.
| Structures | % residue with score > 0,2 | |
| OLIGOPEPTIDASE B | L.major
(PDB 2XE4) |
93,20 |
| L.brasilienses | 95,62 | |
| L.donovani | 97,12 | |
| L.infantum | 94,93 | |
| L.mexicana | 95,62 | |
| L.panamensis | 94,93 |
Источник: Автор.
Таблица 3: Сравнение вторичных структур, предсказанных psipred и которые найдены через Pymol.
| Models | α-Hélix | Sheet β | PSIPRED
α-Hélix |
PSIPRED
Sheet β |
| L.brasiliensis | 15 | 38 | 11 | 36 |
| L. donovani | 16 | 38 | 11 | 36 |
| L. infantum | 16 | 38 | 11 | 36 |
| L. mexicana | 15 | 38 | 10 | 36 |
| L. panamensis | 15 | 38 | 11 | 36 |
Источник: Автор.
Таблица 4: RMSDs OPBs, генерируемые Модельером, имеющие с ориентацией альфа-углероды формы OPB L. major.
| Mold | Models | RMSD (Å) |
| L. major
(2XE4) |
L.brasiliensis | 0,15 |
| L. donovani | 0,15 | |
| L. infantum | 0,16 | |
| L. mexicana | 0,19 | |
| L. panamensis | 0,14 |
Источник: Автор.
Таблица 5: Значения, относящиеся к возможным регионам соединения OPBs (полученные сервером).
| Structures | DogSiteScoore | |||
| Volume | Area | Drug Score | ||
| OP OLIGOPEPTIDASE B | L. major
(PDB 2XE4) |
1690,62 | 1818,41 | 0,80 |
| L.brasiliensis | 1527,84 | 1766,63 | 0,80 | |
| L. donovani | 1074,57 | 1428,55 | 0,79 | |
| L. infantum | 1309,97 | 1572,19 | 0,80 | |
| L. mexicana | 800,92 | 799,38 | 0,85 | |
| L. panamensis | 971,96 | 1083,40 | 0,81 | |
Источник: Автор.
[1] Биомедицинская и степень магистра в области медицинской биохимии.
[2] Магистр фармацевтических и фармацевтических наук от UFRJ.
[3] Кандидат химических наук, магистр органической химии и промышленной фармацевтики.
Отправлено: май 2020 года.
Утверждено: май 2020 года.