ARTIGO DE REVISÃO
JÚNIOR, Adriano Menino de Macedo [1]
JÚNIOR, Adriano Menino de Macedo. Cinética e dinâmica enzimática com ênfase no distúrbio a intolerância à lactose. Revista Científica Multidisciplinar Núcleo do Conhecimento. Ano 03, Ed. 10, Vol. 07, pp. 05-16 Outubro de 2018. ISSN:2448-0959
RESUMO
Este trabalho objetiva discutir os distúrbios orgânicos causados pela intolerância à lactose, a partir de uma pesquisa bibliográfica, apontando as suas causas e sintomas, bem como as formas de diagnóstico e os tratamentos existentes. Metodologicamente, promoveu-se uma revisão de literatura. Ao longo de nossa investigação, constatamos que, por diversos fatores, a má absorção da lactose acomete boa parte da população mundial, provocando determinados indícios que variam de acordo com a quantidade ingerida. Por fim, algumas alternativas foram apontadas, com o intuito de amenizar o problema da intolerância
Palavras-chave: Farmácia, Intolerância, Lactose, Diagnóstico, Tratamento.
INTRODUÇÃO
Consoante destacam Harvey e Ferrier (2012), quase todas as reações do organismo são mediadas por enzimas, que funcionam como proteínas catalisadoras aumentando a velocidade das reações sem sofrerem alterações no processo global.
As enzimas como todos os catalisadores, aumentam a velocidade das reações. Elas não alteram a constante de equilíbrio ou variação de energia livre. A velocidade da reação depende da energia livre de ativação (energia de ativação) (ΔG°‡), a quantidade de energia que e requerida para iniciar a reação. A energia de ativação para uma reação não-catalisada é maior do que a de uma reação catalisada: em outras palavras uma reação não catalisada requer mais energia para ser iniciada, e é por que a sua velocidade e menor do que a reação catalisada. (CAMPBELL, 2000, p.158).
As enzimas também possuem uma estrutura primária, secundária, terciária e quaternária de modo que, se no processo a enzima for dissociada de sua subunidade, a catálise será perdida e se por outro fator a enzima for degradada os seus aminoácidos são destruídos. Alguns tipos de enzimas necessitam de cofator que são componentes químicos denominados íons inorgânicos como Fe2+, Mg2+, Mn2+ ou Zn2+, ou ainda de moléculas orgânicas derivadas geralmente das vitaminas, denominadas de coenzima, para terem sua ação enzimática. As enzimas possuem em sua nomenclatura a terminação “ase”, no nome de cada substrato específico, que pode ser colocada posterior à palavra que descreve a presente atividade, como no caso da uréase que catalisa a hidrólise da ureia e a DNA-polimerase que catalisa a polimerização de nucleotídeos para formar o DNA.
As enzimas funcionam de modo específico e sem sua ausência as reações não catalisadas são lentas. Assim, devido ao ambiente estável das células com seu interior de pH neutro, temperatura incompatível com a enzima e ambiente aquoso, as reações não ocorrerão de forma rápida, dificultando a digestão dos alimentos, envio de impulsos nervosos e contração muscular. Campbell (2000) também aborda em sua obra que para as moléculas reagirem, deve existir energia suficiente para superar a barreira energética do estado de transição, no qual os reagentes e produtos ficam separados pela energia livre de ativação. Quanto maior for a energia de ativação mais lenta a reação química será. Quando uma determinada enzima catalisa uma reação química o substrato (S) vai se ligar por interações não-covalentes ao sítio ativo da enzima (E), formando um complexo enzima–substrato (ES), que vai sofrer reação modificando sua estrutura, dando origem ao produto (P) que se desprende da enzima, repetindo novamente o procedimento em outros substratos já que a enzima não sofre nenhum tipo de alteração, conforme demonstram Michael & David (2012) em gráfico abaixo:
Figura 01 – Demonstração da inalteração enzimática
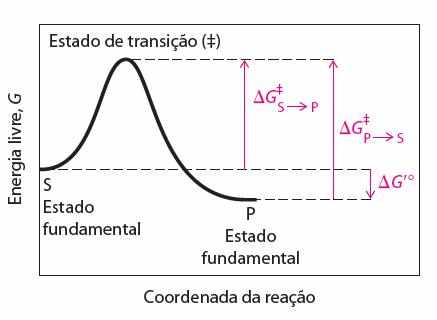
O gráfico abaixo mostra, transcrito de Michael & David (2012), como o substrato é convertido em produto com auxílio da enzima, veja que o substrato não precisa superar a barreira energética pois a enzima atua como catalisador acelerando a reação:
Figura 02 – Conversão do substrato em produto
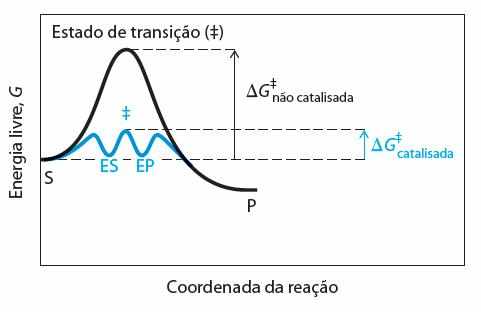
A metodologia da presente pesquisa caracteriza-se como revisão de literatura, a qual foi lastreada em artigos constantes na base eletrônica SciELO, assim como repositórios de universidades públicas e privadas, empregando-se as palavras chave: farmácia, intolerância, lactose, diagnóstico e tratamento. A pesquisa considerou artigos publicados entre os anos de 2008 e 2018, de forma que se realizou, inicialmente, a seleção, por vias das palavras chave. Em seguida, promoveu-se o fichamento do material selecionado e elegeram-se os artigos que faziam alusão ao tema. Os critérios de inclusão foram: artigos correlatos ao tema, publicados entre 2008 e 2018. Os critérios de exclusão foram: artigos concernentes ao tema, entretanto, fora da área farmacêutica.
DESENVOLVIMENTO
O aleitamento materno é o primeiro e único alimento do recém-nascido, proveniente das glândulas mamarias. Conforme observam Mathiúset al. (2016), ele é uma fonte poderosa de cálcio, proteínas vitaminas e sais minerais. A lactose presente no leite é formada pela união de dois monossacarídeos formando um dissacarídeo: glicose e galactose. Esse carboidrato compõe grande parte da lactose conhecido popularmente como o açúcar do leite. (BARBOSA; ANDREAZZI, 2011). Durante o período de lactação, a atividade enzimática da lactase é alta em todos os mamíferos lactantes, passando a diminuir após o desmame e, posteriormente, por outras causas abordadas no prosseguimento de nossa fala (MATHIÚS et al., 2016).
Após o indivíduo se alimentar com derivados do leite, começa a ocorrer a catálise da lactose. As moléculas estão com sua energia de ativação em alto pico de forma que a reação química vai demorar para acontecer. Na borda em escova do intestino delgado, existe a enzima lactase (cientificamente conhecida como β-D-galactosidase) dentre outras. Essa enzima apresenta especificidade ao fazer a hidrólise do substrato (S) em questão que é denominado lactose o qual vai se ligar ao sítio ativo da enzima (E), formando um complexo enzima–substrato (ES) que vai sofrer reação modificando sua estrutura, o que vai diminuir o tempo dessa reação dando origem ao produto (P) dois monossacarídeos que vão se desprender da enzima, repetindo novamente o procedimento em outros substratos já que a enzima não sofre nenhum tipo de alteração. Assim, esse açúcar já hidrolisado e absorvido pela parede intestinal é liberado na corrente sanguínea para servir de energia, conforme a equação química (FAEDO et al., 2013); (MICHAEL; DAVID, 2012):
Lactose ⇌ glicose + galactose
Esse mecanismo de ação e conhecido como “chave-fechadura” onde a lactose é a fechadura e lactase vai funcionar como chave ao dissociar o açúcar em duas moléculas: glicose e galactose para então ser absorvidas pelo mucosa intestinal tendo proveito de total beneficio energéticos (FERNANDES, 2018).
Embora muitas pessoas apresentem intolerância a esse açúcar ou ausência da enzima específica para fazer a hidrólise, a lactose é um importante dissacarídeo que tem que estar incluso na dieta, pois traz uma série de benefícios. Ele é a maior fonte de cálcio que existe, auxiliando na reposição do cristal de fosfato de cálcio dos ossos, também é fonte de proteínas que auxiliam na formação de músculos, e fonte de energia e vitaminas, com tudo de nada vale a lactose sem a lactase pra catalisar todos esses benefícios. (FERNANDES, 2018).
A intolerância à lactose, conhecida também como má absorção ou má digestão da lactose, é um condição em que o indivíduo se encontra impossibilitado de digerir o açúcar derivado do leite e de produtos lácteos. Com essa intolerância, o organismo não vai produzir a enzima ou vai produzir uma quantidade significativa pequena na qual não vai dar conta em assimilar toda a catálise do açúcar, que vai chegar sem qualquer tipo de alteração no intestino grosso o que vai desencadear uma série de sintomas e problemas na saúde do paciente. Entretanto, as pessoas com baixa produção de lactase pode tolerar 115 gramas de leite de uma só vez, o que equivale a até meia xícara, sem ter sintomas (PEREIRA et al., 2012).
A intolerância à lactose foi descrita por volta do ano de 1963. Estudos mostram uma estimativa que 75% da população mundial está afetada pela perda da enzima, causando-lhes sintomas que são facilmente diagnosticados e que serão descritos no desenvolvimento desse texto. Não se sabe o porquê nem o mecanismo pelo qual o organismo do mamífero para de produzir a enzima lactase, após o período de lactação (MATTAR; MAZO, 2010), mas sabe-se que a má digestão da lactose podem ocorrer de três formas: primaria, secundaria e congênita (MATHIÚS et al., 2016).
3. CAUSAS E SINTOMAS
A intolerância à lactose primaria é a que mais acomete a população adulta, ela se caracteriza pela alteração no gene das células que é responsável por codificar a lactase. Esse distúrbio é geneticamente programado a partir do desmame da criança e acontece de forma progressiva decorrente de fatores hereditários, iniciando desde a infância, passando pela fase adulta se estendendo até à velhice. Nessa transição, a intolerância à lactose pode ser parcial ou definitiva, desenvolvendo o quadro clínico da hipolactasia no organismo, em que os sintomas se apresentarão com severidade ou não dependendo da quantidade de lactose consumida. Em caso de um consumo excessivo, mais do que as enzimas possam catalisar, o paciente vai sentir inúmeros sintomas. (PEREIRA et al., 2012);
A intolerância à lactose secundaria é adquirida por uma alteração na borda de escova do intestino delgado, causadas por lesões na mucosa intestinal decorrentes de doenças como gastroenterite, desnutrição, doença de crohn, colite ulcerativa, doença celíaca, e também podem ocorrer após cirurgias no aparelho digestivo como gastrostomias, ileostomias, colostomias, ressecções intestinais e anastomoses de delgado, além de infecções virais como a do HIV – vírus da imunodeficiência adquirida – e infecções parasitarias causadas pelos microrganismos giardíase, teníase etc. Também acometem esse caso de intolerância à lactose, os medicamentos para tratamento do câncer. Nessa causa da intolerância à lactose quando os problemas são sanados a atividade enzimática da lactase é geralmente restabelecida (MATHIÚS et al., 2016; MATTAR; MAZO, 2010).
A terceira classificação da intolerância a lactose é a congênita conhecida também como herança autossômica. Nesse caso, os pais não transferem o gene da intolerância a lactose. Trata-se de uma causa mais rara, porém mais perigosa pois o recém-nascido já nasce sem qualquer tipo de atividade enzimática da lactase e os sintomas se manifestam após a primeira amamentação ou outros alimentos contendo lactose. Como consequência, seu organismo vai produzir fezes diarreicas e se não for diagnosticado imediatamente pode levar o bebê a óbito (PEREIRA et al., 2012).
De maneira geral, após o consumo do leite ou derivados, a lactose vai ser fermentada no intestino grosso, a lactose não absorvida nem utilizada vai ser encaminhada até o colón pela pressão osmótica, onde se iniciará o processo de fermentação pelos micro-organismo da microbiota dessa flora intestinal. Toda essa lactose acumulada no colón junto à fermentação da microbiota resulta nos sintomas como a produção de gases metano, dióxido de carbono e hidrogênio. Esses gases são responsáveis pela flatulência, distensão e dores abdominais, com a pressão osmótica aumentada o intestino grosso retém certa quantidade de água dando origem a diarreia, os ácidos graxos produzidos de cadeia curta como o acético, butírico e propiônico que são responsáveis pela redução do pH do meio, o que vai eliminar eletrólitos e fluidos nas fezes diarreicas. (SOARES et al., 2011).
4. DIAGNÓSTICO
O teste da intolerância à lactose, conhecido como o teste da curva glicêmica, consiste em fazer a coleta do sangue do paciente com jejum de 8 a 10 horas. Após essa etapa, o paciente faz a ingestão de uma quantidade de lactose pura entre 25g a 50g e uma nova coleta com três amostras será realizada para análise, sendo a primeira com 15 minutos, a segunda com 30 minutos e a terceira com 60 minutos, após a administração via oral. Nos pacientes que não possuem má absorção da lactose a glicose vai aumentar, o contrário acontecerá se o paciente for intolerante à lactose, as duas amostras permanecerá com os resultados semelhantes não havendo curva glicêmica (CUNHA et al., 2008).
O teste do hidrogênio expirado é um dos testes mais utilizados nos dias atuais. Para a realização desse exame é necessário o paciente seguir algumas regras, entre as quais se destacam: evitar o consumo de alimentos derivados do leite por um mês; não fumar, pois a nicotina aumenta o nível de hidrogênio interferindo do resultado do exame; não fazer uso de antibiótico com um mês de antecedência, uma vez que é necessário que a flora bacteriana esteja 100% para poder fazer a fermentação no dia do exame; e jejum de 10 a 12 horas. Para o diagnóstico através desse exame, observa-se que a lactose que se acumula no colón não é absorvida e quando fermentada produz hidrogênio. Em seguida, a metade desse gás vai ser eliminado pelos pulmões e expirado pelas narinas para ser capitado pelo exame. Esse aumento de hidrogênio sinaliza que houve má absorção da lactose, o resultado é positivo quando o paciente ingere lactose e expira o hidrogênio e o sopro é sempre feito intervalado após 60, 90, 120, 150 e 180 minutos. No teste, o aparelho registra 20 ppm (partes por milhão) com relação ao valor basal. (MATTAR; MAZO, 2010; CUNHA et al., 2008).
5. TRATAMENTO
Com o avanço das alternativas na área de alimentos, é possível conviver bem com a intolerância à lactose graças a produção cada vez mais em alta de uma série de mantimentos com a lactose já hidrolisada em até 80%, há ainda a substituição da lactose por derivados da soja e alimentos já fermentados, tudo isso para pacientes hipolactásicos (GASPARIN; TELES; ARAÚJO, 2008).
Uma das formas de conviver com a intolerância à lactose pode ocorrer através da mudança dos hábitos alimentares, quando o paciente entra numa nova dieta sem a presença desse elemento. Com tudo, vale ressaltar que, como destacamos neste artigo, a lactose é uma poderosa fonte de cálcio indispensável para o ser humano, repondo a massa óssea, além de ser fonte de energia vitaminas e minerais. Quando o indivíduo suspende totalmente o leite e derivados de suas refeições pode sofrer diminuição da densidade mineral óssea e ter mais facilmente fraturas. Optando por esse tratamento, deve-se fazer a reposição de cálcio, vitaminas e minerais através de suplementação (BARBOSA; ANDREAZZI, 2011).
Outra forma de não desenvolver os sintomas da hipolactasia é o indivíduo consumir até 12g de lactose por dia. Essa quantidade pode ser em uma única dose, caso o paciente tenha maior necessidade existe uma alternativa que é a de consumir a lactose com outros alimentos ao longo do dia, não causando nenhum sintoma. Contudo a manifestação de sintomas pode ocorrer se exceder 50g de lactose no mesmo dia. (SOARES et al., 2011).
Adotar um terapia de reposição enzimática da lactase exógena (+â-galactosidade) também é viável pois sanciona os problemas da hipolactasia primária obtida graças a leveduras e fungos. O tratamento é feito adicionado 5 gotas ou conforme orientação médica ou do nutricionista em qualquer alimento ou refeição que possua a lactose, reduzem os sintomas e valores do hidrogênio expirados. A lactase líquida também pode ser fundida a 15 gotas por litro de leite, que deve ser consumido só após 24 horas para garantir a hidrólise total da lactose (MATTAR; MAZO, 2010).
Figura 03 – Fórmula da Lactose inalterada
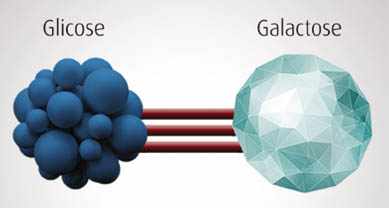
Figura 04 – Rompimento ocasionado pela lactase (catálise)

Uma outra alternativa é consumir alimentos lácteos já fermentados que possibilitam ao paciente com má absorção consumir produtos com baixo teor de lactose. Nesse grupo destacam-se os queijos duros, doce de leite com lactase, e leites com lactose reduzida. Os alimentos fermentados são recomendados porque os micro-organismo que fazem parte desse processo fazem a hidrólise de metade da lactose presente, como é o caso do iogurte e queijo coalho. O iogurte pode ser fermentado pelos micro-organismos lactobacillus delbrueckii subsp, Bulgaricus e streptococcus salivarius subsp, Thermophilus. Essas bactérias possuem alta atividade da lactase o que torna o iogurte mais tolerável para o paciente que apresenta o distúrbio. Na fabricação dos queijos duros a parte sólida se concentra e a grande parte da lactose fica no soro, porém o que ficar na parte sólida durante o processo será convertida em ácido lático. É possível encontrar leites fermentados com 90% de lactose reduzida conhecidos como lactose zero, leite deslactosado etc. Esse tipo de leite já vem hidrolisado em glicose e galactose pela lactase sem alterar seu valor nutricional para o organismo. (OLIVEIRA; SILVA, 2011; WENDLING; WESCHENFELDER, 2013).
O consumo de alimentos lácteos com probióticos também é uma alternativa bastante viável visto que a microbiota intestinal produz a β-D-galactosidase que vai fornecer auxilio na hidrólise da lactose. Nos alimentos com probióticos ativos a β-D-galactosidase enzima microbiana, sobrevive ativamente a passagem pelo ácido gástrico presente no estômago. Ela vai ser responsável pela hidrólise da lactose tornando-a em moléculas menores absorvível pelo intestino delgado (OLIVEIRA; SILVA, 2011). De acordo com as pesquisas de Maczucha et al., (2015), a reposição da enzima sintética lactase tem eficácia mesmo após 8 horas da ingestão de leite e derivados já apresenta melhoras nos sintomas do distúrbio.
CONSIDERAÇÕES FINAIS
Todas as formas de tratamento apresentadas não curam a má digestão da lactose, mas previne os desconfortos causados por esse distúrbio. Neste artigo mostramos que a lactose é rica em cálcio, porém de nada vale para o mamífero sem a presença da lactase pra catalisá-lo, o que provoca a não absorção de todo o cálcio presente no leite. Através deste estudo, enfatizamos as alternativas para amenizar e prevenir os sintomas desse mal, propondo, sobretudo, um tratamento por meio de dietas acompanhadas por um nutricionista e um profissional médico.
REFERÊNCIAS
BARBOSA C.R., ANDREAZZI M. A. Intolerância á lactose e suas consequências no metabolismo do cálcio. Revista saúde e pesquisa, v. 4, n.1, p. 81-86, jan./abr.2011.
CAMPBELL M. K. Bioquimica. 3. Ed. Porto alegre, PA: Artmed, 2000. P. 158-163
CUNHA M. E. T., SUGUIMOTO H. H., OLIVEIRA A. N., SIVIERI K., COSTA M. de R. Intolerância á lactose e alternativas tecnológicas. UNOPAR cientifica ciências biológicas e da saúde, Londrina, v. 10, n. 2, p. 83-88, out. 2008.
FAEDO R., BRIAO V.B., CASTOLDI S., GIRARDELLI L., MILANI A. Obtenção de leite com baixo teor de lactose por processos de separação por membranas associados á hidrolise enzimática. Revista cientifica – UFP, v.3, n. 1, p. 44-54, 2011.
FERNANDES T. F. intolerância a lactose. Revista brasileira de medicina, v. 72, n.6, p. 267-270, 2018
GASPARIN F.S.R., TELES J.M., ARAUJO S.C. Alergia á proteína do leite versus intolerância á lactose: As diferenças e semelhanças. . Revista saúde e pesquisa, v. 3, n.1, p. 107-114, jan./abr.2010.
HARVEY R. A., FERRIER D. R. bioquímica ilustrada. 5. Ed. Porto alegre, PA: Artmed, 2012. P. 54
MACZUCHA J. M., CESTONARO T., MEDEIROS C. O., CAVAGNARI M. A. V. Uso da enzima lactase sintética e consumo de leite e derivados entre intolerantes á lactose. revista brasileira de nutrição clinica, v.30 n. 1 p. 55-59, 2015.
MATHIÚS L.A., MONTANHOLI C.H.S., OLIVEIRA L.C.N., BERNARDES D.N.D., PIRES A., HERNANDEZ F.M. de O. Aspectos atuais da intolerância a lactose. Revista odontológica de Araçatuba, v.37, n.1, p 46-52, janeiro/abril, 2016.
MATTAR R., MAZO D.F.de C. Intolerância a lactose: mudança nos paradigmas com a biologia molecular. Revista da associação médica brasileira, São Paulo, v.56, n.2, p. 230-240, 2000.
NELSON D. L., COX M. M. Princípios de bioquímica de Lehninger. 6. Ed. Porto alegre, PA: Artmed, 2012. P. 190
OLIVEIRA C. P., SILVA A. J. Leite fermentado probiótico e suas implicações na saúde. Revista verde (Mossoró – RN – Brasil) v. 6, n. 3, p. 25-31, julho/setembro de 2011.
PEREIRA M. C. S., BRUMANO L. P., KAMIYAMA C.M., PEREIRA J. P. F., RODARTE P. M., PINTO M. A. de O. Lácteos com baixo teor de lactose: uma necessidade para portadores de má digestão da lactose e um nicho de mercado. Revista do instituto de laticínios cândido torres, v. 67 n.389, p. 57-65, 2012.
PIMENTEL T. C. probióticos e benefícios á saúde. Revista saúde e pesquisa, v. 4, n. 1, p. 101-107, jan./abr. 2011.
SANTOS R. B., BARBOSA L. P. J. de L., BARBOSA F. H. F. Probióticos: microrganismos funcionais. Revista do colegiado de ciências farmacêuticas, v. 1, n. 2, p. 26-38, 2011.
SOARES L. F., PERACINI L. C., FREITAS S., FERREIRA F. P., SANTOS L. F., MANHANI L. C., BENEDITE T. L., MANOCHIO-PINA M.G. Aspectos nutricionais e metabólicos da intolerância a lactose. Revista investigação medicina veterinária, v.15, n.4, p. 103-107,2016.
WENDLING L. K., WESCHENFELDER S. Probióticos e alimentos lácteos fermentados – uma revisão. Revista do instituto de laticínios cândido torres, juiz de fora, v. 68 n.395, p. 49-57, 2013.
[1] Acadêmico de Farmácia. Faculdade Natalense de Ensino e Cultura – FANEC.
Enviado: Outubro, 2018
Aprovado: Outubro, 2018


2 respostas
Parabéns Adriano Júnior! Mas um passo na sua grandiosa carreira. O céu é o limite para você.
Tinha certeza seu artigo seria publicado. Vc é muito competente. Parabéns!!!