ОБЗОРНАЯ СТАТЬЯ
SBRUZZI, Felipe Augusto [1], SILVA, Kelly Cristina da [2], TELLES, Sérgio Mazero [3], LIMA, Sirlene de Sousa [4], SANTANA, Claudinei Alves [5]
SBRUZZI, Felipe Augusto. Et al. Последующая форма для взрослых пациентов с лейкемией с использованием Imatinib. Revista Científica Multidisciplinar Núcleo do Conhecimento. 05-й год, Эд. 10, Вол. 02, стр. 92-112. Октябрь 2020 года. ISSN: 2448-0959, Ссылка доступа: https://www.nucleodoconhecimento.com.br/здравоохранение/использованием-imatinib
РЕЗЮМЕ
Введение: Хронический миелоидный лейкоз – это тип злокачественной неоплазии крови, который в основном характеризуется наличием филадельфийской хромосомы, которая является источником онкопротеина BCR-ABL. Он обладает повышенной активностью тирозинкиназы, что вызывает изменения во внутриклеточных сигнальных путях и способствует неконтролируемой пролиферации, клеточной дисфункции и отсутствию апоптоза. Несмотря на низкую заболеваемость, 1,5 случая на 100000 жителей, терапия иматинибом, мощным ингибитором BCR-ABL, изменила прогноз заболевания и увеличила продолжительность жизни пациентов, превратив смертельную болезнь в хроническое состояние. Цель: разработать форму для регулярного наблюдения за этими пациентами клиническим фармацевтом для обеспечения безопасной и эффективной фармакотерапии. Методология. Обзор литературы описательного типа был начат с проблемного вопроса: «Какие данные должен собирать клинический фармацевт во время оказания фармацевтической помощи для оценки и улучшения приверженности лечению у взрослых пациентов с хроническим миелоидным лейкозом, использующих иматиниб?» с последующим поиском статей в базах данных PubMed и на государственных сайтах. Впоследствии был проведен отбор работ и критический анализ для создания типовой формы, которая будет применяться в процессе выдачи. Результат и обсуждение. Было отобрано одиннадцать статей. Низкая приверженность пациента лечению хронического миелоидного лейкоза может привести к потенциально опасным для жизни последствиям. Следовательно, форма последующего наблюдения, которую должен применять клинический фармацевт при отпуске мезилата иматиниба, является жизнеспособной и недорогой стратегией для улучшения приверженности к фармакотерапии и содействия лучшему ответу на лечение. Заключение: систематизированная и стандартизованная документация клинического фармацевта о соблюдении режима лечения и побочных эффектах позволяет многопрофильной группе специалистов выполнять действия по постоянному совершенствованию с целью максимального повышения качества обслуживания пациентов, а также качества жизни.
Ключевые слова: лейкемия, фармакотерапевтические последующей деятельности, Imatinib.
ВВЕДЕНИЕ
Рак это имя, данное набор из более чем ста патологий, который имеет как общие характеристики инициации повреждения в конкретных генах ДНК и автономного и неупорядоченного роста клеток, которые приобретают способность вторгаться в соседние органы и ткани в результате функциональных расстройств (THAVAMANI et al., 2014).
Это аномальное пролиферации клеток известен как неоплазия и на практике это называется опухоль, и может быть классифицирована как злокачественные или доброкачественные (INSTITUTO NACIONAL DO CÂNCER, 2019).
Особой группой злокачественных новообразований являются лейкозы, которые характеризуются аномальным распространением клеток костного мозга предшественниками белой линии (JULIUSSON и HOUGH, 2016; LIU et al., 2019). Лейкемии могут быть классифицированы в зависимости от типа пораженных клеток, лимфоцитов или миелоидов, а также в зависимости от характеристики, острой или хронической (SACHDEVA et al., 2019).
Хронический миелоидный лейкоз (LMC) является одним из видов расстройства крови характеризуется увеличением числа лейкоцитов с левым отклонением, splenomegaly и наличие Филадельфии хромосомы (Ph), что является результатом взаимной транслокации между хромосомами (9;22) (q34;q11), что приводит к bcr-abl белка, с увеличением активности тирозина киназы (FLIS и CHOJNACKI, 2019).
Белок BCR-ABL присутствует у более чем 90% пациентов с LMC, а его гиперактивность стимулирует высвобождение эффекторов пролиферации клеток и ингибиторов апоптоза, а его активность отвечает за процесс образования рака в LMC (DI FELICE et al., 2018).
Открытие этого молекулярного изменения в дополнение к оптимизации диагностики LMC также обеспечило развитие терапии, направленной на это молекулярное изменение, и методы мониторинга минимального остаточного заболевания, обеспечивая улучшение лечения (BORTOLHEIRO И CHIATTONE, 2008).
LMC представляет 3 различных клинических фаз, которые возникают на протяжении всего заболевания, классифицируются как хроническая фаза, фаза трансформации и заключительная или взрывная фаза (HEFNER et al., 2016).
Традиционно лечение рака может проводиться с помощью хирургических, химиотерапевтических и лучевых методов, и комбинация является общей для получения лучшего клинического результата (INSTITUO NACIONAL DE CÂNCER, 2019).
Классическая химиотерапия направлена на разрушение клеток в быстрой репликации, которые предполагают от мутаций и / или важные изменения в ДНК, однако, нормальные клетки тканей, которые также имеют быструю репликацию разрушаются, обеспечивая многочисленные побочные эффекты для пациентов (BAGNYKOVA et al., 2010).
В раковых клетках, таких как LMC, изменяются внутриклеточные сигнальные пути, способствуя неконтролируемому пролиферации, клеточной дисфункции и отсутствию апоптоза (ANDERSON et al., 2015). На основе лучшего понимания этих процессов, начатых в 1980-х годах, начали изучаться препараты, называемые ингибиторами тирозинкиназы (CHABNER и ROBERTS, 2005).
В LMC из-за его характеристики патогномоника, онкоген BCR-ABL, стал идеальным кандидатом на “волшебную пулю”, задуманную Paul Ehrlich (Chabner and Roberts, 2005). Таким образом, “Целевая терапия” с ITQ стремится избирательно ингибировать дерегулированные сигнальные пути неопластических клеток пациентов с LMC, имея в качестве первого препарата используется иматиниб мезиат, мощный ингибитор BCR-ABL (DREWS, 2006; MOULIN et al., 2017).
В связи со старением и ростом населения, заболеваемость раком и смертность растет во всем мире (BRAY et al., 2018). В Бразилии, по оценкам Национального института рака (INCA), за каждый год двухгодичного периода 2018/2019 года диагностируется 600 000 новых случаев рака, среди этих лейкозов 9-е место среди мужчин с 5940 новыми случаями заболевания и 10-е место у женщин с 4860 новыми случаями (INSTITUTO NACIONAL DE CÂNCER, 2017).
На LMC приходится примерно 15% новых случаев лейкемии, при этом, по оценкам, риск заболевания составляет 1,5 случая на 100 000 человек (RYCHTER et al., 2017). Несмотря на низкую заболеваемость по сравнению с другими видами рака (легкие, простата, грудь), из-за иматиниб мезилат терапии, пациенты с LMC показали значительное улучшение пятилетней выживаемости и изменили прогноз заболевания (TRIVEDI et al., 2014; SAUSSELE et al., 2018; TAN et al., 2019; LATREMOUILLE-VIAU et al., 2017).
Для пациентов с диагнозом в середине 1970-х годов пятилетнюю выживаемость составила 22%, с 2008 по 2014 год – 69%, и в настоящее время большинство пациентов, получающих ITQ , имеют продолжительность жизни, совместимую с нормальными людьми, что делает LMC в настоящее время хроническим заболеванием, которое требует регулярного последующего лечения со стороны медицинской команды (SIEGEL et al. , 2019).
Лечение LMC требует комплексного действия междисциплинарной команды, и фармацевтический специалист незаменим в фармакотерапевтическом последующем лечении рака (ЛP) для обеспечения безопасной и эффективной фармакотерапии (SOUZA et al., 2018).
ЛP является персонализированной практикой, в которой клинический фармацевт несет ответственность за руководство, выявление, профилактику и решение проблем, связанных с наркотиками, охватывающих неблагоприятные последствия химиотерапии и используемой терапии, а также методы введения, соблюдение лечения и лекарственных взаимодействий (CALADO et al., 2019).
Учитывая сложность LMC, последующее лечение, выполняемое клиническим фармацевтическим специалистом, имеет важное значение для эффективности лечения.
ЗАДАЧА
Построить модель фармакотерапевтического наблюдения для взрослых пациентов с хроническим миелоидным лейкозом, положительным BCL-ABR, с использованием мезилата иматиниба.
МЕТОДОЛОГИЯ
Произведение является литературным обзором типа повествования. Так, из проблемного вопроса: «Какие данные должен собирать клинический фармацевт при оказании фармацевтической помощи для оценки и улучшения приверженности взрослых пациентов с хроническим миелоидным лейкозом с использованием Иматиниба?» был проведен поиск на платформе PubMed на основе стратегии PICO и были использованы дескрипторы: «leukemia, myelogenous, chronic, bcr-abl positive» AND «medication adherence». Были рассмотрены статьи последних 5 лет, и поиск проводился в базе данных с июня по декабрь 2019 года.
Были использованы следующие критерии включения: статьи, доступные в полном объеме в Интернете, на английском языке, население которых было взрослыми пациентами, и посвященные оценке приверженности к лечению при LMC. В качестве критериев исключения были приняты статьи, в которых оценивались исключительно лекарственные препараты, кроме мезилата иматиниба, без использования формы.
Кроме того, для того, чтобы составить форму были проведены консультации правительственных сайтов.
РЕЗУЛЬТАТЫ И ОБСУЖДЕНИЕ
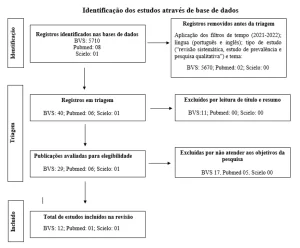
Поиск на веб-сайте Pubmed с дескрипторами привел к 52 статьям, и из них, на основе критериев включения и исключения, 11 были отобраны, чтобы составить обзор литературы в подготовке формы.
Эти статьи представлены в таблице 1 в порядке убывания даты публикации.
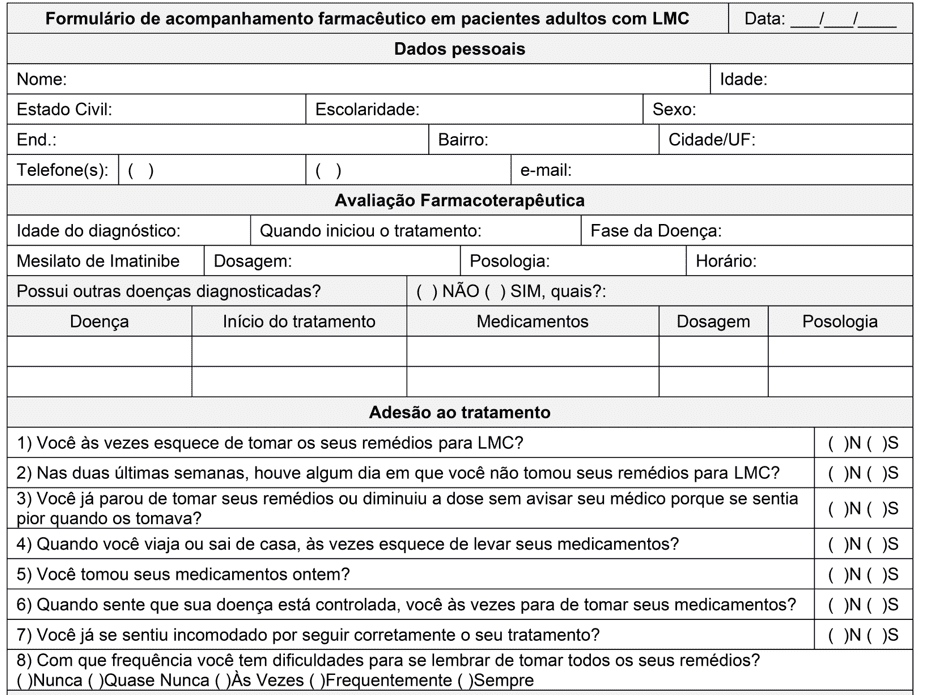
Согласно тому, что наблюдалось Moulin et al. включение клинического фармацевта во время лечения пациентов с LMC не только улучшило соблюдение лечения и уменьшило побочные реакции препарата (ПРП), о которых сообщили пациенты, но и улучшило цитогенетические параметры (MOULIN et al., 2017). В этом исследовании, после 4 месяцев наблюдения, авторы обнаружили более низкое выражение хромосомы Филадельфии в группе мониторинга по отношению к неконтролируемому контролю. В наблюдаемой группе полная цитогенетическая реакция увеличилась с 87,0% до 95,6% пациентов, в то время как в неконтролируемой группе она осталась на 61,5%. Таким образом, применение формы во время диспансеризации является эффективной стратегией сопровождения пациента и улучшения соблюдения лечения. Для достижения этой цели у взрослых пациентов с LMC (приложение I) была разработана фармацевтическая форма последующей деятельности.
Первая часть формы предназначена для сбора персональных данных пациентов для выявления и облегчения контакта с пациентом. Это потому, что некоторые из выбранных исследований показывают, что в некоторых популяциях ады могут быть благоприятствования некоторых социально-экономических характеристик, но исследования отличаются от которых более присутствуют в популяции. Tsai et al (2018) обнаружили в популяции исследования, что пожилые пациенты и женатые пациенты имеют лучшую приверженность. По данным Rychter et al (2017), наличие не менее 1 сопутствующих заболеваний и возраст старше 65 лет являются благоприятными характеристиками для адеринга. В отличие от этого, Unnikrishnan et al (2016) и Hefner et al (2016) не обнаружили корреляции между социально-экономическими характеристиками изучаемого населения и соблюдением лечения. Таким образом, отмечается, что корреляция между социально-экономическими данными и соблюдением варьируется в зависимости от изучаемого населения, не являясь прогностический параметр для присоединения пациента или несоблюдения.
Таблица 1.A – Статьи, отобранные на основе критериев включения и исключения, порядка убывания года публикации.
| Автор/Год | Название | Целей | Форма адецина | N(1) | Страны | Лекарства |
| MULU FENTIE et al., 2019 | Prevalence and determinants of non-adherence to Imatinib in the first 3-months treatment among newly diagnosed Ethiopian’s with chronic myeloid leukemia. | Оценить распространенность и причины несоблюдения Imatinib у пациентов с LMC(2), которые были недавно диагностированы в первые 3 месяца лечения. | MMAS-8(3) | 147 | Эфиопии | Imatinibe |
| TSAI et al., 2018 | Side effects and medication adherence of tyrosine kinase inhibitors for patients with chronic myeloid leukemia in Taiwan. | Уточните влияние неблагоприятного воздействия на соблюдение у тайваньских пациентов с LMC(2). | MMAS-8(3) | 58 | Тайвань | Imatinibe
Dasatinibe Nilotinibe |
| HEFNER et al., 2017 | Adherence and Coping Strategies in Outpatients With Chronic Myeloid Leukemia Receiving Oral Tyrosine Kinase Inhibitors. | Оценить соблюдение и стратегии выживания у пациентов вне больничной среды с помощью LMC(2). | BAASIS(4) | 35 | Германия | Ингибиторы тирозинкиназы |
(1)N – Количество участников; (2)LMC – Хронический миелоидный лейкоз;(3)MMAS-8= элементная шкала лечебного присоединения Morisky в 8 предметы;(4)BAASIS = Базельская шкала оценки соблюдения иммуносупрессивных препаратов; (5)MMAS-4 = элементная шкала терапевтического присоединения Morisky .
Таблица 1.B – Статьи, отобранные на основе критериев включения и исключения, порядка убывания года публикации.
| Автор/Год | Название | Целей | Форма адецина | N(1) | Страны | Лекарства |
| RYCHTER et al., 2017 | Treatment adherence in chronic myeloid leukaemia patients receiving tyrosine kinase inhibitors. | Оцените лечение взрослых польских пациентов с LMC(2) | Форма разработана для исследования. | 140 | Польша | Imatinibe
Dasatinibe Nilotinibe |
| GEISSLEr et al., 2017 | Factors influencing adherence in CML and ways to improvement: Results of a patient-driven survey of 2546 patients in 63 countries. | Оценить степень неоптимальных соблюдения и исследовать причины и модели соблюдения поведения пациентов с LMC(2) по всему миру. | MMAS-8(3) | 2546 | 63 страны | Imatinibe
Dasatinibe Nilotinibe Другое лечение |
| MULUNEH et al., 2016 | Patient perspectives on the barriers associated with medication adherence to oral chemotherapy. | Проанализируйте с помощью анкеты использование пероральной химиотерапии и определите возможности для улучшения в следующем. | Анкета адаптирована с 30 вопросами | 93 | США | Устная химиотерапия |
(1) N = количество участников; (2) ХМЛ = хронический миелоидный лейкоз; (3) MMAS-8 = позиционная шкала терапевтической приверженности Мориски; (4) BAASIS = Базельская шкала для оценки адгезии к иммунодепрессантам; (5) MMAS-4 = позиционная шкала терапевтической приверженности Мориски.
Таблица 1.C – Статьи, отобранные на основе критериев включения и исключения, порядка года публикации.
| Автор/Год | Название | Целей | Форма адецина | N(1) | Страны | Лекарства |
| МУЛИН et al.
Ноябрь/201614 |
The role of clinical pharmacists in treatment adherence: fast impact in suppression of chronic myeloid leukemia development and symptoms | Оценить роль клинического фармацевта в лечении пациентов с LMC(2), а также участие клинического фармацевта. | MMAS-4(5) | 23 | Бразилия | Ингибиторы тирозинкиназы |
| KEKÄLE et al., 2016 | Impact of tailored patient education on adherence of patients with chronic myeloid leukaemia to tyrosine kinase inhibitors: a randomized multicentre intervention study. | Оценить влияние персонализированного образования на пациента на присоединение к ITQ у пациентов с LMC(2). | MMAS-8(3) | 86 | Финляндия | Ингибиторы тирозинкиназы |
| UNNIKRISHNAN et al., 2016 | Comprehensive Evaluation of Adherence to Therapy, Its Associations, and Its Implications in Patients With Chronic Myeloid Leukemia Receiving Imatinib. | Оцените облесение и качество жизни пациентов с LMC(2), получающих Иматиниб в течение длительного периода времени. | MMAS-8(3) | 221 | Индия | Иматиниб |
(1) N = количество участников; (2) LMC = хронический миелоидный лейкоз; (3) MMAS-8 = 8-позиционная шкала терапевтической приверженности Morisky; (4) BAASIS = Базельская шкала для оценки адгезии к иммунодепрессантам; (5) MMAS-4 = 4-позиционная шкала терапевтической приверженности Morisky .
Таблица 1.D – Статьи, отобранные на основе критериев включения и исключения, порядок убывания года публикации.
| Автор/Год | Название | Целей | Форма адецина | N(1) | Страны | Лекарства |
| HOSOYA et al., 2015 | Failure mode and effects analysis of medication adherence in patients with chronic myeloid leukemia | Определите, как низкая приверженность происходит у пациентов с LMC(2) с помощью режима отказа и анализа эффекта. | Форма, разработанная для исследования | 54 | Япония | Imatinibe
Dasatinibe Nilotinibe |
| BRECCIA et al., 2015 | Adherence and future discontinuation of tyrosine kinase inhibitors in chronic phase chronic myeloid leukemia. A patient-based survey on 1133 patients. | Исследуйте приверженность и потенциальную выгоду в качестве жизни, удовлетворенность лечением и социальной жизнью у пациентов с LMC(2) | Форма разработана для исследования. | 1133 | Италия | Ингибиторы тирозинкиназы |
(1) N = количество участников; (2) LMC = хронический миелоидный лейкоз; (3) MMAS-8 = 8-позиционная шкала терапевтической приверженности Morisky ; (4) BAASIS = Базельская шкала для оценки адгезии к иммунодепрессантам; (5) MMAS-4 = 4-позиционная шкала терапевтической приверженности Morisky .
Одним из атрибутов клинического фармацевта является оценка фармакотерапии, так что пациент может безопасно использовать лекарства, в которые он нуждается, в соответствующих дозах, частоте и графиках, тем самым достигая терапевтических целей. Для этого были зарезервированы конкретные области для сбора возраста диагностики, начала лечения, фазы заболевания и параметров, связанных с иматиниб фармакотерапией.
В Бразилии Указ No 1219 от 4 ноября 2013 года устанавливает клинический протокол и терапевтические рекомендации по LMC у взрослых и является ссылкой на фармакотерапевтическую оценку этих пациентов. При этом рекомендуется использовать Иматиниб в качестве лечения первой линии и что такое фармакотерапия для хронические фазы (XФ) и трансформационных или ускоренных (ЛP) фаз (BRASIL, 2013).
В XФ рекомендуется разовая доза 400 мг/день в устной форме после крупнейшего приема пищи в день, и может обостриться в двух дозах 300 мг, один утром, а другой вечером, если после трех месяцев неадекватной реакции, потеря предыдущего ответа или прогрессирования заболевания. В отношении XФ рекомендуемая доза составляет 600 мг/день и может быть повышена до 800 мг/день при взрывных кризисах (BRASIL, 2013).
В дополнение к фундаментальной роли в лечении пациентов придерживаясь, клинический фармацевт должен также определить, оценить и вмешаться в лекарственных взаимодействий. Для оценки возможных лекарственных взаимодействий при применении иматиниба оценивается наличие других заболеваний и фармакотерапии этих заболеваний. В случае лекарственных взаимодействий, фармацевт должен быть в курсе препаратов, которые имеют печеночную метаболизацию, потому что иматиниб метаболизируется в этом маршруте ферментом CYP3A4 (GLIVEC, 2020). Поддержание концентрации крови более 300 мг чрезвычайно важно для успеха молекулярной/цитогенетического ответа и повышения выживаемости без прогрессирования заболевания (BRASIL, 2013). Поэтому индукторов этого фермента, таких как фтазон и Hypericum perforatum, которые могут снизить концентрацию плазмы иматиниба, следует избегать. Наряду с ингибиторами, такими как кетоконазол, кларитромицин, который может снизить обмен веществ и увеличить концентрацию иматиниба, приводит к увеличению ПРП (GLIVEC, 2020).
Вторая часть статьи направлена на оценку лечения пациента. Согласно определению Всемирной организации здравоохранения (ВОЗ), соблюдение хронических заболеваний является степенью, в которой поведение человека согласен с рекомендациями медицинского специалиста, и поведение может быть представлено приемом лекарств, соблюдением диеты или изменениями образа жизни (ВОЗ, 2003)
В выбранных статьях, следующие были измерены с помощью вопросников, которые оценивают это поведение через действия, имеющие отношение к лечению LMC , такие как: забывая одну или несколько доз, изменение дозы без уведомления предписывающего, не принимая лекарства, потому что он чувствует себя хорошо или потому, что он имеет неблагоприятную реакцию. Наиболее часто используемой моделью вопросника в статьях (шесть из одиннадцати отобранных) для оценки приверженности была шкала терапевтического присоединения Мориски, при этом 8 пунктов (MMAS-8) были наиболее частыми. Перед этим был выбран ММАС-8 для композиции сопроводительной формы.
Другим важным фактором для выбора было время, необходимое для подачи заявки, и возможность классификации пациента. MMAS-8 состоит из семи вопросов с вариантами «да» или «нет» и пункта (последний), который представляет собой 5-балльную шкалу likert (от 0 баллов за «всегда» до 1 балла за «никогда»). ). Каждый элемент измеряет конкретное поведение при использовании лекарств и не является определяющим фактором поведения при соблюдении режима лечения. Показатели MMAS могут варьироваться от 0 до 8, и пациенты классифицируются по трем уровням приверженности: высокая приверженность (8 баллов); средняя приверженность (от 6 до 7,75); и низкая приверженность (оценка <6).
Hefner et al. (2016) использовали модифицированный вопросник Базельской шкалы оценки адгезии к иммунодепрессантам (BAASIS). У пациента есть четыре вопроса «да» или «нет», и необходим только утвердительный ответ, чтобы считать пациента «несоблюдавшимся», что может вызвать у пациента отрицательный ответ по сравнению с классификацией MMAS-8 (высокий, средний и низкая приверженность). Еще одним фактором, рассматриваемым для выбора, было отсутствие в BAASIS вопросов, связанных с поведением «прекратить прием лекарства, когда он чувствует, что болезнь находится под контролем». Это связано с тем, что в некоторых исследованиях было обнаружено, что пациенты, как правило, более привержены в течение первого и второго года после постановки диагноза, вероятно, из-за уменьшения симптомов и того, что ПPП становится более очевидным, чем само заболевание (GEISSLER et al, 2017) .
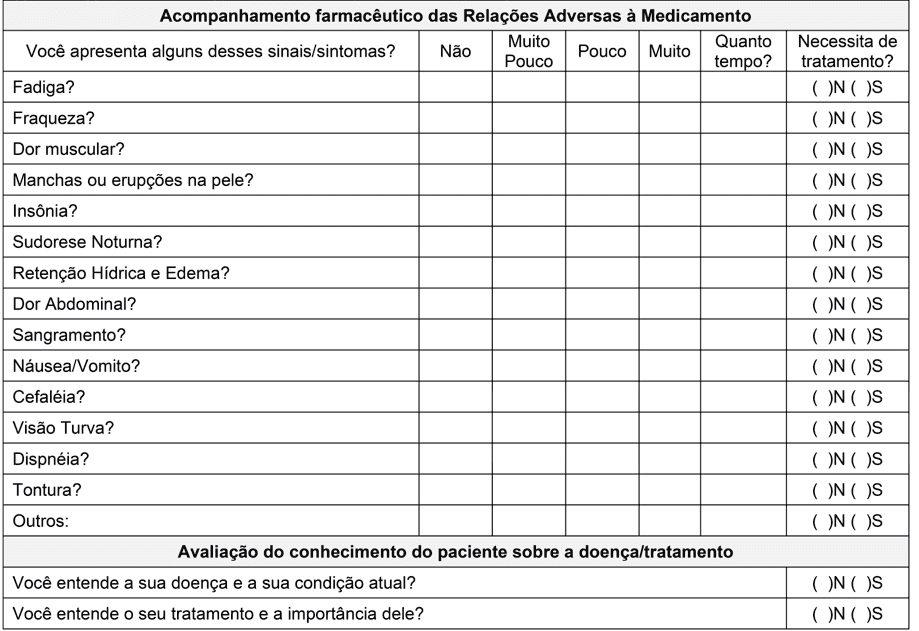
Для оценки ПPП и его последствий на объявление, третья часть была включена в форму с вопросами о наиболее распространенных реакций.
Согласно когортному исследованию, проведенному в Эфиопии Mulu Fentie et al (2019), было установлено, что основной причиной нелечения были побочные явления, связанные с Иматинибом, к препаратам, которые составили 68,8%. А основная жалоба около 68% была связана с желудочно-кишечными эффектами. Исследование также показывает, что пациенты, которые не испытывают каких-либо ПPП были в шесть раз больше шансов придерживаться лечения.
Как упоминалось выше, Moulin et al (2017) показали, что действия клинического фармацевта с помощью фармакологических последующих мер улучшили соблюдение и уменьшили побочные эффекты. В течение четырех месяцев последующей деятельности, исследователи сократили число не-приверженцев с восьми до нуля, используя 4-элемент Мориски терапевтической шкалы присоединения. Кроме того, число пациентов, жалующихся на ПPП , сократилось с 35% до 7%.
Хотя продолжительность исследований и число оцениваемых лиц были относительно небольшими, результаты являются многообещающими. Кроме того, необходимо более точное исследование по отношению к количеству людей и последующей деятельности в течение более длительных периодов времени.
В контр-матч, исследование, охватывающее 63 стран и 2546 пациентов обнаружили, что это не тот факт, что пациент испытывает ПPП, что влияет на соблюдение, а насколько хорошо управление из них осуществляется междисциплинарной команды (GEISSLER и др., 2017).
Учитывая эти результаты, мы обнаружили доказательства того, что лучший способ повысить приверженность к лечению – это избежать нежелательных явлений или даже, если возможно, избежать возможных нежелательных явлений в будущем для повышения приверженности. Это причины, по которым мы вставили в форму вопросы об основном ПPП, описанном для иматиниба мезилата, интенсивности и времени, в течение которого пациент испытывает их и ощущает потребность в лечении. Таким образом, мы надеемся выявить и избежать основных нежелательных эффектов, связанных с приемом лекарств, для повышения безопасности, соблюдения режима лечения и повышения качества жизни пациентов.
Хотя стратегия, выбранная для оценки и улучшения приверженности и сокращения ПPП пациентов является формой, Geissler et al (2017) обнаружили, что важным фактором, влияющим на соблюдение и может быть под влиянием медицинских работников, является информация о LMC пациента. В этом исследовании, пациенты, которые чувствовали себя лучше информированы о болезни были значительно более приверженцами. Таким образом, два вопроса были вставлены в нашу форму для оценки знаний пациента о болезни / лечения и, таким образом, с участием междисциплинарной группы, для планирования дополнительных стратегий. Тем не менее с этой информацией, как ожидается, интегрировать пациента более активно в лечении, подчеркивая информацию, а не только в инструкции, что она должна следовать.
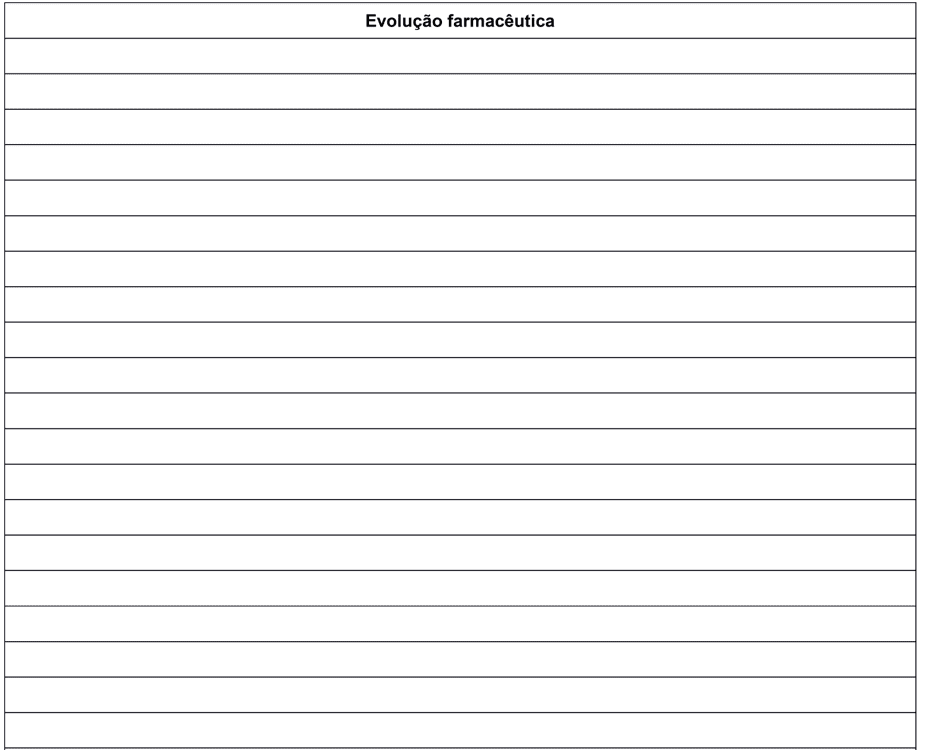
Во время подготовки формы не было возможности предвидеть какие-либо ситуации или ПPП, что пациенты могут сообщить. Тем не менее, задняя часть формы была использована для области “Фармацевтическая эволюция”, где они могут быть отмечены, например: субъективные данные, объективные данные, оценка и конкретное планирование для оцениваемого пациента.
Предложение о создании форм-модели для применения у пациентов с LMC направлено на улучшение реакции на лечение имитинибом мезиратом и качеством жизни. Таким образом, на сегодняшний день нет намерения включать результаты этой деятельности в исследовательский проект. Поэтому никаких условий разъяснения и согласия или какого-либо другого документа в соответствии с Постановлением No 510 от 7 апреля 2016 года Минздрава не было подготовлено. Эта резолюция предусматривает исследования, методологические процедуры которых включают использование данных, непосредственно полученных от участников, или идентифицируемой информации (BRASIL, 2016). Тем не менее, текст, который будет подписан пациентом или его представителем помещается на обратной стороне формы о том, что он / она знает, что предоставленные данные будут использоваться для фармакотерапевтического последующего лечения хронической миелоидной лейкемии.
Приложение I – Фармацевтическая форма последующего лечения у взрослых пациентов с LMC.
ЗАКЛЮЧЕНИЕ
Известно, что несколько факторов служат барьерами для нелечения фармакологического лечения, такие как: неблагоприятные события, распорядок дня лекарства, чувство себя хорошо без лечения, неадекватная информация о лекарстве. Однако, в частности, в хронической миелоидной лейкемии, не лечение Иматиниб Mesilate может привести к потенциальной опасной для жизни лечения, так как результат этого заболевания хорошо известны и документированы. Поэтому необходимо часто следовать клиническому фармацевту для выявления ранних факторов, которые могут способствовать негативному вкладу, способствуя планированию мероприятий в целях содействия лучшей приверженности и, следовательно, достижения терапевтических целей.
С этой целью жизнеспособной и недорогой стратегией является внедрение последующей формы, которая будет применяться фармацевтом во время диспансеризации. Таким образом, стандартизированная документация предоставляемой помощи послужит не только оптимизации фармакотерапии, но и повышению безопасности пациентов, способствуя развитию действий, направленных на развитие пациента, повышению эффективности общения между междисциплинарными бригадами и оказанию помощи в осуществлении непрерывных улучшений в целях максимального качества медицинской помощи, предоставляемой пациентам.
ССЫЛКИ
ANDERSON, Kristin R. et al. Medication adherence among adults prescribed imatinib, dasatinib, or nilotinib for the treatment of chronic myeloid leukemia. Journal of Oncology Pharmacy Practice, v. 21, n. 1, p. 19-25, 2015.
BAGNYUKOVA, Tetyana V. et al. Chemotherapy and signaling: How can targeted therapies supercharge cytotoxic agents?. Cancer biology & therapy, v. 10, n. 9, p. 839-853, 2010.
BORTOLHEIRO, Teresa C; CHIATTONE, Carlos S. Leucemia mielóide crônica: história natural e classificação. Revista Brasileira de Hematologia e Hemoterapia, v. 30, p. 3-7, 2008.
BRASIL. Ministério da Saúde (MS). Resolução nº 510, de 7 de abril de 2016. Disponível em: http://bvsms.saude.gov.br/bvs/saudelegis/cns/2016/res0510_07_04_2016.html. Acessado em: 23 de maio de 2020.
BRASIL. Ministério da Saúde (MS). Portaria nº 1.219, de 4 de novembro de 2013. Disponível em: http://bvsms.saude.gov.br/bvs/saudelegis/sas/2013/prt1219_04_11_2013.html. Acessado em: 23 de maio de 2020.
BRAY, Freddie et al. Global cancer statistics 2018: GLOBOCAN estimates of incidence and mortality worldwide for 36 cancers in 185 countries. CA: a cancer journal for clinicians, v. 68, n. 6, p. 394-424, 2018.
BRECCIA, Massimo et al. Adherence and future discontinuation of tyrosine kinase inhibitors in chronic phase chronic myeloid leukemia. A patient-based survey on 1133 patients. Leukemia research, v. 39, n. 10, p. 1055-1059, 2015.
CALADO, Deysiane Santos; TAVARES, Diego de Hollanda Cavalcanti; BEZERRA, Grasiela Costa. O papel da atenção farmacêutica na redução das reações adversas associados ao tratamento de pacientes oncológicos. Revista Brasileira de Educação e Saúde, v. 9, n. 3, p. 94-99, 2019.
CHABNER BA, ROBERTS TG Jr. Timeline: chemotherapy and the war on cancer. Nat Rev Cancer, v. 5, p. 65-72, 2005.
DI FELICE, Enza et al. The impact of introducing tyrosine kinase inhibitors on chronic myeloid leukemia survival: a population-based study. BMC cancer, v. 18, n. 1, p. 1069, 2018.
DREWS, Jürgen. Case histories, magic bullets and the state of drug discovery. Nature Reviews Drug Discovery, v. 5, n. 8, p. 635-640, 2006.
FLIS, Sylwia; CHOJNACKI, Tomasz. Chronic myelogenous leukemia, a still unsolved problem: pitfalls and new therapeutic possibilities. Drug design, development and therapy, v. 13, p. 825, 2019.
GEISSLER, Jan et al. Factors influencing adherence in CML and ways to improvement: Results of a patient-driven survey of 2546 patients in 63 countries. Journal of Cancer Research and Clinical Oncology, v. 143, n. 7, p. 1167-1176, 2017.
HEFNER J, CSEF EJ, KUNZMANN V. Fear of progression in outpatients with chronic myeloid leukemia on oral tyrosine kinase inhibitors. In: Oncology Nursing Forum. Oncology Nursing Society, 2016. p. 190.
HOSOYA, Kazuhisa et al. Failure mode and effects analysis of medication adherence in patients with chronic myeloid leukemia. International journal of clinical oncology, v. 20, n. 6, p. 1203-1210, 2015.
Instituto Nacional de Câncer Jose Alencar Gomes da Silva. ABC do câncer: abordagens básicas para o controle do câncer, 5. ed. Rio de Janeiro: INCA, 2019.
Instituto Nacional de Câncer Jose Alencar Gomes da Silva. Estimativa 2018: incidência de câncer no Brasil. Rio de Janeiro, 2017. Disponível em: https://www.inca.gov.br/sites/ufu.sti.inca.local/files//media/document//estimativa-incidencia-de-cancer-no-brasil-2018.pdf. Acesso em: 08 out. 2019.
JULIUSSON, G.; HOUGH, R. Leukemia. Prog Tumor Res 2016; 43: 87–100. Google Scholar| Crossref| Medline.
KEKÄLE, Meri et al. Impact of tailored patient education on adherence of patients with chronic myeloid leukaemia to tyrosine kinase inhibitors: a randomized multicentre intervention study. Journal of advanced nursing, v. 72, n. 9, p. 2196-2206, 2016.
LATREMOUILLE-VIAU, Dominick et al. Health care resource utilization and costs in patients with chronic myeloid leukemia with better adherence to tyrosine kinase inhibitors and increased molecular monitoring frequency. Journal of Managed Care & Specialty Pharmacy, v. 23, n. 2, p. 214-224, 2017.
LIU, Tao; PENG, Xing-Chun; LI, Bin. The Metabolic Profiles in Hematological Malignancies. Indian Journal of Hematology and Blood Transfusion, p. 1-10, 2019.
MOULIN, Silmara Mendes Martins et al. The role of clinical pharmacists in treatment adherence: fast impact in suppression of chronic myeloid leukemia development and symptoms. Supportive Care in Cancer, v. 25, n. 3, p. 951-955, 2017.
MULU FENTIE, Atalay et al. Prevalence and determinants of non-adherence to Imatinib in the first 3-months treatment among newly diagnosed Ethiopian’s with chronic myeloid leukemia. PloS one, v. 14, n. 3, p. e0213557, 2019.
MULUNEH, Benyam et al. Patient perspectives on the barriers associated with medication adherence to oral chemotherapy. Journal of Oncology Pharmacy Practice, v. 24, n. 2, p. 98-109, 2018.
Novartis Biociências S.A. Bula do medicamento Glivec®. Disponível em: https://portal.novartis.com.br/UPLOAD/ImgConteudos/1821.pdf. Acessado em: 20 de agosto de 2020.
RYCHTER, Anna et al. Treatment adherence in chronic myeloid leukaemia patients receiving tyrosine kinase inhibitors. Medical Oncology, v. 34, n. 6, p. 104, 2017.
SACHDEVA, Ashwani et al. Association of leukemia and mitochondrial diseases—A review. Journal of family medicine and primary care, v. 8, n. 10, p. 3120, 2019.
SAUSSELE, Susanne et al. Defining therapy goals for major molecular remission in chronic myeloid leukemia: results of the randomized CML Study IV. Leukemia, v. 32, n. 5, p. 1222-1228, 2018.
SIEGEL, Rebecca L.; MILLER, Kimberly D.; JEMAL, Ahmedin. Cancer statistics, 2019. CA: a cancer journal for clinicians, v. 69, n. 1, p. 7-34, 2019.
SOUZA, Jessica de O. et al. Adherence to TKI in CML patients: more than reports. Supportive Care in Cancer, v. 26, n. 2, p. 325-326, 2018.
TAN, Bee Kim et al. Efficacy of a medication management service in improving adherence to tyrosine kinase inhibitors and clinical outcomes of patients with chronic myeloid leukaemia: a randomised controlled trial. Supportive Care in Cancer, p. 1-11, 2019.
THAVAMANI B. Samuel; MATHEW, Molly; DHANABAL, S. P. Anticancer activity of cissampelos pareira against dalton’s lymphoma ascites bearing mice. Pharmacognosy magazine, v. 10, n. 39, p. 200, 2014.
TRIVEDI, Digisha et al. Adherence and persistence among chronic myeloid leukemia patients during second-line tyrosine kinase inhibitor treatment. Journal of Managed Care Pharmacy, v. 20, n. 10, p. 1006-1015, 2014.
TSAI, Yu-Fen et al. Side effects and medication adherence of tyrosine kinase inhibitors for patients with chronic myeloid leukemia in Taiwan. Medicine, v. 97, n. 26, 2018.
UNNIKRISHNAN, Radhika et al. Comprehensive evaluation of adherence to therapy, its associations, and its implications in patients with chronic myeloid leukemia receiving imatinib. Clinical Lymphoma Myeloma and Leukemia, v. 16, n. 6, p. 366-371. e3, 2016.
WORLD HEALTH ORGANIZATION et al. Adherence to long-term therapies: evidence for action. World Health Organization, 2003.
[1] Фармацевт. Специалист по клинической и больничной фармации, Сенак. Специалист по многопрофильных онкологических заболеваниях (HIAE).
[2] Фармацевтической. Специалист по клинической и больничной фармации, Сенак.
[3] Фармацевт. Специалист по клинической и больничной фармации, Сенак.
[4] Фармацевтической. Специалист по клинической и больничной фармации, Сенак.
[5] Фармацевт. Магистр медицинских наук, FMUSP. Специалист по многопрофильной онкологии (HSL). Специалист в больничной аптеке (FOC).
Представлено: Август 2020.
Утверждено: октябрь 2020 года.