ARTIGO ORIGINAL
CARNEIRO, Bruna Almeida [1], MIGUES, Vitor Hugo [2]
CARNEIRO, Bruna Almeida. MIGUES, Vitor Hugo. Determinação de elementos traços em batons vermelhos comercializados em Salvador – BA. Revista Científica Multidisciplinar Núcleo do Conhecimento. Ano. 07, Ed. 01, Vol. 05, pp. 241-264. Janeiro de 2022. ISSN: 2448-0959, Link de acesso: https://www.nucleodoconhecimento.com.br/quimica/tracos-em-batons
RESUMO
O ato de colorir os lábios, principalmente por mulheres, é um evento histórico datado por volta de 5000 a.C. na antiga Mesopotâmia, local onde foi encontrado por historiadores o que se acredita que seja o primeiro registro de batom. Atualmente os batons são compostos de ceras, gorduras, óleos vegetais, ésteres, álcoois e pigmentos ou corantes, geralmente complexados com íons metálicos para incremento da coloração. Dentro desse contexto, a problemática deste artigo, buscou avaliar quais os elementos traços, potencialmente tóxicos, fazem parte da constituição dos batons vermelhos comercializados em Salvador, BA. O método utilizado foi baseado no estudo bibliográfico de artigos e revistas onde abordavam o conteúdo em estudo e, foi realizada a digestão ácida de batons vermelhos através da técnica de Espectrometria de Emissão Atômica com Fonte de Plasma (ICPOES). Embora a presença de metais em batons afete a saúde da população que o utilize, a Agência Nacional de Vigilância Sanitária (ANVISA) permite uma quantidade mínima existente neles. Nas amostras em estudo foram encontrados metais como Cádmio, Chumbo, Cromo, Cobalto e Manganês, mas todas dentro do limite permitido pela ANVISA. Os resultados refletem a presença dos principais metais tóxicos ao organismo. Todavia, estudos adicionais devem ser realizados, como coleta de material biológico para averiguar o fluxo desses elementos no organismo.
Palavras-chave: Batom, Coloração, Metais.
1. INTRODUÇÃO
O ato de colorir os lábios é um hábito muito comum entre mulheres desde a antiguidade até os dias atuais e para muitas é o complemento da sua beleza. Acredita-se que esse hábito de colorir os lábios iniciou-se por volta de 5000 a.C. na antiga Mesopotâmia quando historiadores encontraram o primeiro registro de algo que se acreditava que seria um batom (OLIVEIRA, 2003; RIBEIRO, 2010). Esses “batons” eram produzidos através do esmagamento de pedras semipreciosas para que se obtivessem a coloração desejada (RIBEIRO, 2010).
O segundo registro de batom aparece no Egito, onde a população egípcia utilizava o lodo e o Bromo para obter a coloração vermelho-púrpura e por conta do contato com esses produtos químicos muitos adquiriram doenças na qual passou a ser chamada de “Beijo da Morte” (RIBEIRO, 2010). Segundo (ANURAJ, 2006, p. 1 apud RIBEIRO, 2010): “Cleópatra utilizava besouros de carmim esmagados para obter a coloração vermelha nos lábios.”.
No século XVI o batom continua sendo bastante utilizado e ganhando bastante popularidade entre as mulheres graças à Rainha Elizabete I e as senhoras da sua corte, que usavam em seus lábios uma mistura de cera de abelha com mercúrio vermelho, onde considera ser um batom (MACEDO et al., 2014).
De acordo com Macedo et al. (2014):
No início do século passado, um perfumista francês, criou o que batizou de “baton serviteur” (bastão servidor), que consistia em uma massa de talco, óleo de amêndoas, essência de bergamota e limão, de cor vermelha que era vendido numa embalagem de papel de seda. Fórmula sólida do batom só teve início na década de 1930.
Atualmente, a composição de um batom é feita de pigmentos ou corantes sintéticos com a presença de ceras, gorduras, óleos vegetais, ésteres e álcoois (OLIVEIRA, 2003; MACEDO et al., 2014), além desses componentes passou-se a incorporar compostos para deixá-lo mais sofisticados (OLIVEIRA, 2003).
Devido à popularidade do uso de batons, consequente a isso o aumento do número de indústrias produtoras para que esse tipo de cosmético seja comercializado, é necessário que passe por testes de análise de ingredientes corretos como também testes sensoriais em diferentes tipos de pele e análise da presença ou ausência de metais na sua composição. No Brasil é a Agência Nacional
de Vigilância Sanitária (ANVISA) que regulamenta, fiscaliza e autoriza a comercialização deste tipo de cosmético (DIAS e RAU, 2013; INMETRO, 2017).
Apesar de toda a fiscalização exercida pela ANVISA, é comum que se encontre a presença de metais em batons e essa presença é ocasionada devido aos corantes/pigmentos que são utilizados para garantir a cor do produto, (MAEHATA, 2016).
De acordo com ATZ (2008) apud Maehata (2016):
Os corantes e pigmentos inorgânicos são os responsáveis pela coloração desejada, pela maleabilidade, pela fixação e durabilidade do cosmético labial. Os principais componentes desses pigmentos inorgânicos e corantes são elementos metálicos, que nem sempre apresentam a pureza adequada e acabam por incluir elementos metálicos indesejados no produto que foi utilizado.
Os metais mais comuns encontrados em batons são: chumbo, cádmio, cromo, arsênio, mercúrio, alumínio, manganês e titânio, ambos proibidos na composição química do batom e em contato com o organismo humano, esses metais, podem provocar diversas patologias, podendo também predispor ao surgimento de câncer e neurotoxicidades (DIAS e RAU, 2013).
E segundo a ANVISA (BRASIL, 1977) “Esta substância poderá aparecer apenas como contaminante dos corantes e pigmentos utilizados em maquiagens, sendo que o limite máximo permitido é 20 (vinte) ppm (partes por milhão)”. Porém, essa legislação passou por mudanças e os limites autorizados mudaram e com isso foi criada uma Resolução da Diretoria Colegiada (RDC) de nº 44 de 2012 que traz a lista de substâncias e corantes permitidas para produtos de higiene pessoal, cosméticos e perfumes, ela estabelece que os corantes não possam apresentar impurezas em um valor maior do que 3 ppm de arsênio, 20 ppm de chumbo e 100 ppm de outros metais pesados (BRASIL, 2012).
O contato do batom com o organismo humano acontece por meio do contato direto do mesmo com os lábios e seu uso provoca um possível impacto na saúde, devido à absorção do produto aplicado sob a mucosa bucal e exposição aos efeitos de ingestão, dos possíveis metais pesados que estejam na sua composição (HARRIS, 2013; LIU et al., 2013; LORETZ et al., 2004).
Com o crescimento da indústria da beleza, atualmente encontramos no mercado consumidor batons de diferentes cores, formas e texturas. As diferentes cores são dadas através dos pigmentos inorgânicos e corantes adicionados na composição (MAEHATA, 2016). Já as formas dos batons são dadas de acordo com os excipientes utilizados, o batom em formato bala apresenta como base de sua composição ceras que essas contribuem para um formato mais compacto da formulação, quando refrigeradas em moldes para a obtenção do formato bala, e os batons podem ser acondicionados em embalagens giratórias. Já os batons na forma líquida também apresentam ceras na sua composição, porém os mesmos não passam pelo processo de resfriamento e modelagem, e sim são acondicionados em recipientes com pincel e este é utilizado para auxiliar o uso do batom líquido (OLIVEIRA, 2003).
Entre os tipos de textura encontrados, temos a textura matte e a textura cremosa. O batom de textura “matte”, que em português quer dizer fosco e é esse o efeito que batons com essa textura proporcionam para o mercado consumidor, um batom que após a secagem no lábio fica fosco, sem brilho. Já o batom de textura cremosa é emoliente e promove hidratação e brilho após o uso (PONTES, 2020).
A textura está intimamente relacionada com a matéria prima utilizada na composição do batom (OLIVEIRA, 2003). A diferença na composição entre os dois tipos de textura citados é que o batom cremoso apresenta uma concentração superior de óleo na sua composição, por isso a emoliência. Já os batons mattes apresentam uma baixa quantidade de óleo, em contrapartida apresentam mais pigmentos, onde proporciona uma maior aderência do batom ao lábio (PONTES, 2020).
É de responsabilidade da ANVISA a fiscalização da produção e avaliação do cosmético após sua fabricação (BRASIL, 2015), porém acredita-se que ocorram falhas em alguma etapa do processo de fabricação e aprovação do produto para comercialização e são vendidos com a presença de contaminantes, em específico, metais traço (DIAS e RAU, 2013).
Justifica-se, que as quantidades de casos de batons que apresentam metais pesados devem ser inexistentes, porém, por falta de fiscalização adequada ou até mesmo por falta de notificações dessa existência, ainda se encontra batons que apresentam metais traço com valores acima do permitido.
Levando-se em conta a falta de informações, e de estudos a respeito do índice de metais pesados em batons de coloração vermelha, é de extrema importância a análise de amostras de batons vermelhos com textura matte e bala para que se obtenham valores e seja possível uma avaliação de acordo com a legislação vigente no Brasil. Desta forma, a problemática deste artigo, buscou avaliar quais os elementos traço, potencialmente tóxicos, fazem parte da constituição dos batons vermelhos, com textura matte e bala, comercializados em Salvador, BA. Além disto, o presente trabalho tem como objetivo específico: (1) identificar e quantificar se os metais encontrados nas amostras estão dentro do limite permitido de acordo com a legislação vigente; (2) correlacionar a quantificação dos íons metálicos com os principais problemas de saúde.
2. METODOLOGIA
2.1 INSTRUMENTAÇÃO
A determinação de multi-elementos foi realizada por meio de um espectrômetro de emissão óptica de plasma indutivamente acoplado Vista PRO (ICP OES – Varian Mulgrave, Austrália), com visualização axial e um detector de dispositivo acoplado por carga. Os parâmetros operacionais estão dispostos na Tabela 1.
Tabela 1: Parâmetros operacionais do ICP OES para a determinação dos elementos traços Cr, Mn, Co, Cd e Pb.
| Potência do plasma | 1,4 kW | |
| Radiofrequência | 40 MHz | |
| Aspiração da amostra | 0,7 L min-1 | |
| Tempo de integração | 5s | |
| Fluxo dos gases | ||
| Plasma | 15 L min-1 | |
| Auxiliar | 0,5 L min-1 | |
| Nebulizador | 0,8 L min-1 | |
| Comprimento de onda de detecção | Co (II) 228,616 nm Cr (II) 267,716 nm Mn (I) 257,610 nm Pb (II) 220,353 nm Cd (II) 214,429 nm |
(I) e (II) representam linhas atômicas e iônicas, respectivamente
Fonte: o autor.
2.2 REAGENTES E SOLUÇÕES
A digestão das amostras foi realizada no laboratório de bioquímica do Centro Universitário UniRuy, em Salvador – BA. Para a digestão das amostras de batom foi utilizado um bloco digestor TE-040/25 (Tecnal, São Paulo, Brasil). O material de laboratório foi previamente descontaminado em uma Solução de HNO3 a 10% v/v (65 % v/v, VETEC) durante 24 horas e lavados, várias vezes, com água ultrapura Mill-Q e seco ao ar livre em ambiente livre de poeira. A água utilizada para o preparo das soluções no desenvolvimento deste trabalho foi, primeiramente, deionizada no purificador de água (QUIMIS) e posteriormente ultra purificada através de osmose reversa pelo sistema de purificação de água da MILLIPORE SIMPLICITY 18S – 18 mΩ. Soluções estoques dos elementos As, Ca, Cd, Co, Cr, Cu, Fe, Mg, Mn, Mo, Na, Ni, P, Pb e Zn (1000 a 4000 mgL-1) foram usadas para preparar as soluções padrões de trabalho. Todos os reagentes usados foram de grau analítico.
2.3 PROCESSAMENTO DAS AMOSTRAS – DIGESTÃO ÁCIDA
Foram adquiridas dez amostras de batons vermelhos com textura matte, na forma de bala e líquido, essas foram identificadas em numerais de 01 a 10 e diferenciadas por letras, onde a letra A significava batons em formato bala e a letra B significava batons em formato líquido, comercializadas em Salvador, Ba, Brasil, para o desenvolvimento deste trabalho.
A etapa de mineralização das amostras foi realizada utilizando-se decomposição por via úmida em sistema aberto de acordo com Krug et al. (2008) adaptado por Migues e Yamaki (2014). Aproximadamente, 0,1000 mg de cada amostra foi misturada com 10,00 mL de HNO3 65 % v/v, VETEC), 5,00 mL H2O2 PA (Êxodo) e 5,00 mL de água ultrapura. A mistura foi acondicionada em béquer de 25,00 mL tampado e digerida em chapa aquecedora Tecnal por 5 h a 120 ºC. O material resultante foi dissolvido em HNO3 a 1,00 mol L-1, filtrado em papel de filtro e avolumado com água para volume final de 10,00 mL e armazenado a 4 ºC até o momento da análise.
A determinação da concentração total dos metais foi baseada em um método de decomposição das amostras que evitasse contaminação, mudança na composição química da amostra e perda por volatilização dos metais. As análises foram baseadas no peso da amostra seca realizadas em triplicata, sempre acompanhadas de um branco.
Os níveis de elementos traço encontrados foram comparados com os limites máximos permitidos para cosméticos pela RDC Nº 44/2012 (ANVISA, 2012), órgão brasileiro que regulamenta sobre alimentos e medicamentos no Brasil.
2.4 AVALIAÇÃO DA PRECISÃO DO MÉTODO
A precisão do procedimento foi confirmada pela análise de três diferentes materiais de referência certificados do Instituto Nacional de Padrões e Tecnologia (NIST): apple leaves (1515), spinach leaves (1570a) and peach leaves (1547). A digestão desses materiais foi realizada pelo mesmo procedimento aplicado às amostras.
2.5 ANÁLISE DE DADOS
Na análise dos dados, técnicas multivariadas, como a análise de componentes principais (PCA) e a análise de agrupamento hierárquico (HCA), foram utilizadas para descrever a similaridade entre as amostras considerando o conjunto total de variáveis e as correlações entre elas. Nessas análises estatísticas, o conjunto de dados foi organizado em uma matriz composta por 20 amostras (linhas) e 5 variáveis (colunas) representando os metais determinados. Antes da análise multivariada, foi realizado o escalonamento automático da matriz, visando dar o mesmo peso para todas as variáveis. A análise foi realizada, e os gráficos foram plotados no OriginPro8®.
2.6 VALIDAÇÃO ANALÍTICA
Todas as amostras e padrões foram analisados em triplicado e a precisão foi avaliada pelo desempenho de ensaios intra-dia e inter-dia por seis injeções replicadas das soluções padrão. A precisão intermediária foi obtida comparando os valores obtidos com o ICP OES adquiridos em dois dias diferentes, um dia com troca de analista. O limite de quantificação (LOD) e quantificação (LOQ) foram calculados usando background equivalent concentration (BEC) para estabelecer a mais baixa concentração de metal a ser detectada (µg g-1). A estabilidade da solução multi elemento e as amostras foram avaliadas por 24 h em temperatura ambiente e mantidas a 37 ° C por 2 h a 0,01 e 0,1 mol L − 1 de HCl, verificando as mudanças no sinal analítico após a análise por ICP OES.
3. RESULTADOS
As análises feitas por espectrômetro de emissão óptica com plasma acoplado indutivamente (ICP OES) são comparativas.
Os limites de detecção (LD) e quantificação (LQ) foram calculados como a concentração igual a 3x e 10x o desvio padrão, respectivamente, em 10 medidas do branco, dividida pela inclinação da curva analítica para cada elemento-traço. Estes limites representam a mais baixa concentração dos elementos nas amostras analisadas (mg. Kg-1) que pode ser quantificada por ICP OES (Tabela 2).
A recuperação das medidas das amostras certificadas foi consistente e variaram entre (96,00 – 103,4%) para a maioria dos metais analisados. Tais dados refletem a boa exatidão dos dados em como a precisão dos valores mensurados de acordo com a Resolução Nº 899 de 29 de maio de 2003 (BRASIL, 2003).
Tabela 2: Média e desvio padrão obtidos para três réplicas de material de referência certificado (CRM), porcentagem de recuperação; e limites de detecção (LD) e quantificação (LQ) (mg. Kg-1)
| Metal | Certificado | Medido | % recuperação |
| Co | 0,61±0,02a | 0,60±0,04 | 98,36 |
| Cr | 0,50±0,16a | 0,48±0,13 | 96,00 |
| Mn | 3,66±0,34b | 3,8±0,22 | 103,40 |
| Pb | 1,19±0,18a | 1,17±0,13 | 98,31 |
| Cd | 2,15±0,05 | 2,13±0,14 | 99,12 |
Fonte: o autor.
O método analítico adotado para a determinação do metal foi validado obtendo alguns parâmetros de mérito como o limite de quantificação (LOQ), precisão expressa em repetibilidade (porcentagem de desvio padrão relativo, % RSD), linearidade (expressa como coeficiente de determinação, R2). Os resultados para esses parâmetros são apresentados na Tabela 3.
Tabela 3. Características analíticas da metodologia utilizada na determinação de minerais em batons.
| Elemento | LOQa (mgkg-1) | RDSb (%) | Linearity (R2) |
| Cd | 1,33 | 2,4 | 0,9993 |
| Co | 0,14 | 1,5 | 0,9980 |
| Cr | 0,25 | 1,6 | 0.9954 |
| Mn | 1,02 | 1,8 | 0.9995 |
| Pb | 0,14 | 0,13 | 0.9975 |
aLOQ: Limite de quantificação para massa de amostra de aproximadamente 0,1 g; bRSD: desvio padrão relativo para solução 0.5 mg L-1 (n = 10). Fonte: o autor
Para avaliar a presença e quantificar cada elemento foi construída uma curva de calibração (Gráfico 1) com concentrações já conhecidas dos metais em análise (manganês, cromo, cobalto, chumbo e cádmio) e valores em faixa linear, no qual resultados encontrados após análise foram comparados de acordo com a legislação vigente, Resolução da Diretoria Colegiada (RDC) de nº 44 de 2012, onde está determina os valores de metais permitidos a serem encontrados em cosméticos, classe onde os batons fazem parte, analisados quimicamente (BRASIL, 2012).
Os dados das curvas analíticas obtidos são: y = 0,1141x + 0,0584 R² = 0,9954, y = 0,0784x + 0,0299 R² = 0,998, y = 0,0446x + 0,0168 R² = 0,9975, y = 0,0246x + 0,0187 R² = 0,9995, y = 0,0428x + 0,0014 R² = 0,9993, para manganês, cromo, cobalto, chumbo e cádmio, respectivamente, com linearidade entre 0 e 20,0 mg L-1 (N = 7).
Gráfico 1- Curva de calibração para a determinação dos elementos traços Cr, Mn, Co, Cd e Pb.
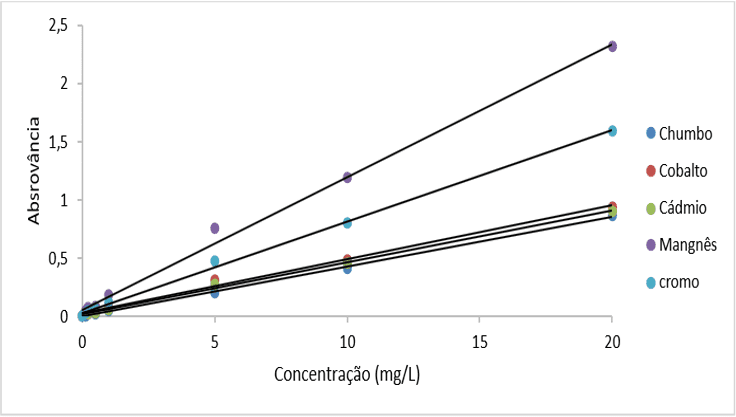
Os resultados obtidos na quantificação dos elementos estão expressos na Tabela 4. Os dados refletem a determinação em triplicata de cada amostra.
Tabela 4. Composição química, em µg g-1, dos metais traço (Cr, Mn, Co, Cd e Pb) das amostras batons determinados por ICP-OES
| Amostra | Pb | Cd | Mn | Co | Cr |
| 1A | 0,010±0,001 | 0,014±0,007 | 0,029±0,001 | 0,256±0,002 | 0,021±0,001 |
| 1B | 0,015±0,003 | 0,025±0,009 | 0,056±0,008 | 0,167±0,016 | 0,017±0,002 |
| 2A | 0,016±0,004 | 0,023±0,003 | 0,154±0,010 | 0,334±0,015 | 0,028±0,005 |
| 2B | 0,012±0,001 | 0,012±0,004 | 0,191±0,006 | 0,311±0,046 | 0,016±0,005 |
| 3A | 0,013±0,009 | 0,031±0,005 | 0,053±0,004 | 0,122±0,018 | 0,017±0,006 |
| 3B | 0,015±0,001 | 0,044±0,010 | 0,055±0,004 | 0,196±0,022 | 0,036±0,002 |
| 4A | 0,014±0,003 | 0,026±0,012 | 0,096±0,001 | 0,225±0,023 | 0,025±0,008 |
| 4B | 0,024±0,006 | 0,037±0,014 | 0,099±0,004 | 0,154±0,016 | 0,023±0,007 |
| 5A | 0,031±0,007 | 0,049±0,010 | 2,014±0,150 | 0,429±0,045 | 0,042±0,001 |
| 5B | 0,033±0,015 | 0,054±0,009 | 2,036±1,020 | 0,415±0,036 | 0,014±0,003 |
| 6A | 0,034±0,013 | 0,011±0,002 | 1,063±0,089 | 0,311±0,029 | 0,021±0,001 |
| 6B | 0,043±0,015 | 0,023±0,008 | 1,068±0,054 | 0,362±0,045 | 0,02±0,003 |
| 7A | 0,041±0,008 | 0,035±0,009 | 5,159±1,025 | 0,263±0,019 | 0,037±0,007 |
| 7B | 0,042±0,009 | 0,021±0,004 | 5,581±0,335 | 0,150±0,034 | 0,038±0,004 |
| 8A | 0,035±0,013 | 0,016±0,003 | 3,158±0,094 | 0,711±0,049 | 0,028±0,002 |
| 8B | 0,039±0,009 | 0,013±0,002 | 3,284±0,976 | 0,255±0,045 | 0,017±0,001 |
| 9A | 0,037±0,011 | 0,049±0,001 | 2,128±0,483 | 0,226±0,011 | 0,014±0,005 |
| 9B | 0,041±0,014 | 0,054±0,012 | 3,185±0,791 | 0,151±0,015 | 0,023±0,003 |
| 10A | 0,024±0,001 | 0,022±0,008 | 8,035±0,150 | 0,353±0,062 | 0,010±0,015 |
| 10B | 0,026±0,009 | 0,013±0,004 | 5,125±0,701 | 0,114±0,009 | 0,021±0,002 |
Fonte: o autor
A avaliação dos dados pelo HCA pelo método de Ward foi realizada para obter a variância mínima entre os vetores que compõem cada grupo, bem como as distâncias euclidianas, a fim de verificar a similaridade entre as amostras, conforme mostrado no dendrograma da Gráfico 2. A avaliação da distribuição dos analitos nas amostras foi realizada por meio de PCA que organizou uma matriz 20 x 5 com a concentração obtida e o analito foi disposto em linhas e colunas, respectivamente. Para avaliar a contribuição relativa de cada componente na variabilidade total dos dados, uma explicação foi o critério dos autovalores, onde apenas PCs com autovalores maiores que 1 são considerados importantes. Assim, dois PCs foram significativos para explicar a variabilidade dos dados e, juntos, eles respondem por 57,3% da variabilidade dos dados (Gráfico 3).
Gráfico 2. Dendrograma dos dados obtidos na determinação de metais em batons.
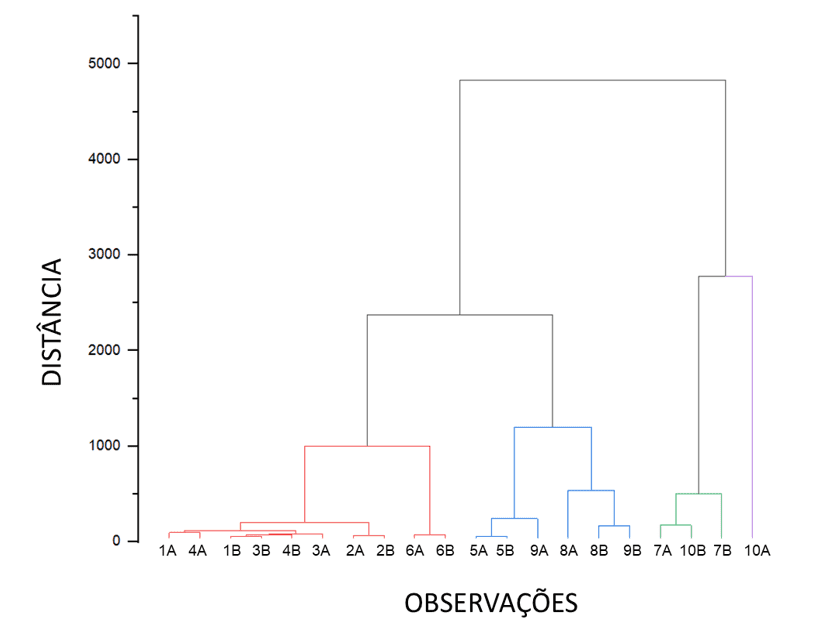
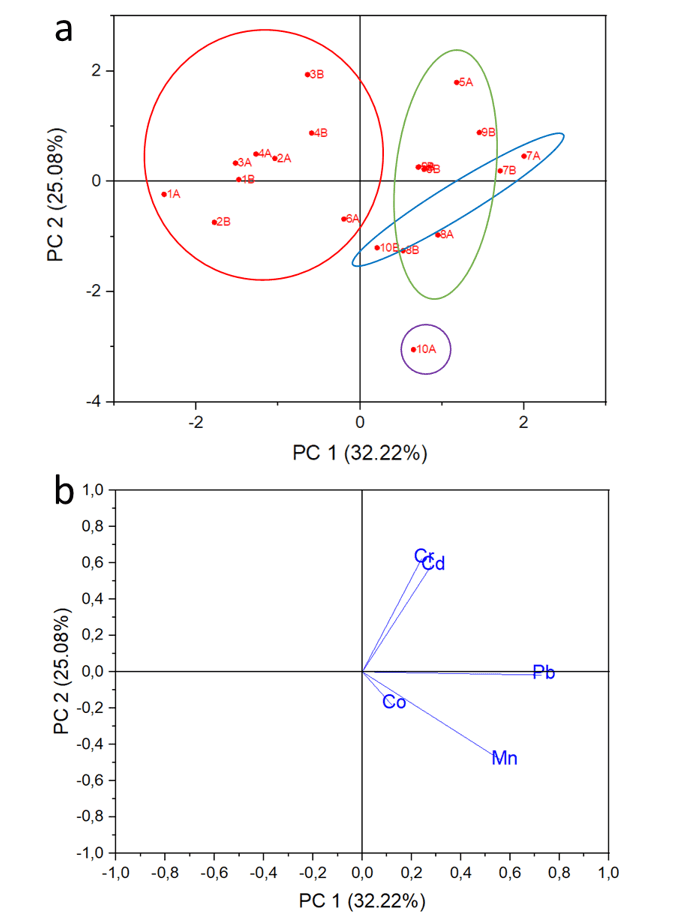
Gráfico 3: Gráfico de scores (a) e loadings (b) dos componentes principais.
4. DISCUSSÃO
As amostras em análise foram satisfatórias para o presente estudo, todas apresentaram traços dos metais analisados (cádmio, chumbo, cobalto, cromo e manganês), porém em todas as amostras as quantidades presentes estavam dentro do limite de quantidade permitido pela ANVISA (BRASIL, 2012) em cosméticos, limites estes encontrados na Resolução da Diretoria Colegiada (RDC) de nº 44 de 2012.
O gráfico 4 demonstra o quantitativo de metais encontrados nas amostras de batons no formato bala (A), a amostra onde o metal Pb (chumbo) apareceu com maior significância foi na amostra 7A, apresentando 0,041mg do metal analisado, porém a legislação vigente permite que em amostras como a analisada seja encontrado um quantitativo de até 20ppm de chumbo (BRASIL, 2012), dessa forma essa amostra está dentro dos limites definidos na legislação.
Para os outros metais, a legislação vigente permite o quantitativo de até 100ppm (BRASIL, 2012), porém podemos destacar que para Ca (Cádmio) as amostras onde o metal aparece com maior quantidade foi nas amostras 5A e 9A, ambas com 0,049g. Para Mn (Manganês), a amostra que teve uma quantidade superior às outras amostras foi a 10A, analisada com um valor de 8,035mg. Para Co (Cobalto), a amostra 8A foi a que expressou uma maior quantidade para este metal, sendo 0,711mg, pôr fim a amostra que teve uma maior quantidade de Cr (Cromo) foi a amostra 7A com 0,037mg, está também foi a que teve maior quantidade de Pb como citado acima, apesar dessas amostras se destacarem pela presença superior às outras quanto ao valor de cada metal, a legislação vigente permite a presença do quantitativo encontrado.
Gráfico 4. Amostras de batons formato bala e metais encontrados.
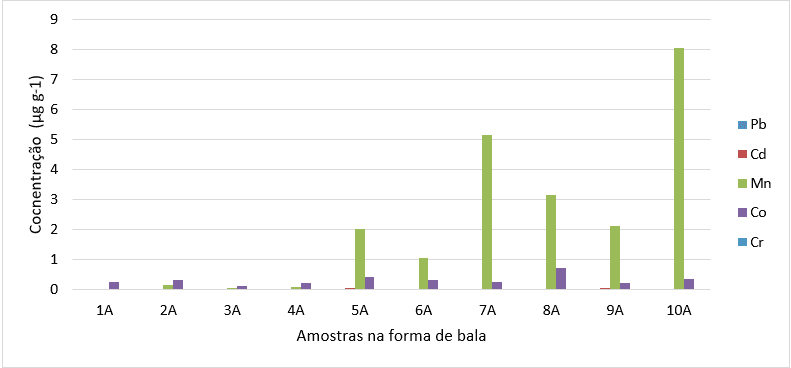
O gráfico 5 demonstra o quantitativo dos metais encontrados nas amostras de formato líquido (B). Sendo que a amostra que expressou maior quantitativo de Pb foi a 6B com 0,043mg, para Cd as amostras 5B e 9B tiveram um quantitativo de 0,054mg, para Mn a amostra 10B foi a que demonstrou maior quantitativo para este metal, sendo de 5,125mg, para Co a amostra com maior presença foi a 5B com 0,415mg e para Cr a amostra que teve o maior quantitativo foi a amostra 7B com 0,038mg.
Gráfico 5. Amostras de batons formato líquido e metais encontrados.
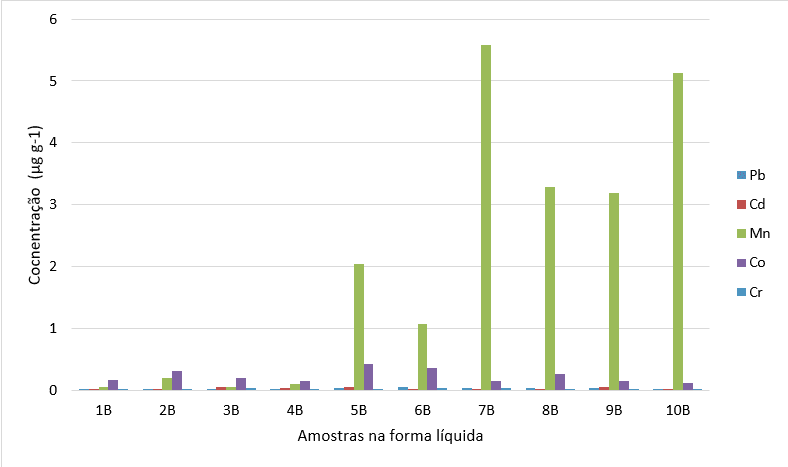
Analisando os dois gráficos podemos perceber uma variação do quantitativo do mesmo metal nos dois tipos de formatos analisados e podemos comparar que as marcas de número 5 e 9 tiveram um quantitativo superior de Cádmio (Cd) em ambos os formatos, em relação às outras marcas. Isso também ocorreu com a marca de número 10 para Manganês (Mn) e a marca de número 7 para Cromo (Cr).
Os metais encontrados nos batons podem advir de diversos meios desde componentes para a sua fabricação, geralmente encontrados mais nos pigmentos e nos corantes, como também dos recipientes onde eles são preparados (LIMA; SILVA; MARTINS, 2020). Entre os contaminantes mais encontrados nos batons, temos o Chumbo como o aquele metal que aparece com grande frequência nas análises químicas posteriores a fabricação (RIBEIRO, 2010).
Utilizando o teor dos metais nas 10 amostras de batons como variável de agrupamento, o HCA dos dados padronizados foi realizado com a distância euclidiana e o agrupamento de ligação de Ward pelo software Origin. O dendrograma mostrado no Gráfico 2 ilustra claramente que todas as amostras poderiam ser categorizadas em quatro grupos com Grupo 1 (G1) contendo 1A, 1B, 2A, 2B, 3A, 3B, 4A, 4B, 6A e 6B; Grupo 2 (G2) contendo 5A, 5B, 8A, 8B, 9A, 9B; Grupo 3 (G3) contendo 7A, 7B e 10 B; Grupo 4 (G4) contendo 10A. O Grupo 1, ainda pode ser subdividido em outros 4 grupos: G1.1 contendo as amostras: 1A e 4A; G1.2: 1B, 3A, 3B, 4B; G1.3: 2A, 2B; G1.4: 6A e 6B. O grupo 2, pode ser dividido em 4 subgrupos: G2.1: 5A e 5B; G2.2: 9A; G2.3: 8A; G 2.4: 8B e 9B. Por fim, o grupo 3 pode ser dividido em dois subgrupos: G3.1 e G3.2 contendo as amostras: 7A, 10 B e 7B, respectivamente. Os resultados mostraram que o HCA pode classificar a similaridade com base no conteúdo dos cinco componentes. Entretanto, para uma discriminação e agrupamento que ofereça melhor separação, há a necessidade de verificar mais variáveis.
Para avaliar o teor dos elementos em estudo, a distribuição deles nas matrizes analisadas, dentre outros aspectos, realizou-se a análise de componentes principais utilizando o programa Origin. Os valores dessa matriz de dados foram autoescalados, a fim de padronizar suas ordens de grandeza em um mesmo nível, permitindo a análise estatística dos dados.
Para a escolha das componentes principais que serão utilizadas no estudo é necessário a avaliação prévia dos autovalores de cada componente principal formado. Admite-se autovalores superiores a 1 como sendo aceitáveis para discriminação da variância dos resultados (MINGOTTI, 2007). Observa-se que as duas primeiras componentes principais formadas (PC1 32,22 %; PC2 25,08 %) apresentam autovalores igual ou superior a 1. Essas três componentes juntas permitem explicar 57,3 % da variância total dos resultados, sendo então utilizadas para análise das amostras em questão.
A observação do PCA, corrobora os dados encontrados no HCA. Verifica-se que a separação está relacionada ao conteúdo de Mn para o grupo 4. O grupo 3, apresenta os maiores teores de Pb. O grupo à esquerda, formado pela maior quantidade de amostras, estão representados pelos menores valores de contaminantes. Ademais, o grupo 2, apresenta os maiores valores de Cr e Cd.
Apesar das quantidades encontradas estarem dentro dos limites permitidos pela legislação, à exposição diária ou de forma contínua com o batom, esse pode ser ingerido oralmente, já que o seu local de uso é nos lábios, e obter o contato posteriormente à ingestão com os órgãos internos do ser humano e gerar danos à saúde no decorrer do tempo de uso (GONDAL et al., 2010). Desta forma é possível analisar separadamente os riscos que cada metal em estudo pode causar à saúde do consumidor.
4.1 CONTAMINANTES E SEUS RISCOS À SAÚDE
4.1.1 CÁDMIO
O cádmio (Cd) é considerado como metal pesado, obtido através da fundição de zinco e chumbo. É encontrado em pigmentos para tintas e plásticos. (KLAASSEN; WATKINS, 2012). Apesar de não se saber de forma exata sobre a origem do cádmio que é encontrado em produtos cosméticos, se sabe que sua presença é proveniente do uso de matérias-primas de baixa qualidade ou através de impurezas no processo de produção do cosmético. (VOLPE et al., 2012).
O cádmio após sua absorção, pode se distribuir pelo organismo e pode ser encontrado em células sanguíneas, ligado a proteínas do soro plasmático como a albumina e outras glicoproteínas, ou até mesmo na metaloproteínas produzidas pelo fígado (MATTIAZZO-PREZOTTO, 1994).
4.1.2 CHUMBO
O chumbo (Pb) é um metal considerado tóxico para a saúde humana, que pode ser detectável em quase todos os sistemas biológicos. Apesar do ideal seja de não ser encontrado em cosméticos, o mesmo pode contaminar um produto através do uso de pigmentos usados na composição do produto ou até mesmo no processo de fabricação, onde recipientes podem liberar chumbo para o produto em confecção. (GUNDUZ; AKMAN, 2013).
Este metal ganha uma atenção especial nos produtos que apresentam coloração vermelha, pois é encontrado principalmente em pigmentos ou corantes com esta tonalidade (vermelho) e em produtos que garantem uma maior duração, como o caso de batons com durabilidade superior a outros, os batons de alta duração (GONDAL et al., 2010).
O processo de intoxicação por chumbo acontece ao longo do período de exposição, onde quanto maior o tempo de exposição maior a quantidade de chumbo no organismo humano, embora o mesmo seja absorvido lentamente sua eliminação ainda acontece de forma mais lenta. O chumbo acumula-se principalmente no fígado, rins e sistema nervoso, porém é no sistema nervoso que ele ganha atenção especial devido aos danos que ele causa, provocando problemas neurológicos e comportamentais, destruindo as células que compõe a barreira hematoencefálica (GONDAL et al., 2010).
4.1.3 COMO
O cromo (Cr) é um elemento químico que em pouca quantidade é essencial para o funcionamento do organismo, atuando no metabolismo de carboidratos, proteínas e lipídios, atua também junto com a insulina no controle do nível de glicose do corpo humano, porém em grande quantidade pode ser considerado tóxico e pode provocar problemas gastrointestinais, hepáticos e renais (GONDAL et al., 2010).
A toxicidade por cromo ocorre de forma ocupacional devido seu uso nas indústrias na produção de pigmentos ou corantes, não se tem muita explicação para a contaminação de cromo em batons, mas acredita-se que seja oriunda na presença natural de cromo em pigmentos de coloração vermelho (COSTA; KLEIN, 2006).
4.1.4 COBALTO
O cobalto (Co) é um elemento químico que em quantidades adequadas é essencial para o organismo humano, é presente na composição da vitamina B12, e é encontrado em indústrias de caráter metalúrgico, na produção de aço. Pode ser apresentado de duas formas, tanto na forma de óxido onde é utilizado como catalisador na indústria química e na indústria de óleos e pode ser encontrado na forma de sal, este sendo usado na produção de indústrias de cerâmica, como pigmento (ALVES; ROSA, 2003).
As principais vias de exposição de toxicidade para o cobalto são as vias respiratória e dérmica. Através dessas vias de exposição o cobalto é captado por todos os tecidos e estar presente em diversos órgãos, porém as concentrações mais altas de cobalto podem ser encontradas no fígado. Não se tem explicações que o cobalto se acumule no organismo por muito tempo, uma vez que ingerido pode ser excretado pela urina e fezes (ALVES; ROSA, 2003).
4.1.5 MANGANÊS
O manganês (Mn) é também um elemento químico que participa de algumas atividades do organismo, sendo essencial para o funcionamento e regulação de diversas reações bioquímicas e celulares. Porém, quando presente em grande quantidade no organismo já é considerado como um agente tóxico, desencadeando problemas neuronais (neurotoxicidade) chamado de manganismo (SIDORYK-WEGRZYNOWICZ; ASCHNER, 2013).
A sua presença em cosméticos, dando ênfase aos batons, é proveniente dos pigmentos ou corantes utilizados na fabricação, principalmente corantes e pigmentos de tonalidade escura entre eles, o violeta e o vermelho (SUJIT KUMAR et al., 2013).
5. CONSIDERAÇÕES FINAIS
Os resultados obtidos, a partir do pressuposto inicial de identificação, refletem a presença de cinco elementos traços presentes nas amostras analisadas, Co, Cr, Mn, Pb e Cd. Esses metais são os que aparecem com frequência em cosméticos como batons e que são prejudiciais à saúde da população.
Apesar de existir legislações que proíbam a presença de metais pesados em cosméticos, existem também legislações que permitem a presença mínima, desta forma gerando uma contradição entre elas. Entretanto, órgãos de fiscalização atuam na inspeção de indústrias de cosméticos para que os mesmos não passem do limite de contaminação e afetem ainda mais a população, assegurando assim a preservação da saúde pública.
Verifica-se que os elementos analisados estão dentro do limite aceito pela ANVISA. De fato, a análise e determinação de lotes deve ser rotina em laboratórios de controle de qualidade, e a técnica por ICP torna-se excelente nesse sentido.
As patologias citadas neste trabalho estão atreladas com o tempo de exposição e com a quantidade de metal que são ingeridos de forma indireta, porém esses metais não deveriam estar presentes na composição destes batons.
REFERÊNCIAS
ALVES, A. N. L.; ROSA, H. V. D. Exposição ocupacional ao cobalto: aspectos toxicológicos. Revista Brasileira de Ciências Farmacêuticas, v. 39, n. 2, abril-junho, 2003. Disponivel em: <https://www.scielo.br/j/rbcf/a/GLnqGsyCrbb5jcWTgktJFsh/?lang=pt&format=pdf>. Acesso em: 15 de maio de 2021.
BRASIL. Decreto nº 79.094, de 5 de janeiro de 1977. Regulamenta a Lei nº 6.360, de 23 de setembro de 1976, que submete a sistema de vigilância sanitária os medicamentos, insumos farmacêuticos, drogas, correlatos, cosméticos, produtos de higiene, saneamento e outros. Diário Oficial da União, Brasília, DF, 07 jan. 1977. Seção 1, p. 11. (Revogado pelo Decreto nº8077/2013). Disponível em: < http://www.planalto.gov.br/ccivil_03/_ato2011-2014/2013/decreto/d8077.htm>. Acesso em: 21 de agosto de 2020.
BRASIL. Ministério da Saúde. ANVISA. Resolução RDC n° 44, de 09 de agosto de 2012. Aprova o Regulamento Técnico Mercosul sobre ―Lista de substâncias corantes permitidas para produtos de higiene pessoal, cosméticos e perfumes e dá outras providências. Diário Oficial da União, Brasília, DF, 09 ago. 2012. Disponível em: <http://bvsms.saude.gov.br/bvs/saudelegis/anvisa/2012/rdc0044_09_08_2012.html >. Acesso em: 22 de agosto de 2020.
BRASIL. Ministério da Saúde. ANVISA. Resolução RDC n° 07, de 10 de fevereiro de 2015. Aprova o Regulamento Técnico que estabelece a definição, a classificação, os requisitos técnicos, de rotulagem e procedimento eletrônico para regularização de produtos de higiene pessoal, cosméticos e perfumes nos termos desta Resolução. Diário Oficial da União, Brasília, DF, 11 de fevereiro de 2015. Disponível em: <http://portal.anvisa.gov.br/documents/10181/2867685/RDC_07_2015_.pdf/c2a1078c-46cf-4c4b-888a-092f3058a7c7>. Acesso em: 21 de agosto de 2020.
BRASIL. Ministério da Saúde. ANVISA. Resolução nº 899, 29 de maio de 2003. Determina o Guia para validação de métodos analíticos e bioanalíticos. Diário Oficial da União Brasília, DF. Disponível em: < http://portal.anvisa.gov.br/ > Acesso em: 27 de março de 2021.
COSTA, M.; KLEIN, C. B. Toxicity and Carcinogenicity of Chromium Compounds in Humans. Critical Reviews in Toxicology, n. 36, p. 155–163, 2006. Disponível em: <http://www.ncbi.nlm.nih.gov/pubmed/16736941>. Acesso em: 15 de maio 2021.
DIAS, A. C. E.; RAU, C. Contaminantes em Batom: Riscos e Aspectos Regulatórios. Goiás: PUC, 2013. Disponível em: <http://www.cpgls.pucgoias.edu.br/8mostra/Artigos/SAUDE%20E%20BIOLOGICAS/CONTAMINANTES%20EM%20BATOM%20RISCOS%20E%20ASPECTOS%20REGULAT%C3%93RIOS%20Ana%20Carolina%20Emidio.pdf>. Acesso em: 05 de setembro de 2020.
GONDAL, M.A. et al. Spectroscopic detection of health hazardous contaminants in lipstick using Laser Induced Breakdown Spectroscopy. Journal Of Hazardous Materials, n. 175, p.726-732, 2010. Disponível em: <http://www.ncbi.nlm.nih.gov/ pubmed/ 19926220>. Acesso em: 03 de março de 2021.
GUNDUZ, S.; AKMAN, S. Investigation of lead contents in lipsticks by solid sampling high resolution continuum source electrothermal atomic absorption spectrometry. Regulatory Toxicology and Pharmacology. n. 65, p. 34–37, 2013. Disponível em: <http://www.sciencedirect.com/science/article/pii/S027323001200195X > Acesso em: 10 de março de 2021.
HARRIS, M. I. Batom, Chumbo e Segurança do Consumidor. Cosmetics & Toiletries (Brasil), São Paulo, V. 25, P.52-55, jan/fev. 2013. Disponível em: < https://www.academia.edu/38806373/Harris_Chumbo_no_Batom>. Acesso em: 03 de setembro de 2020.
INMETRO: Relatório de análise de chumbo em batons. Inmetro. Rio de Janeiro, 2017. Disponível em: <http://www.inmetro.gov.br/consumidor/produtos/Relatorio_de_Analise_de_Chumbo_em_Batons.pdf>. Acesso em: 10 de setembro de 2020.
KLAASSEN, Curtis D. Metais Pesados e seus Antagonistas. In: GILMAN, A. Goodman et al. As bases farmacológicas da terapêutica.8.Ed. Rio de Janeiro: Guanabara Koogan, 1991. p.1061-1065.
LIMA, B. A.; SILVA, L. D. F.; MARTINS, L. F. TOXICIDADE DO CHUMBO EM BATONS: EFEITOS ADVERSOS A SAÚDE HUMANA. Repositório Institucional da Faculdade Evangélica de Ceres. Ceres- GO, 2020. Disponível em: < http://repositorio.aee.edu.br/handle/aee/9543>. Acesso em: 30 de abril 2021.
LIU, S. et al. Concentrations and Potential Health Risks of Metals in Lip Products. Environmental Health Perspectives, Berkeley, V.121, P.705-710, 2013, jun.2013. Disponível em:< https://pubmed.ncbi.nlm.nih.gov/23674482/>. Acesso em: 03 de setembro de 2020.
LORETZ, L. et al. Exposure data for cosmetic products: lipstick, body lotion, and face cream. Food And Chemical Toxicology, Washington, V. 43, P. 279-291. 18 set. 2004. Disponível em: <https://pubmed.ncbi.nlm.nih.gov/15621341/>. Acesso em: 03 de setembro de 2020.
MACEDO, A.P. et al. Batom: Estudo dos pigmentos utilizados. In: III Simpósio de Ciências Farmacêuticas do Centro Universitário São Camilo, 2014, São Paulo. Resumos… São Paulo, 2014. Disponível em: < www.saocamilo-sp.br/novo/eventos-noticias/simposio/14/SCF011_14.pdf>. Acesso em: 31 de agosto de 2020.
MAEHATA, P. Presença de elementos metálicos em cosméticos labiais: Investigação dos impactos na saúde e o descarte no meio ambiente. Dissertação apresentada como parte dos requisitos para obtenção do Grau de Mestre em Ciências na Área de Tecnologia Nuclear – Materiais, São Paulo, 2016. Disponível em: <http://pelicano.ipen.br/PosG30/TextoCompleto/Patricia%20Maehata_M.pdf>. Acesso em: 25 de agosto de 2020.
MATTIAZZO-PREZOTTO, M. E. Comportamento de cobre, cádmio, cromo, níquel e zinco adicionados a solos de clima tropical em diferentes valores de pH. Tese (Livre-Docência) – Escola Superior de Agricultura “Luis de Queiroz”, Universidade de São Paulo, Piracicaba, 1994. Disponível em: < https://www.scienceopen.com/document?vid=d8666824-d253-4251-a294-28e40dc42ea7>. Acesso em: 15 de abril de 2021.
MIGUES, V.H.; YAMAKI, R.T. Determinação de Co(II) em Preparações Farmacêuticas e Estudo das Espécies Formadas Durante a Complexação por UV-Vis com o Reagente Br-TDB. Revista Virtual de Química, Rio de Janeiro, V. 6, N. 6, P. 1533-1548. 2014. Disponível em: <http://static.sites.sbq.org.br/rvq.sbq.org.br/pdf/v6n6a02.pdf>. Acesso em: 23 de setembro de 2020.
MINGOTTI, S. A. Análise de dados através de métodos de estatística multivariada: uma abordagem aplicada. Belo Horizonte: UFMG, 2007
OLIVEIRA, F.F. Contribuição da análise térmica no desenvolvimento de formulações de batons. 2003. Dissertação (Mestrado em Química) – Instituto de Química da Universidade de São Paulo, Departamento de Química Fundamental, São Paulo, 2003. Disponível em: <https://www.teses.usp.br/teses/disponiveis/46/46133/tde-02122015-141614/publico/Floripes_Ferreira_Oliveira_Mestrado.pdf>. Acesso em: 21 de agosto de 2020.
PONTES, L. Batom matte: Como escolher os melhores de 2020?. Guia do Bem Estar, 2020. Disponível em: < https://www.guiadebemestar.com.br/batom-matte/>. Acesso em: 23 de setembro de 2020.
RIBEIRO, D.C.C. Produção e análise sensorial de batom. Assis, SP, 2010. Disponível em: <https://cepein.femanet.com.br/BDigital/arqTccs/0611160021.pdf>. Acesso em: 31 de agosto de 2020.
SIDORYK-WEGRZYNOWICZ, M.; ASCHNER, M. Manganese toxicity in the central nervous system: the glutamine/glutamate-γ-aminobutyric acid cycle. Journal of Internal Medicine, n. 273, p.466-477, 2013. Disponível em: < https://onlinelibrary.wiley.com/doi/epdf/10.1111/joim.12040>. Acesso em: 15 de maio de 2021.
SUJIT KUMAR, et al. Regulation for safety and quality of cosmetics vis-a-vis colourants in India compared with other nations. Der Pharmacia Lettre, v.1, n.4, p.181-191, 2012. Disponível em: <http://scholarsresearchlibrary.com/dpl-vol4-iss1/DPL-2012-4-1-181-191.pdf>. Acesso em: 16 de maio 2021.
VOLPE, M.G. et al. Determination and assessments of selected heavy metals in eye shadow cosmetics from China, Italy, and USA. Microchemical Journal, n. 101, p.65-69, 2012. Disponível em: <http://www.sciencedirect.com/science /article/pii/S0026 265X11002086.> Acesso em: 20 de março de 2021.
[1] Graduado em Farmácia.
[2] Orientador. Doutor em Química Orgânica, Metre em Química Analítica, Graduado em Licenciatura em Química. ORCID: https://orcid.org/0000-0002-3026-8716
Enviado: Setembro, 2021.
Aprovado: Janeiro, 2022.

