ARTICOLO ORIGINALE
CASALOTI, Laís Guadalupe [1], SANTOS, Jorge Alexandre Nogueira [2]
CASALOTI, Laís Guadalupe. SANTOS, Jorge Alexandre Nogueira. Inibizione dell’elastasi da estratto fogliare acquoso ed etanolico di Sedum Dendroideum: uno studio in vitro. Revista Científica Multidisciplinar Núcleo do Conhecimento. anno 04, Ed. 07, Vol. 04, pp. 140-147. luglio 2019. ISSN: 2448-0959
RIEPILOGO
L’attività non regolamentata delle proteasi negli esseri umani è legata a una serie di malattie. Neutrophil Elastase è una proteasi controllata dall’inibitore dell’antimetria (AAT) che è prodotto naturalmente dal fegato. Le mutazioni nel gene SERPINA 1 causano carenza di questo inibitore e la conseguenza di questo è l’emergere di diverse patologie negli esseri umani. Dato che le specie vegetali sono fonti promettenti per la scoperta di nuovi farmaci, il presente studio mirava a valutare l’effetto inibitorio degli estratti sull’elastasi, dove sono stati trovati valori IC50 di 8.1 ± 1.4 µg/ml (estratto acquoso) e 3.3 ± 0.6 µg/ml (Estratto etanolico). Questi risultati suggeriscono che gli estratti di Sedum dendroideum possono essere una potenziale fonte di composti bioattivi per la scoperta di nuovi inibitori per l’elastasi.
Parole chiave: Balsamo, IC50, inibitori.
INTRODUZIONE
Le proteasi sono enzimi essenziali per un gran numero di processi fisiologici come la digestione delle proteine, la riproduzione, la coagulazione del sangue, il sistema Kallikrein-Kinin e la fibrinolisi (Otàn & Bonde, 2008). Nell’uomo, l’attività non regolamentata delle proteasi è correlata a varie condizioni patologiche come il cancro, i processi infiammatori, la trombosi, l’artrite, le malattie della pelle e l’enfisema polmonare. Per questo motivo l’attività proteasi deve essere controllata e regolamentata (Rawlings et al., 2004). Recenti ricerche hanno rivelato che le proteasi sono diventate obiettivi importanti per lo sviluppo di farmaci. Elastase è una proteasi prodotta principalmente dal pancreas e dai neutrofili, e ha la proprietà di componenti idrolisi della matrice extracellulare, come collagene, elastina, Laminin e proteoglili (Thomson & Kapadia, 1979). L’attività proteolitica dell’elastasi neutrofica è strettamente regolata dall’inibitore endogeno delle proteine chiamato anti-antitrypsin (AAT). Le mutazioni nel gene SERPINA 1, Locus Pi, situato sul cromosoma 14 (14q31-32) causano carenza di AAT (Siedle, et al., 2003). Senza la presenza del suo inibitore naturale, l’elastasi in abbondanza genera lesioni tissutali, poiché questo enzima è la proteasi principale rilasciata dai neutrofili nei processi infiammatori.
L’azione di Elastase è legata a una serie di malattie come insufficienza epatica, artrite reumatoide, psoriasi, cancro della pelle, arteriosclerosi e diverse patologie polmonari (Johansson, 2002). In un polmone normale, gli alveoli sono esposti a bassi livelli di elastasi neutrofila. Questa proteasi può distruggere l’elastina nella parete alveolare se non è contenuta dall’azione dell’inibitore dell’antiristina di z-1. Dopo l’infortunio, il tessuto polmonare non può rigenerarsi e può essere innescato un processo di enfisema, asma, lesioni polmonari acute o fibrosi cistica (Abboud & Vimalanathan, 2008).
La prospezione di composti bioattivi da prodotti naturali trova nelle specie vegetali la principale e più promettente fonte di nuovi composti che possono agire come inibitori della proteasi. Per proteggersi da animali erbivori e insetti, le piante di solito producono metaboliti secondari che includono terpeni, polifenoli, tannini, peptidi e proteine (Ibanez et al., 2012). Molti di questi metaboliti sono inibitori delle proteasi e causano una diminuzione del processo di assorbimento degli amminoacidi essenziali per lo sviluppo degli insetti (Cuccilioni et al., 2009).
La specie Sedum Dendroideum, popolarmente conosciuta come Balsam è una pianta appartenente all’ordine Saxifrales, Moc. Et Sessé ex DC, famiglia Crasulaceae è una specie perenne, succulenta, sublenhosa e xerofita, originaria del Sudafrica, dal clima tropicale secco (Epagri, 1998). In Brasile, è ampiamente adattato ed è popolarmente chiamato Balsam (Milaneze Gonaalves, 2001). Il succo delle sue foglie è stato utilizzato per il trattamento di infiammazione cutanea e lividi, e internamente per disturbi gastrici, a causa di attività emollienti e curative (Epagri, 1998; Milaneze & Gonaalvez, 2001).
Gli studi indicano che il genere Sedum presenta composti di diversi gruppi chimici come i polisaccarides (Sendl et al., 1993), tannini (Stevens et al., 1995), Triterpenoids con attività epatoprotettiva (Aimin, et al., 1998), alcaloidi et al., 1985) e Pyrrolidyic (Harth et al., 1996). E attraverso un’analisi fitochimica con la specie Sedum dendroideum è stato possibile identificare la presenza di Kaempferol, una molecola importante con proprietà farmacologiche (Coutinho, Muzitano & Costa, 2009). Tenendo conto dell’esistenza di metaboliti secondari presenti nella specie, e tenuto conto del suo potenziale utilizzo come pianta medicinale, il presente studio mirava a verificare se gli estratti acquosi ed enolici della pianta hanno un potenziale di Inibizione sull’attività proteolitica dell’enzima elastasi.
MATERIALI E METODI
Gli estratti sono stati preparati dalle foglie di Sedum Dendroideum seguendo la metodologia di Heidari-Sureshjani (2015), in cui foglie fresche e sane della verdura sono state raccolte nel quartiere Furnas (latitudine 22° 26′ 27″ e longitudine 46° 21′ 03″), Comune di Bueno Brando.
Circa 10 g di foglie della pianta sono stati essiccati per 72 ore in una serra a 40 gradi centigradi e successivamente macinati fino ad ottenere una polvere dall’aspetto uniforme. Quindi, il materiale ottenuto è stato trasferito su una fiala di vetro e mescolato con 50 ml di acqua distillata, rimanendo a riposo per 12 ore. Dopo questa procedura, la miscela è stata filtrata sulla carta Whatman n. 1 ed è stato ottenuto un liquido chiaro e privo di particelle. La stessa procedura è stata utilizzata per la preparazione dell’estratto di etanolico, tuttavia al posto dell’acqua distillata è stato utilizzato l’etanolo 95%.
Per i saggi di inibizione, l’enzima elastasi del pancreas di maiale (E.C 3.4.21.36, ≥4 U/mg) e il suo substrato cromogenico N-succinyl-AlaAla-Ala-P-nitroanilide (Thomson & Kapadia, 1979) che sono stati acquisiti dalla società Sigma Aldrich utilizzati. L’enzima (alla concentrazione finale di 10 µg/ml) è stato incubato nel tampone di fosfato di sodio (50 mM, pH – 8) con gli estratti vegetali a concentrazioni diverse (gamma da 1 a 20 µg/ml per l’estratto di aquesa e variazione da 1 a 8 µg/ml per l’estratto othanico) a 25 C per Un volume finale totale di 990 . Dopo 30 minuti, alla miscela è stata aggiunta una 10 µL di substrato per una concentrazione finale di 10 µL e l’idrolisi del substrato cromogenico è stata monitorata per 5 minuti utilizzando uno spettrometro Di V-M5 Bel Photonics a una lunghezza d’onda di 410 nm. Come controllo negativo, sono stati utilizzati fosfato buffer 50 mM, pH 8, e come controllo positivo Epigalocatequina-3-galateo.
Tutti gli esperimenti sono stati effettuati in triplice copia e i dati sono stati presentati come media e deviazione standard. I valori del parametro di inibizione IC50, che è la concentrazione di estratto che inibisce il 50% dell’attività enzimatica, sono stati determinati dalla percentuale di inibizione rimanente rispetto alla concentrazione dell’estratto e calcolata dalla regressione non lineare utilizzando il Programma GraFit 5.0 (Leatherbarrow, 1992). La percentuale di inibizione è stata calcolata dall’equazione:
% di inibizione = |Controllo ABS – Estratto Abs| /Abs controlla x 100%
DISCUSSIONI SUI RISULTATI
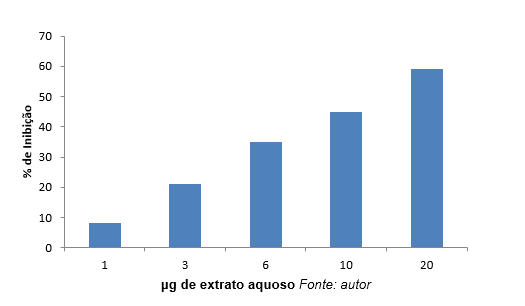
I grafici 1 e 2 mostrano la percentuale di inibizione dovuta a diverse concentrazioni di estratti acquosi e alcolici. Questi estratti inibito elastasi con intensità diverse. Come mostrato nel grafico 1, l’inibizione più elevata (59%) è stata osservata nella concentrazione di 20 µg/ml di estratto acquoso dell’enzima.
Grafico 1: percentuale (%) Inibizione dell’elastasi in funzione di diverse concentrazioni di estratti acquosi.
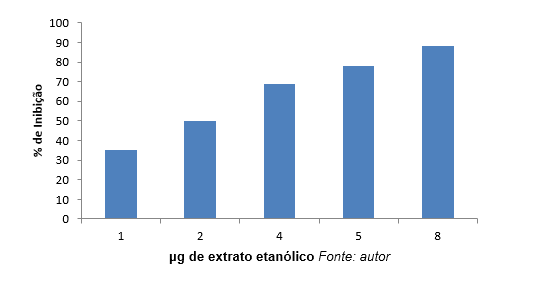
Nel grafico 2, possiamo osservare che l’inibizione più alta (88%) La concentrazione è stata di 8 µg/ml.
Grafico 2: percentuale (%) Inibizione dell’elastasi in funzione della concentrazione di estratti etanolici.
Dai risultati generati dai grafici 1 e 2, sono stati calcolati i valori di IC50 (tabella 1) per i due estratti, 8.1 ± 1.4 µg/ml (estratto acquoso) e 3.31 ± 0.6 µg/ml (estratto etanolico). Questi risultati indicano che l’estratto etanolico ha presentato un migliore potere di inibizione sull’elastasi rispetto all’estratto acquoso.
Tabella 1: Valori IC50 di estratti acquosi ed etanolici sull’elastasi. Valori espressi come media: deviazione standard.
| IC 50 (µg/ml) | |
| Elastasi | |
| Estratto acquoso | 8.1 ± 1.4 |
| Estratto di etanolico | 3.3 ± 0.6 |
Fonte: Autore
Gli estratti vegetali offrono opportunità illimitate per scoprire nuovi inibitori enzimatici, dato che producono un’ampia varietà di metaboliti secondari. Questi composti chimici sono utilizzati dalle piante per proteggersi contro l’azione di animali erbivori e insetti e molti di questi composti sono inibitori di diverse classi di proteasi, tra cui Elastase (Sin & Kim, 2005; Middleton et al., 2000).
Come descritto in precedenza, la specie Sedum Dendroideum produce un’ampia varietà di metaboliti secondari e questi composti possono essere coinvolti nell’inibizione dell’elastasi.
Conclusioni
I risultati del presente studio hanno indicato che gli estratti acquosi ed etanolici di Sedum Dendroideum avevano una significativa attività inibitoria sull’attività proteolitica dell’elastasi. Sono necessari studi più specifici per identificare e isolare i composti bioattivi negli estratti di Sedum dendroideum.
RIFERIMENTI BIBLIOGRAPHICAL
ABBOUD, R.T.; VIMALANATHAN S. Pathogenesis of COPD. Part I: The role of protease-antiprotease imbalance in emphysema. International Journal of Tuberculosis and Lung Diseases. v.12, n.4, p.361–367, 2008.
AIMIN, H.; MINGSHI, W.; HONGYAN, H.; DECHENG, Z.; LEE, K. H. Hepatoprotective triterpenes from Sedum sarmentosum. Phytochemistry, Oxford, v. 49, n. 8, p. 2607-10, 1998.
COUTINHO, M. A. S., MUZITANO, M. F., COSTA, S. S., 2009. Flavonóides: Potenciais agentes terapêuticos para o processo inflamatório. Revista Virtual de Química 1, 241-256.
CUCCIOLONI, M., MOZZICAFREDDO, M., ONFILI, L., CECARINI, V., ELEUTERI, A.M., ANGELETTI, M., (2009): Natural occurring polyphenols as template for drug design. Focus on serine proteases. Chem Biol Drug Des., 74: 1–15.
EPAGRI − Empresa de Pesquisa Agropecuária e Extensão Rural de Santa Catarina. S. A. CD Plantas Medicinais. Versão 1.0. Itajaí, 1998. 1 CD-ROM.
HALIN, F.; SLOSSE, P.; HOOTELÉ, C. Sedum alkaloides – VII – Structure and synthesis of (+)-4- hydroxysedamine and (+)-4-hydroxyallosedamine. Tetrahedron, Oxford, v. 41, n. 14, p. 2891-7, 1985.
HART, H. T.; STEVENS, J. F.; JEONG, H. K. Alkaloids of some Asian Sedum species. Phytochemistry, Oxford, v. 41, n. 5, p. 1319-24, 1996.
HEIDARI-SURESHJANI M.; YAZDI F. T.; MORTAZAVI, S.A.; BEHBAHANI, B.A.; SHAHID F. Antimicrobial effects of Kelussia odoratissima extracts against food borne and food spoilage bacteria “in vitro”. Journal of Paramedical Sciences, v. 5, n.2, 2015.
IBANEZ, S., GALLET, C., DESPRÉS, L., (2012): Plant Insecticidal Toxins in Ecological Networks. Toxins., 4: 228-243.
JOHANSSON, S. U., Neutrophil multitarget functional bioassay to detect anti-inflammatory natural products. J. Nat. Prod., v. 65, p. 32-41, 2002..
LEATHERBARROW, R.J. GraFit Version 5.0, Erithacus Software Ltd, Staines, U.K.,1992.
MIDDLETON, E., Kandaswami, C., Theoharides, T.C., (2000): The Effects of Plant Flavonoids on Mammalian Cells: Implications for Inflammation, Heart Disease andCancer. Pharmacol Rev., 52:673-751.
MILANEZE, M. A.; GONÇALVES, E. Caracterização morfo-anatômica das folhas de Sedum dendroideum DC, CRASSULACEAE In: Simpósio Brasileiro De Farmacognosia, 3., 2001, Curitiba. Anais. Curitiba: Universidade Federal do Paraná, Departamento de Farmácia, Laboratório de Farmacognosia, 2001. p. FB-23.
OTÍN, C. L; BOND, J. S. Proteases: Multifunctional Enzymes in Life and Disease. Journal of Biological chemistry, v.283, 30433-30437, 2008.
RAWLINGS, N.D.; MORTON, F.R. The MEROPS batch BLAST: A tool to detect peptidases and their non-peptidase homologues in a genome. Biochimie, v. 90, p. 243-259, 2008.
SENDL, A.; MULINACCI, N.; VINCIERI, F. F.; WAGNER, H. Anti-inflammatory and immunologically active polysaccharides of Sedum telephium. Phytochemistry, Oxford, v. 34, n. 5, p. 1357-62, 1993.
SIEDLE, L.G., GUSTAVSSON, L., JOHANSSON, S., MURILLO, R., BOHLIN, L., The effect of sesquiterpene lactonas on the release of human neutrophil elastase. Biochem. Pharmacol, v. 7559, p. 1-7, 2003.
SIN, B.Y., KIM, H.P., (2005): Inhibition of collagenase by naturally-occurring flavonoids. Archives of Pharmacal Research., 28(10): 1152-1155.
STEVENS, J. F.; HART, H. T.; VAN HAM, R. C. H. J.; ELEMA, E. T.; VAN EN ENT, M. M.V.X.; WILDEBOER, M.; ZWAVING, J. H. Distribution of alkaloids and tannins in the Crassulaceae. Biochem. Syst. Ecol., Oxford, v. 23, n. 2, p. 157-65, 1995.
STUART, L.M; EZEKOWITZ, R.A. Phagocytosis: elegant complexity. Immunity, v. 5, p. 539-550, 2005.
THOMSON, A., KAPADIA, S.K., The Specificity of the S1 and S2 Subsites of Elastase, Eur.J.Biochem, v.102, p. 311-116, 1979.
[1] Laureato in Scienze Biologiche presso IFSULDEMINAS-Campus Inconfidentes.
[2] Dottorato di ricerca in biochimica presso l’UNIFESP; Professore efficace presso IFSULDEMINAS-Campus Inconfidentes, e ricercatore aggiunto al Laboratorio di Biochimica del Centro per le Procedure Ambientali.
Inviato: Maggio, 2019.
Approvato: luglio 2019.