ОРИГИНАЛЬНАЯ СТАТЬЯ
ROCHA, Ana Paula Coelho [1], ZÁU, Aline Sales Mendes [2], SANTOS, Luciana Mendes dos [3]
ROCHA, Ana Paula Coelho. ZÁU, Aline Sales Mendes. SANTOS, Luciana Mendes dos. Гигантский врожденный меланоцитарный невус с невротизацией: клинический случай. Revista Científica Multidisciplinar Núcleo do Conhecimento. Год. 07, изд. 01, Том. 06, стр. 123-132. Январь 2022 г. ISSN: 2448-0959, Ссылка для доступа: https://www.nucleodoconhecimento.com.br/здравоохранение/гигантский-врожденный
СВОДКА
Врожденный меланоцитарный невусы (ВМН) представляют собой редкие гамартомы, которые характеризуются клональной пролиферацией меланоцитов, происходящих из нервного гребня, гнездящихся в эпидермисе/дерме после их миграции во время эмбриогенеза. Клинически они представляют собой пигментированные поражения с четко очерченными границами, различного размера и внешнего вида. Гигантский врожденный меланоцитарный невус (ГВМН) — это невус диаметром двадцать или более сантиметров, рассчитанный на взрослую жизнь. Наличие ГВМН связано с более высоким риском тяжелых сопутствующих заболеваний, таких как нейрокожный меланоцитоз и меланома, а также необходимо исключить врожденную злокачественную меланому, основной дифференциальный диагноз. Будет ли в этом сценарии наличие пролиферативных узелков худшим прогностическим фактором? В этом отчете представлен сложный клинический случай ГВМН с быстро растущими пролиферативными узлами у 18-дневного новорожденного. Проведен краткий обзор литературы и обобщение клинико-гистопатологических данных рассматриваемой пациентки, находившейся на лечении в дерматологической поликлинике. Сделан вывод о том, что, несмотря на наличие клинических характеристик, указывающих на худший прогноз или возможное злокачественное новообразование, тщательная гистологическая интерпретация и правильная клинико-патологическая корреляция необходимы для адекватной диагностики и терапевтического лечения.
Ключевые слова: врожденная меланома, гигантский врожденный невус, меланоцитарный невус, невротизация, пролиферативные узелки.
ВВЕДЕНИЕ
Врожденный меланоцитарный невусы (ВМН) характеризуются доброкачественными клональными пролиферациями меланоцитов, происходящих из нервного гребня, которые претерпевают изменения при созревании и дифференцировке на этапе миграции в период эмбриогенеза. Клетки невуса образуют гнезда или рассеяны в эпидермисе и глубоких слоях дермы, на любом участке покровов. Около 1-2% населения имеют эти изменения при рождении (SCALVENZI, 2012).
Для начальной дифференциации между ВМН и приобретенным меланоцитарным невусом (NMA) учитываются размер, раннее развитие поражения и гистологические характеристики обоих. ВМН, как правило, больше и присутствуют с рождения или, как правило, до первых 6 месяцев жизни (VIANA, 2013). В гистопатологии ведутся споры о реальных показателях дифференциации врожденных и приобретенных невусов, и зачастую различить их невозможно. Однако, в отличие от NMA, ВМН не ограничиваются дермо-эпидермальным соединением, они обладают большей клеточностью и затрагивают более глубокие слои (ZAAL, 2004).
По данным Simons (2017), при гистопатологии ВМН гнезда меланоцитов и клетки невуса обнаруживаются рассеянными на разной глубине дермы, между пучками коллагена, вокруг придатков, нервов и кровеносных сосудов и могут инфильтрировать подкожные ткани, мышцы и фасции. Часто наблюдается высокая клеточность, разная степень архитектурной дезорганизация и атипия, а также педжетоидное распространение. Такие результаты обычно обнаруживаются при меланоме, что усложняет дифференциацию между ними и может привести к ошибочному диагнозу.
Клинически они представляют собой коричневато-коричневые бляшки, сильно пигментированные, с четкими границами, однородной и часто сосовидной поверхностью, с участками гипертрихоза (MADRIGAL DÍEZ, 2015). Однако более крупные невусы могут быть асимметричными, с неровными краями и неоднородной, шероховатой или узловатой поверхностью из-за избытка меланоцитов и невротизации. Этим термином обозначают процесс созревания клеток невуса, происходящий с поверхности вглубь ткани, где они приобретают более веретенообразную форму. Они напоминают шванновские клетки, из которых состоит нейрофиброма, папуло-узелковая опухоль плотной консистенции, эмбриологическое происхождение которой также находится в нервном гребне (SINGH, 2015).
Согласно Kopf (1979), ВМН можно классифицировать по размеру: он считается малым, если он меньше 1,5 см, средним, если он составляет от 1,5 до 19,9 см, и гигантским, если он больше или равен 20 см, рассчитанным для взрослого возраста. Совсем недавно Krengel (2012) предложил новую классификацию, включающую, помимо размера, клинические факторы с целью сделать описания более стандартизированными и уверенными в отношении риска меланомы. В этом контексте считается, что ГВМН с большей шероховатостью, более темной пигментацией, гипертрихозом, подкожными узелками и наличием сателлитных невусов имеют худший прогноз с более высоким риском малигнизация.
Будет ли в этом сценарии наличие пролиферативных узелков худшим прогностическим фактором? Цель этого сообщения — представить редкий и сложный клинический случай ГВМН с быстро растущими пролиферативными узлами у 18-дневного новорожденного путем раскрытия клинических и гистологических данных рассматриваемого пациента и краткого обзора литературы с целью уточнить взаимосвязь между пролиферативными узелками/нейротизацией и прогнозом.
ИСТОРИЯ БОЛЕЗНИ
Новорожденный, 18 дней, родилась в Амазонас, доношенная, вес 4415 кг. Мать сообщает о кесаревом сечении из-за беременности с высоким риском, осложненной преэклампсией, гестационным диабетом и повторной инфекцией мочевыводящих путей, с несколькими схемами антибиотикотерапия.
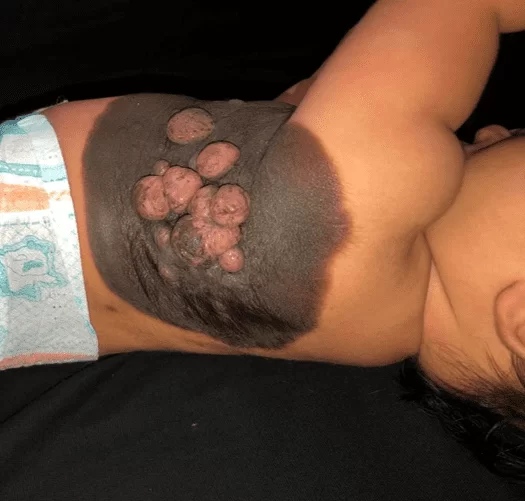
Имеет бархатисто-чернеющую бляшку от рождения на левой половине грудной клетки, простирающуюся от срединно-ключичной линии до ипсилатеральной межлопаточной тыльной области, размером 23 см в наибольшем диаметре, с четко очерченными границами, наличием волосяного покрова по периферии, ассоциированным с центральным и срастающимся, от черноватого до розового, размером от 0,5 см до 1,5 см и размягченной консистенции (Рисунок 1). Также имеется сателлитное поражение размером примерно 0,7 см в левом бедре (Рисунок 2). Через 30 дней после начала лечения наблюдалось значительное увеличение указанных узелков (Рисунок 3). В остальном физикальное обследование не выявило изменений, а нейропсихомоторное развитие было адекватным для его возраста. Подозрительных телесных повреждений не было.
После первоначального дерматологического лечения мы выбрали инцизионную биопсию центрального узелкового поражения из-за клинического аспекта, указывающего на худший прогноз. Однако анатомопатологический отчет показал только доброкачественные признаки, такие как паракератоз, гнезда клеток невуса, лежащие над дермальным компонентом аккуратно расположенных клеток невуса, меланический пигмент в глубоких слоях дермы и области нейральной дифференцировки, без атипии. Таким образом, был подтвержден диагноз ВМН с невротизацией и исключено возможное злокачественное новообразование. Таким образом, вместе с сектором детской хирургии мы выбрали серийное удаление узелков и клиническое наблюдение для периодической оценки невуса.
Рисунок 1. Гигантский врожденный меланоцитарный невус: почерневшая бляшка, с бархатистой поверхностью, хорошо отграниченная, волосатая, с центральными опухолями, размером более 20 см.
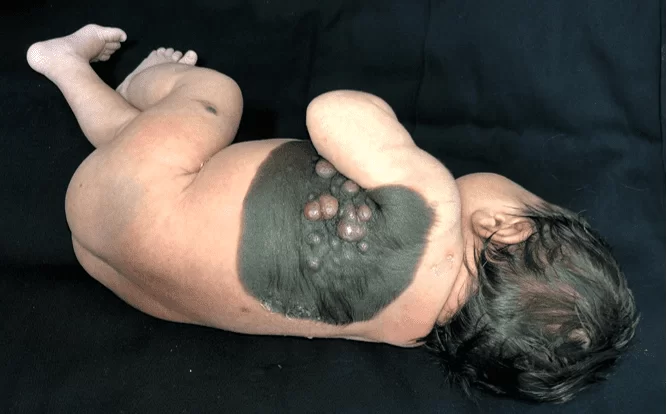
Рисунок 2. Одиночное сателлитное поражение на левом бедре.
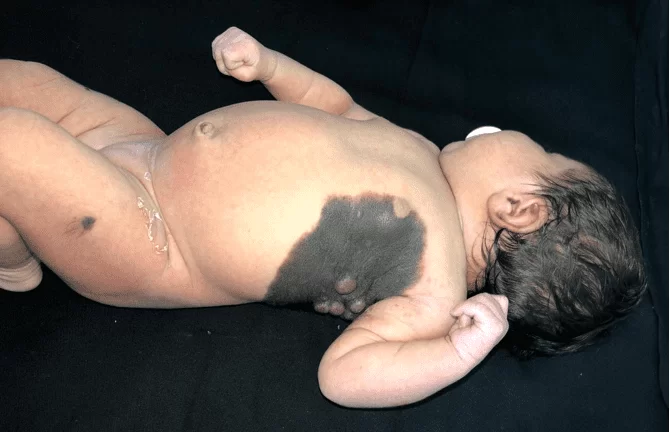
Рисунок 3. Быстрый рост поражений через 30 дней после первоначального лечения с образованием сливных опухолей размягченной консистенции и розоватого цвета с сохранением почерневших участков на поверхности.
ОБСУЖДЕНИЕ
Гигантский врожденный меланоцитарный невус (ГВМН) является редким заболеванием, и его средняя частота встречаемости составляет 1 случай на каждые 20 000 рождений (ESCADÓN-PÉREZ, 2019). Тем не менее, это имеет большое клиническое значение, поскольку связано с более высоким риском тяжелых сопутствующих заболеваний, таких как нейрокожный меланоцитоз (NCM) и меланома (RUGGIERI, 2020). Первый – это синдром, который поражает центральную нервную систему и может привести к внутричерепной гипертензии и судорогам, особенно когда ГВМН имеет узелки, множественные сателлитные поражения и возникает в таких местах, как шея, скальп и средняя линия спины. По данным Alikhan (2012), заболеваемость NCM колеблется от 2,5% до 45%. Известно, что меланомы возникают преимущественно из нормальных меланоцитов JDE, однако Zaal (2003) указывает, что до 11% ГВМН могут развиваться со злокачественным перерождением, которое встречается в первое десятилетие жизни в до 60% случаев.
Клиническое и дерматоскопическое сходство между ГВМН с пролиферативными узелками и врожденной злокачественной меланомой (MMC), редким, но потенциально смертельным заболеванием, требует тщательной интерпретации гистопатологических данных (SCALVENZI, 2012).
Этот отчет свидетельствует о наличии ГВМН без значительных сателлитных поражений и с заметным присутствием узелков, которые обычно присутствуют только в 3% случаев, цитируемых в литературе (SCALVENZI, 2012). Анатомопатологические данные подтверждают тот факт, что пролиферативные кожные узелки не являются независимыми признаками злокачественности (SIMONS, 2017). Тем не менее, он находит пары в отношении наиболее частого расположения в стволе, отсутствия семейного и гистопатологического анамнеза, благоприятного для клинического наблюдения, наблюдаемого в 75% случаев (VIANA, 2017).
Таким образом, возникают большие вопросы о реальной заболеваемости меланомой из случаев ГВМН, а также о необходимости хирургического вмешательства в наиболее клинически сложных случаях либо из-за размера поражения, либо из-за наличия множественных сателлитных невусов (VIANA, 2017). До сих пор нет данных, доказывающих пользу этой практики в качестве профилактики развития злокачественных новообразований, и, в зависимости от глубины расположения клеток невуса, нет возможности тотального иссечения и, следовательно, полного излечения.
Несмотря на терапевтическую проблему, ГВМН по-прежнему становится диагностической проблемой из-за ее способности клинически и гистологически имитировать MMC (ESCADON-PÉREZ, 2019).
Примечательно, что сопутствующее наличие множественных сателлитных невусов должно насторожить в отношении возможности поражения мозговых оболочек и злокачественных или доброкачественных опухолей центральной нервной системы. В этом случае необходимо запросить дополнительные тесты, такие как магнитно-резонансная томография или оценка спинномозговой жидкости, для лучшей оценки и последующего наблюдения за состоянием, учитывая его худший прогноз и связь с потенциально фатальными неврологическими расстройствами (RUGGIERI, 2020).
Наконец, ГВМН несет ответственность за эстетический и социальный ущерб, оказывая сильное эмоциональное воздействие на участников (ZAAL, 2012).
ЗАКЛЮЧИТЕЛЬНЫЕ СООБРАЖЕНИЯ
Принимая во внимание данные литературы и отвечая на наводящий вопрос, делается вывод, что пролиферативные/нейротизированные узлы важны для клинической оценки прогноза ГВМН, однако они не способны определять худший исход изолированно. ГВМН представляют собой самые разнообразные фенотипы, которые различаются с точки зрения риска развития меланомы или NCM, сложности хирургического вмешательства и возможности исключительного клинического наблюдения. Таким образом, необходим тщательный анализ набора клинической информации в сочетании с гистопатологическими данными.
Эти факты иллюстрируют важность углубления изучения ГВМН, редкого события, которое, тем не менее, может добавить большую заболеваемость пациенту, а также создать препятствия для диагностики и лечения, которые должны отдавать приоритет индивидуальности случая и быть подготовлен междисциплинарно.
ИСПОЛЬЗОВАННАЯ ЛИТЕРАТУРА
ALIKHAN, Ali; IBRAHIMI, Omar A.; EISEN, Daniel B. Congenital melanocytic nevi: where are we now?: part I. Clinical presentation, epidemiology, pathogenesis, histology, malignant transformation, and neurocutaneous melanosis. Journal of the American Academy of Dermatology, v. 67, n. 4, p. 495. e1-495. e17, 2012.
COTTON, Colleen H.; GOLDBERG, Gerald N. Evolution of congenital melanocytic nevi toward benignity: a case series. Pediatric dermatology, v. 36, n. 2, p. 227-231, 2019.
ESCANDÓN-PÉREZ, Sabrina et al. Nevo melanocítico congénito gigante. Boletín médico del Hospital Infantil de México, v. 76, n. 6, p. 251-258, 2019.
KRENGEL, Sven et al. New recommendations for the categorization of cutaneous features of congenital melanocytic nevi. Journal of the American Academy of Dermatology, v. 68, n. 3, p. 441-451, 2013.
KOPF, Alfred W.; BART, Robert S.; HENNESSEY, Patrick. Congenital nevocytic nevi and malignant melanomas. Journal of the American Academy of Dermatology, v. 1, n. 2, p. 123-130, 1979.
MADRIGAL DÍEZ, C. et al. Nevo melanocítico congénito gigante. Pediatría Atención Primaria, v. 17, n. 68, p. 351-355, 2015.
RUGGIERI, Martino et al. Neurocutaneous melanocytosis (melanosis). Child’s Nervous System, v. 36, n. 10, p. 2571-2596, 2020.
SCALVENZI, Massimiliano et al. Giant congenital melanocytic naevus with proliferative nodules mimicking congenital malignant melanoma: a case report and review of the literature of congenital melanoma. Case reports in dermatological medicine, v. 2013, 2013.
SIMONS, Emily A.; HUANG, Jennifer T.; SCHMIDT, Birgitta. Congenital melanocytic nevi in young children: Histopathologic features and clinical outcomes. Journal of the American Academy of Dermatology, v. 76, n. 5, p. 941-947, 2017.
SINGH, Nidhi et al. Neurotized congenital melanocytic nevus resembling a pigmented neurofibroma. Indian journal of dermatology, v. 60, n. 1, p. 46, 2015.
VIANA, Ana Carolina Leite; GONTIJO, Bernardo; BITTENCOURT, Flávia Vasques. Giant congenital melanocytic nevus. Anais brasileiros de dermatologia, v. 88, p. 863-878, 2013.
VIANA, Ana Carolina Leite et al. A prospective study of patients with large congenital melanocytic nevi and the risk of melanoma. Anais brasileiros de dermatologia, v. 92, p. 200-205, 2017.
ZAAL, L. H. et al. Classification of congenital melanocytic naevi and malignant transformation: a review of the literature. British journal of plastic surgery, v. 57, n. 8, p. 707-719, 2004.
[1] Дерматолог-ординатор третьего года обучения, бакалавр медицины. ORCID: 0000-0001-9895-706X.
[2] Дерматолог-ординатор третьего года обучения, бакалавр медицины. ORCID: 0000-0002-6561-376X.
[3] Советник. Кандидат тропических и инфекционных болезней Государственного университета Амазонас в партнерстве с Фондом тропической медицины FMT-HVD, специалист по дерматологии, бакалавр медицины. ORCID: 0000-0002-3991-6732.
Подано: Январь 2022 г.
Утверждено: Январь 2022 г.