ARTÍCULO ORIGINAL
DIOCESANO, Kamila Bezerra Fernandes [1], COSTA, Aurélio Antonio Ribeiro [2], LEITÃO, Glauber Moreira [3]
DIOCESANO, Kamila Bezerra Fernandes. COSTA, Aurélio Antonio Ribeiro. LEITÃO, Glauber Moreira. Cáncer de mama multifocal/multicéntrico: Perfil clínico/epidemiológico y patrones inmunohistoquímicos entre los focos: Estudio transversal. Revista Científica Multidisciplinar Núcleo do Conhecimento. Año 05, Ed. 06, Vol. 04, págs. 73-94. Junio de 2020. ISSN: 2448-0959 Enlace de acceso: https://www.nucleodoconhecimento.com.br/salud/clinico-epidemiologico, DOI: 10.32749/nucleodoconhecimento.com.br/salud/clinico-epidemiologico
RESUMEN
El cáncer de mama multifocal/multicéntmo (MF/MC) es una enfermedad que comprende muchos paradigmas en la práctica actual del cáncer de mama. Para combatir la morbilidad y mortalidad de esto la mejor opción es una estrategia terapéutica racional, que debe comenzar con una clara comprensión biológica de la multicentricidad y la multifocalidad, ya que esto se conoce, se puede seguir el tratamiento correcto. Nuestro objetivo era definir el perfil de los pacientes con cáncer de mama multifocal y multicéntrico y evaluar si hay desacuerdo entre los focos tumorales con respecto al receptor hormonal y Her-2. Analizamos retrospectivamente 89 pacientes con cáncer de mama multifocal y multicéntrico invasivo en dos instituciones terciarias en el noreste de Brasil, evaluando el receptor hormonal, Her-2 y ki67 en cada foco tumoral de 25 de estos pacientes, destacando el desacuerdo o no entre ellos, y el tipo y grado histológico, la metástasis de los ganglios linfáticos y la distancia y la edad. De estos pacientes, el 9% presentó heterogeneidad entre los focos tumorales. La proporción de metástasis en ganglio linfático axilar fue del 42% y sólo del 10% para la metástasis distante. El 45% de las mujeres en el estudio tenían grado histológico II o III. Encontramos una prevalencia de 40.5% de Her-2 negativo y 45% del receptor de estrógeno positivo. No hubo diferencia estadísticamente significativa entre el cáncer multifocal y el multicéntrulo. Concluimos que el cáncer de mama MF/MC muestra heterogeneidad entre los focos tumorales en relación con los parámetros biológicos, lo que desempeña un papel crucial en la toma de decisiones sobre el tratamiento y, en consecuencia, sobre la recurrencia del tumor, el pronóstico y la metástasis distante.
Palabras clave: Cáncer de mama, heterogeneidad, multifocal, multicéntrtil.
INTRODUCCIÓN
El cáncer de mama es la neoplasia maligna que afecta más a las mujeres de todo el mundo. Es la segunda causa de muerte por cáncer en los países desarrollados, sólo por detrás del cáncer de pulmón, y la principal causa de muerte por cáncer en los países en desarrollo. En 2013, hubo alrededor de 1,8 millones de nuevos casos en todo el mundo y 471.000 muertes[1]. En el caso de Brasil, la estimación es de aproximadamente 60.000 nuevos casos de cáncer de mama al año, con un riesgo estimado de 56,20 casos por cada 100.000 mujeres. En el estado de Pernambuco es de 2.450 nuevos casos, con una tasa bruta de incidencia de 90,25 casos por cada 100.000 habitantes sólo para Recife, la capita[2]l.
El cáncer de mama se clasifica como multicéntrico (MC) y/o multifocal (MF) cuando presenta más de un foco tumoral y sincrónico en la misma mama. La diferencia entre ellos se basa en la ubicación, ya sea que se encuentran en diferentes cuadrantes de la mama o en ella, respectivament[3,4]e.
La incidencia de tumores MF y/o MC varía entre el 6% y el 60[5,6]%. Las características clínica-patológicas y de pronóstico del cáncer de mama multifocal y multicéntmo aún no están bien establecidas.
Sobre la base del razonamiento de que las lesiones con histología y grado similares deben ser biológicamente similares, el Colegio Americano de Patología recomienda caracterizar todos los focos de MF/MC con inmunohistoquímica sólo cuando la histología y o el grado histológico difieren entre s[7]í. Por lo tanto, la inmunohistoquímica se solicita sólo para el tumor más grande y los otros focos no se evalúan[8].
Un estudio en el que participaron 113 pacientes, en el que se evaluó la inmunohistoquímica de todos los focos tumorales, encontró que el desacuerdo entre los foci estaba presente en el 4,4% – 18,6% de los casos, siendo indicados diferentes tratamientos en comparación con lo que se habría prescrito si hubieran tenido en cuenta sólo la inmunohistoquímica de un solo foco, el más grand[9]e.
La decisión de elegir la mejor opción terapéutica para el cáncer de mama MC/MF debe comenzar con una clara comprensión biológica y epidemiológica de la multicentricidad y el multifondo, ya que se conocen, se puede seguir el tratamiento correcto. La evaluación inmunohistoquímica de los tumores desempeña un papel crucial en la toma de decisiones en el tratamiento del cáncer de mama y cuando se expresa discordantemente en los diversos focos puede proporcionar a los pacientes la oportunidad de diferentes terapias.
Según lo estudiado, el objetivo de este estudio fue describir el perfil clínico y epidemiológico de las mujeres con cáncer de mama MF/MC y los patrones inmunohistoquímicos de los diversos focos de cáncer de mama en cada mujer en dos hospitales terciarios en el noreste de Brasil.
Métodos
El estudio transversal descriptivo se llevó a cabo en el Instituto de Medicina Integral Prof. Fernando Figueira (IMIP) y el Hospital Baro de Lucena (HBL), instituciones del estado de Pernambuco, se centraron en la atención médica en diversas especialidades y se comprometieron con la enseñanza, la investigación y la extensión.
La muestra fue constituida convencionalmente por mujeres identificadas retrospectivamente con cáncer de mama MF o MC asistido en el IMIP de enero de 2013 a junio de 2016 y en HBL en el período de enero de 2012 a junio de 2016 que cumplen con los criterios de elegibilidad de la investigación, que son: tener dos o más focos de diagnóstico tumoral en el mismo seno simultáneamente , excepto en casos de recurrencia de un tumor anterior, estar vivo y tener el mismo tipo y grado histológico entre los focos.
Se realizaron visitas semanales al laboratorio de anatomía patológica HBL y al centro de mama IMIP y se seleccionaron los resultados de la biopsia histopatológica o quirúrgica de tumores mamarios de pacientes con un perfil compatible con los criterios de elegibilidad del estudio.
El tejido tumoral obtenido mediante biopsia de núcleo o en el momento de la cirugía definitiva se conserva y envasa en formalina (10% de formaldehído) amortiguado y procesado en bloques de parafina. Estos bloques se almacenan a temperatura ambiente hasta su posterior análisis, tanto para el examen histopatológico como para el inmunohistoquímico.
Después de identificar a estos pacientes, el investigador se puso en contacto con los pacientes que fueron presentados a la investigación e invitados a participar firmando el formulario de consentimiento libre e informado.
Se solicitó inmunohistoquímica de cada foco tumoral. Esto se obtuvo a través de los bloques de parafina ya almacenados, o, retrospectivamente, de los registros existentes del foco tumoral estudiado.
La inmunohistoquímica es una herramienta vital en el estudio de lesiones mamarias. Uso de anticuerpos específicos contra proteínas intracelulares presentes en una pequeña cantidad en el núcleo, citoplasma y/o membrana celular[10]. La técnica inmunohistoquímica identifica en el tumor los receptores de estrógeno y progesterona, el índice de proliferación de células tumorales y la expresión de la proteína de membrana HER-2. Se solicitó para todos los tumores múltiples presentes simultáneamente en la misma mama y se realizó en un laboratorio con un profesional especializado en patología mamaria, en el que utiliza el método de estreptavidina-biotina marcado a través de la máquina de enlace PT de DAKO.
Los pacientes que no autorizaron la solicitud de inmunohistoquímica aceptaron participar en el estudio únicamente con información contenida en los registros médicos y los datos histopatológicos e inmunohistoquímicos existentes.
Receptor hormonal, Her-2 y ki67 fueron evaluados en cada foco tumoral, destacando el desacuerdo o no entre ellos; tipo y grado histológico; metástasis y distancia de los ganglios linfáticos; invasión linfovascular y la edad del paciente.
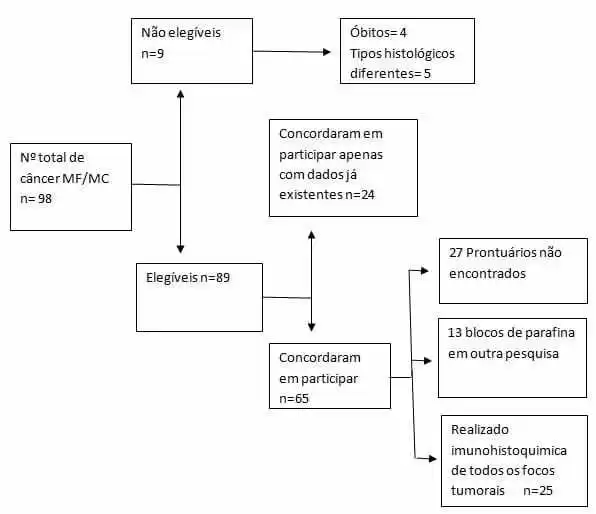
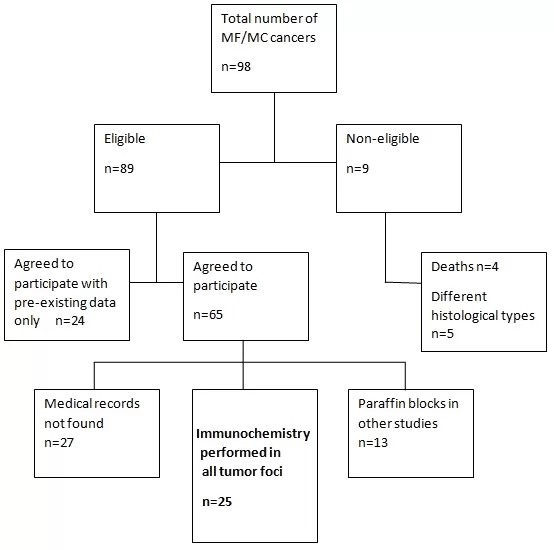
Figura 1. Diagrama de flujo de captura de participantes
La información recopilada se introdujo en doble entrada (el investigador y un colaborador), en diferentes momentos, en una hoja de datos (software de Microsoft Office Excel – 2010), creada con el propósito de validar la escritura. La base de datos se ha sometido a pruebas de revisión y limpieza para detectar errores o incoherencias en los datos. Sólo después de comparar los bancos y realizar las pruebas de consistencia y limpieza se utilizó la base de datos definitiva para el análisis estadístico.
El software SPSS 13.0 (Paquete estadístico para las ciencias sociales) para Windows y Excel 2010 se utilizó para el análisis de datos. Para analizar el comportamiento de las variables del estudio, se realizaron medidas de tendencia central y sus dispersiones, la prueba Quiquadrado de tendencias y Fisher’s Exact, a un nivel de significancia del 5%, cuando es pertinente. Todas las pruebas se aplicaron con un 95% de confianza. Los resultados se presentan en forma de tabla con sus respectivas frecuencias absolutas y relativas.
Resultados
La incidencia de tumores MF/MC en nuestro estudio fue del 4% en 2013 y del 5% en 2015. No se dispone de datos Imip para 2012 y 2014 (Tabla 1). El 64% de las mujeres con cáncer de MF/MC tenían más de 50 años. Con la excepción de que muchos datos no estaban disponibles, encontramos una frecuencia del 33% de las mujeres morenas, el 24% con la escuela primaria incompleta y el 13% de las mujeres casadas (Tabla 2).
TABLA 1 – Incidencia de cáncer de mama unifocal, multifocal y multicéntmo en el Hospital Baro de Lucena, HBL, y el Instituto Materno Infantil Prof. Fernando Figueira, IMIP. Recife, Pernambuco
| CA de Mama | n (HBL/IMIP) | % (HBL/IMIP) |
| 2012 | ||
| Unifocal | (195/-) | (92,4/-) |
| MC/MF | (16/-) | (7,6/-) |
| 2013 | ||
| Unifocal | 477 (184/293) | 95,9 (93,4/97,7) |
| MC/MF | 20 (13/ 7) | 4,0 (6,6/2,3) |
| 2014 | ||
| Unifocal | (150/-) | (92,6/-) |
| MC/MF | (12/12) | (7,4/-) |
| 2015 | ||
| Unifocal | 523 (162/361) | 94,9 (89,5/97,6) |
| MC/MF | 28 (19/9) | 5,0 (10,5/2,4) |
Los datos IMIP de 2012 y 2014 no están disponibles.
Fuente: Búsqueda IMIP/HBL
TABLA 2 – Características de los pacientes con cáncer de mama multifocal y multicéntmo operado en el Hospital Baro de Lucena, HBL, e Instituto Materno Infantil Prof. Fernando Figueira, IMIP. Recife, Pernambuco
| Variables | n | % |
| Edad | ||
| < 50 | 26 | 29,2 |
| ≥ 50 | 57 | 64,1 |
| Cor | ||
| Branca | 16 | 18,0 |
| Negro | 2 | 2,2 |
| Marrón | 30 | 33,7 |
| Escolaridad | ||
| Analfabetos | 6 | 6,7 |
| Escuela primaria incompleta | 22 | 24,7 |
| Escuela primaria completa | 6 | 6,7 |
| Escuela secundaria incompleta | 1 | 1,1 |
| Escuela secundaria completa | 12 | 13,5 |
| Estado civil | ||
| Unión estable | 1 | 1,1 |
| soltero | 8 | 9,0 |
| Casado | 13 | 14,6 |
| Divorciado | 3 | 3,4 |
| Viuda | 9 | 10,1 |
Los datos no desinformados para cada variable se omitieron de la tabla.
Fuente: Búsqueda IMIP/HBL
El tipo histológico ductal fue encontrado en el 82% de las mujeres en nuestro estudio. La proporción de metástasis en ganglio linfático axilar fue del 42% y sólo del 10% para la metástasis distante. El 45% de las mujeres en el estudio tenían grado histológico II o III. Encontramos una prevalencia de 40.5% de Her-2 negativo y 45% del receptor de estrógeno positivo. En cuanto a Ki67, encontramos 41% con una alta tasa de proliferación celular. La proporción de heterogeneidad entre los focos fue del 9% y encontramos el 65% de MF y el 17% de MC (Tabla 3).
TABLA 3 – Características clínicas y tumorales de pacientes con cáncer de mama multifocal y multicéntrico operados en el Hospital Baro de Lucena, HBL, y el Instituto Materno Infantil Prof. Fernando Figueira, IMIP. Recife, Pernambuco
| Variables | n | % |
| Re | ||
| Positivo | 40 | 44,9 |
| Negativo | 20 | 22,5 |
| RP | ||
| Positivo | 35 | 39,3 |
| Negativo | 25 | 28,1 |
| Her-2 | ||
| Positivo | 18 | 20,2 |
| Negativo | 36 | 40,5 |
| Ki67 | ||
| <14% | 16 | 18,0 |
| >14% | 37 | 41,6 |
| Ganglios linfáticos comprometidos | ||
| Out | 23 | 25,8 |
| 1 a 3 | 18 | 20,2 |
| 4 o más | 20 | 22,5 |
| Grado histológico | ||
| I | 9 | 10,1 |
| II | 27 | 30,4 |
| III | 13 | 14,6 |
| Tipo histológico | ||
| Ductal | 73 | 82,0 |
| Lobulado | 1 | 1,1 |
| Otro | 4 | 4,5 |
| Tamaño del tumor más grande | ||
| <2 cm | 24 | 27,0 |
| 2-5 cm | 32 | 36,0 |
| >5 cm | 5 | 5,6 |
| Metástasis distante | ||
| Sí | 9 | 10,1 |
| No | 48 | 53,9 |
| Invasión linfovacular | ||
| Sí | 20 | 22,5 |
| No | 24 | 27,0 |
| Heterogeneidad entre focos | ||
| Sí | 8 | 9,0 |
| No | 17 | 19,1 |
| Distancia entre focos | ||
| 4 cm (multifocal) | 58 | 65,2 |
| > 4 cm (multicéntrito) | 15 | 16,9 |
Los datos no desinformados para cada variable se omitieron de la tabla.
Fuente: Búsqueda IMIP/HBL
No se observaron diferencias significativas en la comparación de variables entre mujeres con o sin heterogeneidad entre los focos tumorales (Tabla 4) y entre MF y MC (Tabla 5).
TABLA 4 – Características clínicas y tumorales de pacientes con cáncer de mama multifocal/multicéntrico operados en el Hospital Baro de Lucena, HBL, y el Instituto Materno Infantil Prof. Fernando Figueira, IMIP, en relación con la heterogeneidad entre los focos. Recife, Pernambuco
| Heterogeneidad entre focos | |||
| Variables | Sí | No | valor p |
| n (%) | n (%) | ||
| Ganglios linfáticos comprometidos | |||
| Out | 2 (40,0) | 3 (60,0) | 1,000 * |
| 1 a 3 | 2 (33,3) | 4 (66,7) | |
| 4 o más | 3 (50,0) | 3 (50,0) | |
| Grado histológico | |||
| I | 2 (66,7) | 1 (33,3) | 0,748 * |
| II | 2 (25,0) | 6 (75,0) | |
| III | 1 (33,3) | 2 (66,7) | |
| Tamaño del tumor más grande | |||
| <2 cm | 4 (57,1) | 3 (42,9) | 0,510 * |
| 2-5 cm | 3 (33,3) | 6 (66,7) | |
| >5 cm | 0 (0,0) | 2 (100,0) | |
| Metástasis distante | |||
| Sí | 1 (20,0) | 4 (80,0) | 0,588 * |
| No | 5 (45,5) | 6 (54,5) | |
| Invasión linfovacular | |||
| Sí | 4 (57,1) | 3 (42,9) | 0,592 * |
| No | 2 (28,6) | 5 (71,4) | |
(*) Prueba exacta de Fisher
Fuente: Búsqueda IMIP/HBL
TABLA 5 – Características clínicas y tumorales de pacientes con cáncer de mama multifocal y multicéntrico operados en el Hospital Baro de Lucena, HBL, y el Instituto Materno Infantil Prof. Fernando Figueira, IMIP. Recife, Pernambuco
| Distancia entre focos | |||
| Variables | 4 cm (multifocal) | >4cm (multicéntrito) | valor p |
| n (%) | n (%) | ||
| Re | |||
| Positivo | 29 (80,6) | 7 (19,4) | 1,000 * |
| Negativo | 12 (80,0) | 3 (20,0) | |
| Rp | |||
| Positivo | 26 (81,3) | 6 (18,7) | 1,000 * |
| Negativo | 15 (78,9) | 4 (21,1) | |
| Her-2 | |||
| Positivo | 14 (82,4) | 3 (17,6) | 0,723 * |
| Negativo | 22 (75,9) | 7 (24,1) | |
| Ki67 | |||
| <14% | 13 (86,7) | 2 (13,3) | 0,695 * |
| >14% | 22 (75,9) | 7 (24,1) | |
| Ganglios linfáticos comprometidos | |||
| Out | 16 (84,2) | 3 (15,8) | 0,839 * |
| 1 a 3 | 11 (73,3) | 4 (26,7) | |
| 4 o más | 16 (80,0) | 4 (20,0) | |
| Grado histológico | |||
| Ⅰ | 6 (66,7) | 3 (33,3) | 0,440 * |
| Ⅱ | 20 (87,0) | 3 (13,0) | |
| Ⅲ | 9 (81,8) | 2 (18,2) | |
| Tipo histológico | |||
| Ductal | 49 (80,3) | 12 (19,7) | 0,370 * |
| Lobulado | 1 (100,0) | 0 (0,0) | |
| Otro | 2 (50,0) | 2 (50,0) | |
| Tamaño del tumor más grande | |||
| <2 cm (1,5 in) | 19 (79,2) | 5 (20,8) | 0,884 * |
| 2-5 cm | 20 (76,9) | 6 (23,1) | |
| >5 cm | 2 (66,7) | 1 (33,3) | |
| Metástasis distante | |||
| Sí | 5 (62,5) | 3 (37,5) | 0,331 * |
| No | 35 (83,3) | 7 (16,7) | |
| Invasión linfovacular | |||
| Sí | 13 (72,2) | 5 (27,8) | 0,256 * |
| No | 21 (87,5) | 3 (12,5) | |
(*) Fuente exacta de prueba de Fisher: Investigación IMIP/HBL
Discusión
La incidencia de tumores MF/MC fue de aproximadamente el 5%, siendo 65% MF y 17% MC, ligeramente inferior a la que se encuentra e[5,6,9]n la literatura, lo que muy probablemente se deriva del hecho de que esta tasa varía según la extensión del muestreo de tejido mamario analizado por el patólogo en macroscopia, ya que se demostró que un muestreo más completo resultó en la identificación de lesiones adicionales; con la falta de una definición estándar MF/MC; y con las di[5]ferentes sensibilidades de los métodos de diagnóstico por imágenes utilizados preoperatoriamente para detectar múltiples focos maligno[3,4,11-13]s. Un estudio estadoun[5]idense evaluó a 3.924 mujeres con cáncer de mama y encontró que el 24% de MF/MC solo usaba criterios patológicos en su selección, 79% MF y 20% MC. Un metanálisis que incluyó 22 estudios y 67557 mujeres encontró MF/MC en el 9,5% de los casos, pero algunos estudios utilizaron métodos de diagnóstico por imágenes preoperatorios como criterio de diagnóstic[14]o.
Encontramos una muestra más grande de mujeres marrones/negras y casadas. El bajo nivel escolar observado en este estudio refleja el grado de conocimiento del paciente, que aumenta a medida que aumenta la escolarización. Un estudio brasileño [15]mostró una asociación entre el conocimiento sobre los factores de riesgo para el cáncer de mama y los años de estudio, y no hubo relación entre las variables de color de la piel y estado civil. Un estudio estadouni[16]dense asoció a mujeres afrodescendientes y nunca haber estado casada, con la etapa avanzada de la enfermedad, tal vez porque estas mujeres carecía del apoyo financiero y social proporcionado por el cónyuge y por factores culturales y socioeconómicos relacionados con el color. En nuestro estudio, aunque tuvimos una prevalencia de mujeres con baja escolaridad, marrones y negras, no observamos un aumento en etapa avanzada.
La mayoría de los pacientes en el estudio tenían 50 años o más (64%). Se sabe que el cáncer de mama es más frecuente en este grupo de edad, y esta es una posible explicación para esta muestra. Algunos informes en la literatura asocian MF/MC con mujeres jóvenes menores de 50 años, tipo histo[3,12]lógico lobular y mayor afec[17]tación de los ganglios linfáticos,[3,4,8,12,17] apoyando la hipótesis de que el MF/MC son biológicamente más agresivos, tienen una mayor propensión a la difusión metastásica y están relacionados con un peor resultad[12]o.
La proporción de ganglios linfáticos axilares afectados en nuestro estudio fue del 42% y sólo del 10% para la metástasis distante. Los pacientes con carcinomas invasivos múltiples tienen un mayor riesgo de metástasis en los ganglios linfáticos axilares, sin embargo, no se ha demostrado que aumenten el riesgo de metástasis distante en pacientes con enfermedad ganglionar negativ[4]a. Un estudio australiano [18]con 848 mujeres con cáncer de mama unifocal y MF/MC realizó análisis multivariados comparando varias variables con la medición del tamaño del mayor foco tumoral y con la medición de la suma de los diversos focos tumorales, y concluyó que la tendencia de la metástasis de los tumores mamarios es un reflejo de la carga tumoral total en lugar de la dimensión del mayor enfoque y que el uso del tamaño acumulado de focos en tumores multifocales demuestra una positividad de los ganglios linfáticos idéntica a la del tamaño equivalente de los tumores unifocales. Usando el tamaño del foco dominante, hay una mayor probabilidad de positividad de los ganglios linfáticos y tal vez un peor pronóstico en comparación con los tumores unifocales del mismo tamaño.
El tipo histológico más frecuente fue el ductal (82%), similar al encontrado por varios autores[3,9,17,19]. Lynch y otro[5]s describen un aumento en la tasa de metástasis a ganglios linfáticos regionales en relación con tumores unifocales. Esta asociación plantea la cuestión de si el MF/MC está subestimado con el sistema de ensayo actual, que sólo tiene en cuenta el enfoque tumoral más grande, o si simplemente tienen una biología inherente más agresiva.
El grado histológico es un factor pronóstico conocido en el cáncer de mama. Numerosos estudios han demostrado su importante asociación con la supervivencia. Al mismo tiempo, es un componente importante de la decisión terapéutica y tiene un papel predictivo en la respuesta terapéutic[20]a. Los estudios muestran una fuerte asociación entre MF/MC y grado histológico II/II[11,17,19]I. El 45% de las mujeres en el estudio tenían grado histológico II o III.
Encontramos una prevalencia del 40,5% de Her-2 negativo y 45% del receptor positivo de estrógeno, contra los datos en la literatura que muestran una correlación entre MF/MC y factores clínicos patológicos que sugieren tumores más agresivos, con notable asociación de Her2 positivo y ausencia de receptor de estrógeno hormonal[12]. Creemos que la causa de esta diferencia puede deberse al pequeño tamaño de la muestra, caracterizando así un error estadístico de tipo II. En cuanto a Ki67, el 41% correspondió a una alta proliferación celular. De hecho, algunos casos de tumores con respuesta a hormonas se llevarán a la quimioterapia debido a este hecho.
El Colegio Americano de Patología [7]considera suficiente que la caracterización inmunohistoquímica de lesiones multifocales con grado e histología similares se base únicamente en la lesión más grande. Sin embargo, estudios reciente[9,21,22]s cuestionan esta recomendación, ya que han demostrado que, a pesar de la similitud de las características patológicas, las lesiones pueden ser diferentes en términos de estado del receptor de estrógeno y Her-2, lo que potencialmente afecta a su tratamiento. En nuestro estudio, encontramos 9% de heterogeneidad entre los focos, incluyendo el análisis de ki67. Buggi et al [9]encontraron discrepancia entre los focos en relación con Ki67 en el 15% de los casos.
Los receptores hormonales fueron discretos entre los focos en el 8% de la muestra y Her-2 en el 4%, pero el análisis de estos elementos se vio afectado debido al hecho de que en más del 50% de los casos la inmunohistoquímica se obtuvo sólo del foco tumoral más alto. Buggi et al[9] describieron una tasa de desacuerdo entre los resultados del receptor hormonal para estrógeno de 4.4% y Her-2 de 9.7% entre los focos. Pekar[22] y Choi[21] observaron tasas de discrepancia entre 3-4% para el receptor de estrógeno y 6% para Her-2. Según Pekar, [22]los pacientes que demostraron heterogeneidad tenían un peor pronóstico en comparación con los pacientes que no demostraron heterogeneidad, que no se encontró en nuestro estudio, en el que no se observaron diferencias significativas entre la heterogeneidad y los grupos homogéneos, pero tuvimos limitaciones debido a la pequeña muestra y las pérdidas en el análisis, lo que podría cambiar este escenario.
No hubo significación estadística en la comparación de variables entre MF y MC debido a un pequeño tamaño de muestra. En la literatura, no observamos grandes diferencias entre MF/MC en relación con el tipo y el grado histológico, la metástasis de los ganglios linfáticos y la distancia y el tamaño del tumo[5,13]r.
Las decisiones clínicas en la terapia adyuvante sistémica en el cáncer de mama se basan en criterios histológicos y perfil inmunohistoquímico del mayor enfoque tumoral, ignorando los focos simultáneos más pequeños.
La presencia de focos adicionales no se tiene en cuenta en la decisión de las terapias adyuvante. Si examinamos sólo el tumor más grande en estos casos, podemos perder pacientes que necesitaban terapia específica. Las consecuencias de la heterogeneidad entre los focos tumorales para la toma de decisiones terapéuticas y, por lo tanto, para una mayor supervivencia del paciente rara vez se abordan en la literatura.
Por lo tanto, se debe prestar mayor atención a los tumores MF/MC y se debe evaluar rutinariamente la posibilidad de tener como rutina la solicitud de inmunohistoquímica para todos los focos tumorales, ya que por el enfoque estándar los pacientes con desacuerdo entre los focos habrían dejado de recibir tratamiento hormonal y anti Her-2 para el cáncer de mama.
Hay algunas limitaciones en nuestro análisis. En primer lugar, nuestro trabajo fue retrospectivo, aunque algunos de los enfoques de los datos extraídos fueron solicitados durante el estudio, los datos sobre el tumor histopatológico no pudieron ser detallados, cuando no se hicieron en el momento de la preparación del resultado histopatológico; además del hecho de que algunos bloques de parafina estaban disponibles para investigaciones adicionales, lo que imposibilitó la inmunohistoquímica y, en consecuencia, un pequeño tamaño de muestra. Este hecho puede no resaltar algunas asociaciones que podrían existir, caracterizando así un error estadístico de tipo II. Este hecho perjudica la validación externa de nuestros resultados.
CONCLUSIÓN
La mayoría de los cánceres MF/MC tienen homogeneidad entre los focos tumorales, y evaluar más de un enfoque puede tener consecuencias terapéuticas en sólo una minoría de casos, además de aumentar el costo y el tiempo. Sin embargo, dado que el pronóstico y el tratamiento de los pacientes con cáncer de mama pueden variar según la caracterización molecular del tumor, se puede argumentar, desde el punto de vista biológico, que el análisis de un solo enfoque, como se indica en las recomendaciones actuales, no sería apropiado. Hay pruebas emergentes de que esta recomendación puede no ser sostenible en el tiempo y puede necesitar ser adaptada para ser compatible con la evolución de los paradigmas del cáncer de mama.
Concluimos que el cáncer de mama MF/MC muestra una pequeña proporción de heterogeneidad entre los focos en relación con los parámetros biológicos, sin embargo, esto desempeña un papel crucial en la toma de decisiones sobre el tratamiento adyuvante y, en consecuencia, sobre la tasa de pronóstico, recurrencia tumoral y metástasis distantes para las mujeres con ese hallazgo. Sería extremadamente interesante solicitar rutinariamente inmunohistoquímica para todos los focos tumorales en casos de MF/MC. Sin embargo, teniendo en cuenta la posible carga financiera adicional para los laboratorios al instituir esta recomendación, los laboratorios de patología pueden necesitar desarrollar estrategias adicionales para hacer frente a esta nueva propuesta.
ASPECTOS ÉTICOS
Este proyecto cumple con las leyes vigentes del país, y los postulados de la Declaración de Helsinki, sien[23]do aprobado por el Comité local de ética e investigación (CEP).
REFERENCIAS
- Global Burden of Disease Cancer Collaboration. “The Global Burden of Cancer 2013.” JAMA oncology4 (2015): 505–527.
- MS/INCA. Estimativa 2016: Incidência de Câncer no Brasil/ Instituto Nacional de Câncer José Alencar Gomes da Silva, Coordenação de prevenção e vigilância. Rio de Janeiro: INCA, 2015. ISBN 978-85-7318-283-5, acessado em inca.gov.br/estimativa/2016/estimativa-2016-v11.pdf
- Zhou M, Tang Z, Li J, Fan J H, Pang Y, et al; Clinical and Pathologic Features of Multifocal and Multicentric Breast Cancer in Chinese Women: A Retrospective Cohort Study. Journal of Breast Cancer. 2013;16(1):77-83.
- Salgado R, Aftimos P, Sotiriou C, Desmedt C; Evolving paradigms in multifocal breast cancer. Semin Cancer Biol. 2015 Apr; 31:111-8.
- Lynch S P, Lei X, Chavez-MacGregor M, Hsu L, Meric-Bernstam F, et al; Multifocality and multicentricity in breast cancer and survival outcomes. Annals of Oncology 2012, 23: 3063–3069
- Lynch S P, Lei X, Hsu L, Meric-Bernstam F, Buchholz T A, et al; Breast Cancer Multifocality and Multicentricity and Locoregional Recurrence. The Oncologist 2013, 18:1167-1173.
- Fitzgibbons P L, Bose S, Chen Y, Connolly J L, Baca M E et al. Protocol for the examination of specimens from patients with invasive carcinoma of the breast. Version Invasivebreast 4.0.0.0 June 2017 cap.org/cancerprotocols 2017 College of American Pathologists (CAP)
- Weissenbacher T M, Zschage M, Janni W, Jeschke U, Dimpfl T, et al; Multicentric and multifocal versus unifocal breast cancer: is the tumor-node-metastasis classification justified? Breast Cancer Res Treat (2010) 122:27–34
- Buggi F, Folli S, Curcio A, Casadei-Giunchi D, Rocca A, et al; Multicentric/multifocal breast cancer with a single histotype: is the biological characterization of all individual foci justified? Annals of Oncology 2012 23: 2042–2046
- Chagas C R, et al. Tratado de Mastologia da SBM – Rio de Janeiro : Revinter, 2011. ISBN 978853720346-0
- Boros M, Podoleanu C, Georgescu R, Moldovan C, Molna C, et al; Multifocal/multicentric breast carcinomas showing intertumoral heterogeneity: a comparison of histological tumor and lymph node metastasis. Pol J Pathol 2015; (2): 125-132.
- Neri A, Marrelli D, Megha T, Bettarini F, Tacchini D, et al. “Clinical significance of multifocal and multicentric breast cancers and choice of surgical treatment: a retrospective study on a series of 1158 cases.” BMC Surgery. 2015;15(1):1.
- Kadioğlu H, Özbaş S, Akcan A, Soyder A, Soylu L, et al. Comparison of the histopathology and prognosis of bilateral versus unilateral multifocal multicentric breast cancers. World Journal of Surgical Oncology. 2014; 12:266.
- Vera-Badillo F E, Napoleone M, Ocana A, Templeton A J, Seruga B, et al.; Effect of multifocality and multicentricity on outcome in early stage breast cancer: a systematic review and meta-analysis. BreastCancer Res Treat 2014; 146: 235-244.
- Batiston A P, Tamaki E M, Souza L A, Santos M L M. ; Conhecimento e prática sobre os fatores de risco para o câncer de mama entre mulheres de 40 a 69 anos. RevBras Saúde MaternInfant, Recife; 2011; 11 (2): 163-171.
- Lannin D R, Mathews H F, Mitchell J; Influence of socioeconomic and cultural factors on racial differences in late stage presentation of breast cancer. JAMA. 1998; 279 (22): 1801-1807.
- Yerushalmi R, Kennecke H, Woods R, Olivotto I A, Speers C, et al. Does multicentric/multifocal breast cancer differ from unifocal breast cancer? An analysis of survival and contralateral breast cancer incidence. Breast Cancer Res Treat (2009) 117: 365.
- Coombs J, Boyages J; Multifocal and multicentric breast cancer: does each focus matter? J ClinOncol 2005; 23: 7497-7502.
- M, Marian. C, Moldovan. C, Stolnicu. S, Morphological heterogeneity of the simultaneous ipsilateral invasive tumor foci in breast carcinoma: A retrospective study of 418 cases of carcinomas, In Pathology – Research and Practice, 2012, (208): 604-609, ISSN 0344-0338.
- Curigliano G, Burstein H J, Winer E, Gnant M, Dubsky P, et al. De-escalating and escalating treatments for early-stage breast cancer: the St. Gallen International Expert Consensus Conference on the Primary Therapy of Early Breast Cancer 2017. Ann Oncol.2017 Aug 1;28(8):1700-1712.
- Choi Y, Kim E J, Seol H, Lee H E, Jang M J, et al. The hormone receptor, human epidermal growth factor receptor 2, and molecular subtype status of individual tumor foci in multifocal/multicentric invasive ductal carcinoma of breast. Hum Pathol.2012 Jan;43(1):48-55.
- Pekar, G., Gere, M., Tarjan, M., Hellberg, D. and Tot, T., Molecular phenotype of the foci in multifocal invasive breast carcinomas: Intertumoral heterogeneity is related to shorter survival and may influence the choice of therapy. Cancer, 2014 Jan 1; 120 (1): 26–34.
- Review C, Communication S, Principles G. World Medical Association Declaration of Helsinki: ethical principles for medical research involving human subjects. JAMA. 2013;310:2191-2194.
APÉNDICE – CIFRAS Y TABLAS EN INGLÉS
1 Carta de flujo de selección de participantes
TABLA 1 – Incidencia de cáncer de mama unifocal, multifocal y multicéntrico en el Hospital Baron de Lucena (HBL) y Prof. Instituto Fernando Figueira Madre e Hijo (IMIP). Recife
| Cáncer de mama | n (HBL/IMIP) | % (HBL/IMIP) |
| 2012 | ||
| Unifocal | (195/-) | (92.4/-) |
| MC/MF | (16/-) | (7.6/-) |
| 2013 | ||
| Unifocal | 477 (184/293) | 95.9 (93.4/ 97.7) |
| MC/MF | 20 (13/7) | 4.0 (6.6/ 2.3) |
| 2014 | ||
| Unifocal | (150/-) | (92.6/-) |
| MC/MF | (12/ 12) | (7.4/-) |
| 2015 | ||
| Unifocal | 523 (162/361) | 94.9 (89.5/ 97.6) |
| MC/MF | 28 (19/ 9) | 5.0 (10.5/ 2.4) |
IMIP data for 2012 and 2014 are not available. Source: IMIP/HBL research
TABLE 2 – Characteristics of patients with multifocal and multicentric breast cancer operated at the Barão de Lucena Hospital (HBL) and Prof. Fernando Figueira Mother and Child Institute (IMIP). Recife, Pernambuco
| Variables | n | % |
| Age | ||
| <50 | 26 | 29.2 |
| ≥50 | 57 | 64.1 |
| Skin color | ||
| White | 16 | 18.0 |
| Black | 2 | 2.2 |
| Mixed race black | 30 | 33.7 |
| Schooling | ||
| Illiterate | 6 | 6.7 |
| Incomplete elementary school | 22 | 24.7 |
| Complete elementary school | 6 | 6.7 |
| Incomplete high school | 1 | 1.1 |
| Complete high school | 12 | 13.5 |
| Estado civil | ||
| Sindicato civil | 1 | 1.1 |
| soltero | 8 | 9.0 |
| Casado, Año Nuevo | 13 | 14.6 |
| Divorced | 3 | 3.4 |
| Widowed | 9 | 10.1 |
Data not reported for each variable were omitted from the table. Source: IMIP/HBL research
TABLE 3 – Clinical and tumor characteristics of patients with multifocal and multicentric breast cancer operated at the Barão de Lucena Hospital (HBL) and Prof. Fernando Figueira Mother and Child Institute (IMIP). Recife, Pernambuco
| Variables | n | % |
| ER | ||
| Positive | 40 | 44.9 |
| Negative | 20 | 22.5 |
| PR | ||
| Positive | 35 | 39.3 |
| Negative | 25 | 28.1 |
| HER2 | ||
| Positive | 18 | 20.2 |
| Negative | 36 | 40.5 |
| Ki67 | ||
| <14% | 16 | 18.0 |
| >14% | 37 | 41.6 |
| Compromised lymph nodes | ||
| Absent | 23 | 25.8 |
| 1 to 3 | 18 | 20.2 |
| 4 or more | 20 | 22.5 |
| Histological grade | ||
| I | 9 | 10.1 |
| II | 27 | 30.4 |
| III | 13 | 14.6 |
| Histological type | ||
| Ductal | 73 | 82.0 |
| Lobular | 1 | 1.1 |
| Others | 4 | 4.5 |
| Size of the largest tumor | ||
| <2 cm | 24 | 27.0 |
| 2-5 cm | 32 | 36.0 |
| >5 cm | 5 | 5.6 |
| Distant metastasis | ||
| Yes | 9 | 10.1 |
| No | 48 | 53.9 |
| Lymphovascular invasion | ||
| Yes | 20 | 22.5 |
| No | 24 | 27.0 |
| Heterogeneity between foci | ||
| Yes | 8 | 9.0 |
| No | 17 | 19.1 |
| Distance between foci | ||
| ≤ 4 cm (multifocal) | 58 | 65.2 |
| > 4 cm (multicentric) | 15 | 16.9 |
Data not reported for each variable were omitted from the table. ER: Estrogen receptor PR: Progesterone receptor. Source: IMIP/HBL research
TABLE 4 – Clinical and tumor characteristics of patients with multifocal/multicentric breast cancer operated at the Barão de Lucena Hospital (HBL) and Prof. Fernando Figueira Mother and Child Institute (IMIP), in relation to heterogeneity between foci. Recife, Pernambuco
| Heterogeneity between foci | |||
| Variables | Yes | No | p-value |
| n (%) | n (%) | ||
| Compromised lymph nodes | |||
| Absent | 2 (40.0) | 3 (60.0) | 1.000 * |
| 1 to 3 | 2 (33.3) | 4 (66.7) | |
| 4 or more | 3 (50.0) | 3 (50.0) | |
| Histological grade | |||
| I | 2 (66.7) | 1 (33.3) | 0.748 * |
| II | 2 (25.0) | 6 (75.0) | |
| III | 1 (33.3) | 2 (66.7) | |
| Size of the largest tumor | |||
| <2 cm | 4 (57.1) | 3 (42.9) | 0.510 * |
| 2-5 cm | 3 (33.3) | 6 (66.7) | |
| >5 cm | 0 (0.0) | 2 (100.0) | |
| Distant metastasis | |||
| Yes | 1 (20.0) | 4 (80.0) | 0.588 * |
| No | 5 (45.5) | 6 (54.5) | |
| Lymphovascular invasion | |||
| Yes | 4 (57.1) | 3 (42.9) | 0.592 * |
| No | 2 (28.6) | 5 (71.4) | |
(*) Fisher’s Exact Test. Source: IMIP/HBL research
TABLE 5 – Clinical and tumor characteristics of patients with multifocal and multicentric breast cancer operated at the Barão de Lucena Hospital (HBL) and Prof. Fernando Figueira Mother and Child Institute (IMIP). Recife, Pernambuco
| Distance between foci | |||
| Variables | ≤4 cm (multifocal) | >4 cm (multicentric) | p-value |
| n (%) | n (%) | ||
| ER | |||
| Positive | 29 (80.6) | 7 (19.4) | 1.000 * |
| Negative | 12 (80.0) | 3 (20.0) | |
| PR | |||
| Positive | 26 (81.3) | 6 (18.7) | 1.000 * |
| Negative | 15 (78.9) | 4 (21.1) | |
| HER2 | |||
| Positive | 14 (82.4) | 3 (17.6) | 0.723 * |
| Negative | 22 (75.9) | 7 (24.1) | |
| Ki67 | |||
| <14% | 13 (86.7) | 2 (13.3) | 0.695 * |
| >14% | 22 (75.9) | 7 (24.1) | |
| Compromised lymph nodes | |||
| Absent | 16 (84.2) | 3 (15.8) | 0.839 * |
| 1 to 3 | 11 (73.3) | 4 (26.7) | |
| 4 or more | 16 (80.0) | 4 (20.0) | |
| Histological grade | |||
| I | 6 (66.7) | 3 (33.3) | 0.440 * |
| II | 20 (87.0) | 3 (13.0) | |
| III | 9 (81.8) | 2 (18.2) | |
| Histological type | |||
| Ductal | 49 (80.3) | 12 (19.7) | 0.370 * |
| Lobular | 1 (100.0) | 0 (0.0) | |
| Others | 2 (50.0) | 2 (50.0) | |
| Size of the largest tumor | |||
| <2 cm | 19 (79.2) | 5 (20.8) | 0.884 * |
| 2-5 cm | 20 (76.9) | 6 (23.1) | |
| >5 cm | 2 (66.7) | 1 (33.3) | |
| Distant metastasis | |||
| Yes | 5 (62.5) | 3 (37.5) | 0.331 * |
| No | 35 (83.3) | 7 (16.7) | |
| Lymphovascular invasion | |||
| Yes | 13 (72.2) | 5 (27.8) | 0.256 * |
| No | 21 (87.5) | 3 (12.5) | |
(*) Fisher’s Exact Test. Source: IMIP/HBL research
[1] Máster en salud maternoinfantil por el programa de posgrado stricto sensu del Instituto de Medicina Integral Profesor Fernando Figueira – IMIP, Pernambuco.
[2] Doctor en Tocoginecología por la Universidad Estatal de Campinas, Brasil.
[3] Máster en Oncología por la Universidad de Sao Paulo, Brasil.
Enviado: Febrero de 2020.
Aprobado: Junio de 2020.