ОБЗОРНАЯ СТАТЬЯ
CARNEIRO, Renato Brandi Pereira [1], KFOURI, Flávio de Ávila [2]
CARNEIRO, Renato Brandi Pereira. KFOURI, Flávio de Ávila. Мембраны D-Ptfe Cytoplast® в управляемой регенерации кости в имплантологии. Revista Científica Multidisciplinar Núcleo do Conhecimento. 05-й год, Эд. 09, Vol. 05, стр. 108-135. Сентябрь 2020 года. ISSN: 2448-0959, Ссылка доступа: https://www.nucleodoconhecimento.com.br/лечение-зубов/регенерации-кости, DOI: 10.32749/nucleodoconhecimento.com.br/ru/70943
РЕЗЮМЕ
Вертикальное увеличение кости в альвеолярном гребне важно для получения хороших результатов при реабилитации протезами на имплантатах. В этом библиографическом обзоре проводился поиск статей, посвященных увеличению костной ткани в альвеолярных краях с использованием мембран Cytoplast® с целью оценки устойчивости к проникновению бактерий и способности создавать и поддерживать пространство. Для этого был проведен обзор литературы на поисковых платформах Pubmed и Google scholar. Анализируемые исследования показали аналогичные результаты между мембраной из d-PTFE, титановыми сетками и мембранами из e-PTFE, как в отношении увеличения костной массы, так и в отношении качества кости. Способность сохранять пространство была очевидна в изделиях, в которых использовалась мембрана, армированная титаном. Мембрана из d-PTFE показала большую способность к воздействию окружающей среды полости рта без ущерба для материала трансплантата. Авторы исследования в этом исследовании обнаружили, что мембраны d-PTFE, армированные титаном для увеличения костной ткани альвеолярных краев, являются жизнеспособными и допускают определенный период воздействия среды полости рта без загрязнения трансплантата. Необходимы дальнейшие исследования мембраны Cytoplast® d-PTFE для изучения ее характеристик при процедурах вертикального наращивания кости.
Ключевые слова: Искусственные мембраны, регенерация управляемых тканей, регенерация костей.
1. ВВЕДЕНИЕ
Имплантология произвела революцию в стоматологии, позволив искусственно восстановить отсутствие зубного органа. Часто имплантодонт, планируя реабилитацию с помощью имплантатов, сталкивается с небольшой высотой или шириной оставшегося альвеолярного гребня, что препятствует идеальному позиционированию имплантатов в соответствии с выполненным ретроградным планированием, и для продолжения планирования можно использовать технику регенерации. управляемая кость (GBR) для увеличения костной ткани в области установки имплантатов.
4 биологических принципа, необходимых для успеха в управляемой регенерации костей (т.е. PAEE) являются: “(i) первичное закрытие раны; ii) ангиогенез для обеспечения необходимого кровоснабжения; iii) создание и поддержание пространства и (iv) устойчивость ран” (WANG; BOYAPATI, 2006, стр. 8-11)
Urban et al. (2016) описал технику лоскута, где происходит высвобождение периотеума, сделанного с периосомными и радиальными разрезами и лоскутным продвижением с рывками в коронаном направлении, значительно увеличивающий поверхность лоскута, позволяющий заполнять биоматериал и получать первичное закрытие раны.
Исследователи отметили, что если мембрана не подвергается воздействию и остается без событий в течение 6 до 9 месяцев, полное формирование костей получается и что, когда есть сбой, чаще всего это было из-за воздействия мембраны и последующего загрязнения трансплантата. (CUCCHI et al., 2017)
Urban et al., (2017) подчеркнул, что мембрана должна быть закреплена языком и вестибулярными винтами, чтобы она была неподвижной во время вертикального процесса GBR.
Исследователи описали 5 характеристик мембраны для вертикальной управляемой регенерации костей: “(i) Биосовместимость; ii) создание и содержание пространства; iii) инклюзивность и избирательная проницаемость; iv) интеграция тканей; v) возможности клинического управления”. (NAUNG; SHEHATA; VAN SICKELS, 2019, стр. 2)
Многие мембраны были предложены для GBR, как абсорбируемые и неаспасимые и может быть коллагена, человеческой плаценты, человеческого перикардия, сухожилия человека, из полигликолевой кислоты, полилактической кислоты, расширенной или плотной полиэтиленовой и титановой сетки. (NAUNG; SHEHATA; VAN SICKELS, 2019)
Lee et al. (2020) проанализировали влияние L-PRF в качестве мембраны на горизонтальный GBR в альвеолах, приподнятых у собак, через 4 недели сравнили результаты L-PRF с другими абсорбируемыми и неабсорбируемыми мембранами. После еще 4 недель заживления кости новое количество кости для каждой группы измеряли с помощью микроскопии и микрокомпьютерной томографии, подтверждая, что L-PRF играет эффективную роль в качестве мембраны для бокового увеличения гребня.
Salomão et al. (2010) сообщили о двух случаях использования полипропиленового барьера (Bone Heal® – INP, São Paulo) без ассоциации любого наполнителя (трансплантат или биоматериал имплантата), был использован для того, чтобы сохранить сгусток в ловушке для того, чтобы восстановить альвеолярной архитектуры края и содействовать неоформации костей, с тем чтобы обеспечить надлежащую установку остеоинтегрируемого имплантата. Перед тем, как поставить барьер, альвеоло стимулировали быть полностью заполнены кровью.
Неаспасаемые мембраны при воздействии имеют более высокий уровень инфицирования, чем абсорбируемые мембраны. Плотная мембрана PTFE предотвращает прохождение бактерий даже при воздействии хлоргексидина для полоскания рта (0.12%) и применение хлоргексидина гель (1%). (GHENSI et al., 2017)
Патент US7296998B2 2007 года описывает лист гидрофильных политетрафторэтиленового полиэтилена (PTFE) полимерного материала, который существенно нерасширяется, имеет полости, которые имеют глубину меньше, чем толщина листа. (CHADDICK; BARTEE, 2007).
2. ПРЕДЛОЖЕНИЕ
Целью данного исследования является обзор последней литературы об использовании мембраны d-PTFE (Cytoplast® остеогенная биомедицинская, Техас) в управляемой регенерации костей в имплантодонтии, обращаясь к ее устойчивости к проникновению бактерий и ее способности поддерживать пространство.
3. ОБЗОР ЛИТЕРАТУРЫ
Barber et al. (2007) сообщили о двух случаях GBR с одновременной установкой имплантата и d-PTFE мембранного покрытия (Cytoplast® Regentex GBR-200 или TXT-200 остеогенной биомедицинской, Лаббок, TX) без подкрепления. Он сообщил о технике GBR, где он оставил мембрану подвергается без разоблачения края в течение 6 недель в случае извлечения и немедленной имплантации верхней 1-й премоляра. Во втором случае доклада, травма аварии поддерживается Цитопласт Cytoplast® в течение 4 недель, легко удаления и получения последовательного слоя остоидной ткани при размещении имплантатов в передней челюстной области 5 элементов без осложнений и эпителиальной миграции произошло на остоидной ткани в неделю 6, увеличивая ширину кератинизированной ткани до травмы пострадали. Barber et al. (2007) отметил, что “плотность мембраны d-PTFE предотвращает колонизацию флоры-хозяина и предотвращает загрязнение биоматериала под мембраной”. Он также заметил, что с помощью этой техники кератинизированная слизистая оболочка заживает вторым намерением, заканчивая ее закрытие большей площадью. Пришел к выводу, что, поскольку первичное закрытие мембраны d-PTFE не является необходимым, хирург может лечить большие дефекты, сохранять межзубчатые сосоцы и сохранять всю ширину кератинизированной слизистой оболочки, без беспокойства загрязнения или бактериальной инфекции, а также что использование цитопласта d-PTFE Cytoplast® является идеальным вариантом лечения альвеол экзодонтии без первичного закрытия раны , благодаря простоте в его размещении и удалении без ущерба для качества регенерации. (BARBER et al., 2007)
Hoffmann et al. (2008) исследовал клиническую регенерацию альвеолос экзодонтии, используя d-PTFE мембраны, без использования трансплантатного материала, для этой цели, оценили 276 альвеол экзодонтий в 276 человек (151 мужчин и 125 женщин; средний возраст, 50,2 лет; возраст: от 24 до 73 лет). Процент костной массы, полученной после GBR с использованием цитопластовой мембраны, Cytoplast®, без использования первичного закрытия раны. Перед извлечением он сделал персонализированное руководство, которое может быть закреплено на соседние зубы с пятью отверстиями, где через пародонтальный зонд может получить измерения глубины альвеоло после извлечения. После экстракции закрылки были повышены, а на местную добычу была помещена мембрана d-PTFE (Cytoplast® Regentex GBR-200) без титанового подкрепления. Заслонки были перемещены и закинули на месте. Первичное замыкание на мембранах не было получено. Мембраны были удалены через 4 месяца. В качестве ориентиров использовались цементно-эмалированные соединения соседних зубов. Измерения были проведены с помощью руководства, после извлечения и 12 месяцев после операции в тех же областях, переменные, описанные на уровне костей были зарегистрированы индивидуально для всех рассмотренных случаев, а также в группах по факторам интереса исследованы: один альвеоло или бок о бок, челюсти, и регион, увеличение костной ткани в вертикальных дефектов были выражены в среде и по-прежнему выполняется 10 биопсии твердых тканей 12 месяцев после сохранения альвеоло во время размещения имплантата, получая в результате значительное увеличение костного ядра образцов, значительную регенерацию объема альвеолоса, которую можно было наблюдать по гистологической оценке, указывая, что новообразованная ткань на местах извлечения была в основном костной. Он не обнаружил влияния пола, курения < 10 сигарет, возраста или клинического уровня костей на процент увеличения костной ткани. Она пришла к выводу, что использование мембраны Cytoplast d-PTFE® привело к сохранению мягких и твердых тканей на участках экзодонтии.
Что касается рандомизированных клинических испытаний, в соответствии с 2010 CONSORT заявление (SCHULZ; ALTMAN et al., 2010):
При правильном планировании, проведении и отчетности они представляют собой золотой стандарт оценки медицинских вмешательств. Чтобы точно оценить исследование, читатели опубликованного отчета нуждаются в полной, четкой и прозрачной информации о его методе, технологии и результатах. Таким образом, состояние CONSORT 2010 соответствует минимальным критериям, хотя это не должно препятствовать авторам включать другую информацию, если они считают ее важной (SCHULZ; ALTMAN, et al., 2010, стр. 698).
Urban et al. (2014) оценили использование мембраны из d-PTFE (Cytoplast ® Ti-250), армированной титаном, в сочетании со смесью аутогенной кости и BioOss®, чтобы выполнить двадцать вертикальных увеличений альвеолярного гребня с использованием армированной мембраны из d-PTFE. с Cytoplast® Ti-250 Osteogenics Biomedical titanium, фиксируется титановыми костными кнопками Master Pin Control®, винтами для палатки Messinger и / или Pro-Fix Tentin Screw®, Osteogenics Biomedical и смесью аутологичной кости и Biooss® в соотношении 1: 1 и закрытие без натяжения двойным швом горизонтального и простого матраса, обнажения мембраны не было. В результате они получили средний прирост кости 5,45 мм и стандартное отклонение 1,93. Гистология показала, что частицы Biooss® «были связаны с густой сетью вновь сформированной кости, во всех образцах костномозговое пространство было хорошо перфузировано кровеносными сосудами, и не наблюдалось воспалительной реакции или реакции на инородное тело». (URBAN et al., 2017). Они пришли к выводу, что использование мембраны Cytoplast® Ti-200 возможно для техники увеличения вертикального альвеолярного гребня с помощью аутологичной кости плюс Biooss® 1: 1 и закрытия раны без натяжения без обнажения мембраны.
Ronda et al. (2014) провели проспективное и рандомизированное контролируемое исследование, предназначенное для тестирования мембран d-PTFE Cytoplast® Ti-250 и e-PTFE Goretex®, армированных титаном, связанного с аутологичной костью, и алло-наполненных минерализованных гранул (Puros®, Zimmer Dental, Carlsbad CA, USA), 1: 1 из 23 пациентов, которым потребовалось вертикальное наращивание кости альвеолярного гребня с помощью процедур GBR для установки имплантата в задние атрофированные нижние челюсти (доступная высота кости <7 мм). Имплантаты были размещены на запланированном уровне, оставляя видимые повороты, которые были покрыты биоматериалом трансплантата, и только после этого была рандомизирована мембрана, которую использовал хирург. Ушивание раны проводилось без натяжения двойным швом. Результаты показали, что не было значительной разницы между процентами прироста костной массы в двух группах. Две биопсии, собранные во время процедуры удаления мембраны, показали две области: «одна из хорошо организованной пластинчатой кости, а другая с небольшими промежутками, в которых находятся остеоциты, и коронковая часть, характеризующаяся в основном костной тканью, состоящей из небольших и незрелых трабекул». (RONDA et al., 2014, с. 863). Они пришли к выводу, что мембраны из d-PTFE и e-PTFE показали идентичные клинические результаты при лечении вертикальных костных дефектов вокруг имплантатов с использованием этой техники и что процедуру удаления мембраны было легче выполнить в группе d-PTFE, чем что в группе e-PTFE, приписываемой пористости внешнего слоя, который прилипает к соединительной ткани, Ronda et al. (2014) указали, что «хотя наличие пористой части одной из мембран, по-видимому, играет важную роль в стабилизации устройства, способствуя его интеграции с мягкими тканями, оно, по-видимому, не было существенным для достижения регенерации кости.».
Maridati et al. (2016) предложили и протестировали управление воздействием мембраны d-PTFE Cytoplast® для достижения окончательного клинического успеха, сообщили о случае процедуры вертикального наращивания костной ткани альвеолярного гребня, у 63-летнего пациента, где он установил имплантат размером 3,4 x 11 мм, оставив несколько витков и гладкую сторону имплантата открытыми, заполнил его Biooss® и адаптировал мембрану, армированную титановой фиксацией Cytoplast® с 4 штифтами, после чего обнажил мембрану d-PTFE. , хотя рана была закрыта без натяжения. На 14-й день обнаружено воздействие> 3 мм без признаков инфекции. Мембрану оставили на месте еще на две недели. На 4-й неделе была удалена мембрана и был установлен соединительный трансплантат с неба для защиты костного трансплантата на 7-м месяце. Основываясь на том факте, что мембрана Cytoplast имеет высокую плотность и размер пор меньше 0,2-0,3 микрометра, и поскольку она уже была протестирована в лунке после экстракции без первичного закрытия раны без натяжения, это исследование дало хорошие результаты после обнажение мембраны> 3 мм и последующая пересадка соединительной ткани при удалении мембраны. Они пришли к выводу, что наблюдение за воздействием мембраны без ее удаления в течение 4 недель гарантирует сохранение необходимого пространства из-за устойчивости мембраны к бактериальному заражению.
Ghensi et al. (2017) продемонстрировали, что можно управлять воздействием мембраны Cytoplast® d-PTFE. В своем отчете о клиническом случае они наблюдали воздействие <3 мм мембраны d-PTFE, усиленной аутогенным трансплантатом и BioOss® 1: 1. Больше шурупов, первичное закрытие раны с высвобождением надкостницы без натяжения было получено через 14 дней при мембрана была обнажена, однако было доказательство эпителиального уплотнения на пораженном участке без ослабления зонда или нагноения. Проблема была решена продолжением полоскания рта хлоргексидином (0,12%), нанесением геля хлоргексидина с концентрацией 1% два раза в день до повторного открытия и удалением любого налета один раз в неделю в кабинете, где он следил. 4 месяца до удаления, заполнение вертикального дефекта в области удаления премоляра и первого моляра. Когда участок был повторно открыт, исходный дефект, казалось, был заполнен, поэтому два имплантата (CLC Conic; CLC Scientific, Виченца, Италия), соответственно 4 × 10 мм и 5 × 6 мм, были вставлены в положения первого пре- молярное и молярное положение. Они заметили, что благодаря неабсорбируемым мембранам из d-PTFE, имеющим поры диаметром 0,2 мкм, они предотвращают бактериальную инфильтрацию и, даже если мембрана обнажена, риск осложнений и инфекций намного ниже, чем в e- ПТФЭ. Это делает первичное закрытие мягких тканей важным, но не строго необходимым, поскольку мембрана действует как непроницаемый барьер для пищи и бактерий, и был сделан вывод о том, что обнажением мембраны d-PTFE можно управлять с помощью тщательного знания используемых материалов и адекватная гигиена полости рта.
Cucchi et al. (2017) оценили скорость осложнений и вертикальное увеличение костной ткани после GBR с мембраной Cytoplast® Ti-250, усиленной титаном по сравнению с титановой сеткой, покрытой коллагеновой абсорбируемой мембраной. Несравненный вертикальный прирост костей и осложнения после GBR в атрофических задних челюстях с мембраной Cytoplast® Ti-250XL и титановой сеткой задних челюстей, с размещением имплантатов в 1 стадии, проанализировали 39 частично беззубых пациентов с атрофической задней челюстью, случайно разделенных на две группы: 20 пациентов лечились одноступенчатой GBR, т.е. с размещением имплантатов одновременно. , использовали корковые перфорации, чтобы ангиогенез и смесь аутогенной кости и алотрансплантата (EnCore®, Osteogenics, Biomedical, Lubbock, Texas), только в это время хирург получил мембраны, которые будут использоваться случайным образом, d-PTFE (группа А) и титановой сетки покрыты сетчатые коллагеновые мембраны (группа B), 19 пациентов, первоначально было 40, но 1 пациент этой группы бежали, были зафиксированы с мини винты и первичное закрытие раны без напряжения с двойной горизонтальной и вертикальной шва. Все осложнения были зарегистрированы, различая “хирургическое” и “исцеление” и между “незначительным” или “основным”. Была также оценена стабильность первичного имплантата и вертикальное увеличение костной ткани. Получено в результате: В группе А показатели хирургических осложнений, в этих случаях, временная парестезия аментуального нерва и заживление составили 5,0% и 15,0%, соответственно, в группе В показатели хирургических и лечебных осложнений составили 15,8% и 21,1% соответственно, следовали в течение 9 месяцев до удаления мембран. Увеличение костной ткани измерялось с помощью пародонтального зонда с делением 1 мм и степенью точности измерения 0,5 мм, которые измерялись от плеча имплантата до кости, перед заполнением биоматериалом устным, лингвинным, мезиальным и дистальным, в каждом имплантате и после регенерации проводились новые измерения. И они пришли к выводу, что предварительные результаты этого рандомизированного контролируемого исследования показали, что мембраны d-PTFE и титановые сетки, покрытые коллагеновой мембраной, дали аналогичные результаты как по скорости, так и по типам с точки зрения лечебных осложнений. В отличие от этого, d-PTFE мембраны показали более низкий средний уровень хирургических осложнений. Аналогичный вертикальный прирост костей и формирование костей были достигнуты в обеих группах.
Herzberg (2017) описал 10 случаев вертикального увеличения кости в альвеолярном гребне в области зуба, поскольку это критическая область из-за зубов, прилегающих к области трансплантата, а небольшой лоскут сложнее приспособиться к достигнутому увеличению 3D. Он сделал внутрисосудистый разрез, доходящий до двух соседних зубов и проходящий через гребень, и 10-миллиметровый мезиальный релаксант, за исключением случаев, когда увеличение было передним, тогда релаксант вводился в задней части разреза. Установлен имплантат у семи пациентов, и у троих уже были имплантаты, с трансплантацией смеси аутогенной кости с аллотрансплантатом (Raptos®, Citagenix) 1: 1 и покрытой усиленной мембраной d-PTFE (Cytoplast® Ti-250AS, Osteogenics) путем разрезания и адаптация и фиксация с помощью саморезов (Pro-Fix PFMF®, Osteogenics) и коллагеновой мембраны (Remaix®) были помещены поверх мембраны d-PTFE и закрыли рану без натяжения. Через 6 месяцев мембраны d-PTFE не было обнажено, поэтому он удалил мембрану, и из 10 пациентов один потерял трансплантат, двое потеряли 0,5 мм, а один потерял 1 мм, остальные были успешными без потерь. Он заметил, что этот метод является надежным, и в своих ссылках упоминает, что это обычное явление для физиологической потери костной массы от 0,47 до 1,16 мм в течение первого года при вертикальной процедуре GBR с использованием мембран PFTE, что может быть связано с резорбцией незрелой кости в наиболее коронарной части. регенерированной кости, предпочитая установку имплантата во второй операции, чтобы ее можно было исправить в этот второй момент. Он также приписывает успешность закрытию хирургической раны, которая в случаях небольших областей предлагает меньший лоскут, который труднее приспособить к более высокой среде. Он пришел к выводу, что вертикальный ROG в области 1 зубного элемента с использованием мембраны Cytoplast является надежным лечением.
Hassan et al. (2017) в своем рандомизированном исследовании сплит-рот сравнил мембрану человеческого амния/корио (MAC) с мембраной Cytoplast® из 22 альвеоло из 9 участников в аспектах: количество сохранения размеров альвеолярного хребта, Следуя процедурам сохранения хребта, т.е. вертикальному изменению высоты хребта в миллиметрах, для этого они построили радиографический стент с радиопакетной эталонной плоскостью с 5 отверстиями, которые можно использовать с помощью миллиметрового зонда и измерения по томографии, были сделаны измерения профессионалом, который не знал о цели исследования после отходов и через 3,5 месяца после того, как отходы и данные были использованы для статистического анализа. Он также оценил качество костей, собирая образцы регенерированных костей для гистологического и гистоморфометрического анализа и дискомфорта через шкалу VAS. Рандомизация проводилась на той же стороне или вправо и влево. Результаты были: Среднее горизонтальное увеличение на 2,54 (1,29) и 2,72 (1,01) для MAC и Cytoplast® соответственно, следующие с вертикальным средним увеличением: -0,24 (0,91) и 1,18 (2,22) для Cytoplast. Он пришел к выводу, что минерализованная область костей и области мягких тканей не были существенно отличаются между двумя лечения. Mac сайты были значительно ниже послеоперационных VAS баллов по сравнению с d-PTFE. Mac подвергается намеренно одинаково эффективен в сохранении гребня по сравнению с d-PTFE. Кроме того, использование MAC может помочь уменьшить баллы VAS в послеоперационный период и потенциально привести к улучшению качества костей, доступных для размещения имплантатов, о чем свидетельствует улучшение гистоморфометрических измерений.
Trobos et al. (2018) в своей работе с культурами in vitro оценили барьерную функцию мембран Cytoplast®TXT200 d-PTFE и NeoGen® e-PTFE против бактерий в течение 2, 12 и 48 часов. В его эксперименте использовались пробирки с адаптированными мембранами, которые позволяли контактировать стерильный супернатант с внутренней поверхностью мембраны, а культура S. oralis контактировала с внешней поверхностью и при анализе супернатанта в культуральной среде агара с лошадиной кровью. Сбор материала изнутри мембраны после 48 часов эксперимента при 37 ° C в анаэробных условиях и отсутствие бактерий ни внутри мембран, ни в супернатанте, контактирующем с мембранами. Однако d-PTFE способствовал образованию большего количества биопленки S. oralis по сравнению с титаном и e-PTFE после промывки сывороткой снаружи. Они пришли к выводу, что все мембраны из PTFE являются эффективными барьерами против проникновения бактерий in vitro.
Gallo; Díaz-Báez (2019) с целью описания управления осложнений, таких как воздействие и инфекции после вертикальной и горизонтальной GBR с мембраны Cytoplast®. Использование нового протокола управления осложнениями сообщили для этого типа мембраны. Для этого они оценили осложнения в регенерации костей, выполняемые с мембраной d-PTFE, усиленной титаном Cytoplast Ti-250, Остеогенная биомедицинская в период с 2000 по 2017 год из 80 случаев, которые имели осложнения и лечение случаев мембранного воздействия меньше или равна 3 мм без инфекции и после 2 месяцев операции, сохраняя в течение 9 месяцев мониторинг гигиены пациента еженедельно путем очистки с хлоргексидином и рекомендации небольшой мембраны чистки и применения хлоргексидина в гель, чтобы предотвратить накопление воздействие появилось до этого мембраны поддерживается в течение 6 до 8 недель, после того же протокола гигиены, а затем удалены. Когда было сообщение о боли и гноя, решили немедленно удалить и вылечить гранулематозные ткани и держать ткани трудно, пациенты были лекарства с (амоксициллин / ac. Клавуланич 1г 12/12ч). Секстантом с наибольшим количеством осложнений была передняя челюстная челюсть (43,75%), за которой следовала левая челюсть (20%). 70% случаев появились через 2 месяца. Он пришел к выводу, что этот протокол управления осложнениями, который был предложен на основе 80 осложнений, может помочь предотвратить потерю всего трансплантата и что инфекция является основным осложнением, которое вызывает потерю трансплантата. Она пришла к выводу, что предлагаемый новый протокол управления осложнениями GBR, основанный на 80 наблюдаемых осложнениях, может помочь предотвратить полную потерю трансплантата.
Koidou; Chatzopoulos; Johnson (2019) сообщил, ряд случаев, когда он использовал ретилетированную коллагеновую мембрану на алоэнчерто и на множестве фиксированной мембраны d-PTFE, которая оставалась в течение 6 недель и была атрауматически удалена, когда мембрана d-PTFE была удалена, незрелые соединительной ткани и было отмечено, что она стала кератинизированной резинки 8 недель после экстракции и пришел к выводу, что использование d-PTFE деградации абсорбируемой мембраны и сохраняет ее целостность.
Cucchi et al. (2019) сравнили результаты GBR между мембраной Cytoplast® и титановой сеткой, покрытой мембраной Osseoguard®, провели двойное слепое исследование, в котором сравнивали гистологические и гистоморфометрические результаты костной ткани, взятой из области трансплантата задней нижней челюсти со смесью 1: 1. аутогенной кости и аллотрансплантата (EnCore® Osteogenics Biomedical), произведена декортикализация с использованием в группе A 13 пациентов с мембраной Cytoplast® Ti-250 XL d-PTFE и в группе B, 12 пациентов с сеткой Trinon Titanium®, Карлшур, Германия покрыта коллагеновой мембраной и зафиксирована двумя или тремя винтами mini ProFix®. Прошита двойным горизонтальным и одинарным слоем, получено первичное закрытие, ожидание 9 месяцев. Воздействия не было, образцы фиксировали в забуференном фосфатом формалине с последующим удалением накипи соляной кислотой и муравьиной кислотой, после удаления накипи образцы обезвоживали в сериях градуированных спиртовых ванн и заливали в парафин, затем гистологические срезы окрашивали гематоксилином и эозином. Слайды сканировали (ScanScope CS®, Aperio Tecnologies, Leica Biosystems) при нескольких увеличениях для оценки характеристик сформированной новой кости, оставшегося трансплантата, интеграции трансплантата с новой сформированной костью, мягких тканей и местного воспаления. Костная регенерация в коронковой части была очевидна в обеих группах, и был тесный контакт между трансплантированным материалом и костью, было обнаружено активное костеобразование во всех областях трансплантированной кости, что отражалось высокой плотностью остеоцитов и вновь образованной трабекулята, связанной интенсивная активность остеобластов на фронтах роста костей. Опосредованная остеокластами резорбция была обнаружена рядом с материалом трансплантата, все биопсии содержали клетки соединительной ткани с множеством вен. Трансплантаты были совмещены во всех образцах, воспалительных процессов или иммунологических реакций на участках регенерации не было. Гистоморфометрические данные продемонстрировали, что обе мембраны предотвращают миграцию неостеогенных клеток. В группе А доля костной ткани, трансплантата и мягких тканей составила 39,7%; 8,6%; 52,1% и в группе B 42,1%; 9,6 и 48,3% не обнаружили существенной разницы между группами. Он пришел к выводу, что результаты исследования показали, что GBR с использованием мембраны d-PTFE Cytoplast® или сетки Ti Trinon Titanium® в сочетании с аутогенной костью и аллотрансплантатом дает аналогичные результаты как гистологически, так и хитоморфометрически.
Mertens et al. (2019) протестировали 4 различных метода in vitro для определения стабильности объема дефекта стенки. Группа 1: GBR с коллагеновой мембраной, ксенотрансплантат в виде частиц, Группа 2: GBR с коллагеновой мембраной, ксенотрансплантатом в виде частиц и липучками, Группа 3: GBR с титановой армированной мембраной Cytoplast® Ti-250, ксенотрансплантатом в виде частиц и штифтами, Группа 4 GBR с аутогенный блок, коллагеновая мембрана, ксенотрансплантат из частиц, зарегистрированный с помощью компьютерной томографии и протестированный. Для этого он создал дефекты челюстей свиньи и выполнил процедуры до закрытия лоскута, после чего он разобрал и провел измерения: до и после наложения шва, рассчитал изменение в мм и процентах и в результате обнаружил, что в 4 группах закрытие лоскута привело к уменьшению объема, группы 2, 3, 4 показали лучшие результаты, чем группа 1: коллаген без штифта. Группы 3 и 4 лучше, чем группа 2: коллаген и штифт и группа: 3 d-PTFE лучше, чем группа 4. Они пришли к выводу, что закрытие лоскута оказывает значительное влияние на стабильность трансплантата в дефектах 1 стенки, дополнительная фиксация спицами улучшает стабильность мембраны Ti-d-PTFE, и блок-трансплантат показал большую стабильность, чем коллагеновые мембраны, особенно в плечевой области имплантата, и что дефекты стабилизации стеночного трансплантата даже более важны, чем дефекты в авто контейнеры.
Ibraheem et al. (2020), после RGB с мембраной Cytoplast® с обнажением, которое развилось в период окостенения трансплантата. С этой целью он сообщил о случае увеличения кости с одновременной установкой трех имплантатов в области зубов 35,36,37 с использованием мембраны d-PTFE Cytoplast®, связанной с костью аллотрансплантата LifeNet® Health, Вирджиния-Бич, штат Вирджиния, вокруг обнаженные витки на 3-4,5 мм с щечной стороны, затем завершили слоем BioOss®, после чего зафиксировали мембрану d-PTFE с помощью мини-винтов ProFix®. Через 21 день шов был удален, и было обнажено 3 мм мембраны, пациенту было предписано пропускать повидон-йод два раза в день с ватой, воздействие продолжало увеличиваться, переходя к серьезному расхождению швов на 16-й неделе, но края мембраны не подвергались воздействию, признаков инфекции не было, мембрана была удалена, открыв фиброзную ткань, покрывающую имплантаты. Через 10 недель после удаления мембраны ее снова открыли, и на винтах-заглушках была регенерированная кость. Ядро удаляли трепаном для гистологического анализа и готовили слайды для окрашивания гематоксилином / эозином, которые выявили жизнеспособную плотную кость и интегрированный алло-заполняющий материал вокруг кости. Они пришли к выводу, что мембрана Cytoplast® при обнажении не обязательно приводит к отказу при правильном обращении с короткими интервалами наблюдения.
Mazzucchi et al., (2020) сравнил образцы из верхней и нижней части мембраны d-PTFE по отношению к бактериальным подсчетам двух поверхностей после 28 дней сохранения альвеоло экзодонтий с воздействием устной среды. Микробиологические и микроскопические анализы показали, что количество бактерий присутствовало во внутреннем слое, ниже периалвеолярных гингиальных тканей. Этот вывод показал, что бактерии могут мигрировать через десны, прилипающие к мембране, и колонизировать внутреннюю часть мембраны, находя путь между внешним слоем и десневыми тканями, которые не придерживались гладкой поверхности мембраны d-PTFE. Другая возможность заключается в том, что колонизация происходит во время хирургических процедур: однако, в обоих обстоятельствах, это не повлияло на процесс заживления, вероятно, из-за небольшого количества бактерий, присутствующих на сайте.
4. ОБСУЖДЕНИЕ
Barber et al., (2007) и Ghensi et al., (2017) зарегистрированы случаи GBR экзодонтических альвеоло, которые получили биоматериал и d-PTFE мембраны был использован Cytoplast® в качестве барьера. Barber et al.(2007), умышленно не получить первичное закрытие раны, которая была описана WANG et al. в 2006 году в качестве принципа PASS, утверждая, что ненужным из-за плотности d-PTFE мембраны предотвращения загрязнения биоматериала под мембраной и хранится в течение 6 недель мембраны подвергаются устной среде с гигиеническим мониторингом и пришел к выводу, что первичное закрытие раны является ненужным в своем обсуждении он отметил, что он и его команда не имеют достаточного опыта, чтобы прокомментировать эффективность поддержания мембраны подвергаются более 6 недель. Ghensi et al., (2017) ровно 10 лет спустя, в своем докладе, несмотря на двойной шов и первоначально получения первичного закрытия раны, он сообщил о воздействии мембраны, где он следовал в течение 4 месяцев. Оба были успешными с GBR, подтверждая, что не было загрязнения трансплантата. И Ibraheem et al., (2020) наблюдали вертикальное увеличение воздействия в течение 4 месяцев, и получил GBR, в данном случае доклад Cytoplast Ti-250 мембрана была зафиксирована с винтами.
Koidou et al. (2019) в своем случае серия получила GBR, используя цитопластовую мембрану® и коллагеновую мембрану между трансплантатом и мембраной, в результате чего мембрана намеренно подвергается воздействию. Hertzberg (2017) в своей серии случае получил GBR с помощью мембраны Cytoplast Ti-250 и коллагеновой мембраны над мембраной d-PTFE, которая была зафиксирована титановыми булавками и первичным закрытием раны.
Hassan et al., (2017) была использована рандомизированная модель сравнительного исследования расколоть рот, что уменьшает предвзятость, потому что можно свести к минимуму межиндивидуальные переменные, так как участники служат в качестве своих собственных элементов управления и, при настоящем, вмешиваться в равной степени в лечении. Мембраны были Cytoplast® и MAC, GBR держал поддержания мембран, подверженных устной среде в течение 3,5 месяцев, несмотря на то, что не получил в качестве основного результата, что Цитопласт мембраны® сопротивлялись бактериального проникновения упоминается в своем заключении, что MAC подвергается намеренно одинаково эффективен в сохранении гребня по сравнению с d-PTFE и Hoffmann et al., (2008) в своем продольном ретроспективном исследовании, GBR выполняется на 276 альвеолос экзодонтий, которые из-за относительно высокой численности населения зачислены, воспроизводит сильную временную связь случайности. Некоторые детали исследования заслуживают того, чтобы быть выделены: сначала маскировка и калибровка эксперта, который измерил дефекты, а затем регенерации, и стандартизированные измерения с отдельными каскадами позволяет 5 измерений отображение каждого дефекта, что повышает надежность результатов. При анализе данных, переменные, описывающие потерю костной массы были зарегистрированы индивидуально во всех случаях, а также отдельно в руках исследуемых факторов, представляющих интерес, которые были: формат альвеоло, верхней или нижней челюсти и области и вертикальной кости увеличение было выражено в средствах ± (DP) и минимальные, максимальные и средние значения. И независимые образцы испытания были использованы для того чтобы обнаружить некоторый эффект связанный к сексу или курить на потере косточки и использовали корреляцию Pearson для того чтобы расследовать влияние времени на усилении косточки. Она не обнаружила никакого влияния упомянутых выше переменных. Он измерил трехмерное увеличение кости, получив среднее вертикальное увеличение кости на 6 мм, а также собрал образцы, которые показали, что в гистологическом анализе была регенерация костей. В описании техники он подчеркнул, что первичное закрытие раны не было получено, удаление мембраны было сделано через 4 месяца, оба автора держали открытые мембраны, включая MAC, в течение периода от 3,5 до 4 месяцев.
В ходе двух экспериментов были собраны соответствующие данные о характеристиках непроницаемости и способности к интеграции мембранных тканей Cytoplast®. Trobos et al., (2018) при тестировании мембраны d-PTFE в своем эксперименте в пробирке с культурой S.oralis 2,12,24 и 48hs, пришел к выводу, что он непроницаем для бактерий уже Mazzucchi, et al., (2020) проанализировали мембраны, взятые из живых пациентов и обнаружили бактерии в нижней части мембраны в небольших количествах, но не повредить трансплантатов, она утверждала, что они могли бы проникли края из-за плохой интеграции тканей или во время операции.
Gallo et al. (2019) при анализе осложнений в своем исследовании 80 случаев, он сообщил мембраны воздействия Cytoplast® которые последовали в течение 9 месяцев руководящих и сопровождающих пациентов в отношении гигиены и использования хлоргексидина 0,2% до лечения. Предлагая протокол для управления d-PTFE мембраны воздействия устной среды, он подтвердил устойчивость к проникновению бактерий, подтверждающие результаты и рекомендации Ibraheem et al., (2020).
Ibraheem (2020) в своем докладе случае сделал GBR в области 3 элементов, и после воздействия >3 мм в течение 10 месяцев и пришел к выводу, что цитопласт® мембраны, при воздействии, не обязательно приводит к сбою, если обрабатываются надлежащим образом с короткими интервалами последующей деятельности, что подтверждает, что Cytoplast® d-PTFE противостоять мембраны бактериального проникновения подтверждающие Maridati, et al., (2016), который мембранного воздействия и следуют в течение 4 месяцев, и при удалении мембраны, также получил GBR, последний автор не упомянул об использовании антисептика, но использование актуальных антисептик, кажется, играет важную роль в прогнозе воздействия Gallo (2019) и Ibraheem (2020).
Urban et al. (2014) в своих исследованиях при фиксации армированной мембраны Ti-d-PTFE Cytoplast® Ti 200 с помощью кнопок Master Pin Control®, Messinger и / или Pro-Fix Tentin Screw®, винтов Osteogenics Biomedical для палаток. , создали необходимые строительные леса для создания пространства. При выполнении кортикальных перфораций, раскрытии лоскута и закрытии лоскута без натяжения с помощью простого горизонтального двойного матрасного шва без воздействия мембраны в течение 9 месяцев он соответствовал следующим принципам Wang’s PAEE (2006): ( i) первичное закрытие раны, (ii) ангиогенез и (iii) создание пространства. Обнаружив результат увеличения костной массы 5,45 мм со стандартным отклонением 1,93, он подтвердил, что способность создавать и поддерживать пространство и стабилизацию раны были соблюдены, потому что если бы мембрана d-PTFE Cytoplast® не имела способности создавать и поддержание пространства и стабилизация раны при вертикальном увеличении кости, не достигли бы увеличения кости, полученного авторами, учитывая, что ангиогенез и первичное закрытие были достигнуты, когда они описали отсутствие воздействия на мембрану, как Mertens et al., (2019) наблюдали в его исследование на свиных челюстях показало, что закрытие створок без натяжения двойным швом вызвало уменьшение вертикального объема трансплантата из твердых частиц, а также наблюдалось, что использование шипов снижает деформацию трансплантата из частиц и Herzberg et al. (2017) признали, что первичное закрытие раны часто бывает трудно достичь, например, в области зуба.
Ronda et al., (2014) получили аналогичные результаты с двумя различными мембранами Ti-d-PTFE и Ti-e-PTFE в GBR, 116,8% и 119,7%, не было воздействия мембран, имплантаты были установлены одновременно с GBR в 1 этапе и декортика была выполнена. Можно заметить, что все принципы PAEE были выполнены в этом исследовании и Cucchi, (2017) в своем сравнительном исследовании между Cytoplast® усиленной мембраной Ti-d-PTFE и титановой сеткой, покрытой коллагеновой мембраной для GBR задних челюстей и размещением 1-ступенчатых имплантатов, получили аналогичные результаты в костной массе. Тем не менее Cucchi, (2019) продолжая работу 2017 года с гистологическими и гистоморфометрическими анализами показали очевидную регенерацию костей в корональных частях обеих групп и интимный контакт между материалом костного трансплантата и трансплантат служил мостом к неоформированной кости, определяя, что существует регенерация костей как рандомизированных, так и замаскированных исследований как в распределении пациентов, так и в измерениях.
Oliveira (2015) в своей статье «Отчеты и серии дел» отметил, что, несмотря на их важность, отчеты и серии дел подвержены риску предвзятости и обычно публикуют успешные кейсы. Поскольку у них низкий риск систематической ошибки, следующие рандомизированные испытания: Ronda (2013) и Cucchi (2017) были отобраны для группирования в диаграмме «Лесной участок». Важно подчеркнуть, что для того, чтобы их можно было опубликовать в журнале Clínical Oral Implant Research, согласно консультации, проведенной на странице отправки в журнал, следует отрывок: «Рандомизированные клинические испытания должны сообщаться с использованием рекомендаций CONSORT. Контрольный список CONSORT 2010 также должен быть включен в материалы для подачи » (AUTHOR GUIDELINES, доступ: 15.09.2020), поэтому, если они соответствуют руководящим принципам рандомизированных испытаний, выполнив требования контрольного списка, можно считать золотым стандартом. Они были сгруппированы в график «Лесной участок», полученный с помощью программного обеспечения Review Manager 5.4, который можно было выполнить из-за низкой гетерогенности между исследованиями и количественными результатами прироста костной массы в мм, которые можно было наблюдать с помощью тестов x² и I², представленных в легендах. с результатами 0,55 и 0% соответственно, что предполагает использование модели анализа фиксированного эффекта. Это просто подтверждает выводы авторов, но показывает тенденцию к предпочтению мембраны Cytoplast® по сравнению с титановой сеткой и мембраной e-PTFE в увеличении костной массы / понимаемой как способность создавать и поддерживать пространство, также зависящее от трансплантата. полностью от мембраны, чтобы сохранить положение, например, если бы в исследованиях было вдвое больше вмешательств, он бы уже сдвинул черный ромб с оси 0, что также предполагает проведение подобных исследований с минимальной выборкой, вдвое большей. Программное обеспечение Review Manager 5.4 использовалось для настройки метаанализа и моделирования.
Рисунок 1. Лесной участок Средняя кость получить d-PTFE х контроль
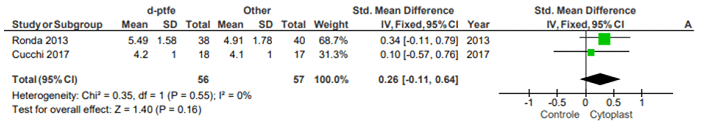
То, как менеджер по обзору 5.4 выполнил расчеты, было описано Deeks и Higgins (2010). Типы данных, обнаруженных в результатах рандомизированных клинических испытаний, были непрерывными, выбранный метод анализа был фиксированным эффектом обратной дисперсии и измерения эффекта в стандартной среднее различие и 95% интервалы доверия.
Анализируя отчеты и серии случаев, когда они решили попытаться покинуть мембрану намеренно подвергаются, на основе характеристики непроницаемости для бактерий и интеграции тканей в мембрану и которые получили регенерации костей и кости получить как в высоту и ширину, а еще некоторые доказали гистологических и гистоморфометрических анализов, по-прежнему разрыв по качеству интеграции d-PTFE мембраны в тканях Cytoplast® , Если он является достаточно полным, чтобы предотвратить лоскут слизистой оболочки от принятия прохождения бактерий в случаях воздействия, использование хлоргексидина в актуальных гель и механическое удаление налета в верхней части мембраны имеют важное значение в контроле воздействия и пародонтального контроля до и после хирургического вмешательства практики, которые могут свести к минимуму этот риск. Было отмечено, что есть доказательства и что она требует моделей исследований с этой мембраной, которые исследуют эти свойства.
5. ЗАКЛЮЧЕНИЕ
Проанализировав научную работу этого обзора, мы приходим к выводу, что d-PTFE мембраны Cytoplast® отвечает потребностям мембраны для сохранения и увеличения альвеолярного обода, что позволяет период воздействия полости рта, без проникновения микроорганизмов в привитой области при условии, что пациент сопровождается жестким протоколом гигиены и края мембраны покрыты тканью и в случаях вертикального расширения при усилении винты, Cytoplast Ti-250 способен создавать и поддерживать пространство так, что есть GBR при получении закрытия первичной раны без напряжения сделано с периостеевым выпустить разрез маневра.
ССЫЛКИ
BARTEE, Chaddick M.; BARTEE, Barry K.. Hydrophilic high density PTFE medical barrier. Depositante: Chaddick M. Bartee, Barry K. Bartee. US7296998B2. Depósito: 21 set 2007.
BARBER, Dexter H.; LIGNELLI, John; SMITH, Brian M.; BARTEE, Barry K. Using a Dense PTFE Membrane Without Primary Closure to Achieve Bone and Tissue Regeneration. Journal of Oral and Maxillofacial Surgery, Estados Unidos, v. 65, n. 4, p. 748–752, abr. 2007. ISSN: 0278-2391. DOI: 10.1016/j.joms.2006.10.042.
CUCCHI, Alessandro; VIGNUDELLI, Elisabeta; NAPOLITANO, Aldo; MARCHETTI, Claudio; CORINALDESI, Giuseppe. Evaluation of complication rates and vertical bone gain after guided bone regeneration with non-resorbable membranes versus titanium meshes and resorbable membranes. A randomized clinical trial. Clinical implant dentistry and related research, Estados Unidos, v. 19, n. 5, p. 821–832, out. 2017. ISSN: 1523-0899. DOI: 10.1111/cid.12520.
CUCCHI, Alessandro; SARTORI, Maria, PARRILLI, Annapaola; ALDINI, Nicolò N.; VIGNUDELLI, Elisabetta; CORINALDESI, Giuseppe. Histological and histomorphometric analysis of bone tissue after guided bone regeneration with non-resorbable membranes vs resorbable membranes and titanium mesh.(Report). Clinical Implant Dentistry and Related Research, Estados Unidos, v. 21, n. 4, p. 693, ago. 2019. ISSN: 1523-0899. DOI: 10.1111/cid.12814.
DEEKS, Johnathan J.; HIGGINS, Julian P. T. Statistical algorithms in Review Manager 5: on behalf of the Statistical Methods Group of The Cochrane Collaboration, Cochrane Collaboration. p. 1–11, ago. 2010. Disponível em https://training.cochrane.org/handbook/statistical-methods-revman5. Acesso em: 08/07/2020.
GALLO, Pier; DÍAZ-BÁEZ, David. Management of 80 Complications in Vertical and Horizontal Ridge Augmentation with Nonresorbable Membrane (d-PTFE): A Cross-Sectional Study. The International journal of oral & maxillofacial implants, Estados Unidos, v. 34, n. 4, p. 927–935, jul. 2019. ISSN: 0882-2786. DOI: 10.11607/jomi.7214.
GHENSI, P;STABLUM, W; BETTIO, E; SOLDINI, M. C.;TRIPI,T. R.;SOLDINI, C. Menagemente of the exposure of a dense PTFE (d-PTFE) membrane in guided bone regeneration (GBR): A case report. Oral & Implantology, Itália, v. 10, n. 3, p. 335, jul. 2017. ISSN: 1974-5648. DOI: 10.11138/orl/2017.10.3.335.
HASSAN, Muyeenul M.; PRAKASAM, Sivaraman; BAIN, Carol; GHONEIMA, Ahmed; LIU Sean Shih-Yao. A Randomized Split-Mouth Clinical Trial on Effectiveness of Amnion-Chorion Membranes in Alveolar Ridge Preservation: A Clinical, Radiologic, and Morphometric Study. The International Journal of Oral & Maxillofacial Implants, Estados Unidos, v. 32, n. 6, p. 1389–1398, nov. 2017. ISSN: 0882-2786. DOI: 10.11607/jomi.5875.
HERZBERG, RAN. Vertical Guided Bone Regeneration for a Single Missing Tooth Span with Titanium-Reinforced d-PTFE Membranes: Clinical Considerations and Observations of 10 Consecutive Cases with up to 36 Months Follow-up. The International journal of periodontics & restorative dentistry, Estados Unidos, v. 37, n. 6, p. 893–899, nov. 2017. ISSN: 0198-7569. DOI: 10.11607/prd.3380.
HOFFMANN, Oliver.; BARTEE, Barry K.; BEAUMONT, Christian; KASAJ, Adrian;DELI, Giorgio; ZAFIROPOULOS, Gregor Georg. Alveolar bone preservation in extraction sockets using non-resorbable dPTFE membranes: a retrospective non-randomized study. Journal of periodontology, Estados Unidos, v. 79, n. 8, p. 1355–69, ago. 2008. ISSN: 0022-3492. DOI: 10.1902/jop.2008.070502.
IBRAHEEM, Ahmed Gamil; BLANCHARD, Steven B. Alveolar ridge augmentation around exposed mandibular dental implant with histomorphometric analysis. Clinical advances in periodontics, Estados Unidos, jan. 2020. ISSN: 2163-0097. DOI: 10.1002/cap.10090. Disponível em: https://aap.onlinelibrary.wiley.com/doi/epdf/10.1002/cap.10090. Acesso em: 15/09/2020.
KOIDOU, Vasiliki P.; CHATZOPOULOS, Georgios S.; JOHNSON, Deborah. The “Combo Technique”: A Case Series Introducing the Use of a d-PTFE Membrane in Immediate Postextraction Guided Bone Regeneration. J Oral Implantol., Estados Unidos, v. 45, n. 6 p. 486-493, dez. 2019.ISSN: 0160-6972. DOI: 10.1563/aaid-joi-D-19-00015.
LEE, Jun-Beom; LEE, Jung-Tae; HWANG, Sukhiun; CHOI, Jung-Yoo; YEO, In-Sung L. Leukocyte- and platelet-rich fibrin is an effective membrane for lateral ridge augmentation: An in vivo study using a canine model with surgically created defects. Journal of periodontology, Estados Unidos, v. 91, n. 1, p. 120–128, jan. 2020. ISSN: 0022-3492. DOI: 10.1002/JPER.19-0186.
MARIDATI, Paolo. C.;CREMONESI, Sergio; FONTANA, Filippo; CICCIÙ, Marco; MAIORANA, Carlo. Management of d-PTFE Membrane Exposure for Having Final Clinical Success. The Journal of oral implantology, Estados Unidos, v. 42, n. 3, p. 289–291, jun. 2016. ISSN: 0160-6972. DOI: 10.1563/aaid-joi-D-15-00074.
MAZZUCCHI, Giulia; LOLLOBRIGIDA, Marco; LAURITO, Domenica; DI NARDO, Dario; BERLUTTI, Francesca; PASSARIELLO, Claudio; SERAFINI, Giorgio; TESTARELLI, Luca; DE BIASE, Alberto G. Microbiological and FE-SEM Assessment of d-PTFE Membrane Exposed to Oral Environment after Alveolar Socket Preservation Managed with Granular nc-HA. The journal of contemporary dental practice, India, v. 21, n. 4, p. 404–409, 1 abr. 2020. ISSN: 1526-3711.
MERTENS, Christian; SEBASTIAN Braun; KRISAM, Johannes; HOFFMANN, Jürgen. The influence of wound closure on graft stability: An in vitro comparison of different bone grafting techniques for the treatment of one-wall horizontal bone defects. Clinical implant dentistry and related research, Estados Unidos. v. 21, n. 2, p. 284–291, 11 abr. 2019. ISSN: 1523-0899. DOI: 10.1111/cid.12728.
NAUNG, Noel. Ye.; SHEHATA, Ehab.; VAN SICKELS, Joseph. E. Resorbable Versus Nonresorbable Membranes: When and Why? Dental Clinics of North America, Estados Unidos v. 63, n. 3, p. 419–431, jul. 2019. ISSN: 0011-8532. DOI: 10.1016/j.cden.2019.02.008.
OLIVEIRA, Marco Aurélio Pinho; VELARDE, Guillermo Coca ; DE SÁ, Renato Augusto Moreira. Understanding the clinical research V: case report and series of case report. Femina, Brasil, v.43, n 5 p. 235-38, set. 2015. Disponível em: http://files.bvs.br/upload/S/0100-7254/2015/v43n5/a5320.pdf. Acesso em: 05/05/2020. ISSN: 0100-7203
REVIEW MANAGER 5.4 (Rev Man 5). The Cochrane Collaboration, set. 2015. Diponível em: https://training.cochrane.org/online-learning/core-software-cochrane-reviews/revman/reasons-downloading-revman-5. Acesso em: 05/06/2020.
RONDA, Marco; REBAUDI, Alberto; TORELLI, Lucio; STACCHI, Claudio. Expanded vs. dense polytetrafluoroethylene membranes in vertical ridge augmentation around dental implants: a prospective randomized controlled clinical trial. Clinical oral implants research, Dinamarca, v. 25, n. 7, p. 859–866, jul. 2014. ISSN: 0905-7161. DOI: 10.1111/clr.12157.
SALOMÃO, M.; F.K. ALVAREZ; J.T.T. SIQUEIRA. Guided bone regeneration after tooth extraction using membrane exposed to the oral environment. Case reports. Implantnews, Brasil, v. 7, n 6, p. 753-9. jun. 2010. ISSN: 2358-905.
SCHULZ, Knneth F.; ALTMANN, Douglas G.; MOHER, David; CONSORT. CONSORT 2010 Statement: updated guidelines for reporting parallel group randomised trials. International journal of surgery, Inglaterra v.9, n. 8, p. 672-677, 2011. ISSN: 1743-9191. DOI: 10.1016/j.ijsu.2011.09.004.
TROBOS, Margarita; JUHLIN, Annika; SHAH, Furqan A.; HOFFMANN, Maria; SAHLIN, Herman; DAHLIN, Christer. In vitro evaluation of barrier function against oral bacteria of dense and expanded polytetrafluoroethylene (PTFE) membranes for guided bone regeneration. Clinical Implant Dentistry and Related Research, Estados Unidos, v. 20, n. 5, p. 738–748, out. 2018. ISSN: 1523-0899. DOI: 10.1111/cid.12629.
URBAN, Istvan A.; MONJE, Alberto; NEVINS, Myron; NEVINS, Marc L; LOZADA Jamie L; WANG, Hom-Lay. Surgical Management of Significant Maxillary Anterior Vertical Ridge Defects. The International Journal of Periodontics & Restorative Dentistry, Estados Unidos, v. 36, n. 3, p. 329–337, mai. 2016. ISSN: 0198-7569. DOI: 10.11607/prd.2644.
URBAN, Istvan A.; MONJE, Alberto; LOZADA Jamie L; WANG, Hom-Lay. Principles for Vertical Ridge Augmentation in the Atrophic Posterior Mandible: A Technical Review. The International Journal of Periodontics & Restorative Dentistry, Estados Unidos, v. 37, n. 5, p. 639–645, set. 2017. ISSN: 0198-7569. DOI: 10.11607/prd.3200.
WANG, Hom. Lay.; BOYAPATI, Lakshmi. “PASS” principles for predictable bone regeneration. Implant Dentistry, Estados Unidos, v. 15, n. 1, p. 8–17, mar. 2006. ISSN: 1056-6163. DOI: 10.1097/01.id.0000204762.39826.0f.
ONLINELIBRARY.WILEY.COM. Author Guidelines: Research Reporting Guidelines. Clinical Oral Implants Research. Dinamarca. Disponível em: https://onlinelibrary.wiley.com/page/journal/16000501/homepage/ForAuthors.html. Acesso em: 15/09/2020. ISSN: 1600-0501
[1] Выпускной в стоматологии.
[2] Советник. Кандидат наук. Профессиональная степень магистра стоматологии. Специализация в Имплантодонтии. Выпускной в стоматологии.
Представлено: Сентябрь 2020.
Утверждено: Сентябрь 2020.