ОРИГИНАЛЬНАЯ СТАТЬЯ
FACCO, Lucas [1], ALMENDRO, Lucas Pablo [2], MARQUES, Cristiane Peres [3], RIBEIRO, Edson Fábio Brito [4], FECURY, Amanda Alves [5], DENDASCK, Carla Viana [6], ARAÚJO, Maria Helena Mendonça de [7], OLIVEIRA, Euzébio de [8], DIAS, Claudio Alberto Gellis de Mattos [9]
FACCO, Lucas. и др. Злокачественная неоплазия яичек: эпидемиологический анализ случаев, зарегистрированных в Бразилии в период с 2015 по 2019 год. Revista Científica Multidisciplinar Núcleo do Conhecimento. Год. 06, Изготовить. 10, Вол. 07, с. 62-74. Октябрь 2021 года. ISSN: 2448-0959, Ссылка доступа: https://www.nucleodoconhecimento.com.br/здравоохранение/неоплазия, DOI: 10.32749/nucleodoconhecimento.com.br/ru/99992
СВОДКА
Неоплазия яичек является относительно редкой злокачественной патологией, составляющей 0,5% всех мужских новообразований, чаще встречающейся среди лиц в возрасте от 15 до 34 лет. Наиболее распространенной клинической картиной является отек яичек или мошонки с или без сопутствующей боли или травмы, а стандартным подтверждающим диагнозом является орхиэктомия. Это исследование было направлено на эпидемиологический анализ зарегистрированных случаев злокачественной неоплазии яичек в Бразилии в период с 2015 по 2019 год. Данные для эпидемиологических исследований были получены из DATASUS, а библиографические исследования проводились через научные статьи. Из информации, выявленной в этом исследовании, можно наблюдать растущую диагностику злокачественных новообразований яичек в Бразилии, причем почти в два раза больше случаев, наблюдаемых в период с 2015 по 2019 год. Хотя рак яичек относительно редко, он потенциально смертелен, и его тяжесть не следует недооценивать и следует диагностировать и лечить как можно раньше. Он имеет высокие шансы на излечение, с окончательным хирургическим лечением, после подтверждающего диагноза, в большинстве случаев, позволяя пострадавшему человеку иметь нормальную жизнь. Таким образом, необходимы дополнительные исследования, чтобы выявить причины роста случаев рака яичек в Бразилии и во всем мире, понять, связаны ли региональные различия с количеством случаев или это сбой в диагностике и регистрации, а также служит основой для действий правительства, с целью планирования и реализации политики, направленной на борьбу с провоцирующие факторами этого заболевания.
Ключевые слова: злокачественные новообразования, урологические опухоли, рак яичек, паховая орхиэктомия, эпидемиология.
ВВЕДЕНИЕ
Рак или неоплазия возникает в результате пролиферации клеток организма, которые представляют морфологические и функциональные изменения и вызывают расстройство тканей. Такие изменения могут иметь генетические или экологические причины (Dias et al., 2017).
Неоплазия яичек является относительно редкой злокачественной патологией, с составляющей 0,5% всех мужских новообразований и 5% урологических опухолей (Rosen et al., 2011; Nci, 2021), и чаще встречается среди лиц в возрасте от 15 до 34 лет (Baird et al., 2018). Кроме того, наиболее распространенным вариантом была опухоль половых клеток, с 95% случаев, и наиболее частый диагноз в клинически локализованных пальпируемых массах стадии I (Adra e Einhorn, 2017; Pierorazio et al., 2018).
Были указаны факторы риска развития этого вида рака: в анамнезе, с риском преодоления контралатерального яичка от 5 до 6%; семейный анамнез, с риском от 8 до 10 раз среди братьев и сестер и от 4 до 6 раз среди детей носителя; крипторхизм, с отношением шансов (ОШ) 4,3, 95% доверительным интервалом 3,6-5,1; поздняя орхидопексия (фиксация яичек в стебле мошонки) с ОШ 5,8 по сравнению с ранней; и синдром Клайнфельтера (Hemminki e Li, 2004; Walsh et al., 2007; Cook et al., 2010; Lip et al., 2012; Chan et al., 2014; Kier et al., 2016; Nery, 2019). Наиболее распространенной клинической картиной является масса яичек или отек мошонки с или без сопутствующей боли / травмы, имеющие в качестве дифференциального диагноза орхит или эпидидимит, могут затем начать лечение антибиотиками (Nery, 2019). Метастазы могут возникать, в зависимости от локализации, такие как: желудочно-кишечные симптомы; гинекомастия; головная боль; боль в пояснице; масса шеи; симптомы (одышка, кашель и смооптиз) (Shaw, 2008).
Диагностическая методика такой неоплазии начинается во время физикального обследования, с пальпации стебля мошонки, но это порождает неоднозначные результаты, поэтому использование рентгенологического исследования с трансскротальной ультрасонографией, которое было отмечено все более широкое применение при обнаружении неуловимых или неоднозначных поражений (Dieckmann et al., 2013; Cheng et al., 2018). Стандартным подтверждающим диагнозом является радикальная орхиэктомия (операция по удалению одного или обоих яичек и всего семенного канатика), которая дает возможность установить характер и часто уже используется при лечении (Ghoreifi and Djaladat, 2019). Золотой стандарт лечения яичковых масс с подозрением на злокачественность, без признаков метастазов, был установлен как радикальная орхиэктомия с удалением до уровня внутреннего пахового кольца, которая часто выполняется во время диагностической процедуры и предлагала возможность замены протезом яичка (Krege et al., 2008; Robinson et al., 2015; Ghoreifi e Djaladat, 2019). Тем не менее, сывороточные опухолевые маркеры (альфа-фетопротеин – АФП – и хорионический бета-гонадотрофия человека – Бета-ХГЧ) используются для оказания помощи в оценке эффективности лечения и оценке прогноза для пациента, поскольку они должны быть установлены до и после лечения, а также в период наблюдения (Gilligan et al., 2019).
В глобальном контексте было 72 000 диагнозов и 9 000 смертей в год для этого опухолевого процесса, а риск развития рака яичек у мужчины в течение некоторого времени его жизни оценивался как 1 из 250 мужчин (Fitzmaurice et al., 2017; Acs, 2021). Предполагаемый прогноз на 2021 год новых случаев рака яичек в Соединенных Штатах Америки составил 9 470 диагнозов и 440 смертей, в дополнение к более высокой частоте среди белых людей (6,9 человека, затронутых 100 000 мужчин) по сравнению с афроамериканцами (1,2 человека, затронутые 100 000 мужчин) (Ghazarian et al., 2014; Acs, 2021).
В свою очередь, на национальном уровне наблюдалась определенная скудость эпидемиологических данных по этому новообразованию, но наблюдался рост смертности по сравнению с данными 2015 года (359 смертей, что составляет 0,05% от общей смертности) и 2019 года (446 смертей, что составляет 0,06% от общей смертности) Атласа смертности от рака – Информационная система смертности (Nery, 2019; Inca, 2021).
ЦЕЛЬ
Эпидемиологически проанализировать зарегистрированные случаи злокачественной неоплазии яичек в Бразилии в период с 2015 по 2019 год.
МЕТОД
В исследовании использовалась кваликантитивная методология (смешанный метод), с правительственными данными, поскольку помимо численных данных предполагалась интерпретация явлений (Facco et al., 2021).
Сбор данных проводился в базе данных DATASUS (http://datasus.saude.gov.br/). Национальные данные были собраны в соответствии со следующими этапами: A) Была открыта ссылка datasus.saude.gov.br, стрелка была перемещена мышью на вкладку «Services in Highlight», затем была выбрана опция «TABNET»; Б) На следующей странице «ТАБНЕТ» мы щелкнули по опции «Эпидемиология и заболеваемость» и поэтому выбрали вариант «Время до начала лечения рака – ПАНЕЛЬ – онкология». Оттуда были выполнены следующие шаги: A) В поле «Строка» на протяжении всего процесса был выбран «Год диагностики»; Б) В поле «Меры» «Случаи» выбирались на протяжении всего процесса; C) В поле «Столбец» было выбрано следующее: «Стадия», «Возрастная группа», «Терапевтический метод», «Время лечения», «Пребывание UF», «UF диагностики» и «UF лечения». Все данные, собранные в системе, охватывают периоды с 2015 по 2019 годы. D) В поле «Доступный выбор» в опции «Диагностика» выберите вариант «Злокачественные новообразования (Закон № 12.732 / 12) и в« Детальной диагностике ». »был выбран вариант« Злокачественное новообразование яичка С62 ». В других доступных полях выбора были сохранены параметры по умолчанию системы DATASUS. Сбор данных проводился с использованием приложения Excel, компонента пакета Microsoft Corporation Office, а данные по регионам Бразилии были агрегированы из данных, предоставленных каждым из штатов в соответствующих регионах. Библиографическое исследование проводилось по научным статьям с использованием персональных компьютеров авторов данной работы для поиска.
РЕЗУЛЬТАТЫ
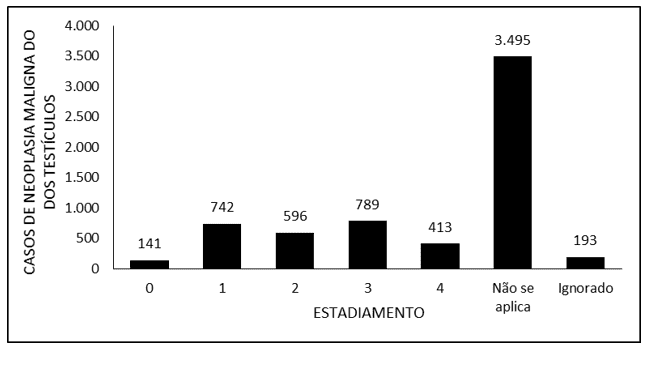
На рисунке 1 обозначено количество случаев злокачественного новообразования яичек в Бразилии в период с 2015 по 2019 год, через постановку. Отмечается, что наиболее полным был 3-й класс (789 случаев), за которым следовали 1 класс (742), класс 2 (596) и 0 (141). Следует отметить, что в подавляющем большинстве зарегистрированных случаев критерий постановки был классифицирован как “не применяется”, в дополнение к 193 случаям, которые были зарегистрированы как “проигнорированные”.
На рисунке 1 – показано количество случаев злокачественного новообразования яичек в Бразилии в период с 2015 по 2019 год, через постановку.
В таблице 1 обозначено количество случаев злокачественного новообразования яичек в Бразилии в период с 2015 по 2019 год по возрастной группе. Отмечается, что 5 возрастных диапазонов с наибольшим числом зарегистрированных случаев злокачественных новообразований яичек: от 25 до 29 лет (1. 312), от 30 до 34 лет (1 157), от 20 до 24 лет (1 072), от 35 до 39 лет (811) и от 0 до 19 лет (563). Кроме того, было отмечено, что наибольшее число зарегистрированных случаев произошло в 2019 году – 1 841 случай.
В таблице 1 – показано количество случаев злокачественного новообразования яичек в Бразилии в период с 2015 по 2019 год по возрастной группе.
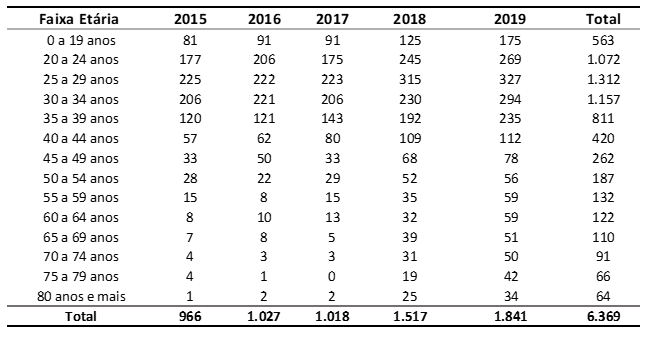
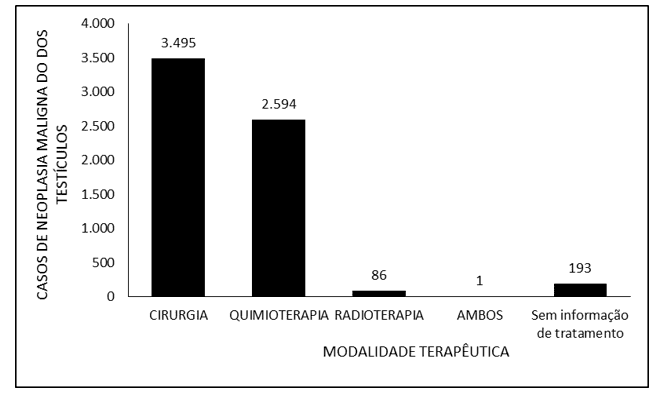
Рисунок 2 охватывает число случаев злокачественного новообразования яичек в Бразилии в период с 2015 по 2019 год с помощью используемой терапевтической модальности. Отмечается, что наибольшая доля пациентов (3 495) лечилась хирургическим путем, а 2 594 лечились с помощью химиотерапии. Лучевая терапия использовалась у 86 пациентов, и только 1 пациент использовал три терапевтических метода. Не было никакой информации о лечении, примененном у 193 пациентов.
На рисунке 2 – показано количество случаев злокачественного новообразования яичек в Бразилии в период с 2015 по 2019 год с помощью терапевтической модальности.
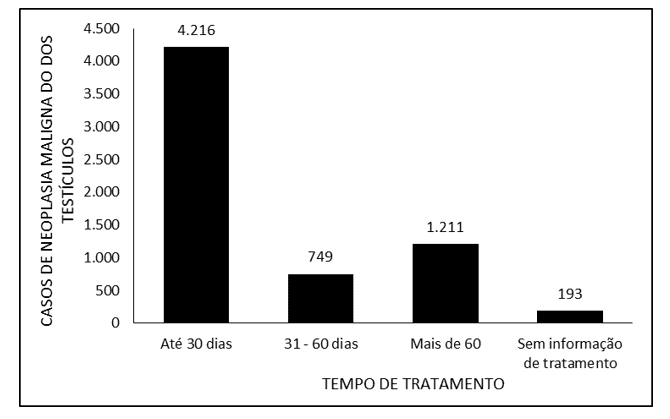
На рисунке 3 обозначено количество случаев злокачественного новообразования яичек в Бразилии в период с 2015 по 2019 год, до момента лечения. Подавляющее большинство зарегистрированных случаев относятся к времени лечения до 30 дней (4 216), за которым следует более 60 дней (1 211) и от 31 до 60 дней (749). Информации о времени лечения 193 больных не было.
На рисунке 3 – показано количество случаев злокачественного новообразования яичек в Бразилии в период с 2015 по 2019 год, до момента лечения.
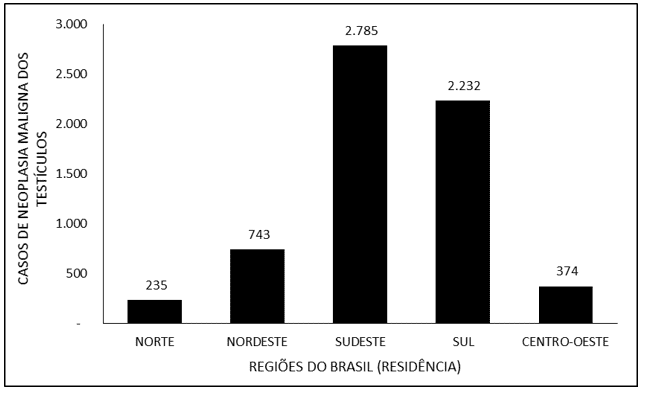
На рисунке 4 обозначено количество случаев злокачественного новообразования яичек в Бразилии в период с 2015 по 2019 год по региону проживания. Большинство случаев относятся к юго-востоку (2 785), за которым следуют южные (2 232), северо-восточные (743), средние (374) и северные (235) регионы.
На рисунке 4 – показано количество случаев злокачественного новообразования яичек в Бразилии в период с 2015 по 2019 год по региону проживания.
На рисунке 5 обозначено количество случаев злокачественного новообразования яичек в Бразилии в период с 2015 по 2019 год по региону диагностики. Отмечается, что наибольшая доля диагнозов пришлась на Юго-Восток (2 829), за которым следуют Юг (2 245), Северо-Восток (731), Средний Запад (333) и Север (231).
На рисунке 5 – показано количество случаев злокачественного новообразования яичек в Бразилии в период с 2015 по 2019 год по региону диагностики.
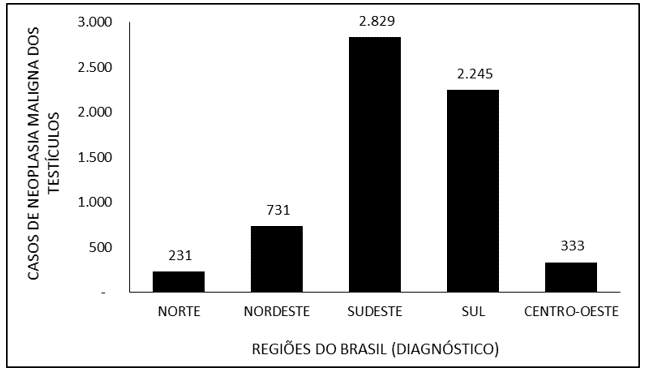
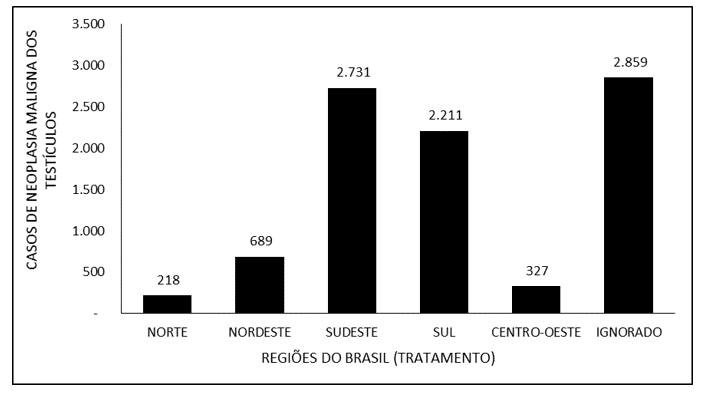
Рисунок 6 охватывает количество случаев злокачественного новообразования яичек в Бразилии в период с 2015 по 2019 год через область лечения. Большинство случаев (2 859) были зарегистрированы как «проигнорированные». Юго-Восточный регион имел самое высокое уведомление о лечении злокачественных новообразований яичек с 2 731 уведомлением, за которым следуют Юг (2 211), Северо-Восток (689), Средний Запад (327) и Север (218).
На рисунке 6 показано количество случаев злокачественного новообразования яичек в Бразилии в период с 2015 по 2019 год через область лечения.
ОБСУЖДЕНИЕ
Как видно из таблицы 1, в период с 2015 по 2019 год в Бразилии наблюдался рост числа случаев злокачественной неоплазии яичек, следуя общемировой тенденции, которая на протяжении десятилетий увеличивала уровень заболеваемости раком яичек во многих странах. Однако причины этого явления до сих пор неизвестны (Acs, 2021).
Большое количество диагнозов злокачественного новообразования яичек на стадии 3 может быть основано на молчаливой эволюции безболезненной твердой массы, которая часто плохо оценивается и диагностируется как орхит или эпидидимит, который в конечном итоге лечится ненадлежащим образом (доброкачественно), порождая задержку в правильном подходе, которая может составлять до 20 недель; способствуя появлению метастазов (Moul, 2007; Shaw, 2008; Nery, 2019). Они, в свою очередь, представляют клинические симптомы, что позволяет диагностировать уже присутствующие опухолевые и метастатические процессы, такие как респираторные симптомы (одышка, кашель и гемоптиз) (Shaw, 2008).
Как было показано в других исследованиях, наиболее распространенной возрастной группой для развития рака яичек было от 15 до 34 лет, что подтверждает данные, представленные в этом исследовании (Baird et al., 2018). Кроме того, факторами, которые могли привести к выявлению неоплазии в этой возрастной группе, могут быть ранний сексархе и активная половая жизнь, которые позволяют больше познанию тела и множественным половым партнерам, что позволяет ранее заметить образование отека мошонки неизвестной причины и последующий поиск медицинской помощи (Adra e Einhorn, 2017). Важно отметить, что скрининг рака яичек не рекомендуется, поскольку есть доказательства того, что его практика приносит больше пользы, чем рисков (Inca, 2021).
Хирургическая процедура была установлена как золотой стандарт лечения, так как она удаляет опухолевый очаг из семенного канатика до уровня нижнего пахового кольца, щадя чрезмерные манипуляции с цепью лимфатического узла и самим опухолевым очагом, тем самым избегая клеточной экстравазации ракового процесса (Krege et al., 2008; Rajpert-De-Meyts et al., 2016; Ghoreifi e Djaladat, 2019; Eau, 2021).
Одним из оправданий для тройного лечения является наличие отда ленных метастазов, что делает необходимым использование химиотерапии и лучевой терапии вместе с хирургической процедурой, увеличивая выживаемость до 96% через 10 лет (Nery, 2019; Nci, 2021), варьируя комбинации и циклы химиолучевой терапии в соответствии с клинической стадией и индивидуальными переменными, такие как 4 цикла БОП (цисплатин 20 мг/м2, внутривенно с 1 по 5 день; этопозид 100 мг/м2, внутривенно с 1 по 5 день; 30 МЕ внутривенное введение блеомицина на 2, 9 и 16 день; повторять каждые 21 день) (Nery, 2019).
Понятно, что зачастую в процессе подтверждающей диагностики выбирается паховая орхиэктомия, которая считается терапевтической процедурой, так как снимает первичный очаг неоплазии (Ghoreifi and Djaladat, 2019). Кроме того, приходится в момент формулирования диагностической гипотезы с радиологическими исследованиями и выбором радикальной орхиэктомии до уровня нижнего пахового кольца, а также замены протезом необходимо исследовать хирургический риск и наличие метастатических очагов в других областях с помощью онкомаркеров. (Krege et al., 2008; Robinson et al., 2015; Ghoreifi e Djaladat, 2019; Gilligan et al., 2019).
Учитывая, что 49,5% больниц, квалифицированных для ведения опухолевых процессов, расположены в Юго-Восточном регионе страны, за которым следует Южный регион с 24,2%, и что оба имеют большую доступность единиц распознавания, можно сделать вывод, что они также имеют лучшую систему диагностического распознавания этого новообразования. Кроме того, самые высокие показатели лечения расположены в южных и юго-восточных регионах Бразилии, причем 37,9% всех диагнозов зарегистрированы только в штате Сан-Паулу (Inca, 2019a; 2019b; 2019c; 2019d; 2019e; 2019f; 2019g; 2019h).
Рак яичек – это злокачественное новообразование, поражаемое значительное число молодых людей с активной половой жизнью и способное привести к летального исходу (Park et al., 2018). Тем не менее, он представляет собой одну из наиболее излечимых злокачественных новообразований, когда ее легко выявить и лечить с помощью мультимодального подхода. При эффективном лечении прогноз отличный, при излечиваемости> 90% и пятилетней выживаемости> 95% (Smith et al., 2018).
ЗАКЛЮЧЕНИЕ
Из информации, выявленной в этом исследовании, можно наблюдать растущую диагностику злокачественных новообразований яичек в Бразилии, причем почти в два раза больше случаев, наблюдаемых в период с 2015 по 2019 год. Хотя рак яичек относительно редко, он потенциально смертелен, и его тяжесть не следует недооценивать и следует диагностировать и лечить как можно раньше. Он имеет высокие шансы на излечение, с окончательным хирургическим лечением, после подтверждающего диагноза, в большинстве случаев, позволяя пострадавшему человеку иметь нормальную жизнь. Таким образом, необходимы дополнительные исследования, чтобы выявить причины роста случаев рака яичек в Бразилии и во всем мире, понять, связаны ли региональные различия с количеством случаев или это сбой в диагностике и регистрации, а также служит основой для действий правительства, с целью планирования и реализации политики, направленной на борьбу с провоцирующие факторами этого заболевания.
ИСПОЛЬЗОВАННАЯ ЛИТЕРАТУРА
ACS. Key Statistics for Testicular Cancer. New York NY, 2021. Disponível em: < https://www.cancer.org/cancer/testicular-cancer/about/key-statistics.html#references >. Acesso em: 05 mar 2021.
ADRA, N.; EINHORN, L. H. Testicular Cancer Update. Clinical Advances in Hematology & Oncology, v. 15, n. 5, p. 386-396, 2017.
BAIRD, D. C.; MEYERES, G.; HU, J. S. Testicular Cancer: Diagnosis and Treatment. American Family Physician, v. 97, n. 4, p. 261-268, 2018.
CHAN, E.; WAYNE, C.; NASR, A. Ideal timing of orchiopexy: a systematic review. Pediatric Surgery International, v. 30, n. 1, p. 87–97, 2014.
CHENG, L. et al. Testicular cancer. Nature Reviews Disease Primers, v. 4, n. 29, p. 1-24, 2018.
COOK, M. B. et al. Systematic review and meta-analysis of perinatal variables in relation to the risk of testicular cancer—experiences of the son. International Journal of Epidemiology, v. 39, n. 6, p. 1605-1618, 2010.
DIAS, A. D. A. et al. Update on the Main Aspects Related to Breast Cancer. Revista Científica Multidisciplinar Núcleo do Conhecimento, v. 4, p. 5-17, 2017. Disponível em: < https://www.nucleodoconhecimento.com.br/health/breast-cancer >.
DIECKMANN, K. P.; FREY; LOCK, G. Contemporary diagnostic work-up of testicular germ cell tumours. Nat Rev Urol v. 10, p. 703–712, 2013.
EAU. Testicular Cancer. Düsseldorf DE, 2021. Disponível em: < https://uroweb.org/guideline/testicular-cancer/#1 >. Acesso em: 06 mar 2021.
FACCO, L. et al. Neoplasia maligna de esôfago: uma análise epidemiológica dos casos notificados no Brasil entre 2015 e 2019. Research, Society and Development, v. 10, n. 2, p. 1-14, 2021. Disponível em: < https://rsdjournal.org/index.php/rsd/article/view/12750/11622 >.
FITZMAURICE, C. et al. Global, Regional, and National Cancer Incidence, Mortality, Years of Life Lost, Years Lived With Disability, and Disability-Adjusted Life-years for 32 Cancer Groups, 1990 to 2015: A Systematic Analysis for the Global Burden of Disease Study. .JAMA Oncol, v. 3, n. 4, p. 524-548, 2017.
GHAZARIAN, A. A. et al. Recent trends in the incidence of testicular germ cell tumors in the United States. Andrology, v. 3, n. 1, p. 13–18, 2014.
GHOREIFI, A.; DJALADAT, H. Management of Primary Testicular Tumor. Urologic Clinics of North America, v. 46, n. 3, p. 333–339, 2019.
GILLIGAN, T. et al. Testicular Cancer, Version 2.2020, NCCN Clinical Practice Guidelines in Oncology. Journal of the National Comprehensive Cancer Network, v. 17, n. 12, p. 1529-1554, 2019.
HEMMINKI, K.; LI, X. Familial risk in testicular cancer as a clue to a heritable and environmental aetiology. British Journal of Cancer, v. 90, n. 9, p. 1765–1770, 2004.
INCA. Onde tratar pelo SUS. Brasília DF, 2019a. Disponível em: < https://www.inca.gov.br/onde-tratar-pelo-sus#:~:text=Existem%20atualmente%20317%20unidades%20e,exame%20até%20cirurgias%20mais%20complexas >. Acesso em: 06 mar 2021.
______. Paraná. Brasília DF, 2019b. Disponível em: < https://www.inca.gov.br/onde-tratar-pelo-sus/parana >. Acesso em: 06 mar 2021.
______. Santa Catarina. Brasília DF, 2019c. Disponível em: < https://www.inca.gov.br/onde-tratar-pelo-sus/santa-catarina >.
______. Rio Grande do Sul. Brasília DF, 2019d. Disponível em: < https://www.inca.gov.br/onde-tratar-pelo-sus/rio-grande-sul >. Acesso em: 06 mar 2021.
______. Minas Gerais. Brasília DF, 2019e. Disponível em: < https://www.inca.gov.br/onde-tratar-pelo-sus/minas-gerais >. Acesso em: 12 jan 2021.
______. São Paulo. Brasília DF, 2019f. Disponível em: < https://www.inca.gov.br/onde-tratar-pelo-sus/sao-paulo >. Acesso em: 15 jan 2021.
______. Rio de Janeiro. Brasília DF, 2019g. Disponível em: < https://www.inca.gov.br/onde-tratar-pelo-sus/rio-janeiro >. Acesso em: 15 jan 2021.
______. Espírito Santo. Brasília DF, 2019h. Disponível em: < https://www.inca.gov.br/onde-tratar-pelo-sus/espirito-santo >. Acesso em: 01 jul 2021.
______. Câncer de testículo. Brasilia DF, 2021. Disponível em: < https://www.inca.gov.br/tipos-de-cancer/cancer-de-testiculo >. Acesso em: 06 mar 2021.
KIER, M. G. et al. Second Malignant Neoplasms and Cause of Death in Patients With Germ Cell Cancer. JAMA Oncology, v. 2, n. 12, p. 1624–1627, 2016.
KREGE, S. et al. European consensus conference on diagnosis and treatment of germ cell cancer: a report of the second meeting of the European Germ Cell Cancer Consensus group (EGCCCG): part I. Eur Urol v. 53, n. 3, p. 478–496, 2008.
LIP, S. Z. L. et al. A meta-analysis of the risk of boys with isolated cryptorchidism developing testicular cancer in later life. Archives of Disease in Childhood, v. 98, n. 1, p. 20–26, 2012.
MOUL, J. W. Diagnosis of Testicular Cancer. Urologic Clinics of North America, v. 34, n. 2, p. 109–117, 2007.
NCI. Cancer Stat Facts: Testicular Cancer. USA, 2021. Disponível em: < https://seer.cancer.gov/statfacts/html/testis.html >. Acesso em: 03 mar 2021.
NERY, R. C. Câncer de Testículo. In: SANTOS, M. (Ed.). Diretrizes oncológicas 2. São Paulo SP: Doctor Press Ed. Científica, 2019.
PARK, J. S. et al. Recent global trends in testicular cancer incidence and mortality. Medicine, v. 97, n. 37, p. 1-7, 2018. Disponível em: < https://www.ncbi.nlm.nih.gov/pmc/articles/PMC6155960 >.
PIERORAZIO, P. M. et al. Non–risk-adapted Surveillance for Stage I Testicular Cancer: Critical Review and Summary. European Urology, v. 73, n. 6, p. 899–907, 2018.
RAJPERT-DE-MEYTS, E. et al. Testicular germ cell tumours. The Lancet, v. 387, n. 10029, p. 1762–1774, 2016.
ROBINSON, R. et al. Is it safe to insert a testicular prosthesis at the time of radical orchidectomy for testis cancer: an audit of 904 men undergoing radical orchidectomy. BJU International, v. 117, n. 2, 2015.
ROSEN, A. et al. Global Trends in Testicular Cancer Incidence and Mortality. European Urology, v. 60, n. 2, p. 374–379, 2011.
SHAW, J. Diagnosis and Treatment of Testicular Cancer. American Family Physician, v. 7, n. 4, p. 469-474, 2008.
SMITH, Z. L.; WERNTZ, R. P.; EGGENER, S. E. Testicular Cancer: Epidemiology, Diagnosis, and Management. Medical Clinics of North America, v. 102, n. 2, p. 251-264, 2018. Disponível em: < https://www.sciencedirect.com/science/article/abs/pii/S0025712517301578?via%3Dihub >.
WALSH, T. J. et al. Prepubertal Orchiopexy for Cryptorchidism May be Associated With Lower Risk of Testicular Cancer. The Journal of Urology, v. 178, n. 4, p. 1440–1446, 2007.
[1] Студент медицинского курса Федерального университета Амапе (UNIFAP).
[2] Студент медицинского курса Федерального университета Акко (UFAC).
[3] Студент курса «Технология производства» Федерального университета Мату-Гросу-ду-Сул (UFMS).
[4] Студент медицинского курса Федерального университета Амапе (UNIFAP).
[5] Биомедицинская, кандидат биологических наук в области тропических болезней, профессор и исследователь медицинского курса Федерального университета Амапе (UNIFAP).
[6] Богослов, кандидат клинических психоанализов. В течение 15 лет он работал с научной методологией (методом исследования) в научно-производственной ориентации магистрантов и докторантов. Специалист в области маркетинговых исследований и медицинских исследований, докторант в области коммуникации и семиотики (PUC SP).
[7] Доктор педагогических и медицинских наук, профессор и исследователь медицинского курса кампуса Макапе, Федеральный университет Амапе (UNIFAP).
[8] Биолог, доктор философии в области тропических болезней, профессор и исследователь курса физкультуры, Федеральный университет Паре (UFPA).
[9] Биолог, кандидат теоретических и летных исследований, профессор и исследователь Высшей программы профессионального и технологического образования (PROFEPT), Федеральный институт Амапе (IFAP).
Представлено: Oктябрь 2021 года.
Утверждено: Oктябрь 2021 года.