ОРИГИНАЛЬНАЯ СТАТЬЯ
BEDIN, Rafael Antonio Caldart [1], SCHULTZ, Maisa [2], BEDIN, Antonio [3]
BEDIN, Rafael Antonio Caldart. SCHULTZ, Maisa. BEDIN, Antonio. Анестезия для кроликов, перенесших экспериментальную операцию: отчет о серии из восьми анестезий. Revista Científica Multidisciplinar Núcleo do Conhecimento. 05-й год, Эд. 06, Vol. 03, стр. 151-158. Июнь 2020 года. ISSN: 2448-0959, Ссылка доступа: https://www.nucleodoconhecimento.com.br/здравоохранение/анестезия-для-кроликов
РЕЗЮМЕ
Анестезия для лабораторных животных является источником биомедицинской озабоченности и одной из самых актуальных дилемм в текущих биоэтических дебатах. Использование анестезии в экспериментальной хирургии направлено на облагодие и сдерживание животных, с тем чтобы достичь разумной степени расслабления мышц и производить достаточную анальгезию. Эта практика требует использования протоколов для введения безопасных и эффективных доз. Восемь новозеландских кроликов, представленных на лапаротомии, демонстрируют дисциплину хирургической техники местного медицинского курса. Для преанестетических препаратов, ацепромазин 1 mg.kg-1, связанных с кетамином 15 mg.kg-1 подкожно был использован для преданестетических препаратов. Анестезия поддерживалась с изофлюраном и кислородом под ларингальной маской в системе кленсона d анестезии и при спонтанном дыхании. Гидратация выполнялась с 10-ml.kg-1 раствором каждый час. Использовался тепловой матрас. Для мониторинга использовались прекордиальный стетоскоп, оксиметрия пульса и клинические параметры. Для эвтаназии использовался кетамин 10 mg.kg-1, связанный с хлоридом калия 19,1% 1 ml.kg-1 внутривенно. Средний вес кроликов составил 2721,25±275,01 грамма, а продолжительность обезболивающей процедуры составила 120±87 минут. Обсуждения. При длительной анестезии, такой как лапаротомия, рекомендуется и применение преданестетических препаратов, а затем анестезируемой индукции, сделанной комбинацией агентов. Тем не менее, анестезия требует мониторинга, чтобы предотвратить недостаточные или преувеличенные дозы не происходит.
Ключевые слова: Кролики, изофлюран, общая анестезия.
ВВЕДЕНИЕ
Анестезия для лабораторных животных является предметом этических дебатов и была одной из самых противоречивых тем в этой области знаний (BEDIN et.al., 2013). Использование анестезии в экспериментальной хирургии направлено на сдерживание животного, для того, чтобы достичь разумной степени мышечной релаксации и производить достаточную анальгезию. Эта практика требует использования протоколов для введения безопасных и эффективных доз (BEDIN et.al., 2013).
БИБЛИОГРАФИЧЕСКИЙ ОБЗОР
Кролики обычно испытывают стресс из-за предоперационного обращения, во время предварительной анестезии и во время индукции венозными или летучими анестетиками. Здесь может быть добавлен стресс к обращению с животным для проведения анестезии, что может привести к остановке дыхания и сердца. Возникновение респираторной инфекции Pasteurella multocida может привести к серьезным респираторным осложнениям во время анестезии. При предоперационном обследовании этих животных мы должны обращать пристальное внимание на наличие респираторных симптомов (насморк и сопутствующие звуки при аускультации), которые могут указывать на инфекцию дыхательных путей (BEDIN et.al., 2013).
Анестезия у кроликов может варьироваться от простого седации до глубокой анестезии плоскостей, которые позволяют меньше и больше хирургических процедур. Использование галогенированных летучих анестезий у кроликов часто используется для длительных процедур, особенно когда он предназначен для держать гомеостаз животных как можно более сбалансированным (BEDIN et.al., 2013).
После введения преанестезиологического препарата подождите 15 минут, чтобы ларингеальная маска адаптировалась, подключив ее к наркозному аппарату. Можно использовать от 50 до 100% O2 и от 1 до 5% изофлурана (BEDIN et.al., 2013; RAILLARD et.al., 2019; TUNCALI et.al., 2018). Процедура интубации трахеи представляет большую техническую сложность, когда животные являются кроликами (BEDIN и др., 2013). Визуализация голосовой щели с помощью ларингоскопа у этих животных практически невозможна (BEDIN и др., 2013). Слепой метод, основанный на дыхании, обычно является наиболее частым методом интубации у кроликов. Из-за сложности интубации трахеи многие, кто работает в этой области, используют трахеостомические или гортанные маски (THOMPSON et.al., 2017). Анестезиологические процедуры у кроликов можно проводить под лицевой маской или ларингеальной маской с кислородом и галогенированным анестетиком при спонтанном дыхании (BEDIN et.al., 2013).
В процедурах, в которых необходима легочная вентиляция легких, это может быть ручной, с использованием системы Mapleson D, или механической управляемой вентиляции с круговым фильтром (BEDIN et.al., 2013). Мониторинг в первую очередь клинически основан на наблюдении жизненно важных данных, таких как частота сердечных сокращений, частота дыхания, слизистое окрашивание и наличие окулопалпебраальных рефлексов. Они регулярно используются для этого мониторинга прекордического стетоскопа, электрокардиоскопа и импульсной оксиметрии. Другие мониторы должны использоваться в соответствии с потребностями, навязанными дизайном исследования, и капнографы, инвазивные и неинвазивное кровяное давление могут быть полезны.
Послеоперационный период является частью обезболивающего протокола, и уход за животным имеет основополагающее значение в настоящее время. Осложнения, такие как угнетение дыхания, которые могут возникнуть во время анестезии, становятся смертельными в этот период. После окончания обезболивающе-хирургической процедуры, животные должны быть направлены для анестезии восстановления. Это место должно хранить молчание, с низкой освещенностью, и, чтобы избежать стресса животных, нужно иметь минимальную управляемость. Если эвтаназия предусмотрена в протоколе исследования методы для этого господина должны обеспечить бессознательное следуют прекращение сердцебиения и дыхательных путей и окончательное прекращение функций мозга. В идеале, техника позволит свести к минимуму беспокойство, с которыми сталкиваются животные до потери сознания.
Для кроликов наиболее часто используемыми методами эвтаназии являются: вдыхаемый CO2, вдыхаемые агенты, венозные барбитураты и венозный хлорид калия, который используется только у животных при глубоком сечении, потому что венозная инъекция болезненна (BEDIN et.al., 2013).
На основе этих данных из литературы, он был принят в качестве анестезии процедуры, используемой в качестве обычно в дисциплине оперативной техники и анестезиологии медицинского курса Университета Joinville региона (UNIVILLE) для анестезии у кроликов (BEDIN et.al., 2013):
- После идентификации проводится взвешивание: эта идентификация и регистрация животных являются неотъемлемой частью предоперационного периода. После взвешивания, это животное должно быть идентифицировано с его числом и соответствующим весом.
- Для преанестетических препаратов, ацепромазин 1 mg.kg-1 и кетамин 15 mg.kg-1 используются примерно за пятнадцать-двадцать минут до начала трихотомии.
- Трихотомия проводится в передней части шеи, живота и уха.
- Иммобилизация выполняется на операционном столе вообще.
- Венозная катетеризация проводится в маргинальной вене уха с катетером 24 Г. Впоследствии проводится внутривенная установка 0,9% 250 мл солевого раствора.
- При анестезии кетамин от 5 до 10 mg.kg-1 в последовательных дозах, при необходимости. Для вентиляции используется лариса маска No1. В определенных ситуациях (торакальные операции) проводится трахеальная индубация канюлой No 2 или 3 или трахеостома.
- Мониторинг осуществляется с помощью прекордического стетоскопа (или, по возможности, пищевода), оксиметрии пульса (при наличии) и электрокардиокопии (при наличии).
- Для ингаляционной анестезии, используемой для технического обслуживания, изофлюран состоит из 1% до 3% изофлюрана и кислорода от двух до трех литров в минуту под маской в системе Mapleson D.
- Каждые 5-10 минут для подготовки формы анестезии отмечаются жизненно важные признаки.
- В постанестетический период данные отмечаются с самого начала восстановления до восстановления сознания и физиологические закономерности находятся в пределах нормального диапазона.
- Для послеоперационного контроля боли, устные парацетамол используется между 10 и 15 mg.kg-1, три раза в день, имея дидирон здесь в качестве альтернативы.
- Если протокол исследования предусматривает эвтаназию, он может быть выполнен в ингаляционной камере CO2 с 10 л.мин-1 в течение 10 минут. Вторым выбором может быть хлорид калия при 19,1% 1 ml.kg-1 венозной, но с животным седан с кетамином от 1 до 10 мг mg.kg-1 венозной или подкожной пятнадцать-двадцать минут до хлорида калия (BEDIN et.al., 2013).
ОТЧЕТ О СЛУЧАЯХ
Анестезии, которые являются частью этой серии были санкционированы Комитетом по этике по исследованию использования животных Университета Joinville региона (CEUA) номер 0103/2018.
Восемь новозеландских кроликов, представленных на лапаротомии, демонстрируют дисциплину оперативной техники местного медицинского курса (таблица 1).
Таблица 1. Демография.

Для преанестетических препаратов, ацепромазин 1 mg.kg-1 был использован с кетамином 15 mg.kg-1 подкожно (таблица 2).
Таблица 2. Преданестетические и интраоперационные препараты.
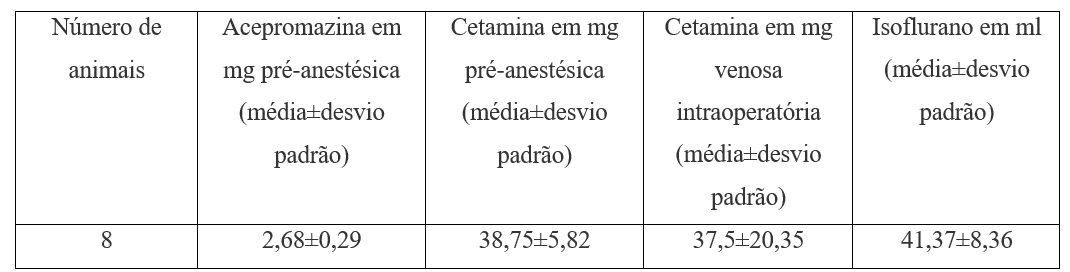
Для поддержания анестезии, изофлюран и кислород был использован в некалиброванном испаритель после прохождения ларингальной маски No 1 и Mapleson D ингаляционной системы анестезии при спонтанном дыхании всегда. Гидратация была с солевым раствором 10 ml.kg-1 (таблица 2). Использовался тепловой матрас. Для мониторинга использовались прекордический стетоскоп, оксиметрия пульса и клинические параметры (непроизвольные движения, окулопалпебральный рефлекс). Для эвтаназии, 10 mg.kg-1 кетамин следуют 5 до 15 минут после хлорида калия 19,1% 1 ml.kg-1, а также внутривенно (таблица 3) был использован.
Таблица 3. Эвтаназия лекарства.

ОБСУЖДЕНИЕ
Изофлуран часто используется в качестве единственного агента или в сочетании с опиоидами для анестезиологических процедур у кроликов (BAILEY et.al., 2017; TEARNEY et.al., 2015). Введение фентанила кроликам, анестезированным изофлураном, приводило к улучшению среднего артериального давления и сердечного выброса по сравнению с одним изофлураном (BAILEY et al., 2017; TEARNEY et.al., 2015). Ацепромазин (основной транквилизатор) и кетамин (диссоциативный анестетик) – это препараты, которые часто используются в качестве преанестезирующих препаратов и анестетиков для кроликов1,8,9. И ацепромазин, и кетамин снижают потребление изофлурана в качестве основного анестетика у кроликов (BEDIN et.al., 2013; BOTMAN et.al., 2019; ECKLEY et.al., 2020).
ЗАКЛЮЧЕНИЕ
При длительной анестезии, такой как лапаротомия, рекомендуется и применение предантетических препаратов, а затем анестезируемой индукции, сделанной комбинацией агентов (ECKLEY et.al., 2020). Тем не менее, анестезия требует мониторинга, чтобы предотвратить недостаточные или преувеличенные дозы не происходит. Для предотвращения вариаций рекомендуется следить за жизненными признаками с начала пользования животными, представленными ингаляционной анестезией, и весь период, в течение которого сохраняется анестезия до эвтаназии (BEDIN et.al., 2013).
ССЫЛКИ
ATALAN, Güneri e colab. Comparison of systemic effects of midazolam, ketamine, and isoflurane anaesthesia in rabbits. Journal of Veterinary Research (Poland), v. 63, n. 2, p. 275–283, 2019.
BAILEY, Ryan S. e BARTER, Linda S. e PYPENDOP, Bruno H. Pharmacokinetics of dexmedetomidine in isoflurane-anesthetized New Zealand White rabbits. Veterinary Anaesthesia and Analgesia, v. 44, n. 4, p. 876–882, 1 Jul 2017.
BEDIN, Antonio e JUNIOR, Harry e KRELING, Patricia. Anestesia para cirurgia experimental em coelhos. v. 42, n. 2, p. 33–37, 2013.
BOTMAN, Julie e colab. Postanaesthetic effects of ketamine-midazolam and ketamine-medetomidine on gastrointestinal transit time in rabbits anaesthetised with isoflurane. Veterinary Record, 2019.
ECKLEY, Samantha S e colab. Acepromazine and Chlorpromazine as Pharmaceutical-grade Alternatives to Chlorprothixene for Pupillary Light Reflex Imaging in Mice. Journal of the American Association for Laboratory Animal Science : JAALAS, 8 Jan 2020. Disponível em: <http://www.ncbi.nlm.nih.gov/pubmed/31915106>. Acesso em: 10 fev 2020.
RAILLARD, Mathieu e colab. Anaesthetic and perioperative management of 14 male new zealand white rabbits for calvarial bone surgery. Animals, v. 9, n. 11, 1 Nov 2019.
TEARNEY, Caitlin C. e BARTER, Linda S. e PYPENDOP, Bruno H. Cardiovascular effects of equipotent doses of isoflurane alone and isoflurane plus fentanyl in New Zealand white rabbits (Oryctolagus cuniculus). American Journal of Veterinary Research, v. 76, n. 7, p. 591–598, 6 Jul 2015.
THOMPSON, Krista L. e MEIER, Thomas R. e SCHOLZ, Jodi A. Endotracheal intubation of rabbits using a polypropylene guide catheter. Journal of Visualized Experiments, v. 2017, n. 129, 13 Nov 2017.
TUNCALI, Bahattin e colab. Retrospective Evaluation of Patients who Underwent Laparoscopic Bariatric Surgery. Turkish Journal of Anesthesia and Reanimation, v. 46, n. 4, p. 297–304, 16 Ago 2018. Disponível em: <http://www.ncbi.nlm.nih.gov/pubmed/30140537>. Acesso em: 29 set 2019.
[1] Окончил медицину.
[2] Выпускник медицинской школы.
[3] Анестезиолог. Магистр здравоохранения. Доктор анестезиологии.
Отправлено: апрель 2020 года.
Утверждено: июнь 2020 года.