CANALES, Inácia Maria da Silva [1], RIBEIRO, Alessandra Maximiano [2], SOARES, Amata dos Santos [3], KLINGELBT, Ingrid [4], ANDREOLLI, Rafael [5], SANTANA, Claudinei Alves [6]
CANALES, Inácia Maria da Silva. Эт аль. Исследование эффективности и безопасности препаратов, используемых во внутритериотерийной химиотерапии при лечении ретинобластомы. Revista Científica Multidisciplinar Núcleo do Conhecimento. 05-й год, Эд. 10, Вол. 04, стр. 35-51. Октябрь 2020 года. ISSN: 2448-0959, Ссылка для доступа: https://www.nucleodoconhecimento.com.br/здравоохранение/безопасности-препаратов
РЕЗЮМЕ
Ретинобластома является злокачественной опухолью, характерной для детства, которая когда-то была признаком энуклеации, с 2005 года применяется инновационное лечение внутриартериальную химиотерапию, которая оказалась эффективной, принося хороший контроль опухоли и минимальные системные осложнения. Исследования представляют результаты эффективности и безопасности этой терапии, используемой в некоторых странах, а также основные используемые препараты и положительные результаты в лечении ретинобластомы. Информация была получена в результате исследования, опубликованного в научной литературе, в ходе которого было установлено, что наиболее часто используемыми препаратами внутрипрусной химиотерапии являются мелфалин, карбоплатин и топотекан. Из этих результатов можно сделать вывод, что препаратом выбора является мелфан, который может быть использован в монотерапии или в сочетании с карбоплатином или топотеканом. В настоящее время продолжаются исследования, оценивающие эффективность и безопасность топотекана и карбоплатина в педиатрии, будь то в монотерапии или комбинированной терапии с другими антинеопластическими препаратами.
Ключевые слова: Ретинобластома, Внутриартериальная химиотерапия, мелфан, топотекан, карбоплатин.
1. ВВЕДЕНИЕ
Ретинобластома является заболеванием, характеризующимся внутриглазной злокачественной опухоли, происходящих из эктодермальной невра мембраны эмбриональной сетчатки, которая проявляется в детстве, с признаками и симптомами, меняющихся в зависимости от размера и местоположения, наиболее распространенным является лейкококк, также называемый рефлекс “кошачий глаз”, будучи важным диагностическим критерием, и другие проявления могут возникнуть, которые могут возникнуть, которые могут возникнуть , глаукома, косоглазие и конъюнктивальный гиперемия (SELISTRE, 2013; INSTITUTO ONCOGUIA, 2017; DEPARTAMENTO CIENTÍFICO DE ONCOHEMATOLOGIA, 2015).
Существует две формы проявления заболевания: односторонняя (около 3 случаев у 4 детей) и двусторонняя (около 1 случая у 4 детей), без предрасположенности к расе и этническому признаку, это происходит почти в равной степени у мальчиков и девочек, а также может повлиять на правый или левый глаз, но это может быть спорадическим или наследственным (INSTITUTO ONCOGUIA, 2017).
С процентом от 30 до 40% наследственного происхождения с двусторонней или многофокалиптической мутацией зародышей и от 60 до 70% являются ненаправленными формами, и связана соматическая, односторонняя и однофокальцевая мутация (FABIAN, 2017; PINA, 2012).
Классификация в настоящее время наиболее часто используемых в постановке локализованных форм этого типа опухоли в соответствии с Международной системой классификации внутриглазной ретинобластомы. Эта классификация основана на размере поражения, расстоянии от опухоли по отношению к фотону и зрительному диску, а также наличии субретинского или стекловидного распространения (Revista da Sociedade Portuguesa de Oftalmologia).
Международная классификация внутриглазной ретинобластомы показана в таблице ниже:
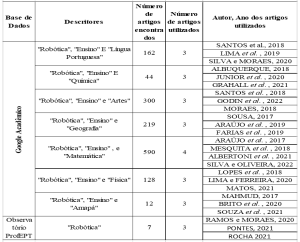
Таблица 1. Международная классификация внутриглазной ретинобластомы и скорость сохранения глазного яблока.
| Международная система классификации внутриглазной ретинобластомы | Скорость консервации глазного яблока в литературе |
| Группа A:
Небольшие опухоли (диаметром до 3 мм) ограничиваются сетчаткой, которые не близки к важным структурам, таким как зрительный диск (место, куда входит зрительный нерв) или фовеола (центр зрения). |
100% |
| Группа B:
Все остальные опухоли (больше 3 мм, но близко к зрительного диска или foveola), которые по-прежнему ограничивается сетчатки. |
93% |
| Группа C:
Четко определенные опухоли, с небольшой дисперсией под сетчаткой или в желатиновый материал, который наполняет глаз. |
90% |
| Группа D:
Большие или плохо определенные опухоли с скомпрометированным стекловидного юмора или субретинского участия. Сетчатка может отделяться от задней части глаза. |
47% |
| Группа Е.
Опухоль очень большая, простирается близко к передней части глаза, является геморрагической или вызывает глаукому, или имеет другие особенности, которые означают, что практически нет возможности глаз может быть сохранен. |
0%* |
Fonte: Adaptado de Instituto Oncoguia (2017).
Заболеваемость колеблется от 1/16 000 до 1/18 000 живорождений, затрагивающих 8102 ребенка в год во всем мире (NETO, 2016).
В Бразилии ожидается около 400 новых случаев заболевания в год, как правило, у младенцев и детей младшего возраста, а средний возраст при постановке диагноза составляет 2 года, редко затрагивая детей старше 6 лет (NETO, 2016; AMERICAN CANCER SOCIETY, 2018).
В Соединенных Штатах ежегодно от 200 до 300 детей с диагнозом ретинобластома (AMERICAN CANCER SOCIETY, 2018).
Двадцать лет назад лечение ретинобластомы было синонимом энуклеации или внешней лучевой терапии, которая чаще всего вызывала энофтальмию и отмеченные деформации лица (RODRIGUES; LATORRE e CAMARGO, 2004; CARDOSO et al., 2011).
Тем не менее, новые методы показали эффективность регрессии опухоли или, по крайней мере, контроля, с эстетическими и функциональными преимуществами от таких методов, как лазерная фотокоагуляция, внутриартериальная химиотерапия, криотерапия, интравитреальная химиотерапия, брахитерия, протонное облучение частиц или ионы гелия и энуклеации (ERWENNE, 1998; AMERICAN CANCER SOCIETY, 2018; INSTITUTO ONCOGUIA, 2018; LIANG, 2020).
Одной из применяемых в настоящее время форм является внутриартериальная химиотерапия, разработанная в Соединенных Штатах в середине 2005 года и затрагивающая весь мир, при этом Бразилия является одной из стран с большим опытом в этой области, представляя себя в качестве эффективной альтернативы в лечении прогрессивной детской ретинобластомы, минимизируя потребность в энуклеации (INCA, 2019).
Для этой методики используются препараты, относящиеся к классической химиотерапии, характеризующиеся тремя терапевтическими классами: алкилатинными агентами, ингибитором платины и топоизомеразы. Мелфалин является антинеопластическим агентом, который действует как алкилатинный агент / азотная горчица, полученная из мезлоретамина, вмешиваясь в пересечение цепей ДНК, предотвращая репликацию и приводит к гибели клеток, неспецифического фазового агента клеточного цикла (MOC BRASIL, 2020).
Карбоплатин, принадлежащий к второму поколению платиновых аналогов, действует аналогично алкилятивным агентам и имеет биохимические свойства, похожие на цисплатин, преимущественно производит межцепные перекрестные связи в ДНК, изменяя его структуру и препятствуя его синтезу, неспецифическому фазовому агенту клеточного цикла (MOC BRASIL, 2020).
Топотекан имеет противоопухолевую активность, связанную с ингибированием топоизомеразы-I, фермента, тесно участвующая в репликации ДНК, снятия стресса, введенного перед движущаяся вилкой репликации, стабилизирующей ковалентный ферментный комплекс с цепочкой проливов ДНК, которая является промежуточным каталитическим механизмом, вызывая индукцию белка, связанную с простыми разрывами цепи ДНК (EMA, 2009).
Процедура основана на введении микрокатер в бедренной артерии медленно вставляется через кровеносные сосуды в офтальмологическую артерию, таким образом, препараты вводятся непосредственно в кровеносный сосуд, который орошает глаз, повышая точность достижения желаемой цели, обеспечивая высокую концентрацию химиотерапии в месте опухоли, и присутствие специализированного специалиста необходимо (PETERSON et al. , 2011).
Оказание помощи онкологическим больным включает в себя несколько интегрированных специальностей, из которых фармацевтический специалист играет важную роль в связи с высокой сложностью лечения, будучи фундаментальными конкретными техническими знаниями, навыками и компетенциями, направленными на повышение эффективности и безопасности лечения (ANDRADE, 2009; MATILE, 2008; GEUM, 2016; INCA; REDE CÂNCER, 2019).
2. МЕТОДОЛОГИЯ
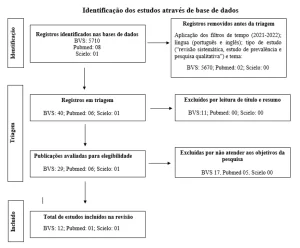
Это обзорная статья научной литературы с поиском в базах данных (PubMed, SciELO, клинические испытания и Кокрановская библиотека) и правительственных веб-сайтах (INCA, SBOC, Oncoguia, GRAAC, American Cancer Society e Sociedade Mineira de Pediatria).
Ключевыми словами для исследования были на португальском и английском языках: Ретинобластома. Внутриартериальная химиотерапия, мелфалан, топотин, карбоплатин и соответствующие английские корреспонденты, “ретинобластома”, “внутрижелутная химиотерапия”, “мельфалан”, “топотин”, “карбоплатин”.
Период поиска был с мая/2019 по февраль/2020.
3. Обсуждения
Ретинобластома считается серьезным раком, при котором лечение требует использования специфических методов и антинеопластических препаратов (таких как мелфан, карбоплатин и топотекан) по отношению к внутриартериольную химиотерапию, в которой безопасность и эффективность требуют оценки (INSTITUTO ONCOGUIA, 2018).
3.1 МЕЛФАЛИН
Наиболее часто используемым химиотерапевтическим агентом в этом методе является мелфалин, благодаря его безопасности и минимальной системной токсичности. Инъекционная форма содержит 50 мг лиофилинизированного вещества, с 10 мл разгрунтного раствора. Полученный из мезлоретамина, мелфалин препятствует скрещиваниям цепей ДНК, предотвращая репликацию и приводит к гибели клеток, неспецифического фазового агента клеточного цикла (ABRAMSON, 2008; ANVISA, 2018).
Хотя нет протокола в качестве ссылки на дозировку, эффективная и безопасная офтальмологическая доза составляет менее 0,5 мг/кг; его системное поглощение является минимальным и токсичность представлена как незначительные нейтропении. Перед процедурой рекомендуется фильтровать мелфан, так как могут быть мелкие частицы, которые эмболизируют глазные сосуды, вызывающие осложнения в процедуре (MOC BRASIL, 2020).
Анализ, проведенный в международной базе данных клинических испытаний, показал, что в настоящее время проводятся исследования, доказываемые безопасность препарата мелфалин в внутритериальной терапии. На этапе тестирования было обнаружено три исследования и одно завершено (ABRAMSON, 2008; NIH US, 2013; NIH US, 2017; DUANGNATE et al., 2019).
В ноябре 2017 года было опубликовано исследование, проведенное в штате Мэриленд – США, чтобы указать на безопасность внутриартериальных методов при использовании мелфана с целью найти терпимую дозу препарата. Мелфалин использовался через бедренную артерию, пролитую в течение 30 минут у 10 детей с прогрессивной ретинобластомой (фаза V), уже с указанием энуклеации. Результаты показали, что техника представляет минимальные системные и локальные побочные эффекты (класс 3 нейтропения). Из 10 глаз 7 были восстановлены, 1 не увенчался успехом из-за сосудистой аномалии в артерии, 1 развилась ишемия сетчатки и 1 развилась лучевая ретинопатия после брахитерапии. Этот метод был впервые описан Дэвидом Х. Абрамсон в фазе I / II клинических испытаний, проведенных в Мемориал Слоун-Кеттеринг онкологический центр больницы в Нью-йорке, с использованием мелфана во внутриартериальной химиотерапии в офтальмологической артерии для лечения внутриглазной ретинобластомы (ABRAMSON, 2008).
Дальнейшие исследования все еще продолжаются. В Испании, неугадированных фазы II клинических испытаний направлена на сохранение остроты зрения пациентов, использующих мелфалин во внутритериальной терапии у 5 пациентов (NIH US, 2013).
Детская онкологическая группа США направляет клинические испытания с 14 участниками, чтобы оценить скорость восстановления глаз после лечения внутритериальным мелфалином у детей с недавно диагностированной односторонней ретинобластомой с болезнью группы D. , имеет в качестве членов детских больниц, университетов и онкологических центров в Северной Америке (NIH US, 2017).
В Калифорнии, Сан-Франциско, проводится исследование для проверки безопасности комбинации стандартной, чередуя химиотерапевтическую терапию и внутриартериальную химиотерапию с использованием мелфана в сочетании с другими антинеопластическими препаратами (карбоплатин, этопозид и винкристин) в различных интервальных режимах. В исследовании использовались 6 пациентов с передовой и недавно диагностированной внутриглазной ретинобластомой (NIH US, 2017).
Исследования доказали эффективность внутритериальной терапии. Опрос, проведенный в Таиланде с января 2009 года по ноябрь 2017 года, показал положительные результаты, где мельдоний используется в качестве основного препарата. Из 27 глаз 26 пациентов с ретинобластомой 7 (26%) внутритериальная химиотерапия в качестве первичного лечения и 20 (74%) мак (внутритермальная химиотерапия) в качестве вторичного лечения. Глаза были классифицированы по Международной классификации ретинобластомы (ICRB) как группа B (n 3,11%), группа C (n 1,4%), группа D (n 12,44%) и группа E (n No 11, 41%). Среднее число сессий МАК составило 3 (диапазон от 1 до 7). В среднем за 32 месяца (диапазон от 3 до 95 месяцев) общий показатель восстановления земного шара составил 52%, при этом 100% в группах В и С, 75% в группе D и 9% в группе Е. Осложнения ASD включали окклюзионную васкулопатию (n – 4,15%), кровоизлияние в стекловидное заболевание (n – 3,11%), осадки сетчатки (n – 2,7%), косоглазие (n 2,7%) и транзиторная ишемическая атака (n 1,4%). (n = 25) (DUANGNATE, 2019).
3.2 КАРБОПЛАТИН
Карбоплатин широко распространен без белковых переплетов, с печеночным метаболизмом и выделением почек. Введение и разбавление происходят внутривенно (EV) в 30 до 120 минут, внутриперитонеальный. Разбавление происходит в SF или SG 5% (желательно) при концентрации от 0,5 до 2 мг/мл, не требуя корректировки функции печени, а для функции почек формула AUC (область под кривой) автоматически корректирует дозу (MOC BRASIL, 2020).
Благодаря исследованиям, зарегистрированным на веб-сайте клинических испытаний, было найдено только одно исследование для лечения ретинобластомы с использованием карбоплатина с помощью внутритериальная химиотерапия. Это исследование началось 6 марта 2019 года в онкологическом центре Memorial Sloan Kettering, Нью-йорк, Сша, и было в фазе добровольного набора (NIH US, 2019).
Целью данного исследования является определение того, является ли лечение внутритериальным карбоплатином причиной потери слуха у детей. Для исследования был создан метод когорты наблюдений, в котором, по оценкам, приняли участие 50 добровольцев обоих полов, с этим заболеванием, в возрасте от 3 месяцев до 18 лет. Результаты будут иметь внутритериальную пост-слуховую оценку (ИИ) с карбоплатином допускается только через 9 месяцев или примерно через год с начала лечения. Ожидается, что исследование будет завершено в марте 2021 года (NIH US, 2019).
Согласно исследованию, проведенному в Японии специалистами по внутритериальной химиотерапии, применение препарата карбоплатин, который является производным платины, имеет меньше побочных эффектов, чем его прекурсор цисплатин, то есть более низкую почечную, неврологическую и желудочно-кишечную токсичность (MANJANDAVIDA et al., 2019).
Тем не менее, карбоплатин через протокол используется с двумя препаратами для односторонней внутрипрусной химиотерапии (МАК), наряду с мелфалином и топотеканом. В двустороннем МАК, чтобы избежать кумулятивной токсичности мелфана, что приводит к миелосупрессии, доза мелфалина уменьшается с добавлением карбоплатина без ущерба для эффекта МАК. Рекомендуемая доза составляет от 15 до 30 мг (MANJANDAVIDA и др., 2019).
3.3 ТОПОТЕКАН
Доклинические данные по глазной фармакологии суперселективного внутритериевого топотекана (SSOAI) были основаны на экспериментах в свиной модели. После введения 1 мг топотекана SSOAI в течение 30 минут, топотекан достиг стекловидной концентрации выше ic50 рассчитывается до 4 часов, доля в пять раз выше в стекловидной плазмы по сравнению с Melphane, наиболее часто используемый агент для SSOAI. В дополнение к найти в стекловидном юморе до 16 часов после инфузии, в отличие от быстрого ухудшения Мельфан в той же прикладной технике (SOUZA и др., 2019).
Оптимальная доза топотекана по этому маршруту еще предстоит установить, но все признаки того, что доза будет между 0,5 мг до 4 мг. Таким образом, топотекан является интересным кандидатом препарат для SSOAI на основе проникновения и благоприятного проживания в стекловидномозе (SOUZA и др., 2019).
Из-за высокой скорости облучения плазмы топотекана такая ситуация может способствовать благоприятному проникновению препарата через кровено-ретинский барьер, а значит, достигать более глубоких слоев оптической области. Предварительные исследования показывают, что в этой внутренней структуре глаз топотекан клиренс ограничивается стекловидного тела и его устранение через разрыв, при этом, это связано с более низкой токсичностью препарата в системных регионах (SCHAIQUEVICH et al., 2014).
Вопросы, благоприятные для офтальмологического применения, связаны со стабильностью в растворах разбавления, избегая образования осадков, которые могут быть вредны для пациента. И плазменная фармакокинетика, сопутствуя которой связаны внутриартериальный топотекан и мельфалин, где не было клинических нарушений в лечении (SCHAIQUEVICH et al., 2014).
С ноября 2011 года в базе данных клинических испытаний было проведено постоянное исследование, в котором приняли участие 36 пациентов обоих полов в возрасте до 15 лет с историей рецидивирующей и/или огнеупорной двусторонней ретинобластомы, которые имели внутритерильную офтальмологическую топотеканную администрацию для проверки эффективности и безопасности. Вмешательство было связано с настойом топотекана в течение 30 минут, каждые 21 день, в течение периода до 18 недель. Результаты будут иметь в качестве параметров остроту зрения, электроретинограмму, визуальный потенциал и функциональную магнитно-резонансную томографию (NIH US, 2017).
Как указывалось ранее, это продолжающееся исследование, и по этой причине нет убедительных данных, так как последнее обновление с момента исследования датируется 1 марта 2017 года. Поэтому трудно установить роль топотекана как единого агента для лечения ретинобластомы. Но из-за низкой токсичности глаз, по всем маршрутам введения, вполне вероятно, что его место в терапевтическом арсенале против ретинобластомы, находится в комбинированных многоагентных схем химиотерапии (NIH US, 2017).
4. ЗАКЛЮЧЕНИЕ
Безопасность и эффективность изученных препаратов доказали, что мелфалин является основным используемым препаратом и что он соответствует этим характеристикам. Мелфан может быть использован индивидуально или вместе в дозах ниже 0,5 мг/кг, варьирующихся в зависимости от размера и тяжести внутриглазной опухоли, и его побочные эффекты были доказаны в исследованиях, как легкая нейтропения.
Как видно, Есть в настоящее время исследования в несколько этапов, которые оценивают эффективность и безопасность других препаратов, таких как карбоплатин и Топотекан, которые будут применяться индивидуально или в связанных с ними схеме химиотерапии у педиатрических пациентов.
Потому что последние исследования не доступны до сих пор убедительные результаты, но все указывает на то, что в будущем эти препараты будут частью терапевтического арсенала, либо индивидуально или быть частью комбинированных многоагентных схем химиотерапии.
ССЫЛКИ
ABRAMSON, David et al. Estudo de fase I / II da quimioterapia intra-arterial direta (artéria oftálmica) com melfalano para resultados iniciais de retinoblastoma intra-ocular. Nova York, EUA, Volume 115, Edição 8, p.1398-1404.E1, 14 de março de 2008. Disponível em: <https://pubmed.ncbi.nlm.nih.gov/18342944/?dopt=Abstract>. Acesso em: 20 Jun. 2019.
AGÊNCIA EUROPEIA DE MEDICAMENTOS (EMA). ANEXO I RESUMO DAS CARACTERÍSTICAS DO MEDICAMENTO: Topotecano. EUROPA, 2009.
AMERICAN CANCER SOCIETY. Principais Estatísticas do Retinoblastoma. 2018.
AMERICAN CANCER SOCIETY. Quimioterapia para retinoblastoma: Quimioterapia intra-arterial. 2018.
AMERICAN CANCER SOCIETY. Terapia a laser (fotocoagulação ou termoterapia) para retinoblastoma. 2018.
ANDRADE, Cinthya. Farmácia Hospitalar: FARMACÊUTICO EM ONCOLOGIA: INTERFACES ADMINISTRATIVAS E CLÍNICAS. Comissão de Farmácia Hospitalar do Conselho Federal de Farmácia, 2009.
ANVISA, bulário eletrônico. ALKERAN® (melfalana), 2018.
DEPARTAMENTO CIENTÍFICO DE ONCOHEMATOLOGIA. Teste do olhinho e o RETINOBLASTOMA. 2015.
DUANGNATE, Rojanaporn et al. Quimioterapia Intra-Arterial para Retinoblastoma: Experiência de 8 anos de um Instituto de Referência Terciária na Tailândia. Filadélfia, Pensilvânia, Volume 8, Edição 3, p. 211-217, Maio-junho 2019.
ERWENNE, Clélia. ATUALIZAÇÃO CONTINUADA: Os métodos de tratamento e as rotinas em tumores intraoculares. São Paulo, 61(5), Outubro/1998.
FABIAN, Ido et al. Tratamento focal a laser, além de quimioterapia para retinoblastoma. Reino Unido, 07 junho 2017. Disponível em: <https://www.cochranelibrary.com/cdsr/doi/10.1002/14651858.CD012366.pub2/full>. Acesso em: 21 Nov. 2019.
GEUM. Atuação do farmacêutico hospitalar na oncologia: Performance of hospital pharmacist in oncology. Piauí, v. 7, n. 1, p. 54-63, jan/mar 2016. Disponível em: <https://revistas.ufpi.br/index.php/geum/article/view/4018/2916>. Acesso em: 21Out. 2019.
INSTITUTO NACIONAL DE CÂNCER. Educação: Os múltiplos papéis do farmacêutico na atenção oncológica. Rede Câncer, p. 24-29.
INCA – Instituto Nacional de Câncer. QUIMIOTERAPIA INTRA-ARTERIAL PRESERVA OLHO E VISÃO EM TUMOR OCULAR COMUM NA INFÂNCIA: Direto no alvo. p. 11-13, Rede Câncer.
INSTITUTO ONCOGUIA. Quimioterapia para Retinoblastoma. 2017.
INSTITUTO ONCOGUIA. Diagnóstico do Retinoblastoma. 2017.
INSTITUTO ONCOGUIA. Tipos de Câncer RETINOBLASTOMA: Estadiamento do Retinoblastoma. 2017.
KRONBAUER, Fernando et al. O uso da quimioterapia no tratamento do retinoblastoma: Avaliação retrospectiva: The use of chemotherapy in the treatment of retinoblastoma: Retrospective analysis. Porto Alegre (RS), 63(6), Dezembro/2000.
LIANG, Ting et al. Quimioterapia intra-arterial combinada e melfalano intravítreo para o tratamento de retinoblastoma unilateral avançado. China, 13(2): 257–262, 18/fevereiro/2020. Disponível em: https://www.ncbi.nlm.nih.gov/pmc/articles/PMC7013797/>. Acesso em: 10 Fev. 2020.
MANJANDAVIDA, Fairooz et al. Quimioterapia intra-arterial no retinoblastoma – Uma mudança de paradigma. Filadélfia, EUA, Volume 67, Edição 6, Página: 740-754, 24/Maio/2019. Disponível em: <http://www.ijo.in/article.asp?issn=0301 4738;year=2019;volume=67;issue=6;spage=740;epage=754;aulast=Manjandavida>. Acesso em: 20 Jun. 2019.
MATILE, Elisa. Papel do Farmacêutico na Oncologia: da manipulação à assistência farmacêutica: The Role of the Pharmacist in Oncology: drug manipulation and pharmaceutical support. Curitiba, Vol. 5, N.º 14, p. 29-31, Mai/Ago 2008.
MOC Brasil: Manual de Oncologia Clínica do Brasil. CARBOPLATINA: (Platamine CS®, Carboplatina genérico). 2020.
MOC Brasil: Manual de Oncologia Clínica do Brasil. MELFALANA: (Alkeran®).2020.
NETO, Joaquim. Diagnóstico Precoce do Retinoblastoma: Boletim Científico – Oncologia. 2016. Sociedade Mineira de Pediatria – SMP. Minas Gerais.
NIH US. National Library of Medicine – Clinical Trails. Quimioterapia Intra-arterial com Melfalan para o Tratamento de Retinoblastoma (RTB) em Estágio Intraocular Avançado. Espanha, 05/2013. Clinical Trails. Disponível em: <https://clinicaltrials.gov/ct2/show/NCT01393769?term=melfalano&cond=Retinoblastoma&draw=2&rank=1>. Acesso em: 11 Fev. 2020.
NIH US. National Library of Medicine – Clinical Trails. Melfalano intra-arterial no tratamento de pacientes mais jovens com retinoblastoma unilateral. Califórnia, EUA, 2017. Disponível em: <https://clinicaltrials.gov/ct2/show/NCT02097134?term=NCT02097134&draw=2&rank=1>. Acesso em: 11 Fev. 2020.
NIH US. National Library of Medicine – Clinical Trails. Quimioterapia sistêmica alternada e quimioterapia intra-arterial do melfalano em crianças com retinoblastoma intraocular. Califórnia, São Francisco, 2017. Disponível em: <https://clinicaltrials.gov/ct2/show/NCT02116959?term=NCT02116959&draw=2&rank=1>. Acesso em: 11 Fev. 2020.
NIH US. National Library of Medicine – Clinical Trails. Determinando se a carboplatina intra-arterial causa perda auditiva em crianças. Nova York, EUA, 2019. Disponível em: <https://clinicaltrials.gov/ct2/show/NCT03866460?term=NCT03866460&draw=2&rank=1>. Acesso em: 12 Fev. 2020.
NIH US. National Library of Medicine – Clinical Trails. Estudo da infusão de topotecano da artéria intra-oftálmica para o tratamento de retinoblastoma (IARB1). 2017. Disponível em: <https://clinicaltrials.gov/ct2/show/NCT01466855?term=01466855&draw=2&rank=1>. Acesso em: 6 Fev. 2020.
ORESTES-CARDOSO, Silvana et al. Epidemiologia das Perdas do Globo Ocular por Retinoblastoma: Eyeball Loss Epidemiology by Retinoblastoma. Camaragibe/PE, v.11, n.2, p. 33-44, abril/junho 2011.
PETERSON, Eric et al. Infusão seletiva de quimioterapia na artéria oftálmica para retinoblastoma intra-ocular avançado: experiência inicial com 17 tumores. Miami, EUA, Volume 114, Edição 6, junho/2011. Disponível em: <https://pubmed.ncbi.nlm.nih.gov/21294621/>. Acesso em: 20 Out. 2019
PINA, Susana et al. Retinoblastoma: A nossa experiência. In: CONGRESSO PORTUGUÊS DE OFTALMOLOGIA, 55. Lisboa, 2012.
REVISTA DA SOCIEDADE PORTUGUESA DE OFTALMOLOGIA. 10 anos de experiência no tratamento do retinoblastoma. Lisboa, Volume 39, nº 2, p. 97-102, Abril-junho 2015. Disponível em: <https://repositorio.hff.minsaude.pt/bitstream/10400.10/1559/1/Oftalmologia%2C%2039%2C%2097-102.pdf>. Acesso em: 15 Fev. 2020.
RODRIGUES, Karla; LATORRE, Maria do Rosário; CAMARGO, Beatriz de. Atraso diagnóstico do retinoblastoma. Porto Alegre, volume 80, nº 6, Novembro/Dezembro 2004. Disponível em: <http://www.scielo.br/scielo.php?script=sci_arttext&pid=S0021-75572004000800014>. Acesso em: 15 Jul. 2019.
SELISTRE, Simone. Caracterização de pacientes com diagnóstico de retinoblastoma identificados nos Serviços de Oncologia Pediátrica, Oftalmologia e Genética no Hospital de Clínicas de Porto Alegre/RS. Porto Alegre (RS), 114 f., 2013.
SCHAIQUEVICH, Paula et al. Farmacologia ocular do topotecano e sua atividade no retinoblastoma. Buenos Aires, Argentina, Volume 34, Edição 9 – p. 1719-1727, Setembro 2014. Disponível em: <https://www.ncbi.nlm.nih.gov/pubmed/25099219>. Acesso em: 6 Fev. 2020.
SOUZA, Izabella et al. Análise das diferentes abordagens da quimioterapia no tratamento de retinoblastoma. Anápolis, volume 7, suplemento 1, 2019. Disponível em: <http://revistas.unievangelica.com.br/index.php/educacaoemsaude/article/download/3769/2617/>. Acesso em: 6 Fev. 2020.
[1] Фармацевтической. Специалист по клинической и больничной фармации (Senac), выпускной в области фармации и биохимии (UNINOVE).
[2] Фармацевтической. Специалист по клинической и больничной фармации (Senac), выпускной в аптеке (UNIP).
[3] Фармацевтической. Специалист по клинической и больничной фармации (Senac), выпускной в аптеке (ANHANGUERA).
[4] Фармацевтической. Специалист по клинической и больничной фармации (Senac), выпускной в аптеке (FOC).
[5] Фармацевт. Специалист по клинической и больничной фармации (Senac), выпускной в аптеке (UNIP).
[6] Советник. Фармацевт. Магистр медицинских наук, FMUSP. Специалист по многопрофильной онкологии (HSL), специалист по больничной фармации (FOC), выпуск в биохимической аптеке (USJT).
Представлено: Август 2020.
Утверждено: октябрь 2020 года.