ARTIGO DE REVISÃO
LINDESAY NETO, Edgard [1], SOUZA, Lucieny de Faria [2]
LINDESAY NETO, Edgard. SOUZA, Lucieny de Faria. Gestão De Qualidade Em Laboratórios De Análises Clínicas. Revista Científica Multidisciplinar Núcleo do Conhecimento. Ano 06, Ed. 06, Vol. 16, pp. 86-95. Junho de 2021. ISSN: 2448-0959, Link de acesso: https://www.nucleodoconhecimento.com.br/saude/analises-clinicas, DOI: 10.32749/nucleodoconhecimento.com.br/saude/analises-clinicas
RESUMO
A preocupação básica deste estudo é refletir sobre a gestão de qualidade em laboratórios de análises clínicas, este por se tratar de uma ferramenta essencial no processo saúde de uma população. Este artigo tem como objetivo descrever e entender a ação da gestão de qualidade nos laboratórios frente às possíveis interferências, falhas e erros. Realizou-se uma pesquisa bibliográfica considerando as contribuições de autores como Plebani (2007), Guimarães e colaboradores (2008), Bonato (2011), Marteli (2011), Carvalho (2012), Lemes e Rabelo (2013), Coriolano (2015), Dias e colaboradores (2018), entre outros, procurando descrever e entender as ações do sistema de gestão da qualidade relacionadas aos exames realizados no laboratório clínico. Conclui-se que a melhoria contínua é um caminho a ser percorrido para todos os laboratórios que desejam se manter no mercado. Adesão as normas da qualidade são é uma boa alternativa, os erros pré-analíticos são um desafio para o sistema da qualidade, automação e aplicação das tecnologias de informação ajudam a reduzir erros, a padronização é uma ferramenta obrigatória e útil para um sistema de qualidade eficiente agindo de forma preventiva.
Palavras-chave: Gestão de Qualidade, Laboratório Clínico, Ferramentas da Qualidade, Erros em Laboratórios.
INTRODUÇÃO
O presente trabalho tem como tema Gestão de Qualidade (GQ) em Laboratórios de Análises Clínicas (LAC), por ser um estabelecimento essencial no processo saúde da população.
Neste ponto de vista, desenvolveram-se questões que guiaram este trabalho:
- O que são desvios da qualidade em laboratórios de análises clínicas?
- Quais fases os erros são mais frequentes?
- Qual deve ser a contribuição da gestão de qualidade a fim de minimizar esses erros?
Quando se fala em laboratórios de análises clínicas lembra-se de exames e o mínimo esperado são resultados que retratem a situação real do paciente. Daí a necessidade de pesquisar GQ em LAC.
Segundo Juran (1992): “Qualidade é adequação ao uso”. Uma das contribuições de Juran foi à implantação do conceito de cliente externo/interno.
A necessidade de melhoria das análises laboratoriais faz o tema qualidade em LAC’s evoluir. A GQ em LAC’s inclui processos de gestão, melhoria e garantia da qualidade (MARTELLI, 2011).
Os testes feitos em laboratórios se tornaram parte de extrema importância na prática médica, apesar da consagrada frase “a clínica é soberana”, a participação de dados obtidos através das análises laboratoriais nunca foi tão importante como nos dias de hoje, pelo menos 70% das decisões médicas são tomadas com bases nos resultados laboratoriais (GUIMARÃES et al., 2008; XAVIER, 2011, p. 31). A melhoria dos serviços prestados aumenta: segurança do paciente, lucro e competitividade (LEMES; RABELO, 2013). Para obtenção de laudos fiéis e confiáveis, se torna essencial a gestão adequada (FERREIRA e PEREIRA, 2018).
O GQ é uma fase de grande importância em um LAC’s, por propiciar redução de erros e consequentemente, de custos. Neste contexto, o objetivo primordial deste estudo é descrever e entender a importância da GQ em LAC’s frente às possíveis interferências, falhas e erros que podem ocorrer.
Para alcançar os objetivos propostos, utilizou-se como recurso metodológico, a pesquisa bibliográfica, realizada a partir da análise pormenorizada de materiais já publicados na literatura e artigos científicos divulgados no meio eletrônico.
O texto final foi fundamentado nas ideias e concepções de autores como: Plebani (2007), Guimarães e colaboradores (2008), Bonato (2011), Marteli (2011), Carvalho (2012), Lemes e Rabelo (2013), Coriolano (2015), Dias e colaboradores (2018) entre outros citados ao longo do texto e referenciados ao final.
DESENVOLVIMENTO
A qualidade é um desafio contínuo que faz parte da humanidade desde o Egito antigo, porém com o avanço das tecnologias, as exigências sobre o aspecto qualidade também aumentaram, nos trazendo a necessidade de ações para melhoria contínua (CARVALHO, 2012).
Com o avanço da tecnologia e percepção dos clientes hoje é uma condição de pré-existência de todas as organizações, tanto na área industrial quanto na área da saúde (CARVALHO, 2012; DIAS et al., 2018). Em busca de altos índices de atividade com resultados de sucesso, competividade, eficácia e eficiência dos processos, foram adotados os Sistemas de Gestão de Qualidade (BONATO, 2011).
O LAC ou laboratório clínico é o local destinado à realização de testes laboratoriais e prática da “Medicina Laboratorial” ou “Patologia Clínica” (XAVIER, 2011, p. 31). Os exames clínicos têm a finalidade de realizar o prognóstico, acompanhamento, prevenção e diagnóstico de enfermidades. Devido à importância dos serviços executados em laboratórios, eles precisam ser acurados, exatos, precisos, e necessitam mostrar de forma fidedigna a real situação do paciente (GUIMARÃES et al., 2011; CORIOLANO, 2015).
A realização de exames é algo complexo, devido aos diversos processos e suas inter-relações, tipos de matrizes examinadas tornam o controle e padronização dos processos uma tarefa difícil e dividem o laboratório em três fases, pré-analítica, analítica e pós-analítica. A incidência de erros nas fases laboratoriais pode ser vista na tabela 2.
Tabela 1 – Dados da literatura científica sobre frequência de erros nas fases analíticas em percentual.
| Autor/ano | Nutting et al., 1993. | Goldschimidt e Lent, 1995. | Plebani e Carraro, 1997. | Sthahl et al., 1998. | Wiwanikit, 2011. | Carraro e Plebani, 2007. |
| Período de obtenção de dados | 6 meses | 6 anos | 3 meses | 3 anos | 6 meses | 3 meses |
| Frequência (%) | 0,11 de pacientes | * | 0,47 dos pacientes | 0,61 dos pacientes | * | * |
| Fase pré-analítica | 55,6 | 53 | 68,2 | 75 | 84,52 | 61,9 |
| Fase Analítica | 13,3 | 23 | 13,3 | 16 | 4,35 | 15 |
| Fase pós-analítica | 30 | 24 | 18,5 | 9 | 11,13 | 23,1 |
Legenda: * – Não analisado. Fonte: Guimarães et al., 2011.
Conforme mostrado em estudos de Guimarães et al. (2011), os motivos dos erros ocorridos na fase pré-analítica são falta de padronização, alta rotatividade de profissionais envolvidos nessa etapa, não entendimento e/ou falta de utilização das boas práticas em laboratórios e treinamento ineficiente.
A automação e envolvimento de tecnologias de informação presentes na fase analítica faz com que ela apresente com o passar dos anos grande redução dos erros (MARTELLI, 2011).
Segundo Vieira (2011) na fase pós-analíticas tem a maior participação os erros advindos da interpretação dos resultados, podendo ser diminuídos com uma comunicação efetiva entre o solicitante e o laboratório responsável pela execução do exame.
Plebani (2007), define erro de laboratório como:
Uma falha ocorrida em qualquer parte do ciclo laboratorial, ou seja, desde a solicitação médica até a interpretação e a reação do médico diante do resultado reportado, ou qualquer defeito na realização do teste que gere um resultado inapropriado ou uma interpretação equivocada.
No Brasil o grande avanço nas políticas da qualidade das indústrias do país, inclusive laboratórios clínicos, aconteceu na década de 80, tendo como grande marco a inserção de programas de controle de qualidade como a Programa Nacional de Controle da Qualidade (PNCQ) administrado pela SBAC e do Programa de Excelência para Laboratórios Clínicos (PELM) de propriedade SBPC/ML (MARTELLI, 2011).
Os programas de acreditação PALC e DICQ são modelos de qualidade onde por meio de suas normas e diretrizes, verificadas por auditorias externas periódicas que avaliam estrutura, processos e resultados, possuem adesão voluntária e comprovam por meio do certificado de acreditação que o laboratório possui um sistema de qualidade baseado na norma, capacidade técnica e organizacional (SANTOS, 2010; SBPC/ML, 2016).
Com todos os interferentes e falhas, a padronização em todas as fases de análise é essencial para se garantir a qualidade, de todas as partes envolvidas, desde o atendimento ao paciente até a liberação do laudo, nos permite chegar à qualidade desejada e a gestão da qualidade é responsável em garanti-la, padronização esta obrigatória (BRASIL, 2005; CHAVES, 2010; LEMES e RABELO, 2013). Desta forma, o SGQ do laboratório necessita de organização e disciplina em todas as fases dos diversos processos (VIEIRA et al., 2011).
O SGQ de LAC é responsável por criar manuais, normas e diretrizes da qualidade, Procedimento Operacional Padrão (POP), treinamento da equipe, inserção de indicadores e ferramentas da qualidade, de forma que consiga monitorar os processos e definir erros em potencial através de auditorias internas, e todas as ações para se garantir e/ou manter a qualidade já alcançada (LEMES e REBELO, 2013; DIAS et al., 2017).
Os indicadores são variáveis representativas e quantificáveis dos processos tem o objetivo de avaliar e fornecer informações para as tomadas de decisão (FUNDAÇÃO NACIONAL DA QUALIDADE, 2007; VIEIRA et al., 2011). Conforme observado no estudo de Vieira et al. (2011) não existe a definição de quais indicadores utilizar, pela falta de padrão nacional e internacional.
As ferramentas da qualidade são vastas, onde cada uma nos apresenta benefícios e limitações, podem ser usadas em conjunto, onde torna o sistema mais seguro, não existindo um padrão nacional ou internacional de quais das muitas ferramentas existentes são utilizadas em LAC´s e há poucos estudos nesta área. A SBPC/ML na norma PALC 2016, recomenda o uso de Failure Mode Effects Analysis (FMEA) ou outra similar. De acordo com Machado e Viegas (2012), a gestão da qualidade obteve bons resultados utilizando diagrama de Ishikawa também conhecido como espinha de peixe.
O FMEA ferramenta com seu nome em inglês, conhecida no Brasil como análise de modos de falhas e efeitos, tem sua utilização semelhante à matriz de riscos, porém é uma ferramenta mais completa e poderosa quando compreendida e utilizada da forma correta, identifica as falhas e define correções e os responsáveis por ela, pode ser utilizado para produtos e processos (RODRIGUES, 2004; SBPC/ML 2010; MARTINS, 2012).
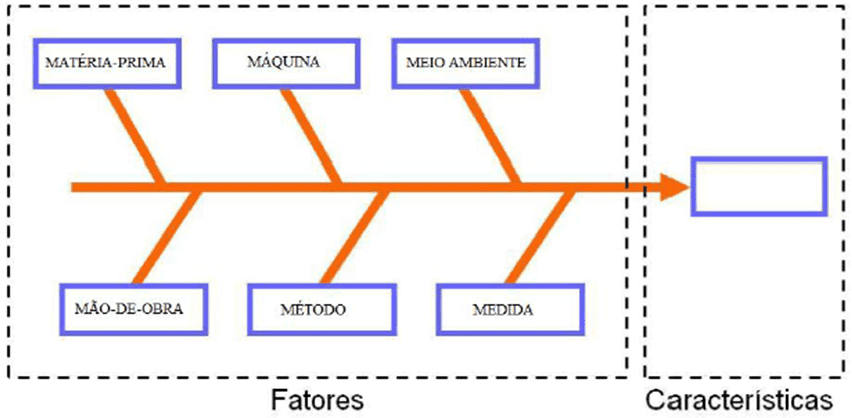
O diagrama de Ishikawa ou diagrama de causa efeito, ferramenta desenvolvida em 1943 por Kaoru Ishikawa, utilizada para sintetizar opiniões sobre o mesmo assunto e suas diversas causas, classificando de acordo com matéria, máquina, meio ambiente, mão de obra e medida (SILVA e OLIVEIRA, 2016). Estudo de Machado e Viegas (2012) aponta que a utilização do diagrama de causa e efeito facilitou a análise de problemas em LAC´s pela sua abordagem ampla das causas em potencial.
Figura 5 – Diagrama de causa e efeito (Ishikawa).
A auditoria interna é definida por Răvaş (2011) como “uma abordagem disciplinada para avaliar e melhorar a eficácia da gestão de riscos, controle e governança dos processos”. O Instituto de Auditores Internos define em 2012 a auditoria como um processo independente e objetivo, prestando serviço avaliativo e consultivo com o objetivo de somar valor e melhorar os processos de uma organização.
CONCLUSÃO
Diante do exposto no estudo que a busca pela melhoria contínua é um caminho a ser percorrido por todo laboratório que deseja a permanência no mercado se fazendo necessário um sistema de gestão da qualidade aplicado no laboratório clínico, não bastando somente o cumprimento das leis vigentes do setor (mínimo aceitável), mas entregando ao paciente e/ou médico exames que apresentem segurança e confiabilidade.
Os erros pré-analíticos possuem maior incidência e são um dos desafios para os sistemas de qualidade, pois eles podem começar antes do paciente entrar no laboratório, podem ser diminuídos com a instrução correta, sobre o preparo do paciente para realização dos exames, sendo de extrema importância a inserção de métodos para detecção, redução e classificação destes erros, já os erros pós-analíticos podem ser minimizados com a integração médico laboratório, tendo em vista que a maior parte destas falhas ocorre por interpretação errada dos exames, pelo profissional solicitante.
Os sistemas de qualidade eficiente não podem somente tratar os erros, devem ter de forma documentada como tratar e evitar que os erros em potencial se tornem erros. As ferramentas da qualidade são um importante aliado à gestão da qualidade, quando utilizadas da forma correta, sendo necessários mais estudos a cerca da utilização das ferramentas nos laboratórios clínicos.
REFERENCIAS
BERLITZ, F. D. A. Controle da qualidade no laboratório clínico- alinhando melhoria de processos, confiabilidade e segurança do paciente. J Bras Patol Med Lab v. 46,n. 5, p. 353-363 2010.
BONATO, V. L. Gestão da qualidade em saúde: melhorando assistência ao cliente. O Mundo da Saúde, São Paulo: 2011.
BRASIL. Ministério da Saúde. Agência Nacional de Vigilância Sanitária. Resolução RDC no. 302, de 13 de outubro de 2005. Dispõe sobre Regulamento Técnico para funcionamento de Laboratórios Clínicos. Diário Oficial da União da República Federativa do Brasil, Brasília, 14 out. 2005. 2005.
CARVALHO, A. M. O. Gestão da qualidade nos serviços assistenciais públicos. Revista Inova Ação, Teresina, v. 1, n. 1, art. 6, p. 52-70, jan./jun. 2012.
CHAVES, C. D. Controle de qualidade no laboratório de análises clínicas. J Bras Patol Med Lab, 2010.
CORIOLANO, N. L. Análise da frequência de recoletas de amostras biológicas como indicadores de qualidade em laboratório de análises clínicas do Distrito Federal. 2015. 37 f., il. Monografia (Bacharelado em Farmácia)—Universidade de Brasília, Brasília, 2015.
DIAS, F.A. et al. Avaliação dos métodos de controle interno da qualidade no Laboratório Clínico da Pontifícia Universidade Católica de Goiás. RBAC. 2018;50(1):38-43
DICQ. Disponível em: < http://acreditacao.org.br/wp-content/themes/dicq/pdfs/manual_dicq.pdf>. Acesso em: 12 nov. 2018
FERREIRA F. E. W.; PEREIRA J. O Futuro dos Laboratórios de Análises Clínicas no Brasil: Uma abordagem geral da situação dos pequenos laboratórios. Disponível em: < www.crfpe.org.br/website2/downloads.aspx?id=45> Acesso em: 12 nov. 2018. so em: 28 out. 2018
FNQ. FUNDAÇÃO NACIONAL DA QUALIDADE – Caderno de Excelência. São Paulo: FNQ, 2007.
GUIMARÃES, A. C. et al. O laboratório clínico e os erros pré-analíticos. Revista HCPA, v.31, n.1, p.66-72, 2008.
JURAN, J. M. Planejamento para a Qualidade. 2ª Ed. São Paulo: Pioneira. 1992.
LEMES, V. F.; RABELO, M. S. Gestão da qualidade no laboratório de análises clínicas: características e dificuldades do gestor. Goiânia. 2013.
MACHADO, B.S.B.; VIEGAS, M.C. Estudo de caso: as ferramentas da qualidade utilizadas no laboratório de análises clínicas de um hospital para a otimização de processos. UNOPAR Cient., Ciênc. Juríd. Empres., Londrina, v. 13. n. 1, p. 75-80. 2012.
MARTELLI, A. Gestão da qualidade em laboratórios de análises clínicas. São Paulo. 2011.
MARTINS, R. Análise de Modos de Falhas e Efeitos (FMEA). 2012. Disponível em: <http://www.blogdaqualidade.com.br/analise-de-modos-de-falhas-e-efeitos-fmea/>. Acesso em: 12 nov. 2018
PLEBANI, M. Errors in laboratory medicine and patient safety: the road ahead. Clin Chem Lab Med, v. 45. n. 6, p. 700-7. 2007.
Răvaş, B. The Role of the Internal Audit in the Tourism Unit’s Risk Management Process. Annals of the University of Petroşani, Economics, 1(11), pp. 215-222. 2011.
RODRIGUES, M. V. Ações para a qualidade: GEIQ, gestão integrada para a qualidade: padrão seis sigma, classe mundial. Rio de Janeiro: Qualitymark, 2004.
SANTOS, P. E. Boas práticas de laboratório (BPL). Uma questão de qualidade. Revista Intertox de Toxicologia, v. 3, n. 2, p. 37-39, 2010.
SBPC/ML, Sociedade Brasileira de Patologia Clínica/ Medicina Laboratorial. Programa de acreditação em laboratórios: Norma PALC 2016. Rio de Janeiro, 2016. Disponível em: < http://www.sbpc.org.br/upload/conteudo/norma_palc_2016_web.pdf>. Acesso em: 12 nov. 2018
SBPC/ML, Sociedade Brasileira de Patologia Clínica/ Medicina Laboratorial. Notícias medicina laboratorial. 2010. Disponível em: < http://www.sbpc.org.br/wp-content/uploads/2017/04/679564a065c02427245ca3575dcaa4a1.pdf>. Acesso em: 12 nov. 2018
SILVA, V. L.; OIVEIRA, C. C. Análise da aplicabilidade de Ferramentas da Qualidade em empresas: um mapeamento de estudos aplicados. 2016 Disponível em: http://www.fecilcam.br/anais/x_eepa/data/uploads/4-engenharia-da-qualidade/4-02.pdf>. Acesso em: 12 nov. 2018
VIEIRA, K. F. et al. A utilidade dos indicadores da qualidade no gerenciamento de laboratórios clínicos. • J Bras Patol Med Lab • v. 47 • n. 3 • p. 201-210 • junho 2011
XAVIER, R. M. O médico e o laboratório. IN: Xavier, Ricardo M. et al Laboratório na prática clínica. Porto Alegre: Artmed, 2011. Cap 1, p. 31.
[1] Farmacêutico, Especialista em Gestão da Qualidade, Especialista em Ciência do Laboratório Clínico e MBA em Marketing e Gestão de Pessoas.
[2] Dra. Em Microbiologia Médica, Mestre em Medicina Laboratorial e Tecnologia Forense. Especialista em Docência do Ensino Superior, Especialista em Ciência do Laboratório Clínico, Especialista em Bacteriologia. Farmacêutica. Bióloga.
Enviado: Fevereiro, 2021.
Aprovado: Junho, 2021.