ARTIGO ORIGINAL
AMARAL, Tatiane Domingues do [1], TAVEIRA, Stephanie Fratin [2], SOUZA, Thatiane Paulino de [3], NORIEGA, Carlos López [4]
AMARAL, Tatiane Domingues do. Et al. Comparativo das metodologias da produção de ácido lático a partir do melaço de cana-de-açúcar e sua aplicação como biopolímero (PLA). Revista Científica Multidisciplinar Núcleo do Conhecimento. Ano. 07, Ed. 09, Vol. 02, pp. 150-193. Setembro de 2022. ISSN: 2448-0959, Link de acesso: https://www.nucleodoconhecimento.com.br/quimica/producao-de-acido-latico, DOI: 10.32749/nucleodoconhecimento.com.br/quimica/producao-de-acido-latico
RESUMO
Sabe-se que os polímeros convencionais se originam de derivados de petróleo, os quais geram diversos impactos ambientais quando descartados incorretamente, principalmente quando se trata de embalagens plásticas. Devido a isso, pesquisadores têm realizado buscas para substituir polímeros convencionais por alternativas sustentáveis. O ácido lático, por sua vez, é bastante utilizado no ramo industrial em razão da sua vasta gama de aplicações, tornando-o um ácido de grande valia para as indústrias, podendo ser concebido por meio da fermentação de resíduos agroindustriais, como o melaço da cana-de-açúcar, e assim gerar subprodutos, como por exemplo o biopolímero Poli-Ácido Lático (PLA), uma alternativa biodegradável viável nesta aplicação. Mediante a isso, este artigo proverá a seguinte questão norteadora: por quais métodos se é possível obter, a partir do resíduo da cana-de-açúcar, uma melhor concentração, e consequentemente, um melhor rendimento de ácido lático para, posteriormente, originar o biopolímero Poli-Ácido Lático (PLA) a fim de que minimize o impacto ambiental? Com isso, tem-se por objetivo apresentar, por meio de uma revisão bibliográfica, um estudo comparativo entre diferentes metodologias de trabalhos experimentais de outros autores que envolvam análise do uso residual da cana-de-açúcar para a concepção do ácido lático e que, posteriormente, possa ser utilizado na fabricação do biopolímero de ácido lático, a fim de que seja analisado a viabilidade daquela que melhor se adequa ao reaproveitamento desse resíduo. A metodologia empregada foi a concepção de uma tabela comparativa contendo diferentes condições e parâmetros de artigos científicos realizados por outros autores. Logo, constatou-se que para uma maior concentração de ácido lático a melhor metodologia empregada seria a de fermentação batelada, realizando um pré-tratamento inicial de hidrólise com invertase e, utilizando o microrganismo Lactobacillus casei, obtendo-se então uma concentração final de 58,86 g/L de ácido lático. Já no processo de fermentação contínua o melhor resultado encontrado foi de 20,70 g/L, sem utilização de pré-tratamento. Portanto, através das metodologias citadas, a utilização de resíduos agroindustriais na produção do ácido lático e PLA tornaria a produção mais rentável e diminuiria os impactos ambientais causados pelos polímeros oriundos de petróleo e, também, dos resíduos descartados no meio ambiente.
Palavras-chave: Poli-ácido Lático (PLA), ácido lático, melaço de cana-de-açúcar, resíduos agroindustriais, plástico biodegradável.
1. INTRODUÇÃO
Dentre os segmentos industriais que aceleram a economia do Brasil, o setor de agronegócio apresenta uma relevante contribuição para o PIB (Produto Interno Bruto) do país, com uma participação de 27,4% em 2021, segundo dados da CEPEA (CENTRO DE ESTUDOS AVANÇADOS EM ECONOMIA APLICADA, 2022), da Esalq/USP, em parceria com a CNA (CONFEDERAÇÃO DA AGRICULTURA E PECUÁRIA DO BRASIL). Além disso, o Brasil é o produtor mundial de cana-de-açúcar, tendo produzido 654,5 milhões de toneladas (Mt) na safra referente a 2020/21, sendo que 54,1% correspondem à produção no estado de São Paulo, de acordo com as pesquisas da IEA (Instituto de Economia Agrícola).
Em relação a produção de açúcar, de acordo com dados de 2022 da CONAB (COMPANHIA NACIONAL DE ABASTECIMENTO, 2022), a safra do período 2021/22 corresponde a uma estimativa de aproximadamente 35 Mt de açúcar produzido, sendo a região Centro-Sul responsável por 32,2 Mt. O melaço, resíduo líquido proveniente da fabricação do açúcar cristalizado, corresponde a 18 Mt por ano (VARGAS, 2016). Uma grande quantidade de resíduos gerados e, na maioria das vezes, descartada de forma incorreta na natureza, resulta na poluição de solos, vegetação e águas e, consequentemente, afeta na saúde humana e dos demais seres vivos (OLIVEIRA, 2018).
Com uma adequada gestão de resíduos, os mesmos podem ser reaproveitados para a elaboração de novos produtos, diminuindo o custo com matérias-primas, além de adotar uma prática mais sustentável (MORAES et al., 2017). Como exemplo disso, é possível citar a respeito da produção de ácido lático, visto que o maior problema econômico que a sua produção enfrenta é o custo da matéria-prima elevada, tendo-se assim uma busca ativa por substratos alternativos, dentre eles subprodutos de indústrias de alimentos, agrícolas e biomassas naturais (PINHO et al., 2019). Posteriormente, esse mesmo ácido lático produzido através de resíduos agroalimentícios pode ser utilizado no desenvolvimento de biopolímeros, substituindo aqueles oriundos do petróleo (PEREIRA, 2019).
De acordo com dados emitidos pela ABRE (ASSOCIAÇÃO BRASILEIRA DE EMBALAGENS, 2021), no ano de 2019, a produção de embalagens alcançou um valor de R$ 75,9 bilhões, sendo que 39,6% desta produção total correspondem à categoria de plásticos. Ademais, com base nos dados da WWF (Fundo Mundial para a Natureza, em inglês) de 2019, o Brasil, um dos maiores produtores de plástico do mundo, produziu 11.335.220 milhões de toneladas de lixo plástico por ano, sendo que apenas 1,2% foram reciclados, ou seja, apenas 145.043 toneladas. Além disso, 2,4 milhões de toneladas são descartadas de forma indevida. Segundo a Anna Carolina Lobo, coordenadora do Programa Mata Atlântica e Marinho do WWF-Brasil, uma ação conjunta deve ser tomada, tal como as indústrias desenvolvendo novas tecnologias para a substituição do plástico comum e, também, a própria conscientização do consumidor (WWF, 2019).
O ácido lático, um composto químico bastante aplicado em diferentes setores industriais, pode ser uma alternativa na substituição desses plásticos pelo bioplástico conhecido como ácido polilático (PLA), visto que este, por ser biodegradável, desaparece em poucos dias após ser descartado, evitando a formação de resíduos (GROCHOLSKI, 2019).
É possível obter esse ácido por meio de dois processos: síntese química ou fermentação (PEREIRA, 2019). Como o preço do ácido lático para a produção de PLA é muito elevado, materiais alternativos, como os resíduos agroindustriais, têm sido levados em consideração como uma alternativa mais econômica e sustentável (PINHO et al., 2019). Dentre eles, podem-se citar os resíduos oriundos da cana-de-açúcar.
Tendo em vista a problemática referente à quantidade de lixos plásticos produzidos anualmente no Brasil e, também, aos descartes incorretos de resíduos agroindustriais, os quais prejudicam não só o meio ambiente como também a saúde humana, o presente trabalho levantou a seguinte questão norteadora: por quais métodos se é possível obter, a partir do resíduo da cana-de-açúcar, uma melhor concentração, e consequentemente, um melhor rendimento de ácido lático para, posteriormente, originar o biopolímero Poli-Ácido Lático (PLA) a fim de que minimizem esse impacto ambiental?
Por meio de uma revisão bibliográfica, tem-se, por objetivo, encontrar alternativas que minimizem esse impacto por meio de metodologias que reutilizem o resíduo do melaço da cana-de-açúcar para produzir o ácido lático que, por sua vez, possa ser utilizado na fabricação do biopolímero de ácido lático (PLA), podendo assim ser utilizado na fabricação de embalagens plásticas biodegradáveis.
A aplicação destas metodologias em larga escala pode revolucionar o processo produtivo das indústrias, visto que estará beneficiando o meio ambiente, com a diminuição de recursos naturais; o custo de produção, pelo fato de reutilizar o resíduo agroindustrial; e às gerações futuras, com a minimização de lixos gerados.
2. REVISÃO BIBLIOGRÁFICA
2.1 AGROINDÚSTRIA
Mediante dados estimados pela EMBRAPA (Empresa Brasileira de Pesquisa Agropecuária, 2020) o Brasil está entre os cinco maiores países produtores e exportadores de alimentos do mundo. A agroindústria, segundo o Ministério da Agricultura, Pecuária e Abastecimento (2021), pode ser definida como um agrupamento de atividades que se relacionam a fim de transformar matérias-primas oriundas da agricultura, pecuária e/ou silvicultura em subprodutos voltados, principalmente, ao consumo alimentício.
A produção agroindustrial é um dos principais setores que contribui positivamente nos âmbitos social e econômico do Brasil, além de permitir um aumento de empregos (SANTOS, 2014). Contudo, é importante salientar que as atividades desse negócio englobam não só os trabalhadores, como também os animais, veículos, maquinários, ferramentas, plantio, armazenamento e conservação de produtos (CALLADO, 2015 apud COSTA FILHO et al., 2017).
2.2 RESÍDUOS AGROINDUSTRIAIS
Apesar das vantagens da agroindústria, o seu processo produtivo resulta numa grande quantidade de resíduos (SILVEIRA, 2017 apud COSTA FILHO et al., 2017). Estima-se que são gerados aproximadamente 1,3 bilhões de toneladas por ano de resíduos agroindustriais no mundo (ORGANIZAÇÃO DAS NAÇÕES UNIDAS PARA A ALIMENTAÇÃO E A AGRICULTURA – FAO, 2013), sendo que boa parte destes são desperdiçados durante a colheita e armazenamento dos produtos, como também durante o seu processamento e consumo (OLIVEIRA, 2018).
De acordo com a Política Nacional de Resíduos Sólidos, instituída pela Lei Nº 12.305, de 2 de agosto de 2010, pode-se entender resíduo como qualquer material, objeto, substância ou bem descartado no ambiente resultante da ação humana, podendo ser prejudicial à saúde. Além disso, a responsabilidade de reaproveitamento desses resíduos sejam eles sólidos, líquidos ou gasosos, não cabe apenas aos fabricantes, distribuidores e comerciantes, como também aos próprios consumidores (SOUZA et al., 2021).
2.3 TIPOS DE RESÍDUOS AGROINDUSTRIAIS
Dentre os principais resíduos agroindustriais que podem ser utilizados para a concepção do biopolímero de ácido lático, destaca-se o uso do melaço da cana-de-açúcar:
2.3.1 MELAÇO DA CANA-DE-AÇÚCAR
O melaço é um resíduo proveniente da etapa final da cristalização do açúcar, nas indústrias açucareiras, na qual toda a sacarose possível já tenha sido extraída (GROCHOLSKI, 2019). Ele é composto, principalmente, por açúcares fermentescíveis e, também, por componentes inorgânicos, os quais contribuem para o melaço ser uma alternativa como fonte de energia em processos fermentativos, dentre eles do ácido lático (VARGAS, 2016).
No Brasil, a produção de caldo de cana-de-açúcar resulta numa média de 40 a 60 Kg de melaço por cada tonelada de cana (PIACENTE, 2005 apud VARGAS, 2016). O processo que origina o melaço consiste nas seguintes etapas: (a) compressão e moagem da cana-de-açúcar, na qual gera o caldo e o bagaço; (b) peneiramento e clarificação, a fim de purificar o caldo rico em sacarose; (c) aquecimento do caldo, resultando numa cristalização da sacarose presente, aumentando a sua concentração; e (d) separação dos cristais de sacarose do caldo, por meio da técnica de centrifugação/turbinagem, na qual resulta no melaço (VARGAS, 2016).
2.4 O ÁCIDO LÁTICO
Em 1780, o ácido lático fora descoberto pelo químico sueco Carl Wilhelm Scheele, onde o mesmo isolou o ácido lático como um xarope marrom impuro do leite azedo e acabou denominando-o como Mjolksyra. Esse componente denominado como Mjolksyra teve seu nome alterado em 1789 por Lavosier, na qual foi renomeado como “acide lactique”, terminologia utilizada atualmente (GHAFFAR et al., 2014). Por muito tempo, considerou-se o ácido lático, sendo um componente do leite, mas em 1857, o cientista Pasteur descobriu que na verdade essa molécula não era oriunda do leite, mais sim um metabólito provido da fermentação gerado por microrganismos (BENNINGA, 1990 apud KOMESU et al., 2017).
A primeira produção de ácido lático em escala industrial foi realizada em 1881 nos Estados Unidos por um processo microbiano, e sua origem se deu através do cientista francês Frémy, que produziu ácido lático por fermentação (GHAFFAR et al., 2014).
O ácido lático é um líquido higroscópico, sem cheiro, de sabor azedo, com um ponto de fusão de 18 °C, é viscoso, sua fórmula química é CH3CH(OH)COOH e possui um ponto de ebulição de 122 °C (DAINTITH, 2008). Sua estrutura possui um carbono assimétrico, que acaba gerando quatro diferentes grupos de ligação, sendo eles: -CH3, -COOH, -OH e -H. Devido a esses grupos, pode-se apresentar dois enantiômeros do ácido lático, o D(-)-ácido lático e o L(+)-ácido lático. Como esses enantiômeros possuem estruturas químicas e características diferentes, eles podem ser utilizados em aplicações diversas (MARTINEZ et al., 2013 apud PEREIRA, 2019). A figura 1 apresenta os enantiômeros do ácido lático.
Figura 1. Estereoisômeros do ácido lático

A obtenção desse ácido pode acontecer por duas vias, pela via fermentativa ou pela síntese química. Por mais que existam duas formas de obtenção do ácido lático, a via fermentativa é a mais utilizada nas indústrias, uma vez que a síntese química se torna um processo com maior custo e gera algumas desvantagens como, por exemplo, a produção de uma mistura racêmica indesejável no processo (PAL et al., 2009).
2.4.1 APLICAÇÕES DO ÁCIDO LÁTICO E SEUS CUSTOS
Devido aos seus dois grupos de ligações, é possível gerar uma vasta variedade de reações químicas para o ácido lático, nas quais esse ácido pode ser utilizado em aplicações industriais e produtos de consumo (DATTA; HENRY, 2006). Pode-se citar algumas aplicações, como o uso na indústria cosmética, alimentícia, farmacêutica e de biopolímeros que vem ganhando destaque com a expansão do mercado de PLA (PEREIRA, 2019).
O único isômero que pode ser metabolizado pelo sistema humano é o L, devido a isso as indústrias farmacêuticas e alimentícias possuem uma preferência por esse isômero. Já as indústrias químicas precisam dos mesmos puros ou então uma mistura dos dois (MARTINEZ et al., 2013 apud ARCANJO, 2017).
Embora o campo de aplicação do ácido lático tenha um amplo leque, o uso do mesmo torna-se limitado quando o custo de mercado final é levado em consideração. Na maioria dos casos, esse custo é justificado pelos processos de separação do produto final, uma vez que possui várias etapas (LIPINSK e SINCLAIR, 1986 apud CAPELLARI, 2010).
2.4.2 BACTÉRIAS ÁCIDO LÁTICAS
Industrialmente o ácido lático pode ser obtido por meio do processo fermentativo, no qual as chamadas “bactérias láticas” são responsáveis pela conversão de açúcares em ácido lático (HOFVENDAL et al., 2000 apud SILVESTRINI, 2020). Essas bactérias são acidófilas, tolerantes a baixos níveis de pH, possuem um pH ótimo entre 5,5 e 5,8, sendo que seu crescimento é favorável a um pH entre 4,5 e 5,0, e a sua temperatura de crescimento, considerada como ótima, é entre 30 a 40ºC (LOPES, 2008).
As Bactérias Ácido Láticas (BAL) podem ser encontradas em alimentos, como leite e seus derivados, e englobam os gêneros Lactococcus, Lactobacillus, Enterococus, Carnobacterium, Lactosphaera, Melissococus, Leuconostoc, Oenococcus, Pediococcus, Tetragenococcus, Streptococcus, Weissella, Vagococcus, Microbacterium, Propionibacterium e Bifidobacterium (HOLZAPFEL et al., 2001).
Conforme o produto do processo fermentativo da glicose, essas bactérias podem ser classificadas em dois grupos: homofermentativas, as quais têm o ácido lático como principal produto, ou heterofermentativas, em que a processo gera diferentes produtos além do ácido lático, como ácido acético, etanol, entre outros (CARR et al., 2002; apud SILVESTRINI, 2020).
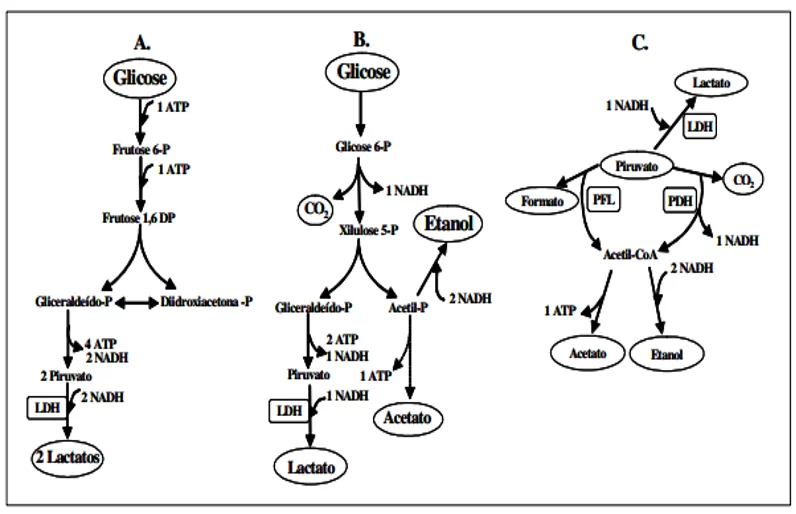
No processo da homofermentação, o metabolismo da glicose por meio da via Embden-Meyerhof-Parnas ou via glicolítica (em que o ácido pirúvico é convertido em ácido lático por meio da ação da enzima lactato desidrogenase) produz unicamente o ácido lático (FIG. 10A). Já na heterofermentação, a glicose, por meio da via oxidativa das pentoses (fosfoquinase), têm como produtos volumes equimolares de ácido lático, dióxido de carbono e etanol ou acetato (FIG. 10B). Por outro lado, no processo homofermentativo do metabolismo do piruvato, por meio da ação da Enzima Formato Liase (PFL), obtém-se, além da formação do ácido lático, a produção de formato e acetil-CoA (FIG.10C) (HOFVENDAHL e HÄGERDAL, 2000; apud LOPES, 2008).
Figura 2. Vias catabólicas das bactérias láticas
2.5 POLÍMEROS
Os polímeros podem ser definidos como compostos, de fontes naturais ou sintéticas, oriundos da reincidência de simples unidades estruturais (poli “muitos; meros “partes”) chamadas de monômeros (AKCELRUD, 2007). Considerados como macromoléculas, os polímeros compõem a estrutura dos materiais plásticos, sendo os mais utilizados, desde 1940: Polietileno (PE), Poliestireno (PS), Poli(Cloreto de Vinila) (PVC), Polipropileno (PP) e Poli(Tereftalato de Etileno) (PET) (FRANCHETTI; MARCONATO, 2006).
Desde 1950 até 2015, o mundo produziu cerca de 8,3 bilhões de toneladas métricas de plástico, sendo que 6,3 bilhões de toneladas se tornaram resíduos descartados em lugares inapropriados, como os oceanos. (SOARES, 2017). Além do descarte incorreto, outros problemas decorrem da utilização de plásticos convencionais no mundo: em maior parte são derivados de hidrocarbonetos fósseis e não biodegradáveis e em 2018 já representavam 12% da composição do lixo global (WORLD BANK GROUP, 2018, apud FORTUNA, 2020).
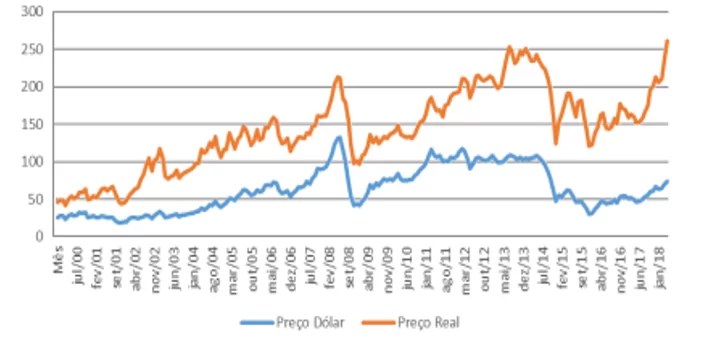
A produção de plásticos utiliza o petróleo como fonte fóssil devido às suas altas propriedades mecânicas e térmicas, assim como sua versatilidade (CALABRIA, 2010). Contudo, essa fonte apresenta desafios, visto o contínuo aumento de consumo e concorrência pela matéria prima, assim como seu crescente valor do preço do barril (CASTRO, 2019).
Figura 3. Preço do barril de Petróleo (Dólar e Real)
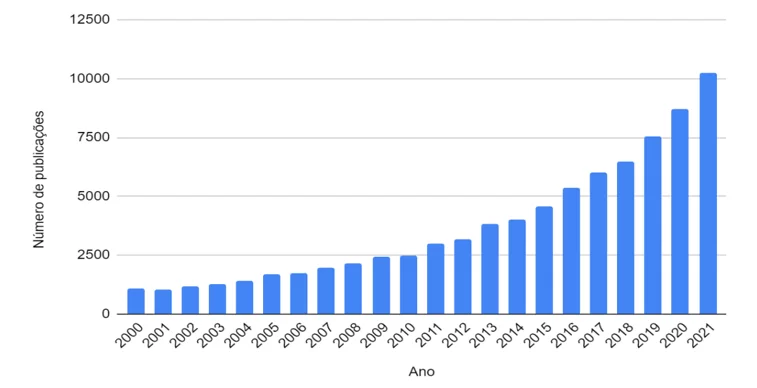
Visto isso, cada vez mais pesquisadores no mundo têm buscado alternativas sustentáveis para a produção plástica, dentre elas, a substituição de polímeros sintéticos não biodegradáveis, provenientes de fontes fósseis, por polímeros biodegradáveis, biopolímeros e polímeros verdes, visto viabilidade econômica, técnica e com potencial de expansão (BRITO et al., 2011).
Figura 4. Número de publicações sobre biopolímeros – Science Direct (2000-2021)
2.5.1 POLÍMEROS SINTÉTICOS
Os polímeros fabricados à base de matérias-primas oriundas do petróleo, como a nafta petroquímica e densas partes do refino do petróleo, são conhecidos como polímeros sintéticos (BASTOS, 2007).
Tendo em vista os principais tipos de plásticos convencionais para a utilização em embalagens alimentícias atualmente, é possível citar: PET para garrafas e bebidas, Polipropileno (PP) para utilização com líquidos quentes, Poliestireno (PS) para embalagens de proteção e recipientes, e Policloreto de Vinila (PVC) para embalagens com flexibilidade ou rigidez, visto incapacidade de escape da água e de oxigênio (ZAMORA et al., 2020).
2.5.2 BIOPOLÍMERO
Define-se como biopolímeros aqueles polímeros, ou copolímeros, caracterizados por sua origem natural, normalmente de fontes renováveis como cana-de-açúcar, milho, entre outras (ASSOCIAÇÃO BRASILEIRA DE NORMAS TÉCNICAS – ABNT, 2008 apud BRITO et al., 2011). De forma semelhante, polímeros biodegradáveis podem ser descritos como materiais resultantes da ação de microorganismos que geram componentes celulares, CO2, CH4, entre outros (FRANCHETTI; MARCONATO, 2006).
Os polímeros biodegradáveis podem ser provenientes de dois tipos de fontes diferentes: naturais, tratando-se de biopolímeros que foram sintetizados por microrganismos, ou sintéticos, quando se diz respeito a biopolímeros sintetizados através de processos industriais de fermentação de monômeros naturais, por exemplo, ácido polilático (PLA) (SILVA; SILVA, 2003).
2.5.2.1 ÁCIDO POLILÁTICO (PLA)
Ácido Polilático (PLA), classificado como ácido 2-hidróxipropanóico, segundo a IUPAC (UNIÃO INTERNACIONAL DE QUÍMICA PURA E APLICADA), pertence à família dos poliésteres alifáticos, termoplásticos e resistentes (WANG et al., 2008 apud. GONÇALVES, 2013).
Figura 5. Estrutura molecular de PLA
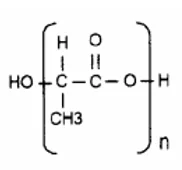
Os grupos funcionais que compõem o monômero, ácido lático, do PLA proporcionam que o mesmo possa assumir diferentes configurações isoméricas: a Dextrógira (D ou +) denominada como PDLA ou Poli (D-lactídeo) e a Levógira (L ou -) denominada como PLLA ou Poli (L-lactídeo) (AURAS et al., 2004).
O PLA é produzido a partir da sintetização química do monômero ácido lático através do processo de fermentação bacteriana. As propriedades do polímero podem ter diferenças dependendo da forma como o ácido foi produzido: via petroquímica, na qual é constituído numa mistura opticamente inativa (50/50) das formas D e L, ou por via biotecnológica, em que é opticamente ativa e vai variar conforme o microrganismo utilizado (PRADELLA, 2006).
Existem diferentes vias para a polimerização do PLA e é possível citar como sendo a mais comum a por abertura de anel por meio de condensação de lactídeo com catalisador metálico, como por exemplo o usual octoato de estanho, eliminando uma molécula de água sob altas temperaturas, contanto que sejam inferiores a 200ºC (ARRIETA et al., 2017).
Figura 6. Processo de produção de PLA
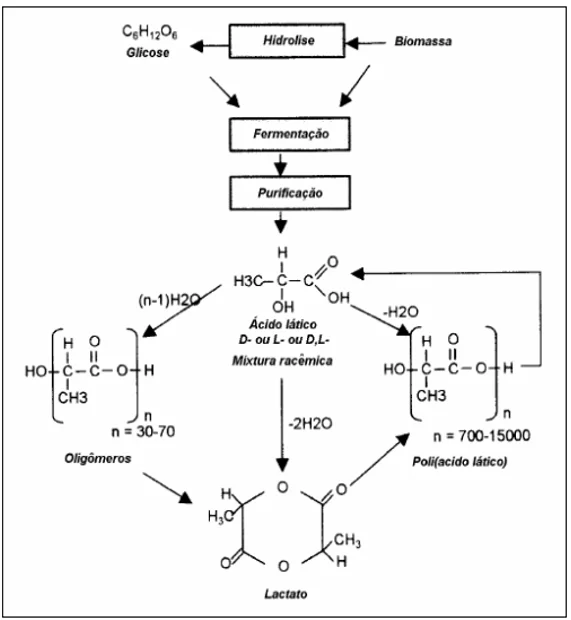
O Ácido Polilático (PLA) possui propriedades similares aos termoplásticos de origens fósseis, e se destaca quanto à fácil processabilidade e resistência mecânica quando comparado ao PET e ao poliestireno, por exemplo (SEEFELDT, 2012).
2.6 IMPACTOS AMBIENTAIS
De acordo com a CMMAD (COMISSÃO MUNDIAL DO MEIO AMBIENTE E DESENVOLVIMENTO, 1991), pode-se definir como desenvolvimento sustentável como aquele em que busca atender às necessidades atuais sem interferir na aptidão das gerações futuras ao atenderem suas necessidades.
Dessa forma, dados e pesquisas alertam sobre problemas atuais que podem impactar gerações futuras, tal como o acúmulo de dejetos plásticos no ambiente que já afetaram quase 700 espécies de animais (NATIONAL GEOGRAPHIC, 2018), e a questão de emissão de resíduos, como os oriundos da agroindústria, dos quais 69% vêm da produção de cana-de-açúcar. (PLANARES – PLANO NACIONAL DE RESÍDUOS SÓLIDOS, 2011 apud CRUZ et al., 2021)
Logo, destaca-se o uso de bioplásticos devido ao fato de que plásticos de fontes biológicas são produzidos a partir de biomassa, as quais se regeneram anualmente e utilizam CO2 para se desenvolver, pode-se dizer que são materiais que economizam recursos fósseis (FORTUNA, 2020).
Figura 7. Emissões de gases do efeito estufa para bioplásticos e petro-plásticos
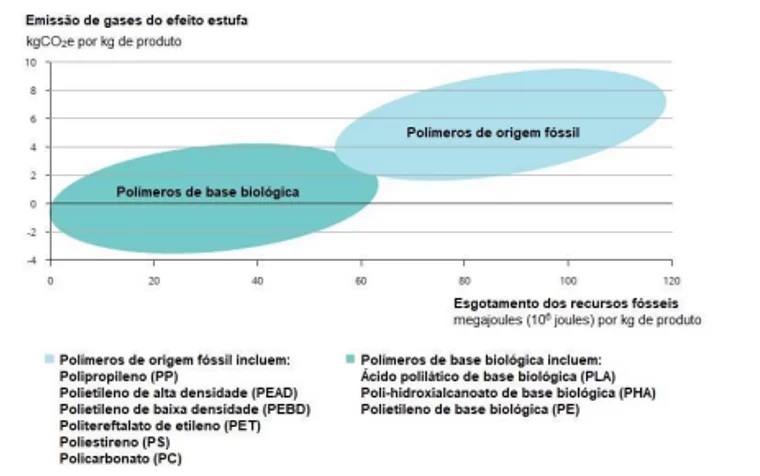
2.7 BIOMASSA LIGNOCELULÓSICA
A biomassa lignocelulósica é um material alternativo a materiais açucarados, que acabam sendo vantajosos para o meio ambiente uma vez que se tornam uma fonte de energia renovável (RUBIN, 2008 apud SANTIAGO; RODRIGUES, 2017), sendo oriundas de florestas, culturas agrícolas, resíduos de culturas e outros resíduos industriais (GONZÁLEZ; CAMBA, 2012). Esse material lignocelulósico é composto por 3 diferentes estruturas: a celulose, a lignina e a hemicelulose (SANTIAGO; RODRIGUES, 2017).
A hemicelulose é composta por vários monossacarídeos polimerizados, onde entre eles estão carboidratos como xilose, arabinose, galactose, glucose e manose, além de possuir ácidos de açúcar, porém o composto mais abundante na hemicelulose é a xilose (SILVA et al., 2009). Alguns desses compostos podem ser utilizados como energia extracelular, e outros tem como função atuar como ligante entre a lignina e a celulose (WYMAN et al., 2005 apud OGATA, 2013).
A celulose é o polissacarídeo mais disponível na natureza, onde o mesmo é um polímero de glucano de unidades de d-glucopiranose ligados entre si (ROWELL et al., 2012). Esse polímero é responsável por organizar as estruturas denominadas como fibrilas, que consequentemente formam as fibras da celulose, e ele é encontrado na forma de fibras compostas por microfibrilas que fornece a rigidez para a estrutura (FENGEL; WEGENER, 1989 apud SANTIAGO; RODRIGUES, 2017).
A lignina é uma molécula amorfa, altamente complexa, contendo assim uma estrutura ramificada. Na parede celular sua função é cobrir o suporte estrutural, e realizar o transporte de água e nutrientes, além de emitir proteção evitando assim ataques biológicos ou químicos (LU et al., 2017).
2.8 METODOLOGIAS QUÍMICAS PARA A PRODUÇÃO DE ÁCIDO LÁTICO
Para a concepção do ácido lático são possíveis as seguintes técnicas:
2.8.1 FERMENTAÇÃO SINTÉTICA (SÍNTESE QUÍMICA)
A hidrólise de lactonitrilo por ácidos fortes é a principal base quando fala-se de síntese química do ácido lático, visto que ela fornece apenas a mistura racêmica de D(-) e L(+) ácido lático. Porém, há outras formas de realizar a síntese química do ácido lático entre elas estão a hidrólise de ácido cloropropiônico, oxidação de propileno por ácido nítrico, oxidação de propilenoglicol, reação de acetaldeído, monóxido de carbono e água com pressões e temperaturas elevadas e a degradação de açúcares catalisada por bases, entre outros. Entretanto, nenhuma dessas rotas técnicas apresentadas chegou a um processo economicamente rentável (DATTA et al., 1995). A via síntese química do ácido lático se encontra esquematizada na Figura 7.
Figura 8. Processo de síntese química do ácido lático
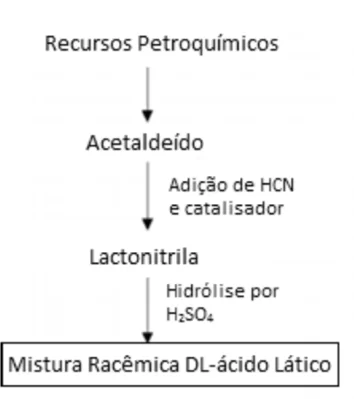
O método de síntese química do ácido lático é estimado em apenas 10% da produção industrial total do ácido lático, uma vez que a mesma gera uma mistura racêmica, um item indesejável na produção, pois acaba gerando um controle impossível das características do produto final (DE OLIVEIRA et al., 2018 apud DORNELLES 2021).
2.8.2 FERMENTAÇÃO DESCONTÍNUA (BATELADA)
De acordo com López-Gómez et al. (2019), o processo de batelada ou fermentação descontínua é o mais utilizado para a fabricação de ácido lático, atualmente. Este procedimento, de operação simples, consiste na adição do resíduo (o melaço, no caso da cana-de-açúcar), juntamente aos microrganismos e, em seguida, incubados num sistema fechado para que a fermentação se inicie, sendo que nada é adicionado após o seu início (MALTA, 2006).
Essa técnica permite uma alta concentração de produto além de possuir baixos riscos de contaminação. Por outro lado, não garante uma alta produtividade e a concentração de substrato e/ou produto final pode resultar numa inibição do processo fermentativo (ABDEL-RAHMAN, 2011 apud VARGAS, 2016), visto que o crescimento celular se dá de forma produtiva apenas durante uma parte do ciclo de fermentação (NEVES, 2003).
Para que não haja a inibição por consequência do substrato, pode-se optar pela fermentação em batelada alimentada, na qual os microrganismos são adicionados gradualmente durante o cultivo permitindo, assim, o controle da concentração do substrato e evitando o excesso da concentração de açúcar que acarreta esse problema de inibição (JUNIOR, 2016). No que diz respeito à vazão de alimentação desta técnica, ela pode ser constante ou variar com o tempo (sendo regulada conforme a quantidade de concentração do substrato), além de ser possível num volume fixo ou variável (NEVES, 2003).
Figura 9. Processo de fermentação descontínua (batelada)
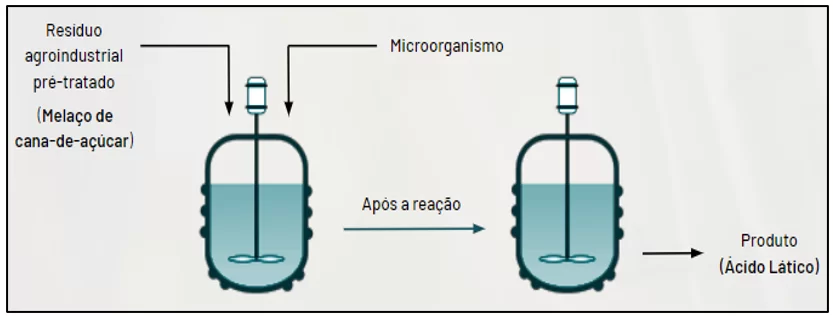
2.8.3 FERMENTAÇÃO CONTÍNUA
Visto que a síntese do ácido lático está relacionada ao crescimento celular, diferentemente das produções em sistema de batelada comum e alimentada, a fermentação contínua permite que as taxas de crescimento celular se mantenham constantes a nível máximo (LÓPEZ-GÓMEZ et al., 2019 apud PEREIRA, 2019).
De ponto de vista técnico, pode-se explicar o processo como sendo a adição simultânea da matéria-prima e do inóculo ao reator de fermentação, sob vazão constante, e o produto, ou meio fermentado, é removido do equipamento na mesma vazão de alimentação (VENTURA, 2007). Além disso, um fator relevante que pode interferir na eficiência do processo da fermentação contínua é a necessária reciclagem dos microrganismos adicionados ao reator. (MOREIRA et al., 2009).
Uma vantagem da fermentação contínua, quando comparada aos demais processos de fermentação, é que nesse não ocorre acúmulo de produto final, no caso o ácido lático, preservando-se, portanto, da inibição provocada pelo produto e pela redução do pH. (ABDEL-RAHMAN; SONOMOTO, 2016; AHRING et al., 2016 apud PEREIRA, 2019).
Figura 10. Processo de fermentação contínua
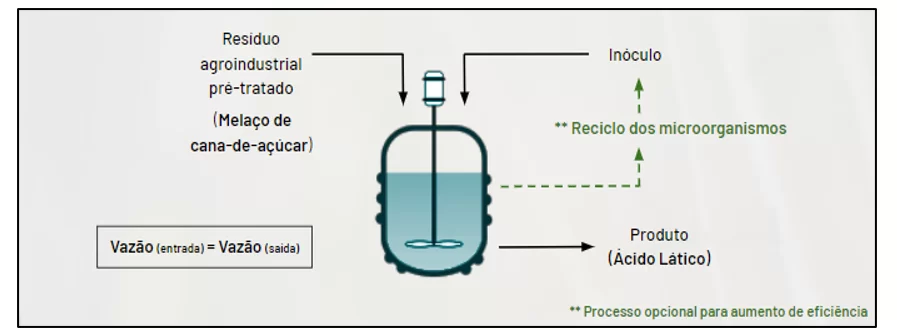
2.8.4 FERMENTAÇÃO SEMICONTÍNUA
No sistema semicontinuo englobam-se aspectos dos processos contínuo e descontínuo, visto que, essa operação consiste na entrada de um substrato e o inóculo, de forma contínua, num reator primário e transfere-se então o meio em fermentação para um, ou mais, reatores para que o processo fermentativo se finalize (VENTURA, 2007).
A fermentação contínua é de fácil implementação e dimensionamento, e seu tempo de ação prolongada promove alta densidade celular e formação de produtos, e alivia os efeitos adversos que o acúmulo excessivo de metabólitos poderia ter no crescimento celular (GUTIÉRREZ; YÁÑEZ, 2013).
2.8.5 FERMENTAÇÃO SUBMERSA EM ESTADO LÍQUIDO (FS)
A fermentação submersa em estado líquido (FS) tem sido bastante empregada para produções em larga escala, devido à sua vantagem de se produzir mais, necessitando de um curto espaço e menos mão-de-obra (SBRT – SERVIÇO BRASILEIRO DE RESPOSTAS TÉCNICAS, 2011).
Esta técnica consiste na imersão da cultura de microrganismos num meio líquido, normalmente com substratos solúveis, sob agitação, garantindo que o meio de cultura flua livremente e de forma homogênea (RODRIGUES, 2006). Devido a isto, a FS permite ter um fácil controle do processo, podendo regular a sua temperatura e o pH; facilidade de esterilização; e boa transferência de calor (STRACK, 2021).
2.8.6 FERMENTAÇÃO EM ESTADO SÓLIDO (FES)
A fermentação em estado sólido se dá na superfície de substratos sólidos, permitindo a intensificação de microrganismos em um meio com baixo teor de umidade (JUNIOR et al., 2001). Ou seja, é necessário um suporte sólido composto por um substrato que esteja consideravelmente úmido para que possa absorver nutrientes, permitindo, assim, o crescimento microbiano (RODRIGUES, 2006).
A FES possui a vantagem de se ter uma produtividade e rendimento maiores, se comparado à FS, além de permitir o uso de reatores pequenos, reduzindo os custos, gastos energéticos e resíduos gerados (ROCHA, 2011). Ademais, como essa técnica possibilita o uso de diferentes tipos de substratos, a reutilização de resíduos agroindustriais acaba se tornando uma boa alternativa. Todavia, há a desvantagem de não conseguir medir o pH, oxigênio dissolvido, concentração do substrato no estado sólido e a quantidade de água (RODRIGUES, 2006).
2.8.7 SACARIFICAÇÃO E FERMENTAÇÃO SIMULTÂNEAS (SSF)
A Sacarificação e fermentação simultânea ou Simultaneous Saccharification and Fermentation (SSF), do inglês, corresponde à junção dos processos de hidrólise enzimática com a fermentação, simultaneamente, a fim de se obter produtos de alto valor numa única etapa (MARULANDA et al., 2019). Sendo assim, o resíduo sólido de biomassa pré-tratado é hidrolisado, por meio de enzimas, num curto período de tempo até que as células responsáveis pela fermentação sejam adicionadas ao mesmo reator (KASSIM, 2022).
Com isso, há a redução da inibição do produto final provocado pelo processo da hidrólise, pois o seu açúcar liberado será consumido pelas células fermentantes em questão de segundos. Além disso, esse sistema simultâneo também permite uma diminuição dos custos de produção, uma vez que é necessário apenas um reator para isso (OLOFSSON et al., 2008).
Entretanto, a sua desvantagem diz respeito à diferença da temperatura ideal para as enzimas e para as células fermentativas (KÁDÁR et al., 2004). Normalmente, a temperatura utilizada na etapa da hidrólise é maior do que a da fermentação, sendo essencial alcançar um ponto de equilíbrio para que o processo opere adequadamente (MARULANDA et al., 2019).
2.8.8 IMOBILIZAÇÃO CELULAR
A técnica de imobilização corresponde no aprisionamento físico de células microbianas ou enzimas num determinado espaço (denominado de suporte) com características diferentes do ambiente ao redor, mas que permitem a ação de suas atividades catalíticas (BASSANI, 2018). Devido à alta concentração de células imobilizadas neste suporte, o processo fermentativo se torna elevado e mais eficiente, além de ser possível o seu desenvolvimento mesmo em ambientes estressantes (SANTOS, 2013)
Embora a produção possua essas vantagens, o material utilizado para imobilização pode aumentar o custo desse método, podendo se tornar inviável em alguns casos (LI et al., 2015 apud PEREIRA, 2019).
2.8.9 RECICLO DE BIOMASSA
Inibição por acúmulo de produto e consumo de nutrientes são algumas das desvantagens do processo de batelada comum, logo, num processo de batelada repetida, o reuso de células é uma opção para o aumento de produtividade (ABDEL-RAHMAN et al., 2013 apud DORNELLES, 2021).
A fermentação que utiliza reuso de células é aquela em que as células de levedura são reutilizadas repetidamente por processo de separação ou adição de células (OLIVEIRA, 2008). O método de reciclo, ou reuso, da biomassa pode resultar numa densidade celular mais alta, e por consequência, torna-se possível alcançar produtividades maiores (Aso et al., 2019 apud PEREIRA, 2019).
A combinação do método da fermentação contínua somada ao reciclo celular pode aumentar a eficiência produtiva em até 1,6 vezes mais do que o método contínuo por si só (LÓPEZ-GÓMEZ et al., 2019 apud PEREIRA, 2019).
2.9 MÉTODOS DA REUTILIZAÇÃO DE RESÍDUOS DE CANA-DE-AÇÚCAR PARA APLICAÇÃO EM ÁCIDO LÁTICO
Pode-se citar como subprodutos principais das indústrias sucroalcooleira oriundas da cana-de-açúcar, o bagaço da cana, vinhaça e o melaço. Devido a sua grande expansão nas últimas décadas a busca para reaproveitamento desses subprodutos como substrato em bioprocessos tem aumentado (WOICIECHOWSKI et al., 2013).
O subproduto denominado como melaço é proveniente das indústrias de açúcar, e pode ser utilizado para a produção via fermentativa do ácido lático (TATE e LYLE, 2009 apud CAPELLARI, 2010).
Para a obtenção do ácido lático e geração de maior rendimento final através de resíduos de cana-de-açúcar pode-se citar algumas metodologias conforme descrito abaixo:
– Fermentação contínua;
– Fermentação descontínua.
Geralmente as bactérias láticas utilizadas para a produção de ácido lático precisam passar por um processo de pré-tratamento quando são oriundas de resíduos agroindustriais, para que assim seus açúcares sejam liberados da matriz polimérica (RODRIGUES, 2012) e, também remover componentes do processo (RODRIGUES et al., 2018). Como exemplo disso, tem-se os tratamentos de hidrólise que podem ser físicos, através de fragmentação; químicos por ácidos ou bases; ou biológicos que podem ocorrer com a ajuda de enzimas (RODRIGUES, 2012 apud PEREIRA, 2019).
A hidrólise ácida tem como principal objetivo remover parte da hemicelulose da biomassa (RODRIGUES et al., 2018), para deixar livre a camada de celulose na próxima etapa de tratamento que a princípio é envolvida pela hemicelulose (TAHERZADEH; KARIMI, 2008). Geralmente nesse tipo de processo pode-se utilizar diversos ácidos, mas o mais empregado é o ácido sulfúrico (HARRIS et al., 1945 apud TAHERZADEH; KARIMI, 2007).
Quando se fala de hidrólise ácida, pode-se utilizar dois tipos de ácidos, o concentrado ou o diluído. A utilização de ácido concentrado geralmente possui um rendimento de açúcar elevado de aproximadamente 90% (rendimento teórico de glicose), quando comparado com ácido diluído que acaba sofrendo degradação de açúcares em seu processo. A principal vantagem do ácido concentrado é sua operação em baixas temperaturas (entre 40 °C), enquanto do ácido diluído acaba sendo em torno de 120 °C a 170 °C, porém sua desvantagem é que ele acaba gerando um processo altamente corrosivo, devido a sua alta concentração, gerando necessidade da compra de equipamentos com ligas caras além acarretar um gasto maior com ácido concentrado, que em hidrólise com ácido diluído não aconteceria (JONES et al., 1984 apud KATZEN et al., 1995 apud WYMAN, 1996 apud TAHERZADEH; KARIMI, 2007).
Já a hidrólise enzimática é realizada por um grupo de enzimas celulases, onde elas realizam uma transformação das cadeias de celulose e hemicelulose em açúcares fermentáveis (AGUIAR, 2010; apud SUN e CHENG, 2002 apud VALLANDER e ERIKSSON, 1985 apud KIEFER, 2018). Essa hidrólise em relação a parâmetros de processos como pressão, temperatura e pH são mais brandos se comparado com hidrólise química, além de possuir especificidade, reduzindo assim a geração de subprodutos indesejáveis (CASTRO; PEREIRA, 2010). Algumas desvantagens da hidrólise enzimática, são os altos custos das enzimas (KARP et al., 2013), o seu tempo de reação que pode chegar até 25 horas enquanto algumas hidrólises ácidas levam apenas 10 minutos (WOICIECHOWSKI et al., 2002), e seu baixo rendimento de açúcar sendo de apenas 20% se não combinada com um pré-tratamento (OGEDA; PETRI, 2010).
3. METODOLOGIA
Este trabalho tem como objetivo estudar e comparar as atuais metodologias disponibilizadas em artigos acadêmicos para a produção de ácido lático através de resíduos agroindustriais, além de determinar os melhores parâmetros para uma produção eficiente deste ácido.
Para isto, foi optado pela busca dos artigos mais recentes (entre os anos de 2000 e 2021), a fim de que fossem analisadas as técnicas mais atuais para esta concepção, considerando as seguintes palavras-chave: “Poli-ácido Lático”, “tratamento Ácido Lático (AL)”, “produção ácido lático”, “resíduos agroindustriais” e “plástico biodegradável”. As buscas das publicações, tanto em português como em inglês, foram realizadas entre os meses de fevereiro a julho de 2022 através de bancos digitais de artigos científicos, como SciELO, ScienceDirect, Google Scholar, IEEE Xplore e Researchgate. E a partir de 18 artigos inicialmente estudados, utilizou-se o critério de seleção das publicações com base naquelas que apresentaram um detalhamento acerca de seus procedimentos e por estes terem feito o uso do melaço da cana-de-açúcar para se obter uma concentração final de ácido lático, totalizando 5 autores no final com suas publicações feitas entre os anos de 2005 e 2019.
Ao estudar as diferentes metodologias, foi observado que para cada uma delas os parâmetros e condições se diferenciavam, tais como, o pH, a temperatura, os microrganismos utilizados para a fermentação e seus nutrientes, o tempo de fermentação, a existência ou não de um pré-tratamento e o método empregado para a produção de ácido lático. Para isso, essas informações e parâmetros de cada pesquisa analisada foram organizados em uma tabela, a fim de que a comparação dessas diferenças se tornasse mais visível.
Por meio dessa tabela, também é possível consultar os dados de uma forma mais rápida e entender as características específicas que cada autor desenvolveu. Ademais, uma breve descrição a respeito dos trabalhos estruturados por eles foi adicionada posteriormente.
A metodologia e os parâmetros estudados devem sugerir o melhor método de produção alternativo às vias hoje adotadas, visando-se no qual a biomassa possui uma maior eficiência, gerando assim um aumento na produção de ácido lático.
4. RESULTADOS E DISCUSSÃO
Para o presente trabalho, foram analisados artigos de diversos autores que efetuaram pesquisas para o desenvolvimento de ácido lático por meio do melaço da cana-de-açúcar. Mediante a isto, foi possível verificar as diferentes metodologias empregadas, as condições mais favoráveis para cada uma delas, além do uso de microrganismos e substratos distintos, os quais proporcionam rendimentos variados.
A seguir, é possível observar uma tabela comparativa, contendo os parâmetros e resultados empregados em cada um deles:
Tabela 1. Comparação de parâmetros e resultados de diferentes autores
| Autor | Ano | Método | Pré-
tratamento |
Microrganismo | Nutrientes | Instrumento | Tempo de fermentação (horas) | pH | Temperatura (ºC) | Concentração inicial melaço | Concentração de ácido lático final |
| Autor 1
(SILVA et al.) |
2010 | Fermentação batelada | Hidrólise com invertase | Lactobacillus casei | Extrato de levedura 2% e peptona 2% | Béquer (600 mL) sob agitação de 100 rpm com agitador de pistão | 48 | 4,0 – 6,2 | 37 | – | 36,20 g/L |
| Autor 2 (GROCHOLSKI) | 2019 | Fermentação batelada | – | Lactobacillus johnsonii e Lactobacillus helveticus | Permeado do soro de leite (2%) | Experimental em laboratório/biorreator sob agitação de 100 rpm | 48 | 5,7±0,2 | 37 | 10% suplementado com 2% de permeado de soro de leite | 9,65 g/L |
| Autor 3 (OLIVEIRA et al.) | 2005 | Fermentação contínua | Invertase | Lactobacillus curvatus | Peptona e extrato de levedura | Fermentador cilíndrico de 0,5L, sob agitação de 150 rpm | – | 6,2 | 37 | – | 13,80 g/L |
| Autor 4 (OLIVEIRA et al.) | 2009 | Fermentação batelada | Hidrólise com invertase | Lactobacillus casei | (2%) Peptona e (2%) de extrato de levedura | Erlenmeyer (500 mL) sob agitação de 100 rpm | 48 | 3,8 – 6,2 | 37 | 10%(m/v) | 58,86 g/L |
| Autor 5 (CAPELLARI) | 2010 | Fermentação contínua | – | Lactobacillus amylovorus CCT 2948, uma espécie amilolítica | Peptona (10,0 g.L-1), extrato de levedura (4,0 g.L1 ), extrato de carne (8,0 g.L-1), glicose (20,0 g L-1), monooleato de sorbitan (1,0 mL.L-1), fosfato de dipostássio (2,0 g.L-1), acetato de sódio (2,0 g.L-1), citrato triamonical (2,0 g.L-1), sulfato de magnésio (0,20 g.L-1) e sulfato de manganês (0,05 g.L-1) | Erlenmeyer (250 mL) e agitador orbital (Shaker) – em condição agitada | 96 | – | 37 | – | 14,80 g/L |
| Autor 5 (CAPELLARI) | 2010 | Fermentação contínua | – | Lactobacillus amylovorus CCT 2948, uma espécie amilolítica | Peptona (10,0 g.L-1), extrato de levedura (4,0 g.L1 ), extrato de carne (8,0 g.L-1), glicose (20,0 g L-1), monooleato de sorbitan (1,0 mL.L-1), fosfato de dipostássio (2,0 g.L-1), acetato de sódio (2,0 g.L-1), citrato triamonical (2,0 g.L-1), sulfato de magnésio (0,20 g.L-1) e sulfato de manganês (0,05 g.L-1) | Erlenmeyer (250 mL) e agitador orbital (Shaker) – em condição estática | 96 | – | 37 | – | 20,70 g/L |
| Autor 5 (CAPELLARI) | 2010 | Fermentação contínua | – | Lactobacillus amylovorus CCT 2948, uma espécie amilolítica | 1,0 mL.L-1 de Tween 80,2 g L-1 de fosfato dipotássico, 2 g.L-1 de acetato de sódio, 2 g.L-1 de citrato triamoniacal, 0,2 g.L-1 de sulfato de magnésio, 0,038 de sulfato de manganês e as melhores concentrações das fontes de carbono e nitrogênio. | Biorreator (Biotron) com cuba 4 L | 96 | – | 37 | – | 10,62 g/L |
Fonte: Elaborado pelas autoras.
4.1 DISCUSSÃO DA METODOLOGIA POR AUTOR
A seguir, é possível verificar um descritivo sobre cada metodologia presente na tabela.
4.1.1 AUTOR 1 (SILVA ET AL., 2010)
Silva et al. (2010), analisou a produção de ácido lático utilizando o método de fermentação batelada e o microrganismo o Lactobacillus casei, onde o mesmo foi ativado através de repiques sucessivos em tubos de ensaios.
Para esse experimento os autores optaram por preparar uma pré-fermentação, onde transferiram 6 mL da cultura ativada a cada 60 mL de meio, melaço de cana-de-açúcar, previamente hidrolisado e suplementado com peptona a 2% (m/v) e extrato de levedura a 2% (m/v). Esse meio foi incubado a uma temperatura de 37ºC durante um período de 24 horas. Para a utilização dessa pré-fermentação em si, foi utilizada uma concentração de 10% (v/v).
Para realizar o uso do melaço de cana-de-açúcar no meio fermentativo, uma solução de 10% (m/v) do mesmo previamente diluída em água destilada e posteriormente hidrolisada através da enzima invertase foi utilizada. Para essa solução os autores ajustaram o pH do meio para 4,7.
Após a inativação da enzima, o pH do meio foi ajustado para 6,2 com hidróxido de sódio 1 mol/L, e então o meio foi suplementado com extrato de levedura 2% (m/v) e peptona a 2% (m/v). Silva et al. adicionaram a pré-fermentação em um béquer com um agitador de pistão contendo 600 mL do meio de cultivo e uma temperatura de 37ºC foi mantida sob uma agitação de 100 rpm.
Assim que os autores obtiveram os resultados através de análises, eles verificaram que foi possível alcançar uma produção de 36,2 g/L de ácido lático utilizando melaço de cana-de-açúcar, além do mesmo consumir 87,5% dos açúcares redutores. Segundos os autores que realizaram o mesmo experimento utilizando outras biomassas como frutose, fécula de mandioca, e farinha de varredura ao invés do melaço, a maior produção de ácido lático se deu através do melaço de cana-de-açúcar devido ao mesmo possuir elementos que propiciam as atividades dos microrganismos.
4.1.2 AUTOR 2 (GROCHOLSKI, 2019)
Grocholski (2019), teve como objetivo a produção de ácido lático por meio da fermentação do melaço de cana-de-açúcar, através dos microorganismos Lactobacillus johnsonii e Lactobacillus helveticus. Para o meio de cultura, Grocholski utilizou o melaço da cana-de-açúcar a uma concentração de 10% e realizou o ajuste de pH para 2,51 com ácido sulfúrico. Para a preparação das soluções o autor preparou 6 amostras de 100 mL, sendo estas distribuídas em Erlenmeyers de 250 mL cada, no qual foram suplementadas com 2% de diferentes fontes de nitrogênio, sendo estes, extrato de levedura, uréia, ou permeado de soro de leite. Após a suplementação, Grocholski autoclavou as soluções por 30 minutos e aferiu o pH de cada amostra.
Para a realização da fermentação batelada, Grocholski adicionou 10 mL de bebida láctea contendo os microorganismos citados anteriormente nas soluções suplementadas previamente. Dando sequência nesse experimento, o autor colocou os Erlenmeyers na estufa, com uma temperatura constante de 37 °C, durante um período de 48 horas. Após esse período, foi medido o pH e as soluções foram analisadas no microscópio, onde verificou-se que nas amostras suplementadas com extrato de levedura continha uma maior quantidade de Lactobacillus e, com isso, a pesagem da massa seca foi realizada.
Considerando a relação de melhor custo e benefício, Grocholski, concluiu que a condição com melhor resultado foi utilizando o método escalonada com o biorreator (TECNAL), onde o mesmo apresentava um volume total de 2,5 L, um sistema de controle de pH, aeração, espuma, agitação e temperatura. E em relação a escolha da fonte de nitrogênio, o autor definiu que seria utilizado no biorreator o permeado de soro de leite, devido a sua melhor rentabilidade e custos quando comparado com o extrato de levedura.
Para realizar o experimento no biorreator, o autor preparou uma solução de 150 mL, onde a mesma continha 10% melaço de cana-de-açúcar e 2% de permeado de soro de leite. Após a preparação da solução a mesma foi adicionada a 2 L de meio de cultivo. Para esse experimento Grocholski, ajustou o pH em 5,70±0,20, manteve a agitação do biorreator em 100 rpm, uma temperatura de 37 °C e o mesmo operou por 48 horas.
Após centrifugar as amostras, congelar o sobrenadante, e secar a fração sólida para obter o peso seco da biomassa, Grocholski realizou a análise da produção de ácido lático através de cromatografia líquida de alta eficiência (HPLC), onde a mesma apresentou os resultados demonstrados na figura 12.
Figura 11. Concentração de ácido lático (g/L) em amostras de fermentado à base de cana-de-açúcar obtido em biorreator
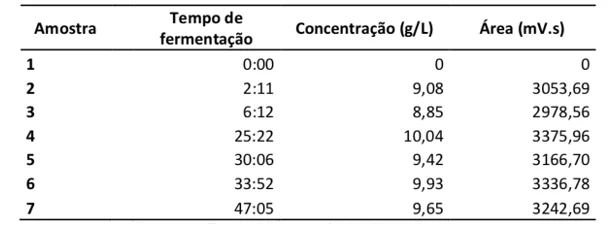
Observa-se que a concentração de ácido lático final na amostra 7 foi de 9,65 g/L utilizando como fonte de nitrogênio o permeado do soro de leite, porém para a base de cálculos Grocholski utilizou a produção de ácido lático apresentado na amostra 2 obtido em 2 horas, pois foi onde obteve-se o pico da produção, atingindo uma produtividade do ácido lático de 4,04 g/Lh. Sendo assim, nota-se que a produção de ácido lático utilizando permeado do soro de leite como fonte de nutrientes e, também, o melaço de cana-de-açúcar é um método viável quando comparado com outras fontes com o custo mais elevado.
4.1.3 AUTOR 3 (OLIVEIRA ET AL., 2005)
Para a produção contínua do ácido lático, Oliveira et al. (2005), optaram por utilizar o microrganismo Lactobacillus curvatus. Para fazer a solução do meio, a fim de realizar a fermentação, os autores utilizaram melaço de cana-de-açúcar tratado com 2% (v/v) de invertase a 37ºC e diluído a 10% (m/v) em água deionizada, a um pH de 4,7 por um período de 20 minutos. Para realizar a suplementação do meio Oliveira et al., ajustaram o pH para 6,2, utilizaram peptona a 4 % (m/v) e extrato de levedura na concentração de 2% (m/v).
Antes do microrganismo Lactobacillus curvatus ser adicionado ao meio fermentativo, o mesmo foi mantido sob refrigeração para ser ativado. Após ser adicionado no meio de fermentação, a temperatura de 37°C foi mantida em um período de 24 horas.
Para dar segmento ao início do método contínuo, Oliveira et al. utilizaram um fermentador cilíndrico de 0,5 L a temperatura de 37ºC sob agitação de 150 rpm, onde o mesmo recebeu uma alíquota de 10 % (v/v) do meio preparado previamente. Os autores iniciaram a fermentação contínua ligando uma bomba peristáltica após um período de 3 horas.
Durante a fermentação os autores optaram por retirar taxas de diluição diferentes entre si para realizar a comparação posteriormente, foi necessário aguardar o cultivo atingir a taxa estacionária de crescimento. Para o método as taxas de diluição escolhidas para serem avaliadas foram de 0,05; 0,10 e 0,15h-1.
Após analisarem o processo fermentativo, os autores calcularam a concentração de ácido lático, a produtividade do mesmo e o consumo de açúcar. Para realizar a extração do ácido lático e realizar as análises, Oliveira et al., optaram por utilizar uma coluna específica para ácidos chamada de Aminex HPX 87H, para assim posteriormente dispor a amostra em um cromatógrafo. Na figura 13 é possível observar os resultados extraídos do mesmo.
Figura 12. Produção de ácido láctico, biomassa e consumo de açúcar redutor pelo Lactobacillus curvatus na fermentação contínua de melaço de cana-de-açúcar tratado com invertase e suplementado com extrato de levedura 2% (m/v) e peptona 4% (m/v).
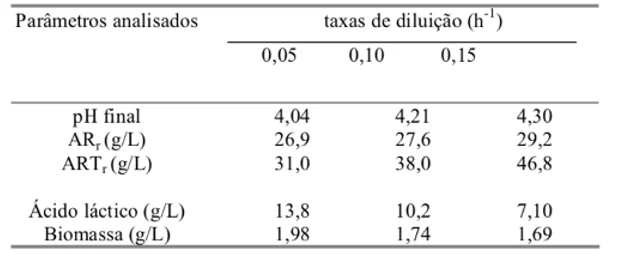
Nota-se que a maior produção de ácido lático e de biomassa se deu na diluição de 0,05h-1, apresentando um resultado de 13,0 g/L e 1,98 g/L, além de ser possível observar através da quantidade de açúcar redutor residual (ARr) e total (ARTr), que quanto maior a diluição menor é o consumo de açúcar, indicando assim que a diluição de 0,05 h-1 é a que mais se adequa ao método empregado.
Com isso, é possível afirmar que utilizando o microrganismo Lactobacillus curvatus, realizar o tratamento do melaço de cana-de-açúcar com invertase, suplementar o meio fermentativo com peptona e extrato de levedura indicado é utilizar a taxa de diluição adequada, ou seja, a menor, é possível obter um processo do meio de cultivo economicamente viável.
4.1.4 AUTOR 4 (OLIVEIRA ET AL., 2009)
Oliveira et al. (2009) optaram em utilizar o microrganismo Lactobacillus casei, para realizar a fermentação do substrato oriundo do melaço de cana-de-açúcar, o qual passou por um pré tratamento de hidrólise da sacarose por meio da ação da enzima invertase, proporcionando, assim, um alto índice de conversão em açúcares redutores. O meio de cultura em questão foi alimentado com 2% de peptona e 2% de extrato de levedura, os quais equivalem a uma concentração de 0,1 m/v cada um, a fim de promover uma maior produtividade.
O método empregado foi o da fermentação em batelada utilizando um Erlenmeyer de 500 mL como reator, com uma concentração inicial de 10% (m/v) de melaço diluído em água destilada. O pH inicial foi de aproximadamente 4,7 sendo ajustado para 6,2 durante o processo e decaindo para 3,8 ao final.
O microrganismo em questão, após ser mantido sob refrigeração, foi adicionado ao meio de cultura por um período de 48 horas sob agitação de 100 rpm e numa temperatura de 37ºC.
Na figura a seguir é possível verificar os resultados obtidos por Oliveira et al., sendo que aqueles que foram incrementados com uma maior quantidade de extrato de levedura e de peptona apresentaram uma produtividade maior de ácido lático:
Figura 13. Produção fermentativa de ácido lático a partir do melaço da cana-de-açúcar por Lactobacillus casei em diferentes concentrações de suplementação em extrato de levedura e peptona.
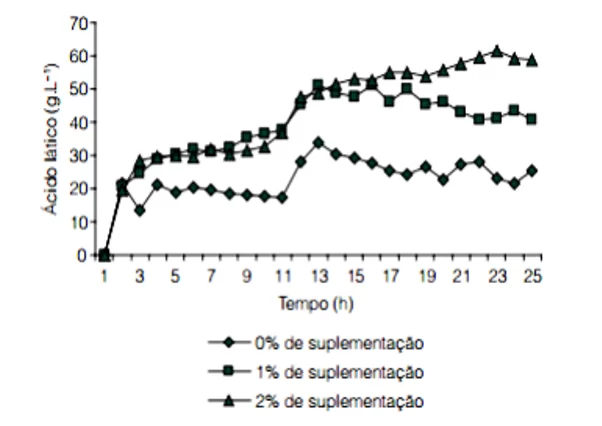
Nota-se que a concentração final de ácido lático obtido foi de 58,86 g/L para o meio de cultivo com 2% de suplementação, enquanto para aqueles cujos suplementos foram menores se obtiveram valores mais baixos. Foram registrados um rendimento de 0,76 g/g e uma produtividade de 1,22 g/L.h, constatando esse método como uma alternativa viável e eficiente para a concepção do ácido lático por meio da fermentação em batelada com melaço a 10% (m/v) e suplementação de 2% de peptona e 2% de extrato de levedura.
4.1.5 AUTOR 5 (CAPELLARI, 2010)
Com o propósito de se obter o ácido lático por meio do melaço da cana-de-açúcar, Capellari (2010) utilizou o microrganismo Lactobacillus amylovorus CCT 2948 no processo de fermentação contínua. O meio de cultura foi preservado com alguns nutrientes, tais quais: 10,0 g/L de peptona; 4,0 g/L de extrato de levedura; 8,0 g/L de extrato de carne; 20,0 g/L de glicose; 1,0 mL/L de monooleato de sorbitan; 2,0 g/L de fosfato de dipostássio;2,0 g/L de acetato de sódio; 2,0 g/L de citrato triamonical; 0,20 g/L de sulfato de magnésio e 0,05 g/L de sulfato de manganês.
Para dar continuidade, Capellari efetuou o experimento por meio de um Erlenmeyer de 250 mL sob um agitador orbital (Shaker) em condição agitada (120 min-1), durante um período de fermentação de 96h e sob uma temperatura de 37ºC.
Após esse tempo de cultivo, a concentração de substrato observado foi de 4 g/L, tendo-se produzido 14,8 g/L de ácido lático, o qual representa uma produtividade de 0,205 g/L.h.
A desvantagem desse processo, segundo a autora e os resultados analisados, refere-se à quantidade de glicose, de 4 g/L, que subsistiu após o processo, impossibilitando que a extração e a purificação do ácido lático ocorram de maneira adequada.
Na mesma linha de pesquisa com metodologia de fermentação contínua, Capellari (2010) seguiu o experimento com o microrganismo Lactobacillus amylovorus CCT 2948, sob mesmas condições de cultivo citadas anteriormente, porém, dessa vez seguindo o experimento com o Erlenmeyer de 250 mL sob um agitador orbital (Shaker) em condição estática.
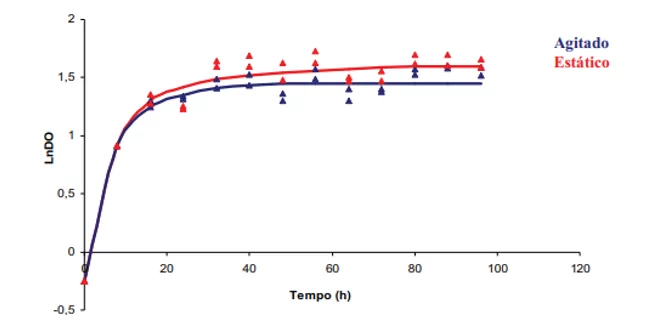
Após 96h de fermentação, a 37ºC, a autora destaca o resultado superior do perfil de crescimento do L. amylovorus ao longo do processo sob condição estática, quando comparada com o processo sob condição de agitação (120 min-1), visto que, a condição de agitação favoreceu a oxigenação, prejudicando o crescimento do microrganismo que é anaeróbio ou aerotolerante, Leite (2006).
Em relação a produção de ácido lático, o ensaio estático alcançou 20,7 g/L, representando produtividade de 0,198 g/L.h. Mesmo o valor de produtividade sendo inferior ao processo de condição de agitação, a autora destaca a vantagem da condição estática, visto que o fator de conversão do substrato foi aproximadamente 9% superior.
Figura 14. Perfil de crescimento do Lactobacillus amylovorus em diferentes condições de agitação.
Além das diferentes condições em agitador orbital, Capellari (2010) também realiza um ensaio num biorreator (Biotron), com cuba de 4 litros. Para isto, utiliza-se ainda o microrganismo Lactobacillus amylovorus, sob as mesmas condições de cultivo dos ensaios anteriores.
Para o experimento em biorreator, utilizou-se 40 g/L de melaço, com um processo de 96h, sob 37ºC. Houve crescimento exponencial de produção de ácido lático entre 16 e 48h de cultivo, e até 57h houve consumo total do substrato.
Como resultados, obteve-se uma produtividade de ácido lático de 0,11 g/L.h, com produtividade máxima de até 0,14 g/L.h, e o fator de conversão alcançou um valor de 1,43 g/g.
5. CONSIDERAÇÕES FINAIS
O presente artigo foi desenvolvido por meio de um estudo comparativo entre procedimentos técnicos de trabalhos experimentais de outros autores, com base na questão norteadora: por quais métodos se é possível obter, a partir do resíduo da cana-de-açúcar, uma melhor concentração, e consequentemente, um melhor rendimento de ácido lático para, posteriormente, originar o biopolímero Poli-Ácido Lático (PLA) a fim de que minimize o impacto ambiental? Tendo-se, portanto, o objetivo de apresentar, por meio de uma revisão bibliográfica, um comparativo de metodologias e parâmetros utilizados para obtenção de Ácido Lático (AL) a partir do resíduo agroindustrial da cana-de-açúcar, o melaço, analisando-se qual foi a mais produtiva.
Nesse contexto, tendo-se em vista determinar a produtividade em termos de valores de concentração final de AL (g/L) dos diferentes processos analisados, pode-se destacar os processos que utilizam a metodologia de fermentação em batelada, seguida da fermentação contínua, onde os maiores valores de concentração encontrados foram de 58,86 g/L e 20,70 g/L. É importante ressaltar que, para a fermentação em batelada, houve interferência da etapa adicional do pré-tratamento de hidrólise com invertase para maiores resultados finais, enquanto para a fermentação contínua a maior concentração encontrada não utilizou nenhum tipo de pré-tratamento. Além disso, a escolha do microrganismo, Lactobacillus casei, e os nutrientes selecionados para seu cultivo, no processo de fermentação batelada, também puderam ser considerados fatores que impactaram diretamente na eficiente conversão do substrato em produto.
Logo, apesar dos desafios de inibição pelo substrato e pelo produto, a linha de pesquisa da produção de ácido lático a partir do resíduo agroindustrial melaço de cana-de-açúcar se mostra factível e promissora, assim que, diferentes estudos e metodologias têm avançado no que diz respeito à eficácia dos diferentes processos possíveis para a obtenção do produto ácido lático, monômero do biopolímero Ácido Polilático (PLA), que pode servir como alternativa sendo uma matéria-prima biodegradável na indústria de plásticos.
REFERÊNCIAS
ASSOCIAÇÃO BRASILEIRA DE EMBALAGENS – ABRE. Estudo abre macroeconômico da embalagem e cadeia de consumo. 2021. Disponível em: https://www.abre.org.br/dados-do-setor/2020-2/. Acesso em: 12 mar. 2022.
AKCELRUD, Leni. Fundamentos da ciência dos polímeros, 1ª edição. São Paulo: Editora Manole Ltda, 2007, p. 126-176, vol. 1. Disponível em: https://books.google.com.br/books?hl=pt-BR&lr=&id=3wJHvsGcjl4C&oi=fnd&pg=PR17&dq=Pol%C3%ADmeros&ots=q4ZW5_FP3d&sig=1rAwYxbRVXcoR6JiLhIZHdpXy_s#v=onepage&q=Pol%C3%ADmeros&f=false. Acesso em: 21 abr. 2022.
ARCANJO, Maria Rosiene Antunes. Conversão de glicerol em ácido lático utilizando catalisadores heterogêneos de paládio e platina suportados em carbono ativado. 2017. 123f. Tese (Doutorado em Engenharia Química) – Universidade Federal do Ceará, Fortaleza, CE, 2017. Disponível em: https://repositorio.ufc.br/bitstream/riufc/28629/5/2017_tese_mraarcanjo.pdf. Acesso em: 23 abr. 2022.
ARRIETA, M. P., SAMPER, M. D., ALDAS, M., LÓPEZ, J. On the Use of PLA-PHB Blends for Sustainable Food Packaging Applications. Materials, v. 10, n. 9: 1008, p. 1-26. 2017. Disponível em: https://doi.org/10.3390/ma10091008. Acesso em: 01 mai. 2022.
AURAS, R., HARTE, B., SELKE, S. An Overview of Polylactides as Packaging Materials. Macromolecular Bioscience, v. 4, ed. 9, p. 835-864, 2004. Disponível em: https://onlinelibrary.wiley.com/doi/10.1002/mabi.200400043. Acesso em: 02 mai. 2022.
BASSANI, Joseane Cristina. Imobilização de células microbianas em esferas de alginato de cálcio e avaliação da viabilidade celular e estabilidade bioquímica em diferentes condições de armazenamento. 2018. 77f. Dissertação (Mestrado em Tecnologia de Processos Químicos e Bioquímicos) – Universidade Tecnológica Federal do Paraná, Pato Branco, PR, 2018. Disponível em: https://repositorio.utfpr.edu.br/jspui/handle/1/3574. Acesso em: 24 abr. 2022.
BASTOS, Valéria Delgado. Biopolímeros e polímeros de matérias-primas renováveis alternativos aos petroquímicos. Revista do BNDES, Rio de Janeiro, RJ, v. 14, n. 28, p. 201-234, 2007. Disponível em: http://web.bndes.gov.br/bib/jspui/handle/1408/11834. Acesso em: 20 abr. 2022.
BRASIL. Lei nº 12.305, de 2 de agosto de 2010. Institui a Política Nacional de Resíduos Sólidos; altera a Lei no 9.605, de 12 de fevereiro de 1998; e dá outras providências. Disponível em: http://www.planalto.gov.br/ccivil_03/_ato2007-2010/2010/lei/l12305.htm. Acesso em: 09 abr. 2022.
BRITO, G. F., AGRAWAL, P., ARAÚJO, E. M., MÉLO, T. J. A. Biopolímeros, Polímeros Biodegradáveis e Polímeros Verdes. Revista Eletrônica de Materiais e Processos. Departamento de Engenharia de Materiais – Universidade Federal de Campina Grande, Campina Grande, PB, v. 6.2, p. 127-139, 2011. Disponível em: http://www2.ufcg.edu.br/revista-remap/index.php/REMAP/article/view/222/204. Acesso em: 24 abr. 2022.
CALABRIA, Luciane. Blendas de biopolímeros para liberação controlada de agroquímicos. 2010. 108f. Dissertação (Mestrado em Ciência e Engenharia de Materiais) – Universidade de Caxias do Sul, Caxias do Sul, RS, 2010. Disponível em: https://repositorio.ucs.br/xmlui/bitstream/handle/11338/454/Dissertacao%20Luciane%20Calabria.pdf?sequence=1. Acesso em: 24 abr. 2022.
CAPELLARI, Jaqueline Boldt. Biossíntese de ácido láctico por Lactobacillus amylovorus a partir de resíduos agroindustriais. 2010. 71f. Dissertação (Mestrado em Engenharia de Processos) – Universidade da Região de Joinville, Univille, SC, 2010. Disponível em: https://www.univille.edu.br/account/mep/VirtualDisk.html/downloadDirect/2828826/Dissertacao_Jaqueline_Boldt_Capellari.pdf. Acesso em: 23 abr. 2022.
CASTRO, A. M. de; PEREIRA Jr, N. Produção, propriedades e aplicações de celulases na hidrólise de resíduos agroindustriais. Química Nova, Rio de Janeiro, RJ, v. 33, n. 1, p.181-188, 2010. Disponível em: https://www.scielo.br/j/qn/a/HbPYKnpgwSf4jhH4dtVSMhr/. Acesso em: 26 abr. 2022.
CASTRO, Thais Hessab Moreira de. Os bioplásticos: Impactos ambientais e perspectivas de mercado. 2019. 83f. Dissertação (Mestrado em Ciência em Planejamento Energético) – Universidade Federal do Rio de Janeiro, Rio de Janeiro, RJ, 2019. Disponível em: http://www.ppe.ufrj.br/images/Disserta%C3%A7%C3%A3o_Thais_Hessab_Vers%C3%A3o_Final.pdf. Acesso em: 24 abr. 2022.
CENTRO DE ESTUDOS AVANÇADOS EM ECONOMIA APLICADA – CEPEA. PIB do Agronegócio Brasileiro. 2022. Disponível em: https://www.cepea.esalq.usp.br/br/pib-do-agronegocio-brasileiro.aspx#:~:text=Diante%20do%20bom%20desempenho%20do,52%2C63%25%2C%20respectivamente. Acesso em: 12 mar. 2022.
COMISSÃO MUNDIAL SOBRE MEIO AMBIENTE E DESENVOLVIMENTO – CMMAD. Nosso futuro comum, 2ª edição. Rio de Janeiro: Editora da Fundação Getúlio Vargas, 1991, p. 47-71. Disponível em: https://edisciplinas.usp.br/pluginfile.php/4245128/mod_resource/content/3/Nosso%20Futuro%20Comum.pdf. Acesso em: 24 abr. 2022.
COMPANHIA NACIONAL DE ABASTECIMENTO – CONAB. Acompanhamento da safra brasileira de cana-de-açúcar – Safra 2022/23. 2022. Disponível em: https://www.conab.gov.br/info-agro/safras/cana/boletim-da-safra-de-cana-de-acucar. Acesso em: 29 abr. 2022.
COSTA FILHO, D. V.; Silva, A. J.; SILVA, P. A. P.; SOUSA, F. C. Aproveitamento de Resíduos Agroindustriais na Elaboração de Subprodutos. III Congresso Internacional das Ciências Agrárias COINTER – PDVAgro, Instituto Federal de Educação, Ciência e Tecnologia do Sertão Pernambucano, PE, 2017. Disponível em: https://cointer-pdvagro.com.br/wp-content/uploads/2018/02/APROVEITAMENTO-DE-RES%C3%8DDUOS-AGROINDUSTRIAIS-NA-ELABORA%C3%87%C3%83O-DE-SUBPRODUTOS.pdf. Acesso em: 07 abr. 2022.
CRUZ, M. A. D., CASANOVA, R. F., BOSCARDIN, D., ZANCHET, A. Análise da viabilidade do uso de resíduos de cana-de-açúcar para produção de aglomerantes sustentáveis. Revista Matéria, Rio de Janeiro, RJ, v. 26, 2021. Disponível em: https://www.scielo.br/j/rmat/a/mQbQWKmK4GRMtdRz7JQ5zdb/?lang=pt. Acesso em: 24 abr. 2022.
DAINTITH, J. A dictionary of chemistry, 6ª edição. Nova Iorque: Oxford University Press, 2008. Disponível em: https://www.academia.edu/6075352/Dictionary_of_chemistry. Acesso em: 30 jul. 2022.
DATTA, R.; HENRY, M. Review Lactic acid: recent advances in products, processes and technologies — a review. Journal of Chemical Technology & Biotechnology, Argonne National Laboratory, Estados Unidos, v. 81, n. 7, p. 1119–1129, 2006. Disponível em: https://www.academia.edu/25459910/Lactic_acid_recent_advances_in_products_processes_and_technologies_a_review. Acesso em: 23 abr. 2022.
DATTA, R.; TSAI, S., BONSIGNORE, P., MOON, S., FRANK, J. R. Technological and economic potential of poly(lactic acid) and lactic acid derivatives. FEMS Microbiology Reviews, Department of Energy, Estados Unidos, v. 16, p. 221-231, 1995. Disponível em: https://www.academia.edu/25459908/Technological_and_economic_potential_of_poly_lactic_acid_and_lactic_acid_derivatives. Acesso em: 24 abr. 2022.
DORNELLES, Emanuel Stingelin. Produção de ácido lático: panorama de melhorias de processos, 2021. 116f. Trabalho de Conclusão de Curso (Bacharel em Engenharia Química) – Universidade Tecnológica Federal do Paraná, Francisco Beltrão, PR, 2021. Disponível em: http://repositorio.utfpr.edu.br/jspui/handle/1/26746. Acesso em: 24 abr. 2022.
EMBRAPA. Brasil é o quarto maior produtor de grãos e o maior exportador de carne bovina do mundo, diz estudo. 2020. Disponível em: https://www.embrapa.br/busca-de-noticias/-/noticia/62619259/brasil-e-o-quarto-maior-produtor-de-graos-e-o-maior-exportador-de-carne-bovina-do-mundo-diz-estudo. Acesso em: 08 abr. 2022.
Food and Agriculture Organization of the United Nations – FAO. O desperdício alimentar tem consequências ao nível do clima, da água, da terra e da biodiversidade. 2013. Disponível em: https://www.fao.org/news/story/pt/item/204029/icode/. Acesso em: 08 abr. 2022.
FORTUNA, Ana Luíza Lobo. Impactos ambientais dos plásticos: Biopolímeros como alternativa para a redução do acúmulo de embalagens flexíveis de polipropileno no meio ambiente, 2020. 123f. Trabalho de Conclusão de Curso (Bacharel em Engenharia Química) – Universidade Federal do Rio de Janeiro, Rio de Janeiro, RJ, 2020. Disponível em: https://pantheon.ufrj.br/bitstream/11422/12581/1/ALLFortuna.pdf. Acesso em: 24 abr. 2022.
FRANCHETTI, S. M. M.; MARCONATO, J. C. Polímeros biodegradáveis-uma solução parcial para diminuir a quantidade dos resíduos plásticos. Química Nova, Rio Claro, SP, v. 29, n. 4, p. 811-816, 2006. Disponível em: https://www.scielo.br/j/qn/a/QXT9wMDfVQ9PrhbVsp8b3Pc/?format=pdf&lang=pt. Acesso em: 21 abr. 2022.
G1. Brasil é o 4º maior produtor de lixo plástico do mundo e recicla apenas 1%. 2019. Disponível em: https://g1.globo.com/natureza/noticia/2019/03/04/brasil-e-o-4o-maior-produtor-de-lixo-plastico-do-mundo-e-recicla-apenas-1.ghtml. Acesso em: 12 mar. 2022.
GHAFFAR, T.; IRSHAD, M.; ANWAR, Z.; AQIL, T.; ZULIFQAR, Z.; TARIQ, A.; KAMRAN, M.; EHSAN, N.; MEHMOOD, S. Recent trends in lactic acid biotechnology: a brief review on production to purification. Journal of Radiation Research and Applied Sciences, Paquistão, v. 7, n. 2, p. 222-229, 2014. Disponível em: https://www.sciencedirect.com/science/article/pii/S1687850714000314. Acesso em: 16 abr. 2022.
GONÇALVES, Paula Fernanda Almeida. Obtenção e caracterização de compósitos poliméricos biodegradáveis obtidos via extrusão a partir de PLA (ácido polilático), amido de mandioca, glicerol e bagaço de cana-de-açúcar. 2013. 83f. Trabalho de Conclusão de Curso (Bacharel em Engenharia Ambiental) – Universidade Tecnológica Federal do Paraná, Londrina, PR, 2013. Disponível em http://repositorio.utfpr.edu.br/jspui/handle/1/11955. Acesso em: 27 abr. 2022.
GONZÁLEZ, A. J. A.; CAMBA, E. A. N. Etanol a partir de biomasa lignocelulósica, 1ª edição. Editora Aleta Ediciones, 2012, p. 1-101. Disponível em https://www.researchgate.net/publication/241216642_Etanol_a_partir_de_biomasa_lignocelulosica. Acesso em: 26 mar. 2022.
GROCHOLSKI, Luís Felipe. Produção de ácido lático a partir do melaço de cana-de-açúcar. 2019. 44f. Trabalho de conclusão de Curso (Bacharel em Engenharia Química) – Universidade Tecnológica Federal do Paraná, Ponta Grossa, PR, 2019. Disponível em: https://repositorio.utfpr.edu.br/jspui/bitstream/1/16484/1/PG_COENQ_2019_2_011.pdf. Acesso em: 30 jul. 2022.
GUTIÉRREZ, P. D. B., YÁÑEZ, R. B. Producción de biomasa probiótica y ácido láctico mediante cultivo discontinuo, semicontinuo y continuo de una cepa Lactobacillus plantarum autóctona. AAIQ – Associación Argentina de Ingenieros Químicos – CSPQ, Buenos Aires, Argentina, 2013. Disponível em: http://www.aaiq.org.ar/SCongresos/docs/06_029/papers/04a/04a_1831_327.pdf. Acesso em: 24 abr. 2022.
HOLZAPFEL, H. W.; HABERER, P.; GEISEN, R.; BJORKROTH, J.; SCHILLINGER, U. Taxonomy and important features of probiotic microorganisms in food and nutrition. The American Journal of Clinical Nutrition. Alemanha, v. 73, n. 2, p. 365-373, 2001. Disponível em: https://academic.oup.com/ajcn/article/73/2/365s/4737564?login=false. Acesso em: 16 jun. 2022.
NACHILUK, K. Alta na Produção e Exportações de Açúcar Marcam a Safra 2020/21 de Cana. Análises e Indicadores do Agronegócio, São Paulo, v. 16, n. 6, p. 1-5, 2021. Disponível em: http://www.iea.sp.gov.br/out/TerTexto.php?codTexto=15925#:~:text=O%20Brasil%20%C3%A9%20o%20maior,de%20litros%20de%20etanol1. Acesso em: 09 abr. 2022.
JUNIOR, A.P; JUNIOR, A. C. B.; BONOMI, A.; KILLIKIAN, B. V.; CAPALBO, D. M. F.; HISS, H.; MORAES, I. de O.; CARVALHO, J. C. M. de; PRADELLA, J. G. da C.; THIEMANN, J. E. Biotecnologia Industrial, 1ª edição. São Paulo: Editora Edgard Blucher Ltda, 2001, p. 247-276, vol. 2. Disponível em: https://www.embrapa.br/busca-de-publicacoes/-/publicacao/1119032/fermentacao-em-estado-solido. Acesso em: 24 abr. 2022.
JUNIOR, Ronan Ribeiro Costa; Estudo de diferentes processos de produção de cachaça e influência nas características físico-químicas do produto, 2016. 57f. Trabalho de Conclusão de Curso (Graduação em Engenharia Agroindustrial Agroquímica) – Universidade Federal do Rio Grande, Santo Antônio da Patrulha, RS, 2016. Disponível em: https://sistemas.furg.br/sistemas/sab/arquivos/conteudo_digital/000008419.pdf. Acesso em: 24 abr. 2022.
KÁDÁR, Zs.; SZENGYEL, Zs.; RÉCZEY, K.. Simultaneous saccharification and fermentation (SSF) of industrial wastes for the production of ethanol. Industrial Crops and Products, Budapeste, Hungria, v. 20, p. 103-110, 2004. Disponível em: https://doi.org/10.1016/j.indcrop.2003.12.015. Acesso em: 21 mai. 2022.
KARP, S. G.; WOICIECHOWSKI, A. L.; SOCCOL, V. T.; SOCCO, C. R. Pretreatment Strategies for Delignification of Sugarcane Bagasse: A Review. Brazilian Archives of Biology and Technology, Curitiba, PR, v. 56, n.4, p. 679-689, 2013. Disponível em: https://www.academia.edu/54392144/Pretreatment_strategies_for_delignification_of_sugarcane_bagasse_a_review. Acesso em: 26 abr. 2022.
KASSIM, M. A.; MENG, T. K.; KAMALUDIN, R.; HUSSAIN, A. H.; BUKHARI, N. A. Chapter 9 – Bioprocessing of sustainable renewable biomass for bioethanol production. Value-Chain of Biofuels. Fundamentals, Technology, and Standardization. Value-Chain of Biofuels, Malaysia, p. 195-234, 2022. Disponível em: https://doi.org/10.1016/B978-0-12-824388-6.00004-X. Acesso em: 21 mai. 2022.
KIEFER, Rayane Grizotti. Estudo da fermentação alcoólica do hidrolisado da biomassa Cacaueira para produção de etanol. 2018. 72f. Dissertação (Mestrado em Engenharia Química) – Universidade Federal do Espírito Santo, Alegre, ES, 2018. Disponível em: http://repositorio.ufes.br/handle/10/10569. Acesso em: 26 abr. 2022.
KOMESU, A.; OLIVEIRA, J. A. R. de; MARTINS, L. H. d. S.; MACIEL, M. R. W.; FILHO, R. M. Lactic Acid Production to Purification: A Review. BioResources, Campinas, SP, v. 12, n. 2, p. 4364–4383, 2017. Disponível em: https://bioresources.cnr.ncsu.edu/resources/lactic-acid-production-to-purification-a-review/. Acesso em: 16 abr. 2022.
LOPES, Angela Romero. Produção de ácido lático por lactobacilos em diferentes meios de cultivo. 2008. 67f. Dissertação (Mestrado em Ciências Biológicas) – Universidade Estadual Paulista “Júlio de Mesquita Filho”, Rio Claro, SP, 2008. Disponível em http://hdl.handle.net/11449/94976. Acesso em: 16 jun. 2022.
LÓPEZ-GÓMEZ, J. P.; ALEXANDRI, M.; SCHNEIDER, R.; VENUS, J. A review on the current developments in continuous lactic acid fermentations and case studies utilising inexpensive raw materials. Process Biochem, v. 79, p. 1-10, 2019. Disponível em: https://doi.org/10.1016/j.procbio.2018.12.012. Acesso em: 24 abr. 2022.
LU, Y.; LU, Y. C.; HU, H. Q.; XIE, F. J.; WEI, X. Y.; FAN, X. Structural characterization of lignin and its degradation products with spectroscopic methods. Journal of Spectroscopy, v. 2017, p. 1-15, 2017. Disponível em: https://doi.org/10.1155/2017/8951658. Acesso em: 11 mai. 2022.
MALTA, Hélia Lucila. Estudos de parâmetros de propagação de fermento (Saccharomyces cerevisiae) para produção de cachaça de alambique. 2006. 70f. Dissertação (Mestrado em Ciência de Alimentos) – Universidade Federal de Minas Gerais, Belo Horizonte, MG, 2006. Disponível em: https://repositorio.ufmg.br/bitstream/1843/MBSA-6XWFAD/1/diss_versao_final.pdf. Acesso em: 24 abr. 2022.
MARULANDA, V. A.; GUTIERREZ, C. D. B.; ALZATE, C. A. C. Thermochemical, Biological, Biochemical, and Hybrid Conversion Methods of Bio-derived Molecules into Renewable Fuels. Woodhead Publishing, Advanced Bioprocessing for Alternative Fuels, Biobased Chemicals, and Bioproducts, Colômbia, cap. 4, p. 59-81, 2019. Disponível em: https://doi.org/10.1016/B978-0-12-817941-3.00004-8. Acesso em: 21 mai. 2022.
Ministério da Agricultura, Pecuária e Abastecimento. MAPA DO LEITE: Políticas Públicas e Privadas para o leite. Disponível em: https://www.gov.br/agricultura/pt-br/assuntos/producao-animal/mapa-do-leite. Acesso em: 09 abr. 2022.
Ministério da Agricultura, Pecuária e Abastecimento. O QUE É AGROINDÚSTRIA?. 2021. Disponível em: https://www.gov.br/agricultura/pt-br/assuntos/sustentabilidade/agroindustria/o-que-e-agroindustria. Acesso em: 07 abr. 2022.
MORAES, M. A.; THEIS, V.; VIER, M. B.; SCHREIBER, D. Análise dos custos ambientais relacionados com a gestão de resíduos em indústrias químicas. Revista de administração, contabilidade e economia, Joaçaba, SC, v. 16, n. 2, p. 505–522, 2017. Disponível em https://dialnet.unirioja.es/servlet/articulo?codigo=6093649. Acesso em: 31 jul. 2022.
MOREIRA, A. L., ALMEIDA, W. S., SCABBIA, R. J. A., TEIXEIRA, R. R. P. Dosagem de ácido lático na produção de etanol a partir da cana-de-açúcar. Biológico, São Paulo, SP, v. 71, n. 1, p. 69-76, 2009. Disponível em: http://201.55.42.151/uploads/docs/bio/v71_1/moreira.pdf. Acesso em: 24 abr. 2022.
National Geographic. Para os bichos, o plástico transforma o oceano em um campo minado, 2020. Disponível em: https://www.nationalgeographicbrasil.com/2018/05/animais-plastico-uso-unico-oceanos-lixo. Acesso em: 01 mai. 2022.
NEVES, Luiz Carlos Martins das. Obtenção da enzima glicose 6-fosfato desidrogenase utilizando ‘Saccharomyces cerevisiae’ W303-181. 2003. 319f. Dissertação (Mestrado em Ciências Farmacêuticas) – Universidade de São Paulo, São Paulo, SP, 2003. Disponível em: https://teses.usp.br/teses/disponiveis/9/9134/tde-08102006-175534/pt-br.php. Acesso em: 24 abr. 2022.
OGATA, Bruna Harumi. Caracterização das frações celulose, hemicelulose e lignina de diferentes genótipos de cana-de-açúcar e potencial de uso em biorrefinarias. 2013. 108f. Dissertação (Mestrado em Ciências) – Universidade de São Paulo Escola Superior de Agricultura “Luiz de Queiroz”. Piracicaba, SP, 2013. Disponível em: https://www.teses.usp.br/teses/disponiveis/11/11141/tde-13112013-143039/pt-br.php. Acesso em: 6 mar. 2022.
OGEDA, T. L.; PETRI, D. F. S. Hidrólise Enzimática da Biomassa. Química Nova, São Paulo, SP, v. 33, n. 7, p. 1549-1558, 2010. Disponível em: https://www.scielo.br/j/qn/a/9n4nqyhZ3dVtZrpHQy5thDh/?format=pdf&lang=pt. Acesso em: 26 abr. 2022.
OLIVEIRA, Aline Pereira de. Resíduos da Indústria de Alimentos para Elaboração de Farinhas: Uma Estratégia para Aproveitamento. 2018. 48f. Trabalho de Conclusão de Curso (Tecnólogo de Alimentos) – Universidade Federal da Paraíba, João Pessoa, PB, 2018. Disponível em: https://repositorio.ufpb.br/jspui/bitstream/123456789/15791/1/APO19092019.pdf. Acesso em: 10 mar. 2022.
OLIVEIRA, A. R. de; BUZATO, J. B.; HAULY, M. C. d. O. Produção contínua de ácido láctico por Lactobacillus curvatus a partir de melaço de cana-de-açúcar suplementado. Semina: Ciências Agrárias, Universidade Estadual de Londrina, Londrina, PR, v. 26, n. 1, p. 53-59, 2005. Disponível em: https://www.redalyc.org/pdf/4457/445744074007.pdf. Acesso em: 10 abr. 2022.
OLIVEIRA, Karen Fernanda de. Efeito do ácido lático adicionado sobre a produção de etanol em fermentações com reutilização de células a 34ºC. 2008. 191f. Tese (Doutorado em Biotecnologia) – Universidade de São Paulo, São Paulo, SP, 2008. Disponível em: https://www.teses.usp.br/teses/disponiveis/87/87131/tde-17042009-171443/en.php. Acesso em: 24 abr. 2022. Acesso em: 10 mar. 2022.
OLIVEIRA, R. F.; SOUSDALEFF, M.; LIMA, M. V. dos S.; LIMA, H. O. dos S. Produção fermentativa de ácido lático a partir de melaço de cana-de-açúcar por Lactobacillus casei. Brazilian Journal of Food Technology. VII BMCFB. p. 34-40, 2009. Disponível em: https://xdocs.com.br/download/produccion-fermentativa-de-acido-lactico-a-partir-de-melaza-de-caa-de-azucar-por-lactobacillus-casei-portuguespdf-2855033m1m8x?hash=f4670f90896d776fe80ea9f9160d63e4. Acesso em: 21 mai. 2022.
OLOFSSON, K.; BERTILSSON, M.; LIDÉN, G. A short review on SSF – an interesting process option for ethanol production from lignocellulosic feedstocks. Biotechnol Biofuels, Lund, Suécia, v. 1, n. 7 p. 1–14, 2008. Disponível em: https://biotechnologyforbiofuels.biomedcentral.com/articles/10.1186/1754-6834-1-7. Acesso em: 21 mai. 2022.
PAL, P.; SIKDER, J.; ROY, S.; GIORNO, L. Process intensification in lactic acid production: A review of membrane based processes. Chemical Engineering and Processing: Process Intensification, v. 48, n. 11-12, p. 1549-1559, 2009. Disponível em: https://www.academia.edu/5233981/Process_intensification_in_lactic_acid_production_A_review_of_membrane_based_processes. Acesso em: 23 abr. 2022.
PEREIRA, Nathália Terra. Produção de Ácido Lático com Resíduos Agroindustriais: Uma Revisão da Literatura. 2019. 67f. Trabalho de Conclusão de Curso (Diplomação em Engenharia Química) – Universidade Federal do Rio Grande do Sul, Porto Alegre, RS, 2019. Disponível em: https://www.lume.ufrgs.br/bitstream/handle/10183/199872/001101868.pdf?sequence=1. Acesso em: 09 mar. 2022.
PINHO, C. L. C de; OLIVEIRA, C. E. S. de; COIMBRA, J. C.; COTRIM; W. S. Produção de ácido lático em meio à base de efluentes da indústria de alimentos por cultura láctea mista imobilizada. Brazilian Journal of Food Technology, Campinas, SP, v. 22, e2018100, p. 1-10, 2019. Disponível em: https://doi.org/10.1590/1981-6723.10018. Acesso em: 12 mar. 2022.
PRADELLA, José Geraldo da Cruz. Biopolímeros e Intermediários Químicos. Centro de Gestão e Estudos Estratégicos. Centro de Tecnologia de Processos e Produtos – Laboratório de Biotecnologia Industrial-LBI/CTPP, São Paulo, SP, Relatório Técnico n. 84 396-205, p. 1-119, 2006. Disponível em: http://www.redetec.org.br/wp-content/uploads/2015/02/tr06_biopolimeros.pdf. Acesso em: 01 mai. 2022.
ROCHA, Nattácia Rodrigues de Araújo Felipe. Produção de celulase por fermentação submersa empregando resíduos agroindustriais para a produção de etanol. 2011. 93f. Dissertação (Mestrado em Engenharia Química) – Universidade Federal de Uberlândia, Uberlândia, MG, 2011. Disponível em: https://repositorio.ufu.br/bitstream/123456789/15165/1/d.pdf. Acesso em: 14 mai. 2022.
RODRIGUES, Cristine. Desenvolvimento de bioprocesso para produção de ácido cítrico por fermentação no estado sólido utilizando polpa cítrica. 2006. 93f. Dissertação (Mestrado em Processos Biotecnológicos) – Universidade Federal do Paraná, Curitiba, PR, 2006. Disponível em: https://acervodigital.ufpr.br/bitstream/handle/1884/14843/disserta%C3%A7%C3%A3ocorrigida.pdf?sequence=1. Acesso em: 24 abr. 2022.
RODRIGUES, Giselle de Arruda. Conversão de bagaço de cana abre frente para produção de polímero verde. Jornal da Unicamp, Campinas, SP, 2012. Disponível em: https://www.unicamp.br/unicamp/sites/default/files/jornal/paginas/ju540pag02.pdf. Acesso em: 26 abr. 2022.
RODRIGUES, M. K.; REICH, M.; PIMENTA, F. D.; PICARDO, M. C. Produção de ácido D-lático por rota fermentativa e hidrólise enzimática a partir de matéria-prima lignocelulósica. Revista Processos Químicos, Rio de Janeiro, RJ, p.65-76, 2018. Disponível em: http://ojs.rpqsenai.org.br/index.php/rpq_n1/article/view/464/451. Acesso em: 26 abr. 2022.
ROWELL, R. M.; PETTERSEN, R.; TSHABALALA, M. A. Cell Wall Chemistry. Handbook of Wood Chemistry and Wood Composites. 2ª edição. Editora CRC Press, 2012, p. 33-72. Disponível em: https://www.routledgehandbooks.com/doi/10.1201/b12487-5. Acesso em: 22 mai. 2022.
SANTIAGO, B. L. S.; RODRIGUES, F. d. Á. Processamento De Biomassa Lignocelulósica Para Produção De Etanol: Uma Revisão. The Journal of Engineering and Exact Sciences, Viçosa, MG, v. 3, n. 7, p. 1011–1022, 2017. Disponível em: https://www.locus.ufv.br/handle/123456789/20138. Acesso em: 15 mar. 2022.
SANTOS, Gesmar Rosa dos. Agroindústria no Brasil: um olhar sobre indicadores de porte e expansão regional. Radar: Tecnologia, Produção e Comércio Exterior, n. 31, p. 7-19, 2014. Disponível em: https://www.ipea.gov.br/radar/temas/agricultura/333-radar-n-31-agroindustria-no-brasil-um-olhar-sobre-indicadores-de-porte-e-expansao-regional. Acesso em: 07 abr. 2022
SANTOS, Vidiany Aparecida Queiroz. Avaliação de suportes para a imobilização de Zymomonas mobilis CCT 4494 visando à produção de etanol e levana. 2013. 116f. Tese (Doutorado em Engenharia e Ciência de Alimentos) – Universidade Estadual Paulista “Júlio de Mesquita Filho”, São José do Rio Preto, SP, 2013. Disponível em: https://repositorio.unesp.br/handle/11449/110990. Acesso em: 24 abr. 2022.
SBRT – Serviço Brasileiro de Respostas Técnicas. Biotecnologia na Produção de Alimentos, Dossiê Técnico, 2011. Disponível em: http://www.respostatecnica.org.br/dossie-tecnico/downloadsDT/NTY3Ng==. Acesso em: 24 abr. 2022.
SEEFELDT, Andressa Thais. Obtenção de nanocompósitos de Poli(ácido lático) e nanocristais de celulose de casca de soja. 2012. 57f. Trabalho de Conclusão de Curso (Bacharel em Química Industrial) – Universidade Federal do Rio Grande do Sul, Porto Alegre, RS, 2012. Disponível em: https://www.lume.ufrgs.br/bitstream/handle/10183/55903/000858376.pdf?sequence=1&isAllowed=y. Acesso em: 24 abr. 2022.
SILVA, A. L. B. B. e; SILVA, E. O. Conhecendo materiais poliméricos. Universidade Federal de Mato Grosso, Instituto de Ciências Exatas e da Terra, Departamento de Física, Grupo de Pesquisa em Novos Materiais, p. 1-84, 2003. Disponível em: http://www.dominiopublico.gov.br/download/texto/ea000223.pdf. Acesso em: 24 abr. 2022.
SILVA, M. V.; GONÇALVES, O. H.; LIMA, M. V. d. S.; LIMA, H. O. d. S. Obtenção de ácido lático via fermentação descontínua utilizando melaço de cana-de-açúcar, farinha de varredura, frutose e fécula de mandioca. Revista Brasileira de Pesquisa em Alimentos, Campo Mourão, PR, v. 1, n. 2, p. 97-102, 2010. Disponível em: https://docplayer.com.br/78423514-Revista-brasileira-de-pesquisa-em-alimentos-campo-mourao-pr-v-1-n-2-p-jul-dez-2010.html. Acesso em: 15 jun. 2022.
SILVA, R.; HARAGUCHI, S.K.; MUNIZ, E.C.; RUBIRA, A.F. Aplicações de fibras lignocelulósicas na química de polímeros e em compósitos. Química Nova, Maringá, PR, v. 32, n. 3, p. 661–671, 2009. Disponível em: https://www.scielo.br/j/qn/a/scTjjqWPjcLKmgMdRR73SQB/?format=pdf&lang=pt.. Acesso em: 17 abr. 2022.
SILVESTRINI, Rafael. Síntese e caracterização de poli(ácido lático) (pla) via microondas. 2020. 94f. Dissertação (Mestrado em Engenharia) – Universidade Federal do Rio Grande do Sul, Porto Alegre, RS, 2020. Disponível em https://lume.ufrgs.br/handle/10183/219154. Acesso em: 16 jun. 2022.
SOARES, Vilhena. Plástico: o mundo produziu 8,3 bi de toneladas em 65 anos e reciclou só 9%. Correio Braziliense, 2017. Disponível em: https://www.correiobraziliense.com.br/app/noticia/ciencia-e-saude/2017/07/22/interna_ciencia_saude,611649/plastico-mundo-produziu-8-3-bi-de-toneladas-em-65-anos-e-reciclou-so.shtml. Acesso em: 17 abr. 2022.
SOUZA, F. R. A. de; OLIVEIRA, J. S. T. de; SILVA, D. P. de, OLIVEIRA, M. G. de; NEVES, D. D.; SILVA, W. E. da; STAMFORD, T. C. M. Biopolímeros na indústria de alimentos: do aproveitamento de resíduos agroindustriais a produção de biopolímeros. Avanços em Ciência e Tecnologia de Alimentos, 1ª edição. Editora Cientifíca, 2021, p. 370-388, v. 4, cap. 24. Disponível em: https://www.editoracientifica.org/articles/code/210303531. Acesso em: 02 mar. 2022.
STRACK, Lariane. Atividade antimicrobiana de biocompostos produzidos por bactérias ácido láticas via fermentação submersa usando subprodutos da agroindústria. 2021. 74f. Dissertação (Mestrado em Ciência e Tecnologia de Alimentos) – Universidade de Passo Fundo, Passo Fundo, RS, 2021. Disponível em: https://docs.google.com/viewerng/viewer?url=http://tede.upf.br//jspui/bitstream/tede/2058/2/2021LarianeStrack.pdf. Acesso em: 14 mai. 2022.
TAHERZADEH, M. J.; KARIMI, K. Acid-based hydrolysis processes for ethanol from lignocellulosic materials: A review. BioResources. Isfahan, Irã, v. 2, n .3, p. 472-499, 2007. Disponível em: https://bioresources.cnr.ncsu.edu/BioRes_02/BioRes_02_3_472_499_Taherzadeh_K_BioEthanol_Review.pdf. Acesso em: 26 abr. 2022.
TAHERZADEH, M. J.; KARIMI, K. Pretreatment of Lignocellulosic Wastes to Improve Ethanol and Biogas Production: A Review. International Journal of Molecular Sciences, n.9, p. 1621–1651, 2008. Disponível em: https://doi.org/10.3390/ijms9091621. Acesso em: 26 abr. 2022.
VARGAS, André Luiz Vasconcellos. Produção de ácido lático e de biomassa de Lactobacillus plantarum CCT 0580, utilizando melaço da cana de açúcar (Saccharum sp). 2016. 97f. Dissertação (Mestrado em Tecnologia Ambiental) – Universidade Federal Fluminense, Volta Redonda, RJ 2016. Disponível em: http://pgta.uff.br/wp-content/uploads/sites/249/2020/06/PGTA-013.Andre-Luiz-Vasconcellos-Vargas.pdf. Acesso em: 22 abr. 2022.
VENTURA, Ricardo. Quantificação do ácido lático na fermentação etanólica como parâmetro de monitoramento do processo. 2007. 92f. Dissertação (Mestrado em Ciências Biológicas) – Universidade Estadual Paulista “Júlio de Mesquita Filho”, Instituto de Biociências de Rio Claro, Rio Claro, SP, 2007. Disponível em: http://hdl.handle.net/11449/94999. Acesso em: 24 abr. 2022.
WOICIECHOWSKI, A. L.; CARVALHO, J. C.; SPIER, M. R.; HABU, S.; YAMAGUISHI, C. T.; GHIGGI, V., SOCCOL, C. R. Emprego de resíduos agroindustriais em bioprocessos alimentares. Biotecnologia de Alimentos. Editora Atheneu, 2013, p. 143-171, v.12, cap. 6. Disponível em: https://www.academia.edu/23279482/Emprego_de_Res%C3%ADduos_Agroindustriais_em_Bioprocessos_Alimentares. Acesso em: 24 abr. 2022.
WOICIECHOWSKI, A. L.; NITSCHE, S.; PANDEY, A.; SOCCOL, C. R. Acid and enzymatic hydrolysis to recover reducing sugars from cassava bagasse: an Economic Study. Brazilian Archives of Biology and Technology, Curitiba, PR, v. 45, n. 3, p.393-400, 2002. Disponível em: https://www.academia.edu/12420368/Acid_and_enzymatic_hydrolysis_to_recover_reducing_sugars_from_cassava_bagasse_an_economic_study. Acesso em: 26 abr. 2022.
WWF – World Wide Fund for Nature. Brasil é o 4º país do mundo que mais gera lixo plástico. 2019. Disponível em: https://www.wwf.org.br/?70222/Brasil-e-o-4-pais-do-mundo-que-mais-gera-lixo-plastico. Acesso em: 12 mar. 2022.
ZAMORA, A. M. et al. ATLAS DO PLÁSTICO – Fatos e números sobre o mundo dos polímeros sintéticos, 1ª edição. Rio de Janeiro: Fundação Heinrich Böll, 2020, p.1-62. Disponível em: https://br.boell.org/pt-br/2020/11/29/atlas-do-plastico. Acesso em: 24 abr. 2022.
[1] Graduação em Engenharia Química. ORCID: 0000-0002-7758-2710.
[2] Graduação em Engenharia Química. ORCID: 0000-0002-5376-2485.
[3] Graduação em Engenharia Química. ORCID: 0000-0002-8201-6350.
[4] Orientador. Doutorado. ORCID: 0000-0001-6262-1177.
Enviado: Agosto, 2022.
Aprovado: Setembro, 2022.