ARTIGO ORIGINAL
ABREU, Luiz Cláudio Santos [1]
ABREU, Luiz Cláudio Santos. Cuidados De Enfermagem No Tratamento Da Hanseniase. Revista Científica Multidisciplinar Núcleo do Conhecimento. Ano 03, Ed. 11, Vol. 06, pp. 49-70 Novembro de 2018. ISSN:2448-0959
RESUMO
A hanseníase é uma doença infecciosa de evolução prolongada causada pelo bacilo denominado Mycobacterium leprae ou bacilo de Hansen, descoberto em 1873 pelo cientista norueguês Gerhard Armauer Hansen, morfologicamente muito semelhante ao bacilo causador da tuberculose. Como não se transmite com facilidade, não são registradas grandes epidemias. No campo, a OMS recomenda, para fins terapêuticos, a classificação operacional baseada no número de lesões cutâneas. A baciloscopia é o exame complementar mais útil no diagnóstico. O tratamento da hanseníase compreende: quimioterapia específica, supressão dos surtos reacionais, prevenção de incapacidades físicas, reabilitação física e psicossocial. A poliquimioterapia com rifampicina, dapsona e clofazimina revelou-se muito eficaz e a perspectiva de controle da doença no Brasil é real no curto prazo. Com base nos dados relacionados a Hanseníase, serão investigados os cuidados inerentes ao profissional de enfermagem no que se refere ao tratamento da Hanseníase.
Palavras- chave: Enfermagem, Tratamento, Hanseníase.
INTRODUÇÃO
A hanseníase chegou ao Brasil na época do descobrimento, espalhou-se e permanece até hoje, sendo considerado um dos mais sérios problemas da saúde pública no país. Ocupamos o 1º lugar da América Latina, com um número estimado de doentes entre 250 e 500 mil casos, que nos coloca também em 4º lugar do mundo em número de doentes.
Há no mundo todo mais de dez milhões de pessoas com hanseníase. Relativamente pouco contagiante, a forma de contágio mais comum é a direta (pessoa a pessoa), entre outras vias, por descargas nasais infectadas. Existe maior predisposição na infância, em condições sanitárias deficientes e de subnutrição. (ASSIS, 1998).
A hanseníase é uma doença sistêmica, dermatoneurológica, infectocontagiosa crônica que pode apresentar alterações imunológicas e também reumatológicas, como resultado da interação parasita-hospedeiro. É encontrada apenas no homem e a transmissão ocorre pelo contágio interpessoal. Apresenta sinais e sintomas clínico-neurológicos específicos característicos de cada uma das formas clínicas em que pode se apresentar esta enfermidade.
1. CONCEITO
A hanseníase é uma doença crônica granulamatosa proveniente de infecção causada pelo Micobacterium Leprae. Doença infecto-contagiosa, crônica, curável, causada pelo bacilo de Hansen. Esse bacilo é capaz de infectar grande número de pessoas (alta infectividade), mas poucos adoecem, (baixa patogenicidade). O poder munogênico do bacilo é responsável pelo alto potencial incapacitante da hanseníase.
Definição de caso – Um caso de hanseníase, definido pela Organização Mundial de Saúde-OMS, é uma pessoa que apresenta um ou mais dos critérios listados a seguir, com ou sem história epidemiológica e que requer tratamento uimioterápico específico: leões de pele com alteração de sensibilidade; espessamento de nervo(s) periférico(s), acompanhado de alteração de sensibilidade; e baciloscopia positiva para bacilo de Hansen. Obs.: a baciloscopia negativa não afasta o diagnóstico de hanseníase. Os aspectos morfológicos das lesões cutâneas e classificação clínica nas quatro formas abaixo devem ser utilizados por profissionais especializados e em investigação científica.
- Sinonímia – Mal de Hansen; antigamente a doença era conhecida como lepra.
- Agente etiológico – Bacilo álcool-ácido resistente, intracelular obrigatório, denominado bacilo de Hansen ou Mycobacterium leprae.
- Reservatório – O homem é reconhecido como única fonte de infecção, embora tenham sido identificados animais naturalmente infectados.
- Modo de Transmissão – Contato íntimo e prolongado com pacientes bacilíferos não tratados.
- Período de Incubação – Em média 5 anos, podendo ir de meses a mais de 10 anos.
- Período de Transmissibilidade – Os pacientes multibacilares podem transmitir hanseníse, antes de iniciar o tratamento específico. A primeira dose de rifampicina é capaz de eliminar as cepas viáveis do bacilo de Hansen em até 99,99% da carga bacilar de um indivíduo.
- Complicações – Quando o diagnóstico é precoce e o tratamento quimioterápico do paciente é adequadamente seguido, com orientações de auto-cuidado para revenir incapacidades, geralmente, a hanseníase não deixa seqüelas e ou complicações. Um grupo de pacientes pode desenvolver episódios reacionais, que são intercorrências da reação imunológica do hospedeiro. Podem surgir durante o tratamento específico, ou após a alta do paciente. Nesse último caso, não requer a reintrodução da poliquimioterapia. As reações (ou episódios reacionais) são agrupadas em 2 tipos:
O Tipo 1: também chamado reação reversa. Ocorre mais frequentemente em pacientes com hanseníase tuberculóide e dimorfa. Caracteriza-se por eritema e edema das lesões e/ou espessamento de nervos com dor à palpação dos mesmos (neurite). A neurite pode evoluir sem dor (neurite silenciosa). É tratado com Prednisona, VO, 1-2mg/kg/dia, com redução em intervalos fixos, conforme avaliação clínica. São também indicação de uso de corticosteroides a rinite / iridocinclite e a orquite (consultar o Guia para o Controle da Hanseníase, da Coordenação Nacional de Dermatologia Sanitária/Ministério da Saúde).
O Tipo 2 ou eritema nodoso: os pacientes com hanseníase virchowiana são os mais acometidos. Caracteriza-se por nódulos eritematosos, dolorosos, em qualquer parte do corpo. Pode evoluir com neurite. Trata-se com talidomida, VO, na dose de 100 a 400mg/dia, somente em paciente do sexo masculino (é proibido o uso em mulheres em idade fértil, devido à possibilidade de ocorrência de teratogeinicidade); ou prednisona, VO, 1-2mg/kg/ dia. A redução também é feita em intervalos fixos, após avaliação clínica.
-
- Diagnóstico – Clínico, baseado na definição de caso. A baciloscopia e a histopatologia podem ser úteis como apoio diagnóstico.
- Diagnóstico Diferencial – Eczemátide, nevo acrômico, pitiríase versicolor, vitiligo, pitiríase rósea de Gilbert, eritema polimorfo, eritema nodoso, granuloma, anular, eritema anular, lúpus, farmacodermias, pelagra, sífilis, alopécia areata, sarcoidose, tuberculose, xantomas, esclerodermias.
1.1 SITUAÇÃO ATUAL DA ENDEMIA
Os países endêmicos para hanseníase adotam programas de controle verticais, modelo assistencial predominante no Brasil há muitos anos. A integração do programa de controle da hanseníase aos serviços de saúde geral tornou-se uma realidade em alguns locais. As implicações desta ação são imprevisíveis em longo prazo, já que a eliminação da hanseníase como problema de saúde pública depende mais de questões operacionais do que de fatos científicos. (MINISTÉRIO DA SAÚDE, 2001)
Os riscos de transmissão e recidiva, assim como, o período de incubação longo da doença são desafios para o controle dela. O diagnóstico precoce é fundamental para a interrupção da transmissão, visto que a doença ocorre sorrateiramente devido ao crescimento lento dos bacilos, evolução insidiosa do comprometimento neural e o preconceito em relação aos portadores desta enfermidade. (MINISTÉRIO DA SAÚDE, 2001)
A prevalência oculta, número de casos de hanseníase não detectados em regiões endêmicas, pode aumentar a detecção de casos novos. A transmissão silenciosa da doença poderá reverter a “eliminação” recém-adquirida em uma situação de alta endemicidade. Os profissionais no campo não possuem instrumentos adequados ao diagnóstico precoce, para monitorar a eficácia da quimioterapia, a incidência de recidivas, identificação de pacientes com alto risco de desenvolver reações após o tratamento e, até mesmo, controlar pessoas sadias que possuem alto risco de desenvolvimento de formas graves de hanseníase. (MINISTÉRIO DA SAÚDE, 2001)
Um teste laboratorial simples para auxiliar ao diagnóstico da hanseníase, evitar erros de classificação e, portanto, administração de terapia inadequada à real forma clínica apresentada pelo paciente, bem como, controlar indivíduos sadios que possuem alto risco do desenvolvimento de formas graves de hanseníase é fundamental nos países endêmicos. (MINISTÉRIO DA SAÚDE, 2001).
Hoje, no período da Idade Moderna, foi visto o interesse pelo controle epidemiológico da hanseníase. A Coordenação do Programa Nacional de Controle da Hanseníase (PNCH) assume como objetivo de saúde pública o controle da doença (WHO, 2008) e privilegia, neste aspecto, o acompanhamento epidemiológico por meio do coeficiente de detecção de casos novos, optando pela sua apresentação por 100.000 habitantes para facilitar a comparação com outros eventos. (BRASIL, 2008).
1.2 ATIVIDADES ADMINISTRATIVAS
NO DIAGNÓSTICO
Na estimativa do número de exames dermatoneurológicos para diagnóstico, utilizam-se os seguintes cálculos:
-
- Estima-se o número de consultas de primeira vez, que corresponde a 20% da população da área de abrangência da unidade de saúde, município ou estado;
- Calcula-se que 10 % das consultas de primeira vez são de portadores de dermatoses e neuropatias periféricas;
- Total de casos a ser diagnosticado deverá corresponder a 100% dos casos novos esperados, segundo estudo de tendência da hanseníase da unidade federada;
- Número de casos novos a serem detectados no ano deve ser estimado utilizando-se modelos de predição que retratam a tendência atual de endemia em cada unidade federada. Com base em série histórica dos coeficientes de detecção, deve-se estimar o modelo estatístico mais adequado para cada estado. Recomenda-se a avaliação contínua dos modelos propostos, através da incorporação de coeficientes mais recentes, bem como análise da confiabilidade das estimativas. (ASSIS, 1998).
1.3 NO CONTROLE
-
- Exames dermatoneurológicos;
- Consulta de enfermagem;
- Atendimento de enfermagem;
- Consulta médica.
1.4 NA VIGILÂNCIA DE CONTATOS
Supondo que a unidade de saúde detecte 120 novos casos num ano, e admitindo que cada paciente convive no domicílio, em média, com 4 pessoas, estima-se o número de contatos a serem examinados e vacinados, multiplicando-se o número de casos novos por 4. (ASSIS, 1998).
Exemplo: 120 casos novos detectados X 4 contatos intradomiciliares = 480 contatos a serem examinados.
1.5 SUPRIMENTO DE MEDICAMENTOS
Fazendo previsão de medicamento:
-
- Consultar normas, esquemas terapêuticos e dados epidemiológicos;
- Fazer cálculos de necessidade conforme normas;
- Verificar estoque existente, consumo médio mensal e prazos de validade;
- Fazer cálculos para solicitação;
- Encaminhar cálculos com a solicitação para setor responsável em formulário padrão;
- Para previsão de cartelas Multibacilar e Paucibacilar ter conhecimento do total geral dos casos e do número de pacientes em abandono;
- Para os casos que apresentam efeitos colaterais, que não podem utilizar o tratamento padrão do PQT (cartela), programar de acordo com o Guia para Utilização do Medicamento e Imunobiológicos na Área de Hanseníase/MS;
- Para os medicamentos anti-reacionais conhecer o número de pacientes que fizeram reação pós-tratamento; os medicamentos utilizados para esse tratamento; número de pacientes que fizeram reação pós-alta. (ASSIS, 1998).
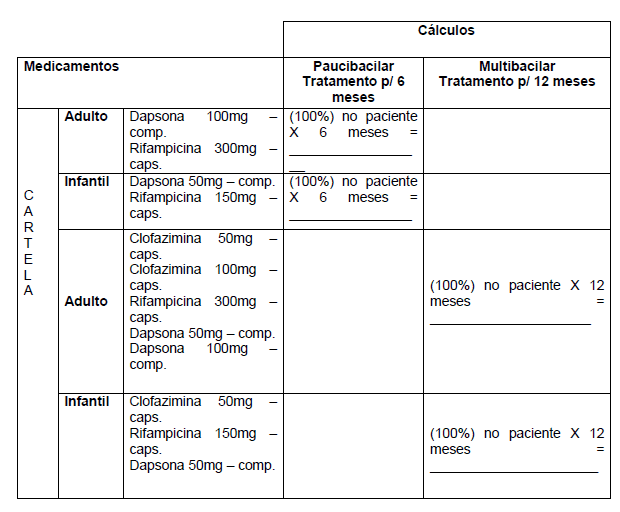
1.6 MATRIZ PROGRAMÁTICA PARA CÁLCULO DE MEDICAMENTOS
A) Esquema padrão – Cálculo por Cortelas
C) Esquema alternativos
2. DADOS EPIDEMIOLÓGICOS
A vigilância epidemiológica, de acordo com o guia de Vigilância Epidemiológica do Centro Nacional de Epidemiologia do Ministério da Saúde (CENEPI/MS) “corresponde a um conjunto de ações que proporcionam o conhecimento, a detecção ou a prevenção de qualquer mudança nos fatores determinantes e condicionantes de saúde individual ou coletiva, com a finalidade de recomendar e adotar medidas de prevenção e controle das doenças e agravos”. (BARROS, 1994).
Ela objetiva embasar tecnicamente, de forma permanente, a execução de ações de controla de doenças e agravos, disponibilizando para tanto, informações atualizadas sobre a ocorrência dessas doenças, bem como dos seus fatores condicionantes em uma área geográfica ou população determinada. (BARROS, 1994).
Segundo BARROS, 1994, a vigilância epidemiológica tem funções intercomplementares que são operacionalizadas através de um ciclo completo de atividades específicas e inter-relacionadas, que devem, necessariamente, ser desenvolvidas de modo contínuo. São elas:
Obter informações atualizadas sobre a doença e sobre o seu comportamento epidemiológico, numa determinada população de uma determinada área geográfica, para que as medidas de intervenção pertinentes possam ser desencadeadas com oportunidade e eficácia. Para isso, desenvolve as seguintes atividades:
- Coleta de dados sobre a doença;
- Processamento de dados;
- Análise e interpretação dos dados: informações sobre o comportamento epidemiológico da doença;
Orientar e avaliar as atividades de controle da doença. A partir das informações sobre a doença e sobre o seu comportamento epidemiológico desenvolve e/ou orienta as seguintes atividades:
- Recomendação de atividades de controle;
- Promoção das atividades de controle;
- Avaliação das atividades de controle – informações sobre essas atividades.
- Divulgar informações sobre a doença e seu comportamento epidemiológico e sobre as atividades de controle para a população em geral e para os responsáveis pelas atividades de controle. (BARROS, 1994).
A vigilância epidemiológica da hanseníase é realizada através de um conjunto de atividades que fornecem informações sobre a doença e sobre o seu comportamento epidemiológico, com a finalidade de recomendar, executar e avaliar as atividades de controle realizadas, tanto para os responsáveis por essas atividades, como para a população em geral. (BARROS, 1994).
As atividades de controle da hanseníase visam a descoberta precoce de todos de hanseníase existentes na comunidade e o seu tratamento.
O objetivo dessas atividades é controlar a doença, reduzindo a sua prevalência, a menos de um caso em 10.000 habitantes, quebrando assim a cadeia epidemiológica da doença e a produção de novos casos. (BARROS, 1994).
A descoberta de casos de hanseníase implica a busca de portadores da doença não tratados anteriormente. Essa busca inclui uma série de atividades essenciais na estratégia de controle da doença. A detecção precoce de casos é fundamental para prevenir as incapacidades causadas pela doença e para controlar os focos de infecção, contribuindo para a eliminação da hanseníase como problema de saúde pública. (BARROS, 1994).
O tratamento integral de hanseníase, como visto anteriormente, é constituído pelo:
-
-
- Tratamento PQT (Tratamento Poliquimioterápico) que mata o bacilo, previne as incapacidades e deformidades provocadas pela doença e cura o doente;
- Acompanhamento do caso, visando diagnosticar e tratar precocemente eventuais neurites, efeitos colaterais dos medicamentos e estados reacionais da doença, bem como manter a regularidade do tratamento para que o paciente possa ter alta no tempo previsto; (BARROS, 1994).
- Prevenção de incapacidades, através de técnicas simples, nas unidades de saúde, e de orientação ao paciente para a realização de auto cuidados. É de fundamental importância envolver o paciente e familiares na adesão ao tratamento, para que estes possam ser responsáveis, tanto quanto a equipe de saúde, pelo tratamento e cura da doença. (BARROS, 1994).
3. BRASIL
O Brasil registrou no final de 2005 um coeficiente de prevalência de hanseníase de 1,48 casos/10.000 habitantes (27.313 casos em curso de tratamento em dezembro de 2005) e um coeficiente de detecção de casos novos de 2,09/10.000 habitantes (38.410 casos novos em dezembro de 2005). Apesar da redução na taxa de prevalência observada no período compreendido entre 1985 e 2005 de 19 para 1,48 doentes em cada 10.000 habitantes, a hanseníase ainda constitui um problema de saúde pública no Brasil, o que exige um plano de aceleração e de intensificação das ações de eliminação e de vigilância resolutiva e contínua. (BARROS, 1994).
O Brasil mantém, nas ultimas décadas, a situação mais desfavorável da hanseníase na América e o segundo maior número casos novos (CN) do mundo.
Apesar da redução do grau II de incapacidade física nos CN, de 15,9 para 6%, a partir da introdução do PQT (1986), cerca de três mil pessoas ainda são diagnosticadas com deformidade física por hanseníase a cada ano no país.
A cobertura de 34% das unidades básicas de saúde oferecendo diagnóstico e tratamento é razoável (14.130/41.105)**, mas sabe-se que a maioria delas não oferece cuidados de prevenção e reabilitação adequados. (MINISTÉRIO DA SAÚDE, 1994)
Ainda que o País registre um importante decréscimo nas taxas de prevalência e de detecção de casos novos de hanseníase, os níveis de magnitude da doença, segundo as regiões geográficas, demonstram a necessidade de se dar continuidade à execução de atividades que impactem a transmissão da doença, de modo a atingir taxas inferiores a 1 caso/10.000 habitantes em cada município. (MINISTÉRIO DA SAÚDE, 1994)
No atual cenário brasileiro e mundial há uma tendência das curvas de detecção ultrapassarem as de prevalência, indicando menor número de casos acumulados (prevalência) do que de casos incidentes, configurando um paradoxo conceitual do ponto de vista epidemiológico, particularmente para uma doença de evolução crônica.(MINISTÉRIO DA SAÚDE, 1994)
O Programa Nacional de Hanseníase por meio do Plano de Eliminação (PEL) tem como objetivo geral atingir a meta de eliminação da hanseníase como problema de saúde pública no Brasil, ou seja, reduzir a taxa de prevalência a < 1 caso/10.000 habitantes até o ano 2000. O modelo lógico adotado atualmente é: 1. diagnosticar e tratar com Poliquimioterapia (PQT/OMS) todos os casos novos esperados; 2. diagnosticar precocemente a hanseníase de maneira que 90% dos casos novos sejam diagnosticados antes do aparecimento de deformidades físicas; 3. dar alta por cura a 80% dos casos que iniciaram tratamento; 4. reduzir em 15% a 20% ao ano a taxa de prevalência. Para a correta execução dos planos, o Ministério da Saúde, em 1996, tipificou 755 municípios prioritários e destes, 119 estão localizados na Amazônia Legal. De forma a motivar e estimular o cumprimento da meta do plano o Ministério da Saúde alocou no ano de 1997 uma quantia superior a seis milhões de reais por meio de convênio para 222 municípios prioritários de todas as regiões do país (MS, 1999).
-
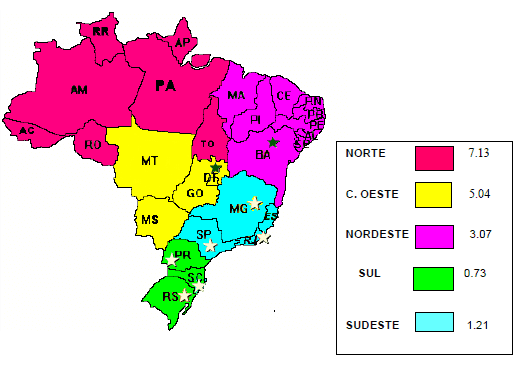
- Mapa da situação da hanseníase no Brasil (Coeficiente de detecção de casos novos em cada 10.000 hab.).
4. AMAZONAS – MUNICÍPIO
Em 1935, teve início o processo de controle da hanseníase, cujo diagnóstico e tratamento foram centralizados até 1955. Atualmente, todos os 62 municípios fazem o diagnóstico e realizam o tratamento poliquimioterápico de acordo com as orientações preconizadas pela Organização Mundial da Saúde (PQT/OMS) – sistemática adotada para todos os pacientes a partir de 1982. (BARROS, 1994).
De 674 unidades básicas, 202 (29,97%) desenvolvem essas atividades. No município de Manaus há um Centro de Referência nacional e estadual na Fundação Alfredo da Mata. (BARROS, 1994).
A partir de 2004 foi adotado o Sistema de Informações de Agravos de Notificação (Sinan), descentralizado para todos os municípios. Nos últimos dois anos (2002/2003), 2.711 profissionais foram treinados.
As principais ações executadas pelo estado com vistas à eliminação da hanseníase são supervisão, treinamento e campanhas educativas. Nenhum município apresentou notificação negativa de casos de hanseníase nos últimos cinco anos. (MINISTÉRIO DA SAÚDE, 2004).
Em 2003, foram registrados 1.127 novos casos. Destes, 132 (11,71%) acometiam menores de 15 anos, 70 (6,12%) apresentavam no momento do diagnóstico incapacidade física severa e 519 (46,05%) formas avançadas da doença.
Mais de 75% da população do estado vivem em municípios com prevalência superior a 5 casos/10.000 habitantes, quando a taxa ideal é menos de 1 caso/10.000 habitantes. (MINISTÉRIO DA SAÚDE, 2004).
COEFICIENTES DE PREVALÊNCIA E DETECÇÃO DE HANSENÍASE AMAZONAS 1994-2003
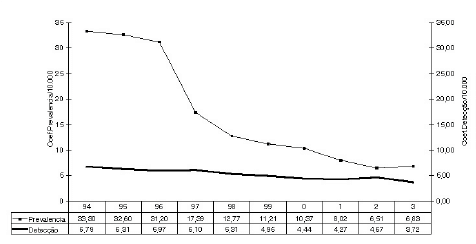
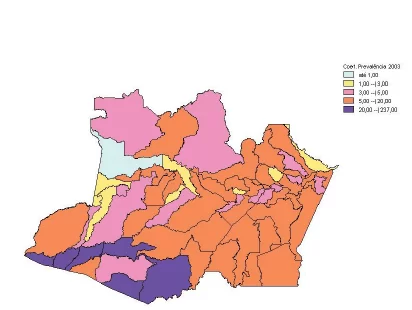
5. RESULTADOS ESPERADOS DO DESENVOLVIMENTO DO PLANO NACIONAL DE ELIMINAÇÃO DA HANSENÍASE / MINISTÉRIO DA SAÚDE 2006- 2010.
-
- Prevalência < 1 caso por 10.000 habitantes, em nível nacional.
- Manter prevalência < 1 caso por 10.000 habitantes: Rio Grande do Sul, Santa Catarina, São Paulo, Minas Gerais, Distrito Federal, Rio Grande do Norte, Rio de Janeiro e Alagoas.
- Atingir a prevalência < 1 caso por 10.000 habitantes: Paraná, Bahia, Mato Grosso do Sul, Paraíba, Amazonas, Ceará e Sergipe.
- Prevalência menos de < 2 casos por 10.000 habitantes: Amapá, Piauí, Pernambuco, Goiás, Espírito Santo e Acre.
- Prevalência menos de < 4 casos por 10.000 habitantes: Roraima, Pará, Tocantins, Rondônia, Maranhão, Mato Grosso. (MINISTÉRIO DA SAÚDE, 2004).
6. PRINCIPAIS DESAFIOS
Continuar o avanço em direção à meta de prevalência de menos de um caso a cada 10.000 habitantes nos estados e municípios que ainda não a alcançaram, assim como o monitoramento da ocorrência dos casos novos:
- Garantir o desenvolvimento de ações que favoreçam o diagnóstico precoce na faixa etária de menores de 15 anos;
- Manter a qualidade dos serviços nos sistemas integrados de saúde e em situações de baixa endemicidade;
- Fortalecer a vigilância epidemiológica, a logística de abastecimento de medicamentos, o desenvolvimento de capacidade orientada ao trabalho para os profissionais de saúde em geral e uma rede eficiente de referência e contra-referência;
- Avaliar a magnitude de carga de incapacidade resultante da hanseníase e desenvolver ferramentas e procedimentos adequados para lidar, nos serviços integrados, com as questões relacionadas às incapacidades e deficiências;
- Expandir a cobertura das atividades de eliminação da hanseníase em comunidades e populações especiais;
- Diminuir ainda mais o estigma e a discriminação contra as pessoas afetadas pela hanseníase e contra suas famílias;
- Desenvolver parcerias eficazes baseadas em confiança mútua, igualdade e unidade de propósito;
- Assegurar o nível apropriado de prioridade para financiamento pelo Governo Federal aos estados e municípios nas ações de eliminação da hanseníase;
- Apoiar a iniciativa do Conselho Nacional de Saúde (CNS) em estabelecer financiamento específico per capita para acelerar a eliminação da doença como problema de saúde pública;
- Contribuir para a inclusão do tema hanseníase na agenda dos Direitos Humanos;
- Participar ativamente do desenvolvimento do Pacto pela Vida, promovendo e acompanhando o alcance das metas. (BARROS, 1994).
7. ATRIBUIÇÕES DA EQUIPE DE ENFERMAGEM
Planejamento / Programação do cuidado
Atribuições do médico, do enfermeiro, do auxiliar de enfermagem e do agente comunitário de saúde:
-
-
-
-
- Planejar ações de assistência e controle do paciente, família e comunidade com base no levantamento epidemiológico e operacional;
- Participar de estudos e levantamentos que identifiquem os determinantes dos processo saúde/doença de grupos populacionais, famílias e indivíduos;
- Estabelecer relações entre as condições de vida e os problemas de saúde identificados estabelecendo prioridades entre tais problemas;
- Identificar a diversidade cultural com que a população enfrenta seus problemas de saúde, destacando as que representam riscos;
- Sistematizar e interpretar informações, definindo as propostas de intervenção;
- Realizar a programação de atividades, observando as normas vigentes;
- Prever o material necessário para a prestação do cuidado a ser realizado. (BARROS, 1994).
-
-
-
Está estabelecido na Portaria GM 648/2006, do Ministério da Saúde, que é papel do enfermeiro não apenas educar e prevenir, mas também participar do tratamento através da Consulta de Enfermagem, a solicitação de exames complementares e a prescrição de medicamentos, conforme protocolos estabelecidos, nas disposições legais da profissão e outras normativas técnicas estabelecidas pelo Ministério da Saúde, nos quais o enfermeiro participa do planejamento, gerenciamento, na coordenação e avaliação das ações que serão desenvolvidas pelos agentes comunitários de saúde. (ALBERICI, 2011)
Em todas essas áreas de atuação do enfermeiro, entendemos que o trabalho deve se dar de forma integrada com os demais membros da equipe multiprofissional da unidade de saúde, respeitando-se um princípio básico da integralidade da assistência. (PEDRAZZANI, 1995).
O cuidar desses pacientes envolve objetivos, como avaliar, confortar, ajudar, favorecer, promover, restabelecer, restaurar e etc. Esse cuidado almeja a cura, mas independe de sua consecução.
Deve ser um cuidado permanente e holístico, envolvendo os vários aspectos da vida do paciente. Por sua vez, o cuidar na enfermagem, tem como finalidade a prioridade em aliviar o sofrimento humano, manter a dignidade e facilitar meios para manejar com as crises e com as experiências do viver e do morrer, podendo ser considerado um cuidado ético (WALDOW, 2001).
O enfermeiro tem um papel de fundamental importância neste controle, e um deles é participar da vigilância epidemiológica, que é um conjunto de ações que proporcionam o conhecimento, a detecção ou a prevenção de qualquer mudança nos fatores determinantes e condicionantes de saúde individual ou coletiva, com a finalidade de recomendar e adotar medidas de prevenção e controle das doenças (BRASIL, 2002).
A vigilância epidemiológica da hanseníase, segundo o Ministério da Saúde, é realizada através de um conjunto de atividades que fornecem informações sobre a doença e sobre o seu comportamento epidemiológico, com a finalidade de recomendar, executar e avaliar as atividades de controle da hanseníase. Visa, também, divulgar informações sobre a doença e sobre as atividades de controle realizadas, tanto para os responsáveis por essas atividades, como para a população em geral (BRASIL, 2002)
8. CONSIDERAÇÕES FINAIS
Foi concluído que através da prevenção, diagnóstico precoce e uso continuo do medicamento, 99% dos bacilos são eliminados e a chance de contaminação é nula, evitando-se assim a propagação da hanseníase. Para um diagnóstico preciso e um tratamento eficaz, necessita-se que os profissionais de saúde estejam bem preparados, teórica e na prática também. Mas acima de tudo, que estejam predispostos a buscarem recursos para que toda a área de saúde sinta-se gratificada em cumprir seu dever. Segundo Brasil. Ministério da Saúde (1989), a hanseníase é compreendida como um problema de saúde pública em nosso país e requer adoção de ações necessárias para o seu controle. Essas medidas devem ser compartilhadas por todos os profissionais de saúde, em todos os níveis de atenção. Dentre as ações de controle são prioritárias o diagnóstico precoce e o tratamento adequado dos pacientes.
A incorporação deste instrumento permitirá que os profissionais possam seguir corretamente todas as medidas propostas e contribuirá efetivamente para a qualificação dos mesmos. Espera-se que a adoção de um protocolo de assistência aos portadores de hanseníase ofereça subsídios para a sistematização dessa assistência em nível de atenção básica, capacitando a equipe para identificar os casos suspeitos, diagnosticá-los corretamente, realizando o tratamento adequado, dessa forma, sendo de extrema importância o acompanhamento da evolução do tratamento.
Avaliar de maneira eficaz para a avaliação e diagnóstico da doença, prescrição de cuidados, e a criação de um sistema de informação essencial para o tratamento e evolução da assistência. Pretende-se a troca de informações entre todos os profissionais que atuam diretamente no atendimento aos portadores de hanseníase, incluindo a efetivação de um sistema de referência e contra- referência, viabilizando a descentralização da assistência a essa clientela, conforme proposto pelo Ministério da Saúde, sem prejudicar a qualidade do atendimento.
REFERÊNCIAS BIBLIOGRÁFICAS
ALBERICI, Priscila de Souza. Revista UNIABEU Belford Roxo V.4 Número 7 Mar. – Ago. 2011.
ASSIS, M. Educação em saúde e qualidade de vida: para além dos modelos, busca da comunicação. Rio de Janeiro: UER: MS, 1998.
BARROS, E. O controle social e o processo de descentralização dos serviços de saúde. In: Incentivo à participação popular e o controle social no SUS: textos técnicos para conselheiros de saúde. Brasília: Ministério da saúde, 1994.
BORDENAVE, J.E.D. Alguns fatores pedagógicos. In: Capacitação pedagógica para o instrutor/supervisor: área de saúde. Brasília: Ministério da saúde, 1994.
BRASIL. Lei n. 8.142, de 28 de dezembro de 1990. Dispõe sobre a participação da comunidade na gestão do sistema Único de saúde (SUS) e sobre transferências intergovernamentais de recursos financeiros na área da saúde e dá outras providências. [S.I.: s.n], [1990].
BRASIL. Ministério da saúde. Ações de informações, educação e comunicação: perspectiva para uma avaliação. Brasília: Ministério da saúde, 1998.
_____________. Ministério da saúde. Hanseníase – Atividade de controle & Manual de Procedimentos. Brasília, 2001. (mimeo).
_____________.Guia para Controle da Hanseníase. Cadernos de Atenção Básica n 10. Brasília: MS. 2002; 1ª ed.
Guia de transferência para o controle social: manual do conselheiro. Brasília: IEC, 1994.
Guia para implantar / implementar as atividades de controle da hanseníase nos planos estaduais e municipais de saúde. Brasília: Secretaria de Política de Saúde, Ministério da Saúde, 1999.
MINISTÉRIO DA SAÚDE. Secretaria Executiva. Subsecretaria de Planejamento e Orçamento. Portaria nº 398, de 22 de fevereiro de 2006. Divulga Pacto. Organização Mundial da Saúde. Estratégia Global para Aliviar a Carga de Hanseníase e Manter as Atividades de Controle da Hanseníase 2006-2010 (document OMS/CDS/CPE/CEE/2005.53). Genebra, 2005. Disponível em: <http://www.who.int/lep/Reports/GlobalStrategy-PDF-verison.pdf> e <http://www.paho.org/Portuguese/AD/DCP/CD/lep-who-global-strategy.htm>.
WALDOW VR. Cuidado Humano: o resgate necessário. Porto Alegre: Sagra; 2001.
[1] Graduado em Enfermagem. Pós-grauduado em UTI.
Enviado: Janeiro, 2018
Aprovado: Novembro, 2018