ARTIGO ORIGINAL
CASTILLO, Naiara Campos Paixão de [1], RÊGO, Aljerry Dias do [2], SILVA, Dyone Karla Barbosa da [3], GONÇALVES, Felipe Noujeimi [4], BATISTA, Thayna Almeida [5], LIMA, Naiara Lorrani Silva de [6], TEIXEIRA, Angela Santana [7]
CASTILLO, Naiara Campos Paixão de. Et al. Resistência Bacteriana em Uroculturas de mulheres em Macapá: comparação dos resultados ambulatoriais e hospitalares. Revista Científica Multidisciplinar Núcleo do Conhecimento. Ano 04, Ed. 10, Vol. 13, pp. 128-165. Outubro de 2019. ISSN: 2448-0959, Link de acesso: https://www.nucleodoconhecimento.com.br/saude/resistencia-bacteriana
RESUMO
O presente estudo tem como objetivo conhecer quais bactérias são mais comuns na urocultura de mulheres maiores de 18 anos na cidade de Macapá, assim como os antibióticos a que apresentam maior resistência, através da análise de dados fornecidos por dois laboratórios particulares, um utilizando metodologia manual e com amostras de mulheres de regime ambulatorial e outro utilizando metodologia automatizada e dados de pacientes hospitalizadas; com o intuito de melhorar a qualidade da assistência médico-hospitalar prestada às pacientes que se confrontam com sintomas e recorrência da infecção urinária, além de dispor literatura de uma atualizada para consulta de outros pesquisadores que se proponham a aprofundar o tema.
Palavras-chave: infecção urinária, urocultura, resistência bacteriana.
INTRODUÇÃO
A infecção do trato urinário (ITU) é definida como o crescimento e multiplicação de bactérias dentro do trato urinário (BAUMGATEN, 2011), e constitui uma das principais doenças que acometem mulheres em idade reprodutiva, gerando preocupação principalmente para aquelas que se encontram em situação gravídica (SANTOS, 2012).
Em categorias normais, o trato urinário é conceituado um ambiente estéril, em que o fluxo natural da urina e a apresentação de determinadas moléculas endógenas com atuação antimicrobiana conserva o sistema isento de bactérias (REU, 2013).
A ITU é uma das infecções bacterianas mais presentes em pacientes recebidos em ambulatório e uma das causas fundamentais para a prescrição de antibióticos. É conhecida como a segunda infecção mais corriqueira no ser humano, com estimação de que aconteçam cerca de 150 milhões de episódios por ano no mundo todo, ocasionando em quase oito milhões de visitas médicas bem como mais de cem mil admissões hospitalares por ano nos Estados Unidos, acarretando a 11,3 milhões de prescrições anuais e uma despesa estimada de 1,6 bilhões de dólares com tratamento (BARBERINO, 2010).
No país, as ITU são consideradas entre as mais reiteradas infecções bacterianas, incumbidas por 80 em cada 1.000 consultas médicas, além de ser uma causa significativa de morbilidade, acompanhantes a altos custos de cuidados com a saúde (BARBERINO, 2010).
Cerca de 80% das uroculturas positivas são de pacientes do sexo feminino. Além disso, é a doença urológica mais constante entre as mulheres, vindo a revelar-se em qualquer faixa etária, sendo mais predominante em três classes: crianças de até seis anos de idade, mulheres ativas sexualmente e idosas acima de 60 anos (NÓBREGA, 2015).
A predominância de ITU em indivíduos do sexo feminino intensifica com a idade, constando-se a bacteriúria existente em 10% a 15% das mulheres entre 65 a 70 anos e em 15% a 20% nas mulheres com mais de 80 anos. Por volta de 40% a 50% das mulheres retratam ao menos um episódio de ITU no decorrer da vida e 30% delas manifestam ITU recorrente (NÓBREGA, 2015).
Esta preponderância, quatro vezes maior nas mulheres deve-se às distinções anatômicas tais como: uretra pequena (medindo 3 cm a 4 cm), condiguidade entre o ânus e o introito vaginal. Tem a possibilidade de estar relacionada à prática sexual ou à instrumentação mecânica, como o cateterismo. Entre outros fatores que inclinam à ITU são: esvaziamento vesical incompleto, obstrução do trato urinário, anomalias do trato urinário, hipoestrogenismo, uso de espermicidas, história familiar de ITU em parentes de primeiro grau, do sexo feminino e história prévia de ITU (NÓBREGA, 2015).
A urina tem propriedades químicas que impedem o crescimento de bactérias. O seu pH ácido (5,5) possibilita reduzir ou inclusive refrear o desenvolvimento bacteriano, uma vez que as bactérias retratam tempo de geração reduzido em meio cujo pH encontrar-se mais perto da neutralidade. A baixa osmolaridade, a apresentação de ureia e ácidos orgânicos fracos na urina estão entre outros aspectos que colaboram no refreamento do desenvolvimento bacteriano. Contudo, o pH e a osmolaridade da urina podem apresentar alteração quando a mucosa do trato urinário sofre qualquer espécie de lesão e/ou durante a gravidez. Esse efeito é inclusive notado em pacientes com diabetes mellitus. Isso deve-se à alta concentração de glicose na urina. Nesse caso, a chance de a bactéria chegar à bexiga é maior, ocasionando em casos de ITU mais sérios (CUNHA, 2011).
A microbiota do aparelho geniturinário feminino é dinâmica e condicionada de fatores hormonais. Em caso de normalidade, é evidente a prevalência de Lactobacillus spp. Uma alteração dos níveis hormonais pode favorecer à colonização por bactérias do cólon ou até mesmo aumentar a parcela de outros organismos comensais da vagina, propiciando dessa forma o risco de infecção urinária (BRAGGIATO, 2016).
Alguns fatores genéticos podem, de igual forma, inclinar ao desenvolvimento de ITU e sua reincidência. Por exemplo, as mulheres que possuem os Antígenos Leucocitários Humanos HLA-A3 e os dos grupos sanguíneos de Lewis LE(a-b) ou LE(a+b-) tem fator de risco de ITU recorrente maior, teoricamente pelo fato da similaridade antigênica com as bactérias em assunto (REU, 2013).
Com a gravidez, traz-se alterações relevantes na fisiologia e na anatomia do aparelho geniturinário, as quais propiciam o aparecimento de infecção. Decorre-se dilatação das pelves renais e ureteres, devido à compressão deles pelo útero gravídico e à redução da atividade peristáltica fomentada pela progesterona, desencadeando a estase urinária. Os rins perdem eficácia e concentram menos a urina, limitando as propriedades antibacterianas (REU, 2013). Além do mais, o aumento das dimensões renais (1 cm), alteração da posição da bexiga (que torna-se um órgão abdominal e não pélvico), desenvolvimento da capacidade vesical (devido à redução do tônus vesical), hormônio-mediado, distensão da musculatura lisa da bexiga e ureter e progesterona-dependente favorecem o surgimento da ITU ao desencadear estase urinária (CUNHA, 2011).
Um fator considerável presente nas amostras de comunidade é que, cerca de 20% das uroculturas positivas são verificadas em gestantes, grupo em que é preciso acompanhamento clínico, isso se deve aos riscos relacionados às ITU assintomáticas. A ocorrência de bacteriúria na fase da gravidez varia de 2% a 5% e há possibilidade de resultar em infecções severas na mãe e no feto. Se não tratada, pode levar à infecção aguda e pielonefrite sintomática, o que geralmente acontece durante o terceiro trimestre, sendo apontada como causa frequente de hospitalização, baixo peso, crescimento da mortalidade perinatal e aumento nos índices de partos prematuros (BARBERINO, 2010).
A ITU é a complicação médica mais recorrente na gravidez, apresentando sintomas em 1% a 2% das gestantes, e 2% a 13% consta-se bacteriúria assintomática. Destas, 20% a 40% avançam para pielonefrite se não forem tratadas adequadamente (BRAGGIATO,2016).
Para o feto, a ITU na gravidez abrange 40% de risco de parto prematuro, baixo peso ao nascer e retardo de crescimento. Para as mães, as complicações apresentam insuficiência ou falência renal, síndrome do desconforto respiratório do adulto e sepse. Dados os motivos, salienta-se veementemente a coleta de uma cultura de urina em todas as mulheres gestantes na primeira consulta do exame pré-natal e uma reavaliação no terceiro trimestre. Caso conste-se positividade, uma cultura de controle de cura deve ser efetivada uma semana após o findar do tratamento com antibióticos. O ressurgimento de infecções do trato urinário afeta cerca de uma em cada 3 mulheres gestantes com diagnóstico de ITU (REU, 2013).
A bacteriúria é mais constantemente ocasionada por E. coli, entretanto, o estreptococo beta-hemolítico do grupo B (Streptococcus agalactiae) que acontece com uma frequência entre 1% e 2% na população em geral, desenvolve-se para 1% a 5% nas gestantes. A colonização acarreta-se normalmente através da ascensão do microrganismo desde a vagina, onde é capaz de manter-se sem causar sintomas. No entanto, mais de 7% das gestações podem se agravar devido a ITU por esta bactéria. Das gestantes que evoluem para pielonefrite, o S. agalactiae é causador de cerca de 10% dos quadros clínicos. Ademais, pode ocasionar corioamnionite, a transmissão vertical do microrganismo, parto prematuro e inclusive sepse neonatal. É aconselhada a ministração de antibióticos durante o parto como profilaxia (REU, 2013).
Após a menopausa, com a ausência de estrogênio, ocorre uma mudança significativa na microbiota endógena da vagina, o que pode contribuir para a colonização de patógenos que ascendem pela uretra, causando ITU. O estrógeno é essencial para manter a acidez da vagina e permitir a manutenção de lactobacilos, importantes na defesa natural do corpo humano (BRAGGIATO, 2016)
A idade avançada é um fator importante a ser enfatizado, pois a ocorrência da ITU aumenta com ela. A manifestação de comorbidades coexistentes como: diabetes, demência, alterações na resposta imune e acidentes vasculares cerebrais aliados à hospitalização e/ou instrumentação mais frequentes, colaboram para a ITU ser mais decorrente nesta faixa etária (NÓBREGA 2015).
O sistema urinário pode ser alcançado pelos patógenos através das vias ascendente, hematológica e linfática (FILHO, 2013).
A via de contaminação ascendente é a mais comum, sendo os microrganismos mais frequentes os da família Enterobacteriaceae, principalmente a Eschericia coli, responsável por 80% a 90% dos casos, a qual coloniza cólon, região perianal e vagina (BORGES, 2014).
A cistite bacteriana inicia-se com a colonização da pele periuretral e da uretra anterior, antes do início na bexiga. São constados fatores de virulência inerentes, que lhes concebem aderir às células vaginais e uroepitelial, resistir à ação bactericida do soro humano, evitar a fagocitose pelos leucócitos e estimular a produção citotoxinas próprias para invasão do tecido. Uma vez no aparelho urinário, a bactéria coloniza a mucosa urogenital, onde se reproduz e causa bacteriúria (BARBERINO, 2010).
Além da rota ascendente, a rota hematogênica também pode ser utilizada pelas bactérias para causar ITU secundária em pacientes com bacteremia. A infecção através desta rota é restrita a determinados patógenos tais como: Candida spp., Staphylococcus aureus, Mycobacterium tuberculosis e Salmonella spp. (REU, 2013).
As ITU nos pacientes da comunidade são diferentes daquelas ocasionadas em pacientes hospitalizados em alguns conceitos, sendo os mais relevantes o perfil de susceptibilidade e a etiologia (BARBERINO, 2010).
A bactéria E. coli é causadora de 75% – 90% dos quadros clínicos de cistite aguda não complicada e de pielonefrite, além de 50% dos quadros de infecção nosocomial. Os outros casos são habitualmente provocados por outras Enterobactérias tais como: Proteus sp., Klebsiella sp., Enterobacter sp., Pseudomonas sp. e por bactérias gram-positivas como Enterococcus faecalis, Staphylococcus saprophyticus e Streptococcus agalactiae. Espécies de Cândida podem desencadear ITU, especialmente em pacientes diabéticas não controladas e em imunocomprometidas (BRAGGIATO, 2016).
A E. coli é componente da microbiota do cólon do ser humano e, normalmente, classificada como não patogênica. Entretanto, algumas cepas podem apresentar fatores de virulência e desencadear doença humana. As situações clínicas infecciosas principais que envolvem E. coli são: meningite, sepse, ITU e infecções gastrointestinais (BARBERINO, 2010).
A maioria das ITU são desencadeadas por um único patógeno, apesar de que infecções mistas possam advir e exijam de tratamento mais complexo (REU, 2013).
Quando aflige pacientes que estão isentos do ambiente hospitalar, sem irregularidades anatômicas e funcionais do trato urinário, designa-se ITU não complicada. Em pacientes com desordens funcionais, metabólicas ou anatômicas, como a obstrução infra vesical, bexiga neurogênica, cálculo renal, diabetes, insuficiência renal, manipulação do trato urinário, imunossupressão, presença de cateteres urinários, idosos, gestantes, podem apresentar risco maior de falha terapêutica ou complicações mais severas, portanto, sendo considerados como portadores de ITU complicada (NÓBREGA, 2015).
Entretanto, elas podem ser classificadas mais especificamente de outras formas: anatomicamente (uretrite, cistite, pielonefrite e urosepse), pelos achados microbiológicos (a espécie encontrada pode ser passível à maioria dos antibióticos, com sensibilidade reduzida ou multirresistente) ou pela avaliação dos fatores de risco (sem fatores de risco conhecidos, risco de infecção recorrente não severa, risco extra urogenital com probabilidade de agravamento, nefropatia com risco de agravamento, risco urológico transitório) (REU, 2013).
Classifica-se como infecção isolada ao primeiro episódio de ITU, ou a episódios que se sucedam com mais de seis meses de intervalo entre si, equivalendo a 25%-40% dos casos que afetam mulheres jovens (NÓBREGA, 2015).
A infecção não resolvida origina-se da falha terapêutica causada por resistência bacteriana, ou ainda pelo fato de a infecção ter sido originada por dois tipos distintos de bactérias, com passibilidades distintas aos antimicrobianos (NÓBREGA, 2015).
Na reinfecção, o desfecho da urocultura será negativo findo o tratamento. Entretanto, duas semanas depois da terapia, o mesmo microrganismo desenvolver-se-á mais uma vez, ou ainda, um microrganismo diferente poderá surgir a qualquer momento. A reinfecção representa cerca de 90% – 95% dos casos de ITU de reincidência (NÓBREGA, 2015).
Cerca de 10% das ITU recorrentes acarretam da não erradicação do agente causal, que perdura no trato urinário e qualifica recidiva. A resistência bacteriana provém do acúmulo de bactérias em áreas de difícil acesso para os antibióticos, como divertículo uretral, cálculos infectados e glândulas parauretrais infectadas (NÓBREGA, 2015).
A infecção urinária de repetição é determinada pelo incidente de três episódios de ITU, atestadas pelos resultados positivos da urocultura, no período de 12 meses, ou ainda pela eventualidade de duas infecções, ao longo dos últimos seis meses. Os fatores de risco determinantes para ITU de repetição são: status não secretor, história prévia de ITU, distúrbios no esvaziamento vesical, incontinência urinária, atrofia genital, distopia genital, cálculo renal, diabetes, obesidade e atividade sexual frequente (NÓBREGA, 2015).
De acordo com o agravo, as ITU podem ser classificadas em uretrite, quando acomete a uretra, cistite, quando a infecção se manifesta na bexiga, e pielonefrite, infecção que alcança o parênquima de um ou ambos rins (DEMILIE, 2012).
Pacientes portadores de ITU podem apresentar sintomas ou não, e quando presentes, estes variam de simples desconforto urinário, até bacteremia ou sepse, podendo até mesmo levar ao óbito. Em geral, 90% das ITU se manifestam como cistite, e 10% como pielonefrite (OLIVEIRA, 2014).
As ITU, quando sintomáticas, podem estar acompanhadas de um ou vários sintomas, entre os quais: alteração na cor e odor urinários, disúria, polaciúria, nictúria, urgência miccional, dor lombar e em 30% dos casos, hematúria macroscópica. Nos casos de pielonefrite, o quadro clínico inclui dor lombar ou em flancos, uni ou bilateral, febre, calafrios, mal-estar geral, anorexia, náuseas e vômitos (DIAS, 2015).
A possibilidade de ocorrência de cistite em uma mulher com disúria, aumento da constância urinaria e hematúria é próxima de 50%. Este índice é superior a 90% quando constadas combinações de sintomas inerentes, com inexistência de corrimento ou irritação vaginal. Na existência de irritação e fluxo vaginal, a possibilidade do diagnóstico de cistite reduz em cerca de 20%. No entanto, quando uma mulher com histórico de cistite manifesta sintomas sugestivos no retorno à unidade de atendimento, tem a probabilidade de 84% a 92% de que a infecção esteja presente (BRAGGIATO, 2016).
O diagnóstico presuntivo de ITU pode ser formulado com base na história clínica e o exame físico do paciente, sobretudo quando os sintomas clássicos estão presentes. Entretanto, somente 65% das mulheres que manifestam sintomas de cistite têm a infecção dada como positiva (NÓBREGA, 2015).
Vários exames de rápida realização são utilizados periodicamente para realizar diagnóstico presuntivo de ITU, abrangendo análise bioquímica da urina, contagem de leucócitos (piuria), teste de nitrito e microscopia direta (Gram) (BARBERINO, 2010).
Estudos foram publicados a respeito da confiabilidade desses testes ao diagnosticar ITU. A detecção de bacteriúria, com o exame de urina não centrifugada e corada através do método de Gram, ainda que pouco realizado na prática clínica, pode contribuir no diagnóstico das infecções urinárias e orientar o médico na seleção da terapia antimicrobiana, sobretudo em serviços que não possuem recursos para verificação de cultura (BARBERINO, 2010).
A microscopia direta corada pelo Gram é um método de rápida utilização, confiável e barato, capaz de estimar uma bacteriúria de 105 UFC/mL. A principal desvantagem que é apontada nesta metodologia é a sensibilidade baixa no referente às amostras com contagem menor que 105 UFC, restringindo seu uso nos pacientes atendidos no ambulatório com ITU não complicada. No entanto, uma grande vantagem retratada é a boa correlação com bacteriúria significativa, e pode proporcionar dados sobre características de tinção e morfológicas do microrganismo para orientar a terapêutica antimicrobiana inicial (BARBERINO, 2010).
A fita reagente, dipstick, é proveitosa na triagem de casos agudos, com suspeita de ITU. A manifestação de esterase leucocitária (indicativa de piúria), de nitrito (formado pela redução do nitrato a nitrito, por algumas enterobactérias) e de hematúria microscópica estão associadas à ITU em, 90%, 76% e 75%, na devida ordem, das pacientes com urocultura positiva (NOBREGA, 2015).
Em mulheres com sintomas de disúria, urgência e frequência miccional, o valor preditivo positivo (VPP) para nitrito é de 96%, com particularidade de 94%, enquanto os índices do valor preditivo negativo (VPN) e a sensibilidade são de 30% e 44%, na mesma ordem. Caso a pesquisa do nitrito for negativa, os índices de VPP para esterase leucocitária é de 79% e a sensibilidade de 82%. Entretanto, se porventura ambos os testes forem negativos, 50% das culturas de urina podem ser positivas. De tal forma, um dipstick negativo não descarta a possibilidade de ITU (BRAGGIATO, 2016)
No exame da amostra urinária, o reconhecimento de leucocitúria (>10 leucócitos/campo) é grande indicador de infecção. Porém, um índice de 20% dos pacientes com ITU positiva pode apresentar contagem comum de leucócitos, assim como leucocitúria relevante pode decorrer da ausência de ITU (NÓBREGA, 2015).
O quadro clínico e o exame de sedimento urinário, assim como a microscopia direta após coloração pelo método de Gram, orientam o diagnóstico dessa patologia (MACHADO, 2016).
O diagnóstico definitivo só se obtém por meio de urocultura, também denominada cultura de urina, considerada padrão ouro para o diagnóstico de ITU, que identifica a presença de bactéria e considera o crescimento bacteriano de pelo menos 100 mil unidades formadoras colônias por mL de urina (100.000 UFC/mL). Quando a cultura se mostra positiva para infecção, é indicado o Teste de Sensibilidade a Antimicrobianos (TSA) ou Antibiograma, método que permite conhecer a sensibilidade e a resistência da bactéria aos principais antibióticos utilizados (MACHADO, 2016).
O critério da presença de bacteriúria significante na urocultura tem sido amplamente questionado e os sintomas clínicos têm sido cada vez mais relevados, de tal modo que, em pacientes sintomáticos, contagens a partir de 103 UFC/mL de urina já indicam ITU (NÓBREGA, 2015).
A predominância da bacteriúria assintomática difere de acordo com a idade, sexo e existência de anomalias no trato genitourinário. Em mulheres saudáveis, a prevalência intensifica de acordo com a idade, variando de 1% – 5% em jovens e até mais de 20% em mulheres acima de 80 anos. A E. coli é o microrganismo mais influente (NÓBREGA, 2015).
A bacteriúria assintomática não causa maiores implicações em mulheres sexualmente ativas em período de vida antes de menopausa e que não estão gestantes. Normalmente, é um quadro de resolução espontânea, porém aumenta o risco de desenvolvimento de infecção urinária sintomática nessas mulheres, quando comparadas àquelas sem bacteriúria (ANS, 2011). Há casos, entretanto, que a existência de fatores de risco requer que a bacteriúria assintomática seja adequadamente tratada. Tais casos incluem a cirurgia e a instrumentação urológica, gravidez, pacientes diabéticos e pacientes pediátricos (LENZ, 2006).
Com o aumento da resistência e pelo fato de algumas cepas de E. coli uropatogênicas não apresentarem perfil de suscetibilidade constante aos antimicrobianos comumente utilizados, é preciso que se realize testes de suscetibilidade (antibiograma). Este teste é feito com o disco difusão ou Kirby-Bauer, cujos pontos de corte se baseiam nos níveis plasmáticos dos antibióticos (REMONATTO, 2006)
O tratamento adequado das ITU de causa bacteriana requer o conhecimento quanto ao perfil bacteriológico, sensibilidade e resistência aos antibióticos utilizados, ressaltando a importância da realização de urocultura combinada ao antibiograma sempre que possível. A eleição do antimicrobiano deve levar em conta a eficácia frente à bactéria em questão, a excreção urinária, a toxicidade, além da comodidade posológica e o custo financeiro (DIAS, 2015).
A escolha do esquema terapêutico deve ser cuidadosa, pois estudos demonstram que o nível de resistência bacteriana vem aumentando, não apenas em pacientes hospitalizados, mas também nos ambulatoriais (DIAS, 2015), e se trata de uma resposta de adaptação inevitável das bactérias à exposição aos antibióticos (SANTOS, 2003).
Sendo assim, essa escolha se mostra um ato complexo, sendo necessário conhecer os mecanismos de ação dos diferentes antibióticos (bactericidas ou bacteriostáticos), os mecanismos de resistência bacteriana, características farmacológicas das moléculas, local e etiologia da infeção, efeitos adversos, incompatibilidade entre medicamentos e história clínica (anamnese) dos doentes, idade e estado funcional renal e hepático (MARQUES, 2015).
A escolha do antibiótico é também condicionada pelo local da infeção, pois o fármaco deverá atingir concentrações terapêuticas nesse local. Sendo assim, para o tratamento da ITU deverão ser utilizados antibióticos de eliminação urinária como beta-lactâmicos, glicopeptídeos, fosfomicina, aminoglicosídeos, quinolonas, sulfonamidas, e nitrofurantoína (MARQUES, 2015).
Os grupos de antibióticos utilizados no tratamento de ITU atuam em diferentes estruturas alvo na bactéria, sendo que os beta-lactâmicos, glicopeptídeos e fosfomicina atuam na inibição da síntese da parede celular, os aminoglicosídeos inibem a síntese proteica, as sulfonamidas e trimetoprim inibem a síntese do ácido fólico e as quinolonas inibem a síntese de DNA (MARQUES, 2015).
Apesar de demonstrar eficácia inquestionável no tratamento da infeção do trato urinário, rapidamente se verificou que diversos microrganismos adquiriram resistência a antibióticos aos quais inicialmente eram sensíveis. Uma terapêutica antimicrobiana racional é importante de modo a evitar o surgimento das resistências bacterianas responsáveis pelo fracasso terapêutico (MARQUES, 2015).
O tratamento específico inicial das ITU comunitárias não complicadas deve ser direcionado à Escherichia coli, e se necessário modificar o esquema terapêutico ou de acordo com o resultado da urocultura (CUNHA, 2011).
A resistência bacteriana é resultado da pressão seletiva pelo uso indiscriminado e intensivo de antibióticos, bem como da habilidade dos agentes etiológicos de se adaptarem frente a um ambiente hostil. Diversas hipóteses foram levantadas como causa do aumento das taxas de resistência, seja na medicina, na produção de alimentos para animais e na agricultura. A aplicação de medidas para erradicação da resistência bacteriana por meio da restrição do uso de antimicrobianos e seu uso racional ainda são um desafio, para um país de grandes dimensões territoriais, com escassa equipe de vigilância e controle da sua venda e uso (BARBERINO, 2010).
A resistência antimicrobiana é basicamente um fenômeno relacionado a existência de genes que codificam mecanismos bioquímicos para impedir a ação de drogas (TAVARES, 2009).
A resistência pode ser natural, compõe a herança genética cromossômica do microrganismo, possuindo um caráter hereditário; ou adquirida, que consiste no surgimento do fenômeno da resistência a um ou vários antimicrobianos numa população bacteriana originalmente sensível, e resulta de modificações na estrutura ou no funcionamento da célula bacteriana decorrente de fatores genéticos adquiridos por mecanismos que alteram o cromossomo ou o plasmídeo bacteriano (TAVARES, 2009).
Os mecanismos genéticos que codificam a resistência bacteriana se exteriorizam pelos seguintes mecanismos de ação: inativação da droga por enzimas, alteração da permeabilidade bacteriana à droga, alteração de sistemas de transporte na célula, retirada ativa da droga do meio intracelular (efluxo), alteração do receptor da droga e modificação do sistema metabólico ativo para a droga e síntese de vias alternativas (FOCACCIA, 2015).
É desaconselhável o uso de antimicrobianos em prescrições empíricas no tratamento de infecções bacterianas em que é notória as taxas de resistência superiores a 20%, sendo assim é mandatória a importância do estudo do perfil de susceptibilidade na eleição da antibioticoterapia empírica (GUPTA, 2011).
Os dados relatados por diversos estudos demonstram que a etiologia das ITU é semelhante a presente em outras partes do mundo. Entretanto, o modelo de resistência desses uropatógenos pode possuir características distintas de acordo com o histórico de demanda de antimicrobianos em cada sociedade (NABER, 2008).
Os resultados de alguns estudos demonstram que as bactérias isoladas de pacientes hospitalizados se mostraram mais resistentes aos antimicrobianos que as infecções oriundas do ambulatório, com frequências mais elevadas de resistência para ácido nalidíxico, amoxicilina/ácido clavulânico, ampicilina, cotrimoxazol e cefalotina. O mesmo estudo demonstra também que o aumento dessa resistência ocorre devido à seleção de cepas resistentes da microbiota endógena dos pacientes e não pela transmissão de cepas hospitalares resistentes (SORLONAZO, 2014).
Apesar da elevada vulnerabilidade das bactérias de origem ambulatorial à gentamicina (apenas 10% de resistência), as amostras de pacientes hospitalizados constaram índices de resistência em torno de 30% para as cepas de E. coli e Klebsiella pneumoniae e 50% para cepas de Pseudomonas aeruginosa. A alta resistência à cefalotina (40% das infecções de ambulatório e 73,3% de pacientes internados) é um evento a ser enfatizado pelo fato de posicionar-se entre os fármacos de primeira escolha para a intervenção de cistite em gestantes nas quais o uso de antibióticos é mais estrito (SANTANA, 2012).
A ampicilina, o sulfametoxazol + trimetoprim, a cefalotina e o ácido nalidíxico demonstraram os menores índices de vulnerabilidade em geral, enfatizando que esses antibióticos devem ser ministrados unicamente após a liberação do resultado do antibiograma. A resistência ao sulfametoxazol/trimetoprim vem se elevando em todo o mundo, inclusive nas infecções de início comunitário, comprovando assim a não recomendação de uso empírico (KIBRET, 2014).
É razoável pressupor que os índices de resistência em patógenos contraídos na comunidade sejam desfechos da pressão seletiva do uso exacerbado de antibióticos na população comum. Em países desenvolvidos, considerando as vendas e realizando pesquisas das prescrições médicas é fácil a determinação de dados estatísticos; mas em países em emergentes estes dados são menos assertivos, pois é habitual a prática da automedicação, bem como o uso de doses inadequadas (SANTANA, 2012).
É notório que a ITU constitui um problema de saúde pública por representar um desafio principalmente em relação à mulher adulta, diante da amplitude de sua incidência, ao incremento da mortalidade e dos custos hospitalares, assumindo consequências de impacto humano, social e econômico.
Assim, a abordagem do tema denota sua relevância na medida em que a análise laboratorial das culturas de urina pode contribuir com a identificação dos principais agentes bacterianos, assim como os que apresentam maior resistência aos antibióticos comumente usados para o tratamento das infecções.
Com esses conhecimentos, será possível melhorar a qualidade da assistência médico-hospitalar prestada às pacientes que se confrontam com os sintomas e recorrência das ITU, ao oferecer informações sobre os antibióticos que apresentam melhores resultados no tratamento dessa patologia. Dessa forma, esse trabalho tem como objetivo conhecer os agentes etiológicos e o perfil de resistência bacteriana em uroculturas de mulheres na cidade de Macapá a nível ambulatorial e hospitalar.
METODOLOGIA
Esse estudo se caracteriza por ser um estudo observacional, retrospectivo e transversal. Utilizou-se amostras de resultados de exame ambulatoriais, realizados no Laboratório Paulo Albuquerque e pacientes internados em unidade hospitalar privada (Hospital São Camilo) feitos no Laboratório Acqualitybio. Ambos laboratórios são de natureza não-pública, isto é, atendem pacientes da rede privada e/ou conveniada com planos de saúde complementares.
As amostras foram entregues nos laboratórios escolhidos no período de janeiro a junho de 2017.
Foram incluídos os exames de urocultura positivo com antibiogramas provenientes de paciente do sexo feminino com 18 anos ou mais. Excluíram-se os exames de pacientes do sexo masculino, de pacientes do sexo feminino com idade inferior a 18 anos incompletos no momento da coleta, uroculturas negativas e uroculturas sem antibiograma.
As variáveis analisadas são: idade, bactéria isolada e antibióticos a que as bactérias são resistentes.
O estudo seguirá os princípios éticos da Declaração de Helsinque (ASSOCIAÇÃO MÉDICA MUNDIAL, 1964) e atenderá as considerações éticas dispostas na Resolução 466 de 2012 do Conselho Nacional de Saúde, a qual foi submetida à avaliação do Comitê de Ética em Pesquisa da Universidade Federal do Amapá após registro na Plataforma Brasil, 76701717.8.0000.0003.
Registra-se aqui que a possibilidade de danos à dimensão física, psíquica, moral, intelectual, social, cultural ou espiritual do ser humano é mínima em qualquer fase desta pesquisa e dela decorrente, uma vez que a pesquisa se baseia em dados retrospectivos, sem contato direto com seres humanos. Além disso, as informações obtidas das bases de dados foram tratadas com total respeito à privacidade e ao sigilo das pessoas que realizaram os exames nos laboratórios participantes, restringindo o uso estritamente científico de tais informações na presente pesquisa. Neste estudo, o risco está relacionado à invasão de privacidade de informações correspondentes aos resultados das uroculturas das pacientes estudadas. Assim, a divulgação de tais informações ou o compartilhamento desses dados individuais poderá causar prejuízos às participantes, na medida em que podem se sentir envergonhadas pela exposição de sua vida íntima, condição a ser evitada ao máximo, sendo garantido às pacientes, o sigilo de dados que possam identificá-las.
Esta pesquisa apresenta benefícios de ordem coletiva, pois possibilitará melhor entendimento a respeito das bactérias causadoras das ITU e os antibióticos a que são resistentes na cidade de Macapá, assim, poderá trazer melhorias nas vertentes de saúde da mulher. Os benefícios individuais serão indiretos, pois não serão realizadas intervenções experimentais nas pacientes.
Após a coleta de dados retrospectivos dos bancos de dados por meio de sistemas informatizados dos laboratórios, os dados foram tratados estatisticamente com utilização do programa Bioestat, versão 5.3. A correlação entre as variáveis foi verificada pelo Qui-Quadrado (C2= 0,05), ao nível de significância p < 0,05.
RESULTADOS
No Laboratório de Análises Clínicas Paulo Albuquerque foram obtidas 359 uroculturas de mulheres entre 18 e 95 anos de idade, com idade média de 56,6 anos.
A bactéria mais frequentemente isolada foi a E. coli, encontrada em 235 uroculturas, correspondendo a 65,4% do total de 359. Em segundo lugar, aparece o Staphylococcus aureus, presente em 113 uroculturas, obedecendo a 31,5% delas. A terceira bactéria isolada foi Staphylococcus sp, presente em apenas 11 uroculturas, correspondendo a 3,1% do total (Figura 1),
FIGURA 1- Distribuição das espécies bacterianas encontradas nas uroculturas no Laboratório de Análises Clínicas Paulo Albuquerque
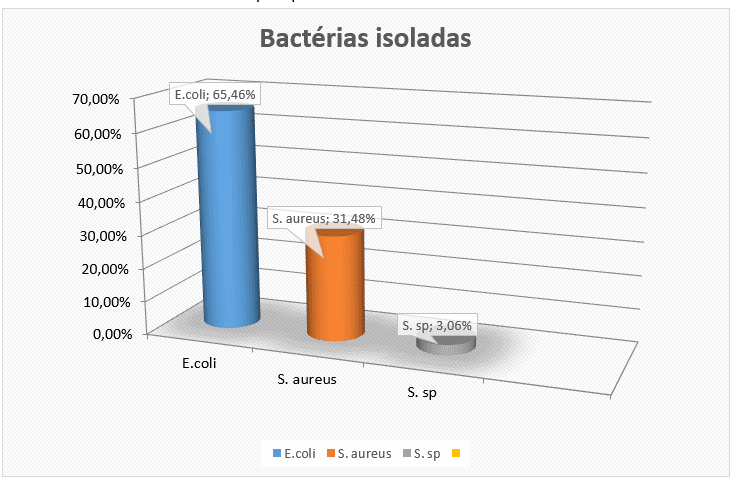
A E.coli apresentou maior resistência à Ampicilina, em 42,9% das uroculturas. Em segundo lugar, está a Amicacina, em 39,1%, seguida pela Cefalotina, em 38,7%. A menor resistência foi observada frente ao Cefepima, em 17,8% das uroculturas (Tabela 1).
TABELA 1- Antibióticos a que a bactéria E.coli apresentou resistência
| Antibiótico | Total de 235 | % |
| Ampicilina | 101 | 42,97 |
| Amicacina | 92 | 39,14 |
| Cefalotina | 91 | 38,72 |
| Ampicilina + Sulbactam | 91 | 38,72 |
| Ácido Nalidíxico | 87 | 37,02 |
| Polimixina B | 84 | 35,74 |
| Levofloxacina | 79 | 33,61 |
| Ácido pepmídico | 78 | 33,19 |
| Cefazolina | 74 | 31,48 |
| Ciprofloxacina | 69 | 29,36 |
| Cefuroxima | 68 | 28,93 |
| Nitrofurantoína | 65 | 27,65 |
| Ceftriaxona | 65 | 27,65 |
| Ceftazidima | 64 | 27,23 |
| Cloranfenicol | 61 | 25,95 |
| Piperacilina + Tazobactam | 58 | 24,68 |
| Meropeném | 57 | 24,25 |
| Ofloxacina | 55 | 23,40 |
| Tobramicina | 53 | 22,55 |
| Cefotaxima | 48 | 20,42 |
| Ticarcilina + Ácido Clavulânico | 48 | 20,42 |
| Imipeném | 47 | 20,00 |
| Aztreonam | 46 | 19,57 |
| Cefepima | 42 | 17,87 |
FONTE: Banco de dados do Laboratório de Análises Clínicas Paulo Albuquerque no período de janeiro a junho de 2017.
A segunda bactéria mais comum, Staphylococcus aureus, apresentou maior resistência à Rifampicina, em 46,9% das uroculturas onde o S. aureus foi encontrado. Na segunda colocação estão três antibióticos, Cefaclor, Clindamicina e Tetraciclina, cada um em 42,47%. Em terceiro lugar está a Amoxicilina, em 41,59%. A Vancomicina foi o antibiótico que apresentou menor resistência, em 11,5% das uroculturas (Tabela 2).
TABELA 2- Antibióticos a que a bactéria S. aureus apresentou resistência
| Antibiótico | Total de 113 | % |
| Rifampicina | 53 | 46,90 |
| Cefaclor | 48 | 42,47 |
| Clindamicina | 48 | 42,47 |
| Tetraciclina | 48 | 42,47 |
| Amoxicilina | 47 | 41,59 |
| Benzilpenicilina G | 46 | 40,70 |
| Eritromicina | 45 | 39,82 |
| Oxacilina | 44 | 38,93 |
| Cefalexina | 42 | 37,16 |
| Azitromicina | 42 | 37,16 |
| Amoxicilina + Ácido Clavulânico | 41 | 36,28 |
| Gentamicina | 41 | 36,28 |
| Cefoxitina | 39 | 34,51 |
| Norfloxacina | 38 | 33,62 |
| Teiclopanina | 36 | 31,85 |
| Levofloxacina | 31 | 27,43 |
| Sulfametoxazol + Trimetoprim | 28 | 24,77 |
| Claritromicina | 27 | 23,89 |
| Nitrofurantoína | 27 | 23,89 |
| Lincomicina | 27 | 23,89 |
| Amoxicilina | 20 | 17,69 |
| Vancomicina | 13 | 11,50 |
FONTE: Banco de dados do Laboratório de Análises Clínicas Paulo Albuquerque no período de janeiro a junho de 2017
A bactéria encontrada em menor número, Staphylococcus sp, apresentou maior resistência à Gentamicina e Oxacilina, ambas em 63,63% das uroculturas positivas, seguidas por três antimicrobianos, Benzilpenicilina G, Norfloxacina e Azitromicina, em 45,45%, e em terceiro lugar estão quatro antibióticos, Eritromicina, Rifampicina, Amoxicilina e Tetraciclina, em 36,36% dessas uroculturas. Os antibióticos que apresentaram menor resistência foram Claritromicina, Amoxicilina + Ácido Clavulânico, Levofloxacina, Moxifloxacina, Teiclopanina e Sulfametoxazol + Trimetoprim, em apenas 09.09% das uroculturas (Tabela 3).
TABELA 3- Antibióticos a que a bactéria Staphylococcus sp apresentou resistência
| Antibiótico | Total de 11 | % |
| Gentamicina | 7 | 63,63 |
| Oxacilina | 7 | 63,63 |
| Benzilpenicilina G | 5 | 45,45 |
| Norfloxacina | 5 | 45,45 |
| Azitromicina | 5 | 45,45 |
| Eritromicina | 4 | 36,36 |
| Rifampicina | 4 | 36,36 |
| Amoxicilina | 4 | 36,36 |
| Tetraciclina | 4 | 36,36 |
| Cefaclor | 3 | 27,27 |
| Vancomicina | 3 | 27,27 |
| Nitrofurantoína | 3 | 27,27 |
| Cefoxitina | 2 | 18,18 |
| Cefalexina | 2 | 18,18 |
| Clindamicina | 2 | 18,18 |
| Lincomicina | 2 | 18,18 |
| Claritromicina | 1 | 09,09 |
| Levofloxacina | 1 | 09,09 |
| Amoxicilina + Ácido Clavulânico | 1 | 09,09 |
| Moxifloxacina | 1 | 09,09 |
| Teiclopanina | 1 | 09,09 |
| Sulfametoxazol + Trimetoprim | 1 | 09,09 |
FONTE: Banco de dados do Laboratório de Análises Clínicas Paulo Albuquerque no período de janeiro a junho de 2017
A análise dos dados do Laboratório de Análises Clínicas Acqualitybio, onde encontramos uroculturas de mulheres hospitalizadas, realizadas de forma automatizada, nos mostra resultados mais variados.
A amostra consta de 75 uroculturas de mulheres de 27 a 94 anos, com média de 60,5 anos. Do total, houve crescimento bacteriano em 52 culturas, que corresponde a 69,3% delas, e fúngico em 23 exames, correspondendo a 30,7% dos exames (FIGURA 2).
FIGURA 2- Distribuição dos microrganismos encontrados nas uroculturas no Laboratório de Análises Clínicas Acqualitybio
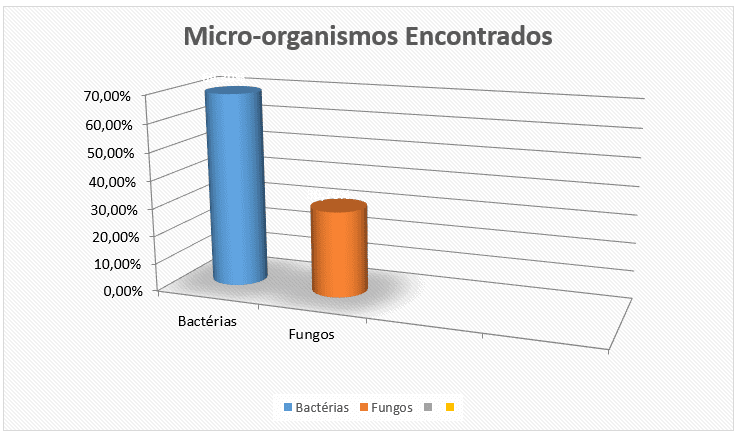
Entre as bactérias encontradas, 29 correspondiam a E. coli, representando 56% de 52 uroculturas, 10 a Klebsiela pneumoniae, que corresponde a 19%, 4 a Staphylococcus haemolyticus, totalizando 7%, 3 a Klebsiela ocytoca, correspondendo a 6%. Correspondendo a aproximadamente 2% do total, estão bactérias com apenas 1 urocultura positiva, são elas: Stapylococcus warneri, Staphylococcus saprophyticus, Staphylococcus sciuri, Enterococcus faecalis, Enterococcus sp e Serratia ficaria (FIGURA 3).
FIGURA 3- Distribuição das bactérias encontradas nas uroculturas no Laboratório de Análises Clínicas Acqualitybio
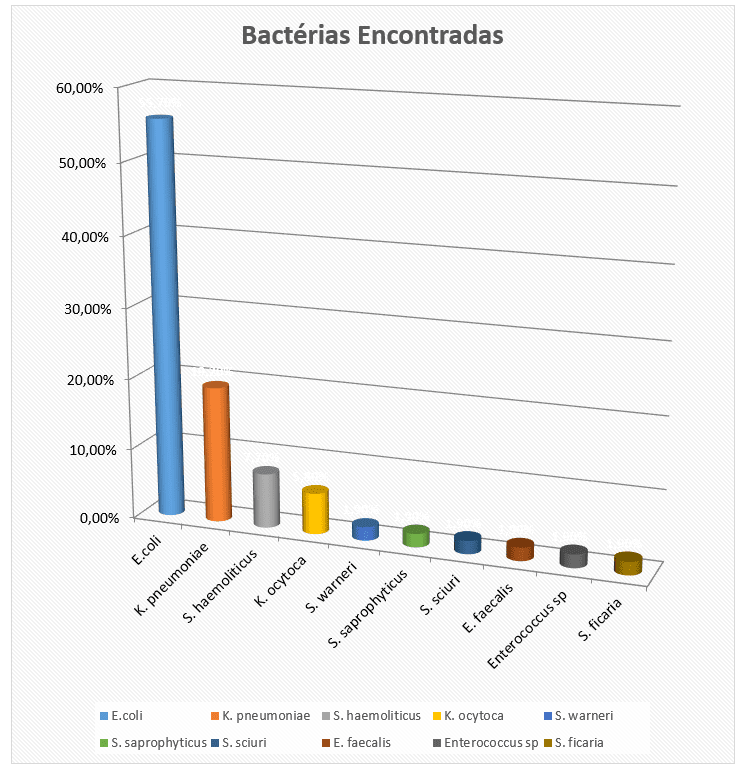
Ao analisar os antibióticos a que a E.coli apresentou resistência, pode-se observar que o antibiótico que aparece em primeiro lugar é a Ampicilina, correspondendo a 82,7% das uroculturas. Em segundo lugar estão os antibióticos Ácido Nalidíxico e Sulfametoxazol + Trimetoprim, o que corresponde a 62,06%, seguidos por Ciprofloxacina, correspondendo a 58,6% dos exames. Não houve resistência ao Ertapeném (TABELA 4).
TABELA 4- Antibióticos a que a bactéria E.coli apresentou resistência
| Antibiótico | Total de 29 | % |
| Extended-Spectrum Betalactamase positivo | 16 | 55,17% |
| Ampicilina | 24 | 82,75% |
| Sulfametoxazol + Trimetoprim | 18 | 62,06% |
| Ácido Nalidíxico | 18 | 62,06% |
| Ciprofloxacina | 17 | 58,62% |
| Cefuroxima | 15 | 51,72% |
| Cefuroxima Axetil | 15 | 51,72% |
| Ceftrixona | 15 | 51,72% |
| Cefepime | 15 | 51,72% |
| Norfloxacina | 13 | 44,82% |
| Cefalotina | 12 | 41,37% |
| Gentamicina | 11 | 37,93% |
| Ceftazidima | 5 | 17,24% |
| Ampicilina + Sulbactam | 4 | 13,79% |
| Amoxicilina + Ácido Clavulânico | 4 | 13,79% |
| Piperacilina + Tazobactam | 3 | 10,34% |
| Nitrofurantoína | 2 | 6,89% |
| Meropeném | 2 | 6,89% |
| Cefoxitina | 1 | 3,44% |
| Amicacina | 1 | 3,44% |
| Ertapeném | 0 | 0% |
FONTE: Banco de dados do Laboratório de Análises Clínicas Acqualitybio no período de janeiro a junho de 2017
A segunda bactéria mais frequente foi a Klebsiela pneumoniae, que apresentou resistência à Ampicilina em 100% das uroculturas. Em segundo lugar estão Cefuroxima, Cefuroxima Axetil, Ceftriaxona e Cefepima, positivas em 90%, e em terceiro lugar a Ciprofloxacina, correspondendo a 60%. Não houve resistência ao Ertapeném nem à Amicacina (TABELA 5).
TABELA 5- Antibióticos a que a bactéria Klebsiela pneumoniae apresentou resistência
| Antibiótico | Total de 10 | % |
| Extended-Spectrum Betalactamase positivo | 10 | 100% |
| Ampicilina | 10 | 100% |
| Cefuroxima | 9 | 90% |
| Cefuroxima Axetil | 9 | 90% |
| Ceftriaxona | 9 | 90% |
| Cefepima | 9 | 90% |
| Ciprofloxacina | 6 | 60% |
| Cefalotina | 5 | 50% |
| Gentamicina | 5 | 50% |
| Ácido Nalidíxico | 5 | 50% |
| Sulfametoxazol + Trimetoprim | 5 | 50% |
| Piperacilina + Tazobactam | 4 | 40% |
| Ceftazidima | 4 | 40% |
| Norfloxacina | 3 | 30% |
| Nitrofurantoína | 2 | 20% |
| Ampicilina + Sulbactam | 2 | 20% |
| Amoxicilina + Ácido Clavulânico | 1 | 10% |
| Meropeném | 1 | 10% |
| Amicacina | 0 | 0% |
| Ertapeném | 0 | 0% |
FONTE: Banco de dados do Laboratório de Análises Clínicas Acqualitybio no período de janeiro a junho de 2017
O Staphylococcus haemolyticus apresentou maior resistência à Oxacilina, em 100% das uroculturas onde dita bactéria foi isolada. Em segundo lugar, estão Benzilpenicilina, Ciprofloxacina, Eritromicina e Norfloxacina, em 75%, seguidas por Moxifloxacina, Clindamicina e Sulfametoxazol + Trimetoprim, em 50%. Não houve resistência à Gentamicina, Linezolida, Teiclopanina, Vancomicina, Tigeciclina, Ácido Fusídico e Rifampicina (Tabela 6).
TABELA 6 – Antibióticos a que a bactéria Staphylococcus haemolyticus apresentou resistência
| Antibiótico | Total de 4 | % |
| Teste de screening de Cefoxitina positivo | 3 | 75% |
| Teste induzido à Clindamicina positivo | 0 | 0% |
| Oxacilina | 4 | 100% |
| Benzilpenicilina G | 3 | 75% |
| Ciprofloxacina | 3 | 75% |
| Eritromicina | 3 | 75% |
| Norfloxacina | 3 | 75% |
| Moxifloxacina | 2 | 50% |
| Sulfametoxazol + Trimetoprim | 2 | 50% |
| Clindamicina | 2 | 50% |
| Gentamicina | 0 | 0% |
| Linezolida | 0 | 0% |
| Teiclopanina | 0 | 0% |
| Vancomicina | 0 | 0% |
| Tigeciclina | 0 | 0% |
| Ácido Fusídico | 0 | 0% |
| Rifampicina | 0 | 0% |
FONTE: Banco de dados do Laboratório de Análises Clínicas Acqualitybio no período de janeiro a junho de 2017
A Klebsiela ocytoca, apresentou maior resistência à Ampicilina, em 66,66% das uroculturas onde a bactéria foi encontrada. Na segunda colocação estão Piperacilina + Tazobactam, Cefalotina, Cefuroxima, Cefuroxima Axetil, Ceftriaxona, Cefepima, Ácido Nalidíxico, Ciprofloxacina, Norfloxacina, Nitrofurantoína e Sulfametoxazol + Trimetoprim, em 33,33% das uroculturas. Não houve resistência a Amoxicilina + Ácido Clavulânico, Ertapeném, Meropeném, Amicacina, Gentamicina, Ceftazidima e Ampicilina + Sulbactam (Tabela 7).
TABELA 7- Antibióticos a que a bactéria Klebsiela ocytoca apresentou resistência
| Antibiótico | Total de 3 | % |
| Extended-Spectrum Betalactamase positivo | 1 | 33,33% |
| Ampicilina | 2 | 66,66% |
| Cefuroxima | 1 | 33,33% |
| Cefuroxima Axetil | 1 | 33,33% |
| Ceftriaxona | 1 | 33,33% |
| Cefepima | 1 | 33,33% |
| Ciprofloxacina | 1 | 33,33% |
| Cefalotina | 1 | 33,33% |
| Ácido Nalidíxico | 1 | 33,33% |
| Norfloxacina | 1 | 33,33% |
| Sulfametoxazol + Trimetoprim | 1 | 33,33% |
| Nitrofurantoína | 1 | 33,33% |
| Ceftazidima | 0 | 0% |
| Piperacilina + Tazobactam | 0 | 0% |
| Gentamicina | 0 | 0% |
| Ampicilina + Sulbactam | 0 | 0% |
| Amoxicilina + Ácido Clavulânico | 0 | 0% |
| Meropeném | 0 | 0% |
| Amicacina | 0 | 0% |
| Ertapeném | 0 | 0% |
FONTE: Banco de dados do Laboratório de Análises Clínicas Acqualitybio no período de janeiro a junho de 2017
Algumas bactérias foram encontradas em apenas uma urocultura, são elas: Staphylococcus warneri, Staphylococcus saprophyticus, Staphylococcus sciuri, Enterococcus faecalis, Enterococcus sp, Serratia ficaria. O S. warneri se mostrou resistente a: Benzilpenicilina, Oxacilina, Eritromicina, Clindamicina, Rifampicina e Sulfametoxazol + Trimetoprim, no entanto o S. saprophyticus esteve resistente à: Benzilpenicilina, Eritromicina e Ácido Fusídico. Já o S. sciuri foi resistente à: Benzilpenicilina, Oxacilina e Eritromicina.
O E. faecalis apresentou resistência à: Estreptomicina Alto Nível, Eritromicina e Clindamicina, enquanto o Enterococcus sp foi resistente a praticamente todos os antibióticos testados (Benzilpenicilina, Ampicilina, Gentamicina Alto Nível, Estreptomicina Alto Nível, Ciprofloxacina, Moxifloxacina, Norfloxacina, Eritromicina, Clindamicina, Linezolida, Teiclopanina e Vancomicina), exceto um, a Tigeciclina.
A S. ficaria esteve resistente a Amoxicilina + Ácido Clavulânico, Piperacilina + Tazobactam, Cefalotina, Cefuroxima, Cefuroxima Axetil, Ceftriaxona, Cefepima, Ertapeném, Amicacina, Gentamicina, Ácido Nalidíxico, Ciprofloxacina, Norfloxacina e Nitrofurantoína, mostrando sensibilidade apenas a Sulfametoxazol + Trimetoprim e Meropeném.
Dentre as 23 uroculturas onde houve o crescimento de fungos, o mais frequente foi Cryptococcus laurentii, presente em 9 uroculturas e correspondendo a 39% dos fungos. Em segundo lugar aparece o Stephanoascus ciferrii, encontrado em 8 uroculturas e correspondendo a 35%. Em terceiro lugar estão Candida tropicalis e Trichosporon asahii, estando presentes em 3 uroculturas, correspondendo a 13% cada um.
DISCUSSÃO
Os achados do presente estudo demonstram maior frequência na presença de E. coli nos resultados de UROCULTURA EM MULHERES ATENDIDADAS EM DOIS LAB PRIVADOS DA CIDADE DE MACAPÁ (65,4% no laboratório Paulo Albuquerque – AMBULATORIAL e 56% no laboratório Acqualitybio – HOSPITALAR) corroboram com estudos realizados (MARQUES, 2015), os quais apontam alta frequência da E. coli como agente etiológico de ITU, inclusive em pacientes assintomáticos (ANS, 2011), e que por estar habitualmente presente no organismo humano e, por conta da proximidade anatômica do sistema digestivo com o canal uretral, aumentam as probabilidades de causarem ITU (FREIRE, 2015).
Embora com resultados um pouco abaixo do observado na literatura internacional, que mostra incidência de E.coli em 70% a 80% as ITU (MARQUES, 2015), sendo de 76,7% em um importante estudo internacional (NABER, 2008), e em 75% a 95% (GUPTA, 2011) dos casos de ITU não complicada, e também em relação à literatura nacional, cuja prevalência de tal bactéria foi de 90% (SANTOS, 2012), os resultados da presente pesquisa se aproximam dos dados de dois estudos, o primeiro relata 54,7% (REU, 2013) e o segundo (SANTOS, 2013) ressalta que 66% dos casos de ITU na América Latina são por E. coli em pacientes não-internadas, valor idêntico ao de um estudo da cidade de São Paulo, (ANDRADE; SADER; JONES, 2006).
Observa-se similaridade com os resultados de exames de urocultura em uma cidade do interior de São Paulo (BRAOIOS, 2009) em que houve presença de 65,97% de E. coli com patógeno principal, seguido de Klebisiella pneumoniae com 6,07%, Proteus mirabilis com 5,51%, Enterobacter sp com 2,88%, Pantoe agglomerans 1,92%, entre outros patógenos com menor frequência na amostra considerada. Embora este estudo tenha coletado dados de amostras de ambos os sexos, o sexo feminino responde por 69% dos resultados.
A E. coli também foi a bactéria mais prevalente em um estudo na cidade de Curitiba, PR (REU, 2013), com 54,7%, porém, ocorreu diferença na presença nos demais patógenos causadores de ITU: Streptococcus agalatiae (18,8%), Proteus mirabilis (5,6%), Enterococcus spp (5,2%) Staphylococcus spp (4,8%) e Klebisiella spp (3,9%).
Os achados deste estudo diferem um pouco dos achados de um outro estudo, que analisou resultados de urocultura em pacientes que desenvolveram e que não desenvolveram sintomas de ITU (BRAGGIATO, 2016). Entre as pacientes assintomáticas, o patógeno principal foi a Klebisiella (30%), seguido pela E. coli (26%), Citrobacter (11%) e Pseudomonas aeruginosa e Candida sp com 4% das amostras cada um. Dentre as pacientes sintomáticas houve identificação de E. coli em 40% das amostras, seguida por Klebisiella sp, citrobacter sp e Proteus sp com 20% das amostras cada um.
Em análise de resultados de uroculturas positivas no Distrito Federal (FREIRE, 2015), houve presença de 52,8% de E. coli, 10,7% de Streptococcus sp, 8% de Staphylococcus sp, 8% de Klebisiella sp, 3,8% de Proteus sp, 2,5% de Enterococcus sp, 0,7% de Pseudomonas sp, e 13,5% de outros patógenos, em que se conclui que houve maior variedade de ocorrências dos patógenos do que nos achados do presente estudo.
O Staphylococcus aureus foi o responsável por 31,5% dos resultados positivos de cultura de urina achados no laboratório Paulo Albuquerque e 2% dos achados no laboratório Acqualitybio. Os resultados ambulatoriais foram consideravelmente maior que os resultados de uma pesquisa (SANTANA, 2012) em São Luís, 8,9% para pacientes ambulatoriais e menor que os resultados da mesma pesquisa para pacientes hospitalares, 6%. Diferem significativamente de outro estudo cujo resultado foi de 3% em pacientes da comunidade (REIRE, 2015), e de 1% para pacientes hospitalares em um estudo de Portugal (MARQUES, 2015). Tamanha discrepância entre a prevalência de S. aureus, observada nas uroculturas realizadas por método manual deste estudo em ralação a outros estudos (MARQUES, 2015), (FREIRE, 2015), (SANTANA, 2012) pode ser consequência de contaminação das amostras durante o procedimento manual, uma vez que tal bactéria é encontrada frequentemente nas narinas e pele humanas (KLOOS; MUSSELWHITE, 1975).
O Staphylococcus sp foi encontrado em 3,1% das amostras do laboratório Paulo Albuquerque e 2% das amostras do laboratório Acqualitybio, em frequência menor do que a observada em outros estudos, sendo de 5% a 15% em um importante estudo internacional (GUPTA, 2011), 4,8% no município de Curitiba (REU, 2013), podendo chegar a 20% em Presidente Prudente (BRAOIOS, 2009). Embora com baixa prevalência nos achados do presente estudo, a ocorrência de ITU por Staphylococcus sp é comum em mulheres jovens e é a segunda mais frequente, precedida da ITU causada por E. coli (BARBERINO, 2010), (BRAGGIATO, 2016), (OLIVEIRA, 2014). Este patógeno é listado como um dos cinco principais causadores de ITU (ANS, 2011).
Nos resultados do laboratório Acqualitybio, foi encontrada maior diversidade de patógenos causadores de ITU corroborando com outro estudo (CUNHA, 2011). Além da E. coli, foram encontrados Klebsiela pneumoniae em 19%, segunda mais frequente em pacientes internadas, concordando com outros estudos, representando 40% a 50% das causas de ITU em ambiente hospitalar em conjunto com outros patógenos como Pseudomonas aeruginosa, Enterococcus faecalis e Klebsiella sp. (FREIRE, 2015). E em consideravelmente maior prevalência do que o estudo de Curitiba, cujo resultado foi de 3,9% dos casos (REU, 2013).
Embora com baixa prevalência, foram encontrados nos exames de origem hospitalar, os seguintes patógenos Staphylococcus haemolyticus (7%), Klebsiela ocytoca (6%), e correspondendo a aproximadamente 2% do total, estão bactérias com apenas 1 urocultura positiva, são elas: Stapylococcus warneri, Staphylococcus saprophyticus, Staphylococcus sciuri, Enterococcus faecalis, Enterococcus sp e Serratia ficaria. Resultados semelhantes a um estudo realizado na cidade de São Luís, MA (SANTANA, 2012), e diferente de uma pesquisa na cidade de Blumenau (CUNHA, 2011), que encontrou maior distribuição das enterobactérias seguidas de Pseudomonas aeruginosa. Os autores mencionam ainda que no ambiente hospitalar os patógenos são mais variados do que nas amostras da comunidade. Tal afirmação pode ser consequência do maior uso de antibióticos em pacientes hospitalizadas, levando à seleção de bactérias, assim como maior exposição das pacientes à contaminação bacteriana (FIGURAS 1 e 3).
Considerando a eficácia dos tratamentos antimicrobianos para a ITU e a alta prevalência desta patologia na população, tem-se observado aumento na resistência dos patógenos causadores frente a estes medicamentos, os quais anteriormente apresentavam sensibilidade (OLIVEIRA, 2014), determinando um aumento considerável nos casos de resistência bacteriana aos tratamentos indicados, condição que pode resultar em um sério problema de saúde pública, posto que restringe as alternativas de tratamento de infecções bacterianas (FREIRE, 2015).
Os resultados das culturas de urina e antibiograma da presente pesquisa, quando considerado o Laboratório Paulo Albuquerque, apontaram maior resistência da E. coli à Ampicilina (42,9%), resultado idêntico ao encontrado em um estudo da Universidade Fernando Pessoa, Porto (MARQUES, 2015); esses dados, porém, foram menores que outros estudos, onde se contabilizou 47% em Salvador, 51,1% (BARBERINO, 2010) em Ceilândia (FREIRE, 2015), 52% em São Luís (SANTANA, 2012), 52,1% em Presidente Prudente (BRAOIOS, 2009); e maior que um estudo da cidade de Prudentópolis, cujo resultado foi 20% (SANTOS, 2012). Entretanto, a análise dos dados de resistência microbiana da E. coli em amostras de pacientes internadas, obtidos do sistema informatizado do Laboratório Acqualitybio, apontou resistência massiva à Ampicilina, correspondendo à 82,7% das amostras em que foi testada, resultado significativamente díspar do observado no referencial teórico selecionado para a presente discussão. Uma hipótese para tal disparidade seria o aumento da resistência da E. coli à ampicilina.
A resistência da E. coli à amicacina observada nas amostras ambulatoriais da presente pesquisa (39,1%) foi consideravelmente maior dos que os achados de uma pesquisa na cidade de Salvador, BA, cujo resultado foi 0% de resistência bacteriana à amicacina na amostra analisada (BARBERINO, 2010). Outros estudos não incluíram a amicacina nos testes (NÓBREGA, 2015; CUNHA, 2011; MARQUES, 2015; BRAOIOS, 2009). Nos resultados do laboratório Acqualitybio, a prevalência de resistência da E. coli à amicacina foi baixa, 3,44%.
A resistência da E. coli à cefalotina observada nas amostras ambulatoriais da presente pesquisa, foi de 38,7%, e cerca de 41% entre as amostras hospitalares, aproximando-se, embora ligeiramente maior, dos resultados da pesquisa em Salvador, cuja prevalência foi de 32% entre as amostras de mulheres, e consideravelmente maior em um estudo no Distrito Federal, que encontrou prevalência de 24,2% (FREIRE, 2015). Nossos resultados hospitalares se assemelharam aos resultados observados em estudo na cidade de São Luís, 41% (SANTANA, 2012); e em Presidente Prudente 41% (BRAOIOS, 2009), e consideravelmente maior que em outro estudo, cuja prevalência de resistência foi de 13,8% (MARQUES, 2015). A resistência à cefalotina não foi testada em dois estudos (SANTOS, 2012; CUNHA, 2011).
A menor resistência da E. coli observada na presente pesquisa, para amostras de pacientes não internadas, foi frente ao cefepime, 17,8%, bem maior que a resistência obtida em análises de uma pesquisa em Portugal, 3,1% (MARQUES, 2015), e a outro estudo em São Paulo, cujo resultado foi de 3,2% de amostras de E. coli resistentes ao cefepime (BRAOIOS, 2009), e houve um estudo em que não foram encontradas amostras resistentes (BARBERINO, 2010). Chama a atenção a prevalência de resistência da E. coli ao cefepime nas amostras hospitalares, cerca de 52%, sendo o presente dado mais alto de todos os referenciais teóricos que subsidiaram esta pesquisa. A resistência da E. coli ao cefepime não foi testada em algumas pesquisas (SANTOS, 2012; SANTANA, 2012; FREIRE, 2015).
Ainda considerando os resultados das amostras hospitalares, observa-se altos índices de resistência bacteriana da E. coli aos diversos antibióticos testados, principalmente às cefalosporinas de 2ª, 3ª e 4ª gerações: cefuroxima 52%; ceftrixona 52%; ceftazidima 17,4%; cefoxitina 3,44%; e cefepime 52%, recomendadas para utilização em casos de infecções mais graves, cujo critério de prescrição deve ser meticulosamente analisado para evitar o incremento da resistência bacteriana, o que diminuiria o leque de medicações disponíveis para o tratamento de infecções graves (GUPTA, 2011).
Além das cefalosporinas, a resistência da E. coli foi bastante alta ao sulfametoxazol + trimetoprim, 62%, mais significante que os achados do estudo em Salvador, 37% (BARBERINO, 2010); e Distrito Federal, 39,6% (FREIRE, 2015) – embora ambos tenham sido realizados com amostras da comunidade – e cerca de 25% em um outro estudo (CUNHA, 2011); e ao ciprofloxacino, 58,6% , resultado maior que o observado em estudos em Salvador, 10% (BARBERINO, 2010); Presidente Prudente, 14% (BRAOIOS, 2009; Distrito Federal, 20% (FREIRE, 2015; São Paulo 26,5% (NÓBREGA, 2015), e absolutamente maior que em estudo realizado no PR, em que não foi observada resistência ao ciprofloxacino (SANTOS, 2012).
Chama a atenção a resistência frente à nitrofurantoína nas amostras ambulatoriais, que alcança 27,65%, valor similar a um estudo etíope (KIBRET, 2014), que constatou 25% de resistência, porém muito acima dos valores encontrados em estudos brasileiros, como um estudo mato-grossense, cujo resultado foi de 19% (MACHADO, 2016) e de um estudo em gestantes, que constatou 9,37%, de um estudo em gestantes em Prudentópolis, onde a resistência era de 4,44%, além de um estudo catarinense, onde o antimicrobiano a que apresentava menor resistência era a nitrofurantoína, com apenas 1,6% (Dias, 2015).
A fosfomicina não foi testada nas uroculturas avaliadas por este estudo, fato esse que chama a atenção devido às baixas taxas de resistência a esse fármaco (NABER, 2008), além da comodidade terapêutica proporcionada pelo tratamento por via oral, em esquema de única dose.
CONCLUSÃO
A ITU tem alta prevalência na população e, considerando a eficácia dos tratamentos antimicrobianos para ITU, tem-se observado aumento na resistência dos patógenos causadores frente a estes medicamentos, os quais anteriormente apresentavam sensibilidade. Isso determina um aumento considerável nos casos de resistência bacteriana aos tratamentos indicados, condição que pode resultar em um sério problema de saúde pública, posto que restringe as alternativas de tratamento de infecções bacterianas.
É desaconselhável o uso de antimicrobianos em prescrições empíricas no tratamento de infecções bacterianas em que é notória as taxas de resistência superiores a 20%, sendo assim é mandatória a importância do conhecimento do perfil de susceptibilidade na escolha da antibioticoterapia empírica.
O desenvolvimento de estudos que delimitem as prevalências regionais de uropatógenos, assim como seu perfil de resistência a antibióticos é extremamente importante. Esse conhecimento permite à comunidade médica local realizar uma escolha consciente quanto à terapêutica adequada, dentre as diversas, considerando o padrão de resistência local.
REFERÊNCIAS
ANDRADE, Soraya S; SADER, Helio S; JONES, Ronald N. Increased resistance to first-line agents among bacterial pathogens isolated from urinary tract infections in Latin America: time for local guidelines? Memórias do Instituto Oswaldo Cruz, Rio de Janeiro, v. 7, nov. 2006.
ASSOCIAÇÃO MÉDICA BRASILEIRA E AGÊNCIA NACIONAL DE SAÚDE SUPLEMENTAR. Diretrizes clínicas na saúde suplementar: Bacteriúria Assintomática. Brasília: Ans, 2011. 10 p. (AMB / ANS, 2011)
BARBERINO, M. G. M. de A. Prevalência de Resistência a Antimicrobianos e Uso de Testes Rápidos no Diagnóstico das Infecções do Trato Urinário Adquiridas na Comunidade. 2010. 100 f. Dissertação (Mestrado) – Curso de Biotecnologia em Saúde e Medicina Investigativa, Centro de Pesquisa Gonçalo Moniz, Fundação Osvaldo Cruz, Salvador, 2010.
BAUMGARTEN, M. C. S; et al. Infecção Urinária na Gestação: uma Revisão da Literatura. UNOPAR Cient Ciênc Biol Saúde, v.13, p.333-342, 2011.
BORGES, A. A; MAGALHÃES, L. G; JABUR, A. P. L; et al. Infecção Urinária em Gestantes Atendidas em um Laboratório Clínico de Goiânia-Go Entre 2012 e 2013. Estudos. Goiânia, v. 41, n. 3, p. 637-648, jul./set. 2014
BRAGGIATO, C. DA R.; LAZAR, C. A. E. L. Infecção do trato urinário não complicada na mulher: relato de caso e revisão da literatura. Revista da Faculdade de Ciências Médicas de Sorocaba, Sorocaba, v. 18, n. 4, p.231-234, dez. 2016. Portal de Revistas PUC SP. http://dx.doi.org/10.5327/z1984-4840201623669.
BRAOIOS, A. et al. Infecções do trato urinário em pacientes não hospitalizados: etiologia e padrão de resistência aos antimicrobianos. Jornal Brasileiro de Patologia Médica Laboratorial, Jataí, v. 45, n. 6, p.449-456, nov. 2009.
CUNHA, A. J.; VEBER, L. M. Perfil e nível de resistência bacteriana em amostras isoladas de infecções do trato urinário de clientes de um laboratório de análises clinicas. 2011. 35 f. Monografia (Especialização) – Curso de Pós-graduação em Doenças Infecciosas e Parasitárias, Centro de Ciências da Saúde, Universidade Regional de Blumenau, Blumenau, 2011.
DEMILIE, T; BEYENE, G; MELAKU, S. et al. Urinary Bacterial Profile and Antibiotic Susceptibility Pattern among Pregnant Women in North West Ethiopia. Ethiop J Health Sci, v. 22, n. 2, jul. 2012
DIAS, I.O.V; COELHO, A.M; DORIGON, I. Infecção do trato urinário em pacientes ambulatoriais: prevalência e perfil de sensibilidade aos antimicrobianos em estudo realizado de 2009 a 2012. Revista Saúde (Santa Maria), v.41, n.1, jan./jul. 2015
FILHO, A. C; CAMARGO, A. C; BARBOSA, F. A, et al. Estudo do perfil de resistência antimicrobiana das infeções urinárias em mulheres atendidas em um hospital terciário. Rev Bras Clin Med. São Paulo, abr./jun. 11(2): 102-7, 2013
FOCACCIA, ROBERTO ET al (Ed.). Veronesi: Tratado de infectologia. 5. ed. Belo Horizonte: Atheneu, 2015. 2 v.
FREIRE, J. O. Perfil de suscetibilidade de escherichia coli isoladas em uroculturas em um laboratório ambulatorial do Distrito Federal. 2015. 38 f. TCC (Graduação) – Curso de Farmácia, Unb, Ceilância, 2015.
GUPTA, K. et al. International Clinical Practice Guidelines for the Treatment of Acute Uncomplicated Cystitis and Pyelonephritis in Women: A 2010 Update by the Infectious Diseases Society of America and the European Society for Microbiology and Infectious Diseases. Clinical Infectious Diseases, [s.l.], v. 52, n. 5, p.103-120, 1 mar. 2011. Oxford University Press (OUP). http://dx.doi.org/10.1093/cid/ciq257.
KIBRET, M.; ABERA, B. Prevalence and antibiogram of bacterial isolates from urinary tract infections at Dessie Health Research Laboratory, Ethiopia. Asian Pacific Journal Of Tropical Biomedicine, [s.l.], v. 4, n. 2, p.164-168, fev. 2014. Elsevier BV. http://dx.doi.org/10.1016/s2221-1691(14)60226-4.
KLOOS, Wesley E.; MUSSELWHITE, Margaret S.. Distribution and Persistence of Staphylococcus and Micrococcus Species and Other Aerobic Bacteria on Human Skin. American Society For Microbiology, Raleigh, v. 30, n. 3, p.381-395, set. 1975.
LENZ, L. L. Bacteriúria assintomática: Artigo de revisão. Arquivos Catarinenses de Medicina, Balneário de Camboriú, v. 35, n. 4, p.7-10, fev. 2006.
MACHADO, S. T; PEREZ, G. T; SANTOS, A. L. V. S; Et al. Análise de resultados de urocultura e antibiograma em amostras suspeitas de infecção urinária em Barra do Garças – MT. Interdisciplinar: Revista Eletrônica da UNIVAR, v. 1, p. 147-163, 2016
MARQUES, B. M. L.. Avaliação dos perfis de resistência a antibióticos em Escherichia coli provenientes de infeções urinárias adquiridas na comunidade. 2015. 112 f. Dissertação (Mestrado) – Curso de Microbiologia, Faculdade de Ciências da Saúde da Universidade Fernando Pessoa, Universidade Fernando Pessoa, Porto, 2015.
NABER, Kurt G. et al. Surveillance Study in Europe and Brazil on Clinical Aspects and Antimicrobial Resistance Epidemiology in Females with Cystitis (ARESC): Implications for Empiric Therapy. European Urology, [s.l.], v. 54, n. 5, p.1164-1178, nov. 2008. Elsevier BV. http://dx.doi.org/10.1016/j.eururo.2008.05.010.
NÓBREGA, MÔNICA MARTINS. Bacteriúria em mulheres após estudo urodinâmico: fatores de risco e análise microbiológica. 2015. 70 f. Dissertação (Mestrado) – Curso de Pesquisa em Cirurgia, Faculdade de Ciências Médicas da Santa Casa de São Paulo, Sao Paulo, 2015.
OLIVEIRA, A. L. D. ET AL. Mecanismos de resistência bacteriana a antibióticos na infecção urinária. Revista Uninga Review, Maringá, v. 20, n. 3, p.65-71, dez. 2014.
REMONATTO, Gabriela. Correlação entre concentração inibitoria minima e niveis urinários de antimicrobianos para o tratamento de infecções do trato urinário. 2006. 67 f. Dissertação (Mestrado) – Curso de Pos Graduação em Ciencias Farmaceuticas, Universidade Federal do Rio Grande do Sul, Porto Alegre, 2006.
REU, C. E. Incidência de bactérias causadoras de infecção urinária em pacientes atendidos pelas unidades de saúde do município de curitiba e análise genética de Escherichia coli Uropatogênica. 2013. 75 f. Dissertação (Mestrado) – Curso de Pós- Graduação em Ciências Farmacêuticas, Área de Concentração em Análises Clínicas, Setor de Ciências da Saúde, Universidade Federal do Paraná, Curitiba, 2013.
SANTANA, TATIANA CRISTINA FONSECA SOARES De et al. Prevalência e resistência bacteriana aos agentes antimicrobianos de primeira escolha nas infecções do trato urinário no município de São Luís-MA. Revista de Patologia Tropical, [s.l.], v. 41, n. 4, p.409-418, 18 dez. 2012. Universidade Federal de Goias. http://dx.doi.org/10.5216/rpt.v41i4.21704.
SANTOS, N. Q; A resistência bacteriana no contexto da infecção hospitalar. Texto Contexto Enfer 2003: 13 (n.esp); 64-70
SANTOS, T.K.P; SANCHES, I.T; PITTNER, E, et al, Identificação e perfil antimicrobiano de bactérias isoladas de urina de gestantes atendidas na Irmandade da Santa Casa de Misericórdia de Prudentópolis, Paraná. Semina: Ciências Biológicas e da Saúde, Londrina, v. 33, n.2, p. 181-192, jul./dez. 2012
SORLOZANO, A. ET AL. Evolution of the resistance to antibiotics of bacteria involved in urinary tract infections: A 7-year surveillance study. American Journal Of Infection Control, [s.l.], v. 42, n. 10, p.1033-1038, out. 2014. Elsevier BV. http://dx.doi.org/10.1016/j.ajic.2014.06.013.
TAVARES, W.ET AL. Antibióticos e Quimioterápicos para o clínico. 3. ed. Rio de Janeiro: Atheneu, 2009. 599 p.
[1] Especialista em Ginecologia e Obstetrícia pela Universidade Federal do Amapá e graduação em Medicina pelo Instituto de Ciências Médicas de Santiago de Cuba.
[2] Mestre em Ginecologia e Obstetrícia pela Universidade de São Paulo (USP) e Médico Especialista em Ginecologia e Obstetrícia pela Universidade Federal do Pará (UFPA).
[3] Acadêmica do 10º período do curso de Medicina da Universidade Federal do Amapá (UNIFAP).
[4] Acadêmico do 10º período do curso de medicina da Universidade Federal do Amapá (UNIFAP).
[5] Acadêmica do 8º período do curso de Medicina da Universidade Federal do Amapá (UNIFAP).
[6] Acadêmica do 8º período do curso de Medicina da Universidade Federal do Amapá (UNIFAP).
[7] Acadêmica do 10º período do curso de Medicina da Universidade Federal do Amapá (UNIFAP).
Enviado: Maio, 2019.
Aprovado: Outubro, 2019.

