ARTIGO ORIGINAL
FILLOS, Letícia [1]
FILLOS, Letícia. Alterações histomorfométricas da mucosa do Íleo distal em ratos diabéticos. Revista Científica Multidisciplinar Núcleo do Conhecimento. Ano 06, Ed. 06, Vol. 16, pp. 05-22. Junho de 2021. ISSN: 2448-0959, Link de acesso: https://www.nucleodoconhecimento.com.br/saude/ratos-diabeticos
RESUMO
O Diabetes Mellitus tipo 1 é um grave problema de saúde que acomete cerca de 7% dos brasileiros, causando, além de outras doenças, alterações no trato gastrointestinal, particularmente na morfometria das vilosidades intestinais. Nessa perspectiva, esta pesquisa teve por objetivo avaliar as alterações histomorfométricas da mucosa do íleo distal em ratos com Diabetes Melittus induzido por estreptozotocina. Foram comparados, para tanto, dois grupos de 15 animais cada, durante nove semanas. Em um grupo foi administrado estreptozotocina intraperitoneal para indução de diabetes mellitus e, o outro grupo, foi mantido normoglicêmico para controle. Após nove semanas, o íleo foi removido e encaminhado para análise histológica. Foram analisados o peso corporal, a glicemia média, peso intestinal e o comprimento de vilosidades, criptas e mucosas. O grupo de ratos diabéticos apresentou menor peso corporal, maior glicemia média, maior peso intestinal e aumento da espessura da mucosa ileal. Esse aumento de comprimento de vilosidades e criptas ileais indicam, portanto, uma hiperplasia intestinal.
Palavras-chave: Diabetes Melllitus, íleo, mucosa, vilosidades, hiperplasia.
1. INTRODUÇÃO
Os primeiros registros que mencionam a patologia Diabetes datam de aproximadamente mil e quinhentos anos antes de Cristo em um documento médico egípcio chamado papiro Ebers. Posteriormente, no ano 80 da era cristã, a nomenclatura da doença foi escolhida por Aretaeus, médico romano que a relatou como uma moléstia, cujos principais sintomas eram eliminação copiosa de urina, sede incontrolável, polifagia e emagrecimento. O termo diabetes vem do grego e significa “passar através de”, pelo fato da poliúria, um dos sintomas mais aparentes da doença, se assemelhar à drenagem de água. Já o termo Mellitus vem de “mel”, o que remete à íntima relação com o aumento da glicose no sangue (ARDUINO, 1980).
No ano 1020, o médico árabe Avicena mencionou a associação de açúcar na urina a essa doença, pelo fato de, ao redor da cama de seus pacientes, se aglomerarem muitas formigas. Contudo, foi somente em 1869 que o cientista Langherans descobriu as ilhotas do tecido pancreático, que mais tarde seriam a base para um maior entendimento da doença e estudo das principais terapêuticas que conhecemos atualmente (ARDUINO, 1980).
O Diabetes Mellitus (DM) inclui um grupo de doenças metabólicas caracterizadas por hiperglicemia, resultante de defeitos na secreção de insulina ou em sua ação. Dados da Organização Mundial da Saúde (OMS) têm apontado para um aumento considerável da prevalência do DM no mundo, uma vez que a doença tem sido responsável, atualmente, por cerca de 5% das mortes globais ao ano. O Brasil é o quarto país com maior número de diabéticos do mundo. Segundo o Ministério da Saúde, são 12,5 milhões (aproximadamente 7%) de brasileiros afetados. Além de provocar um aumento na taxa de mortalidade, o DM causa grande impacto nos gastos em saúde, onerando os serviços públicos.
O DM do tipo 1 pode ser induzido experimentalmente por fármacos, como a estreptozotocina (STZ), que tem propriedades antitumorais e é usada para tratamento de determinados tipos de câncer de pâncreas. A droga é captada pelas células pancreáticas, as quais possuem transportadores de glicose GLUT-2. Assim, células produtoras de insulina que não expressam esse transportador são consideradas resistentes à estreptozotocina.
Dois mecanismos são propostos para explicar a citotoxicidade produzida pela STZ e um quadro diabetogênico: um deles é a alcalinização do DNA celular e subsequente ativação da poli-ADP ribose sintetase, que causa depleção rápida e letal de NAD nas células pancreáticas, com subsequente redução no nível de ATP e posterior inibição da síntese e secreção da insulina. O outro mecanismo diz respeito aos radicais livres, que também podem ter um papel essencial, por causar dano irreversível direto nas células beta pancreáticas e levar a um quadro semelhante ao que ocorre no diabetes mellitus tipo 1 (SILVA et al, 2011).
Embora sejam constatados muitos avanços nos estudos sobre o Diabetes Mellitus, ainda hoje a doença é uma das principais causas de incapacitação física para o trabalho, tornando o seu portador 25 vezes mais propenso à cegueira, 17 vezes mais susceptível à nefropatia, com chances cinco vezes maiores de uma amputação de membros e o dobro de risco de uma doença cardiovascular (LA PORTE, 1985; KRÓLEWSKI, 1987).
Ainda que estas sejam as principais comorbidades associadas ao DM, mais de 75% dos pacientes acometidos também relata algum distúrbio do trato gastrointestinal associado, principalmente em fases mais tardias do DM, por conta de um descontrole glicêmico. São distúrbios manifestados por má absorção, secreção anormal de nutrientes e motilidade gastrointestinal perturbada (RODRIGUES; MOTTA, 2012).
Frente a essa realidade, torna-se imprescindível uma melhor compreensão das alterações histomorfológicas do intestino delgado em indivíduos diabéticos e a formulação de uma hipótese para tal acontecimento. Nessa perspectiva, o presente estudo teve por objetivo quantificar as alterações morfológicas da mucosa do íleo de indivíduos com Diabetes Melittus induzido por estreptozotocina. Foi realizada, para tanto, uma experiência com ratos, nos quais foi induzido o DM e realizado um estudo mais aprofundado no intestino delgado, mais especificamente do íleo desses animais.
2. MATERIAIS E MÉTODOS
O experimento foi realizado de acordo com a legislação brasileira sobre o uso científico de animais (lei 11.794, de 8 de outubro de 2008). O processo de número 017/2018 foi aprovado pela Comissão de Ética no Uso de Animal (CEUA), da Universidade Estadual de Ponta Grossa (UEPG). Na investigação, foram mantidos ratos da raça Wister em 6 gaiolas, sendo 5 em cada uma, totalizando 30 animais machos, oriundos do Biotério Central da UEPG. Quando colocados nas gaiolas, os animais estavam com 90 dias de vida e peso médio de 332g. Durante o período de análise, o ambiente manteve-se com temperatura e umidade controlada, com água e ração “ad libitum”. Os ratos foram avaliados por 9 semanas consecutivas, tomando-se como base o peso corporal e a glicemia.
Do total de animais, foram escolhidos aleatoriamente 15 ratos, os quais, primeiramente, foram mantidos em jejum por 4 horas, antes de receberem a primeira dose do agente diabetizante. Na ocasião, os animais foram pesados e sua glicemia capilar na cauda foi aferida. Um único corte na extremidade da cauda dos animais foi suficiente para a coleta. Em cada um dos ratos foi, então, administrada 40 mg/kg de estreptozotocina (40g/L), diluída em soro fisiológico, através de injeção peritoneal. Essa dose foi escolhida conforme protocolos descritos na literatura.
No segundo dia, a glicemia desses animais foi aferida da mesma maneira. Os que apresentaram valor abaixo de 150 mg/dL receberam novamente a injeção com a mesma dose inicial de 40 mg/kg de estreptozotocina; aqueles que apresentaram glicemia entre 150 e 250 mg/dL receberam uma dose fracionada de 20mg/kg; e os animais que apresentaram glicemia acima de 250mg/dl não tiveram nova administração do fármaco, pois já apresentavam valores de glicemia considerados ideais para o prosseguimento do estudo.
No sétimo dia do experimento, foi realizada uma terceira aferição da glicemia para comprovar o estabelecimento do modelo de rato diabético, ou seja, com glicemia capilar acima de 200 mg/dL. Os animais investigados que não desenvolveram diabetes mellitus tipo I foram descartados do experimento. Dos animais restantes passou-se a aferir a glicemia capilar duas vezes por semana. Quando apresentavam glicemia acima de 350 mg/dL, recebiam Insulina Glargina na dose de 3 UI subcutânea, no intuito de evitar uma provável cetoacidose diabética e a consequente morte do animal.
Após a obtenção dos indivíduos diabéticos, os 30 animais inicialmente tomados na investigação foram divididos em 2 grupos: controle (n=15) e diabético (n=12), considerando que um rato morreu durante o experimento e dois não desenvolveram diabetes.
Após nove semanas, os 27 ratos foram submetidos à eutanásia com superdosagem de anestesia geral (xilazina e quetamina intraperitoneal). O intestino delgado deles foi então retirado e segmentado em duodeno, jejuno e íleo. Para o presente estudo, foi selecionado o segmento ileal, que foi pesado com uma balança de precisão. Após a pesagem, o lúmen foi aberto e, na sequência, isolado um fragmento de íleo com distância média de 1 cm da válvula ileocecal. Por fim, a peça foi fixada em isopor e armazenada em formol 10%.
Para a confecção das lâminas, foi realizada a desidratação dos tecidos em álcool etílico, retirando o solvente de hora em hora e aumentando gradativamente sua concentração. Após este processo, foram realizados dois banhos com Xilol.
Em seguida, o Xilol foi substituído por parafina fundida em pequenos blocos para fixar o material e cada bloco foi catalogado para proceder à identificação das peças. Quando os blocos secaram, foram obtidos cortes com 5 a 6 micrômetros de espessura com auxílio do micrômetro. As fitas obtidas foram transferidas para um banho-maria, para serem distendidas. Os melhores cortes foram selecionados e transferidos para as lâminas de vidro.
Para corar as peças incluídas, foi necessário hidratá-las com banhos de Xilol, álcool e água, nessa sequência, com posterior coloração com Hematoxilina e Eosina.
Tomando como base um corte transversal, cada peça foi submetida à técnica da Hematoxilina e Eosina, sendo realizadas as medidas histomorfométricas. Levando-se em consideração que cada lâmina apresenta o íleo de um animal diferente, foram medidos os comprimentos de 3 vilosidades do íleo por lâmina, sendo selecionadas aquelas com a estrutura mais preservada. Além disso, foram medidas 3 espessuras da camada mucosa e profundidades das criptas, seguindo o mesmo princípio descrito anteriormente. A figura 1 a seguir exemplifica como foram feitas as medidas.
Figura 1. As fotos apresentam a histologia do íleo pela técnica Hematoxilina e Eosina. A foto 1 exemplifica o íleo do grupo controle e, a foto 2, exemplifica o íleo do grupo diabético. A medida em amarelo apresenta a profundidade da cripta; a medida em preto a espessura da mucosa, a medida em vermelho, o comprimento da vilosidade.
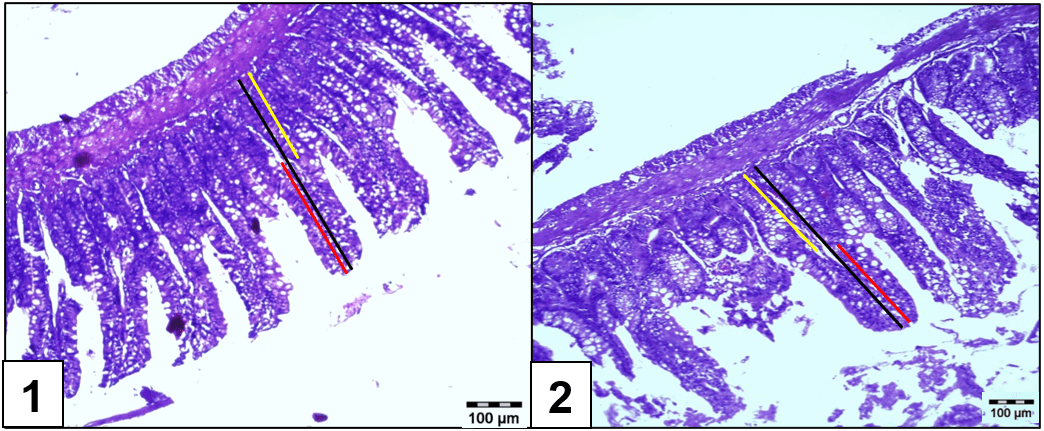
Para padronizar as medidas das vilosidades, foi tomado como ponto de início o ápice da vilosidade, seguindo a linha média da estrutura, visando não ter angulações, até a base da vilosidade. A profundidade da cripta foi obtida tomando-se como ponto inicial o fim da estrutura da vilosidade até a muscular da mucosa. Já o comprimento da espessura da mucosa foi obtido do ápice da vilosidade até a muscular da mucosa, levando com consideração os critérios utilizados com as medidas das vilosidades.
Por fim, as imagens das lâminas foram digitalizadas por meio do programa CellSens Standard. Os dados morfométricos referentes à microscopia foram obtidos com auxílio do software imageJ, procedendo-se, então, a tabulação dos resultados. A análise estatística foi realizada pelo teste t de Student de forma paramétrica e foi adotado um valor de p<0,05 para resultados estatisticamente significativos.
3. RESULTADOS E DISCUSSÃO
Inicialmente, conforme já mencionado, o grupo era constituído por 30 ratos, que foram subdivididos em dois grupos. Dos 15 ratos selecionados para receberem a injeção de estreptozotocina (40mg/kg) intraperitoneal, observou-se que: no segundo dia do experimento, 4 ratos tiveram a glicemia acima de 250 mg/dL; 4 mostraram glicemia ente 150 e 250 mg/dL, sendo, então, submetidos a uma segunda dose fracionada de 20 mg/kg de estreptozotocina; e 7 ratos apresentaram glicemia inferior a 150 mg/dL, os quais receberam novamente a segunda dose inicial de 40 mg/kg de estreptozotocina.
Após nova aferição da glicemia capilar, 7 dias depois, 2 ratos foram excluídos da pesquisa por apresentarem valores de glicemia inferiores a 200 mg/dL. Constatou-se, nesse dia, a morte de um rato, sem causa aparente. Assim, restaram 12 indivíduos diabéticos, além dos outros 15 indivíduos que não receberam o agente diabetizante, grupo utilizado para posterior comparação.
Os valores da glicemia dos ratos diabéticos, após a injeção de estreptozotocina foram maiores, comparados aos do grupo controle, conforme já era esperado (p<0,0001). Os valores médios de glicemia de ambos os grupos, estão dispostos na tabela 1 e no gráfico 1 a seguir:
Tabela 1. Glicemias
| Grupos do estudo | ||
| Controle | Diabético | |
| Glicemias (mg/dL) | 94,517±14,431a | 337,925±134,956b |
Valores expressos como média ± desvio padrão. Letras diferentes denotam diferença significativa (p<0,05). FONTE: Arquivo da autora
Gráfico 1. Média dos valores de glicemia de cada grupo obtidos durante o estudo.
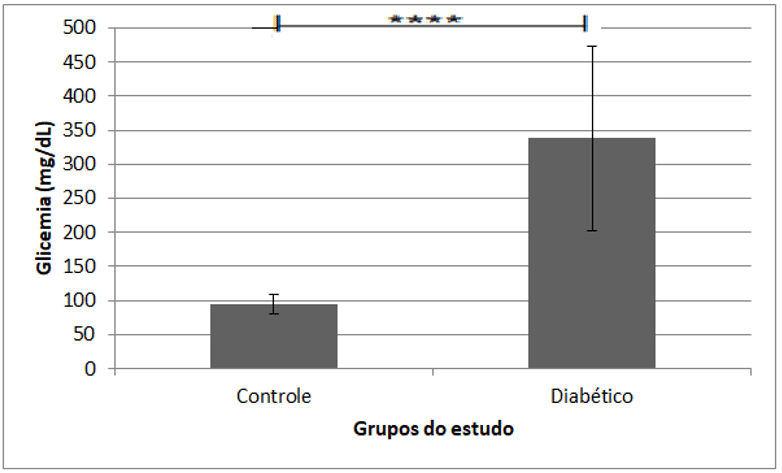
Além das medidas de glicemia, é importante ressaltar que as medidas de peso também foram importantes para o presente trabalho. Todos os ratos tiveram o peso corpóreo medido na primeira, quarta e nona semana. Após a eutanásia, com o auxílio de uma balança de precisão, também foi pesado o segmento ileal do intestino delgado de todos os animais. Os resultados estão dispostos nas tabelas e gráficos a seguir:
Tabela 2. Evolução do peso corpóreo
| Grupos do estudo | ||
| Períodos | Controle | Diabético |
| Semana 1 | 326,666±45,629 | 354±38,138 |
| Semana 4 | 344,266±48,218 | 318,333±39,825 |
| Semana 9 | 370,428±54,015a | 326,666±45,681b |
Valores expressos como média ± desvio padrão. Letras diferentes denotam diferença significativa (p<0,05). FONTE: Arquivo da autora
Gráfico 2. Evolução do peso corpóreo dos animais ao longo das semanas de experimento.
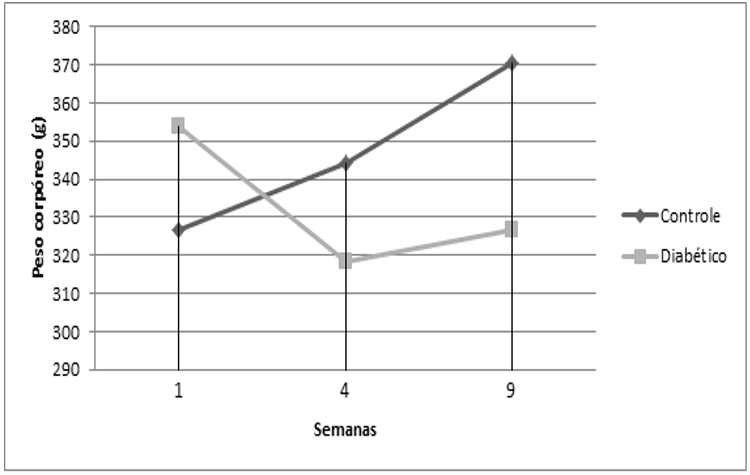
Tabela 3. Peso do segmento ileal do intestino delgado
| Grupos do estudo | ||
| Controle | Diabético | |
| Peso ileal (g) | 0,821±0,109a | 1,041±0,196b |
Valores expressos como média ± desvio padrão. Letras diferentes denotam diferença significativa (p<0,05). FONTE: Arquivo da autora
Gráfico 3. Média do peso ileal dos animais de cada grupo.
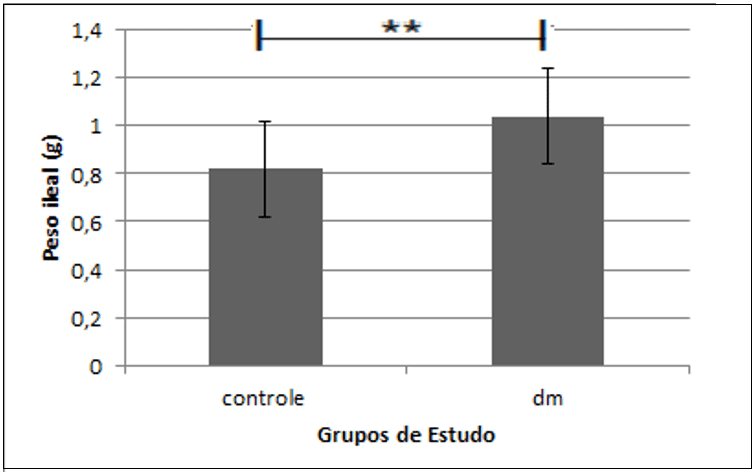
De acordo com os gráficos e tabelas acima, foi possível observar que, embora o peso corporal dos animais diabéticos tenha diminuído no decorrer do estudo (p=0,0271), em decorrência das características próprias do DM tipo 1 que levam ao emagrecimento, o peso ileal isolado foi maior no grupo diabético (p=0,0011) devido à maior massa intestinal, decorrente da hiperplasia, fato também constatado no estudo de Barbosa (2010).
Durante as 9 semanas, os ratos do grupo controle apresentaram aumento progressivo do peso corporal, em contraste com os ratos induzidos por SZT, que perderam cerca de 10% do seu peso nas primeiras 4 semanas de experimento. Entretanto, na sequência do experimento, estes voltaram a ganhar peso até a última semana de estudo, sempre em menor proporção em comparação aos ratos normais, como também observou Lerco (2003) em sua investigação:
Esses animais apresentaram, ao longo do seguimento, progressiva queda do estado geral, perda inicial de peso após a indução e ganho significativamente menor de peso em relação ao rato normal, com declínio progressivo da curva ponderal próximo ao óbito. Também observamos alteração da pelagem, aumento da circunferência abdominal, devido ao intestino grosso distendido e palpável, além de catarata bilateral e episódios freqüentes de pediculose e piodermite (LERCO, 2003).
Nessa perspectiva, entende-se que, após o surgimento dos mecanismos compensatórios que se dão por hiperfagia e alterações no epitélio intestinal, favorecendo o aumento da absorção de nutrientes, o rato hiperglicêmico consegue manter seu peso ou ainda ter aumento pouco expressivo. O principal fator que levou ao aumento do peso intestinal dos ratos diabéticos foi a hiperplasia de mucosa. Esse mecanismo compensatório pode ter como objetivo principal aumentar a absorção intestinal, a fim das células distais ao intestino obterem nutrientes.
Algumas evidências mostram que ratos que foram submetidos à indução ao diabetes tipo I sofreram um remodelamento morfológico e biomecânico no intestino, fato que altera o trânsito de alimentos, levando a uma consequente diarreia (BARBOSA, 2010).
Ainda que a análise do peso corpóreo e intestinal dos animais já tenha apresentado resultados interessantes, a presente pesquisa evidencia o crescimento das vilosidades intestinais, verificado nos animais diabéticos.
Tal assunto já foi estudado em diferentes épocas e locais, no intuito de tentar explicar o motivo de grande parte das pessoas diabéticas apresentarem algum sintoma gastrointestinal durante a evolução da doença. Esse mecanismo já foi testado com variadas drogas e em diferentes regiões do intestino delgado de ratos. Para a presente pesquisa, foi selecionado o segmento ileal, visto que é a fração intestinal que foi menos estudada isoladamente nesse aspecto até o presente momento. O fármaco estreptozotocina foi escolhido devido à resposta mais satisfatória na indução do DM, considerando o desenvolvimento da doença e a mortalidade (FERREIRA, 2017), embora tenha um maior custo em comparação com o aloxane, outro fármaco que também age de maneira semelhante.
Embora haja um estudo que mostra que não houve diferença no tamanho das vilosidades comparando os grupos controle e diabéticos (NEU, J. et al. 2005), na maioria dos trabalhos concluiu-se que houve um aumento significativo no tamanho das vilosidades do grupo diabético em relação ao grupo controle, seja considerando apenas as regiões proximais ou o intestino delgado como um todo (NODA et al, 2001; ZHAO, 2003).
No desenvolvimento do presente estudo, pode-se constatar que o padrão de alimentação dos dois grupos foi bem diferente. Embora não tenha sido feita a quantificação exata dos alimentos ingeridos pelos ratos, foi possível observar que os diabéticos comeram duas a três vezes mais rápido do que os ratos controle, e essa hiperfagia pode ser responsável pelo crescimento intestinal observado nesses animais, conforme já foi relatado no estudo de Jervis e Levin (1966). Contudo, fazendo uma análise do aspecto nutricional, também realizada por Granneman (1984) e Miller et al (1977), os dois grupos foram alimentados com a mesma dieta isocalórica. Ainda assim, os diabéticos exibiram uma maior massa intestinal e maior síntese de DNA nas células das criptas, indicando que o crescimento intestinal nos diabéticos não é causado por um único fator.
Associada à hiperfagia desencadeada pelo DM1, que leva a um desenvolvimento hiperplásico intestinal, sabe-se que a inervação intestinal também participa da regulação da proliferação celular e apoptose, proporcionando uma homeostase entre esses processos. No entanto, alguns estudos demonstram que aqueles indivíduos com neuropatia diabética apresentam prejuízos nessa regulação, contribuindo ainda mais para o aumento do volume da mucosa (ZANONI; PEREIRA, 2008).
Alguns fatores genéticos, luminais e hormonais (como o GLP2 – peptídeo semelhante ao glucagon-2) também influenciam no ritmo de proliferação celular. Desse modo, a hiperfagia pode levar a um aumento do conteúdo no lúmen, estimulando as células L, presentes no intestino delgado, a secretarem GLP2 na circulação, que teria um efeito predominantemente trófico no epitélio intestinal. Sendo assim, há uma relação direta entre a quantidade de glicose ingerida e o crescimento epitelial intestinal, além de agir estimulando a secreção de incretinas. Da mesma forma, o jejum pode diminuir o número de mitoses ao nível de cripta (OKAMOTO et al, 2014; ZHAO, 2003).
Outra explicação para o crescimento intestinal é uma temporária inibição da apoptose celular críptica, fato que também leva em consideração a idade dos animais, sendo mais significativo nos indivíduos mais velhos (NODA et al, 2001).
Em nível microscópico, conforme já indicado, trabalhamos com três medidas do íleo distal para compor os resultados histomorfométricos da pesquisa: comprimento das vilosidades, profundidade das criptas e espessura da mucosa. Os dados obtidos estão indicados na tabela a seguir:
Tabela 4. Histomorfometria do íleo distal
| Grupos do estudo | ||
| Parâmetros | Controle | Diabético |
| Comprimento de vilosidades | 322,912± 54,799 a | 378,193 ± 94,392 b |
| Profundidade de criptas | 179,724 ± 28,292 a | 228,949 ± 40,664 b |
| Espessura de mucosa | 498,918 ± 63,855 a | 596,407 ± 117,365 b |
Valores expressos como média ± desvio padrão. Letras diferentes denotam diferença significativa (p<0,05). FONTE: Arquivo da autora
Comparando-se o íleo distal do grupo controle com o grupo diabético, observa-se um aumento significativo no comprimento das vilosidades do grupo diabético (p=0,012). Essa comparação pode ser mais bem observada no gráfico 4:
Gráfico 4. Comprimento das vilosidades ileais em cada grupo
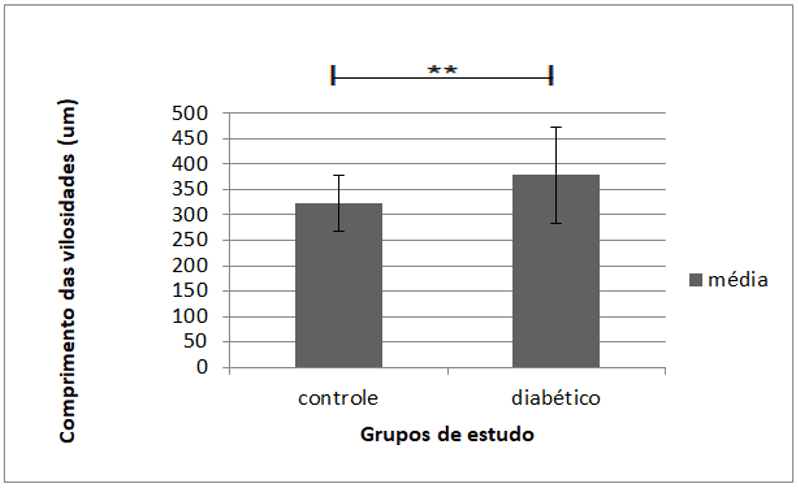
Com relação ao comprimento das criptas do íleo distal, os dados revelam que houve também um aumento expressivo da altura das criptas dos animais diabéticos em relação ao grupo controle (p<0,0001), como mostra o gráfico a seguir:
Gráfico 5: Profundidade das criptas ileais em cada grupo
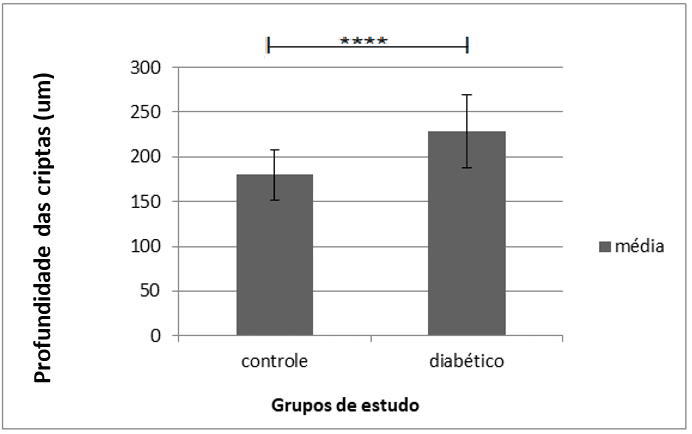
Quanto à espessura da mucosa do íleo distal, nota-se, da mesma forma, um aumento considerável da mucosa intestinal dos ratos diabéticos em relação aos ratos do grupo controle (p<0,0001), melhor observada no gráfico 6:
Gráfico 6: Espessura das mucosas ileais em cada grupo
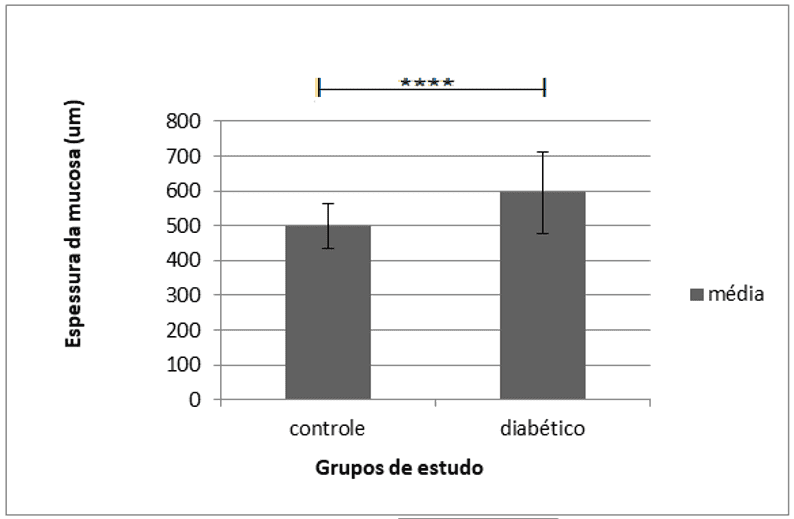
De acordo com os dados, é possível inferir que o DM induzido pela STZ pode provocar uma mudança na remodelação morfológica do íleo distal como um todo, com a proliferação de diferentes camadas, principalmente em se tratando da espessura da camada mucosa.
De forma geral, o crescimento do epitélio intestinal pode ser detalhado como um acréscimo do volume e da espessura. Como o número de vilosidades se mostrou sempre constante, o mecanismo que explica o aumento do comprimento das vilosidades intestinais é a hiperplasia das células presentes nas vilosidades, que altera o tamanho destas estruturas (OKAMOTO et al, 2014; NAKABOU et al, 1974).
Considerando a estrutura, também foi possível constatar que o DM não alterou o diâmetro ou a densidade das microvilosidades na superfície do enterócito. Conforme também constatou Zoubi (1995), “Ao passar da cripta para a vilosidade, a célula média se tornou mais alta e mais volumosa, mas, pelo menos nos animais diabéticos com STZ, não mais gorda”. Isso indica que a adaptação celular no DM se dá devido a uma maior quantidade de células epiteliais que fazem o intestino diabético crescer, confirmando a hiperplasia.
Os estudos de Jorgensen (2001) indicam que o aumento da espessura intestinal se dá por alterações nos processos de remodelação dos níveis de colágeno e pela quantidade de musculatura na parede. Essa teoria de remodelação de carga também pode explicar o alongamento intestinal causado pelo diabetes, visto que o aumento da carga luminal também gera forças na direção longitudinal.
Outra explicação para essa hiperplasia pode ser atribuída a alterações nas vias bioquímicas de estresse oxidativo. Os trabalhos realizados por Uluisik e Keskin (2017), discorrem sobre o aumento de citocinas pró-inflamatórias no estado hiperglicêmico. Dentre elas, a produção aumentada de Produtos Finais de Glicação Avançada (AGE) têm grande evidência, devido ao fato de eles serem resultantes de reações não-enzimáticas, que ocorrem aceleradamente no estado hiperglicêmico do DM. Tais moléculas também podem ser potenciais mediadores patogênicos das complicações do DM, podendo modificar as propriedades químicas e funcionais de diversas estruturas biológicas (BHOR et al., 2004; CHEN et al., 2012)
Todas essas explanações reforçam a ideia de que o processo da hiperplasia intestinal no DM1 pode acontecer por uma série de fatores que, juntos ou isolados, estão envolvidos na patogênese. Espera-se que no futuro, novos estudos mais aprofundados possam explicar, com maior clareza, o que de fato acontece no intestino dos indivíduos diabéticos.
4. CONSIDERAÇÕES FINAIS
O diabetes mellitus do tipo 1 induzido por estreptozotocina levou à hiperplasia do íleo distal, principalmente pelo aumento do comprimento de vilosidades duodenais, associado ao aumento de espessura da mucosa ileal. Esse processo é capaz de explicar algumas queixas comuns em pacientes diabéticos, dentre elas a disfagia, saciedade precoce, refluxo, constipação, dor abdominal, náusea, vômito e diarréia. Dentre as diversas razões para tais distúrbios está o aumento na absorção de nutrientes, de modo a suprir a carência de células que dependem de insulina para internalizar glicose. Contudo, como esse processo é possivelmente multifatorial, há necessidade de mais estudos para esclarecer divergências na literatura e estabelecer um mecanismo único.
REFERÊNCIAS
ARDUINO, Francisco. O diabetes ontem e hoje. Diabetes Mellitus. Rio de Janeiro: Guanabara Koogan. 1980.
BARBOSA, Rodrigo Avelaira. Aspectos morfológicos e histoquímicos do intestino delgado e ultra-estrutura de células caliciformes de ratos diabéticos-induzidos: influência da atividade física. Dissertação (Mestrado em Ciências Biológicas) – Universidade Estadual Paulista, Instituto de Biociências de Rio Claro, 2010.
BHOR, V. M; RAGHURAM, N; SIVAKAMI, S. Oxidative damage and altered antioxidant enzyme activities in the small intestine of streptozotocin-induced diabetic rats. The international journal of biochemistry & cell biology, v. 36, n. 1, p. 89-97, 2004
BRASIL. Ministério da Saúde. Secretaria de Atenção à Saúde. Departamento de Atenção Básica. Cadernos de Rastreamento. Brasília, 2010. (Cadernos de Atenção Básica, n. 29).
CHEN, Pengmin; ZHAO, Jingbo; GREGERSEN, Hans. Up-regulated expression of advanced glycation endproducts and their receptor in the small intestine and colon of diabetic rats. Digestive diseases and sciences. 2012.
FERREIRA, Rafael Carlos . Avaliação comparativa entre dois modelos de indução química de diabetes mellitus tipo 1 em ratos Wistar. Trabalho de Conclusão de Curso (Graduação em Farmácia). Centro de Ciências da Saúde, Universidade Federal da Paraíba, João Pessoa, 2017.
GRANNEMAN, J.G., STRICKER, E.M. Food intake and gastric emptying in rats with streptozotocin-induced diabetes. Am J Physiol.1984.
JERVIS, E.L.; LEVIN, R.J. Anatomic adaptation of the alimentary tract of the rat to the hyperphagia of chronic alloxan-diabetes. Nature. 1966.
JORGENSEN, C. S., AHRENSBERG, J. M., GREGERSEN, H., FLYVBERG, A. Digestive Diseases and Sciences. 2001.
KROLEWSKI, Andrzej S.; WARRAM, James H.; RAND Lawrence I., KAHN Ronald C. Epidemiologic approach to the etiology of type I diabetes mellitus and its complications. N Engl J Med. 1987.
LA PORTE, R.E. Cruickshanks: incidence and risk factors for insulin-dependent diabetes. In: Harris MI, Hamman RF. Diabetes in America. 1985.
LERCO, Mauro Masson, et al. Caracterização de um modelo experimental de Diabetes Mellitus, induzido pela aloxana em ratos: estudo clínico e laboratorial. Acta Cir. Bras.2003.
MILLER, Duane L.; HANSON, Wayne.; SCHEDL, Harold P.; OSBORNE, J.W. Proliferation rate and transit time of mucosal cells in small intestine of diabetic rat. Gastroenterology 73:1326–1332, 1977.
NAKABOU Yukihiro.; OKITA Chiyo.; TAKANO Yasuo.; HAGHIRA, H. Hyperplastic and hypertrophic changes of the small intestine. J Nntr Sci Vitami. 1974.
NEU, Josef et al. Changes in intestinal morphology and permeability in the biobreeding rat before the onset of type 1 diabetes. Journal of pediatric gastroenterology and nutrition. 2005.
NODA, Takahiro.; IWAKIRI, Ryuichi ; FUJIMOTO, Kazuma.; YOSHIDA, Toshifumi.; UTSUMI, Hiroyoshi; SAKATA, Hiroyuki.; HISATOMI, Akitaka.; AW, Tak Yee. Suppression of apoptosis is responsible for increased thickness of intestinal mucosa in streptozotocin – induced diabetic rats. Metabolism, 2001.
OKAMOTO, Jefferson Matsuiti et al. Alterações morfofuncionais intestinais no diabetes. Publ. UEPG Ci. Biologia Saúde,. 2014.
RODRIGUES, Mônica Loureiro Celino; MOTTA, Maria Eugênia Farias Almeida. Mechanisms and factors associated with gastrointestinal symptoms in patients with diabetes mellitus. J. Pediatr. 2012.
SILVA, Maisa; LIMA, Wanderson Geraldo; SILVA, Marcelo Eustáquio; PEDROSA, Maria Lucia. Efeito da estreptozotocina sobre os perfis glicêmico e lipídico e o estresse oxidativo em hamsters. Arq Bras Endocrinol Metab. 2011.
ULUISIK, Deniz.; KESKIN, Ercan. The E ects of Coenzyme Q10 on In ammation Markers in Streptozotocin-Induced Diabetic Rats. Acta Scientiae Veterinariae, 2017.
ZANONI, Jacqueline, Nelisis; PEREIRA, Renata Virginia Fernandes. Cell proliferation of the ileum intestinal mucosa of diabetic rats treated with ascorbic acid. Biocell. 2008.
ZHAO, Jianye ; YANG, Juhong; GREGERSEN, Hans. Biomechanical and morphometric intestinal remodelling during experimental diabetes in rats. Diabetologia. 2003.
ZOUBI, S.A.; WILLIAMS, M.D.; MAYHEW,T.M.; & SPARROW, R.A. Number and ultrastructure of epithelial cells in crypts and villi along the streptozotocin-diabetic small intestine: a quantitative study on the effects of insulin and aldose reductase inhibition. Virchows Archiv. 1995.
[1] Acadêmica de Medicina.
Enviado: Setembro, 2020.
Aprovado: Junho, 2021.

