ARTIGO DE REVISÃO
FINCK, Eduardo Madrid [1], SUGAWARA, Alexandre Massao [2]
FINCK, Eduardo Madrid. SUGAWARA, Alexandre Massao. Associação do uso dos inibidores de bomba de Prótons ao Câncer Gástrico. Revista Científica Multidisciplinar Núcleo do Conhecimento. Ano 06, Ed. 05, Vol. 02, pp. 26-39. Maio de 2021. ISSN: 2448-0959, Link de acesso: https://www.nucleodoconhecimento.com.br/saude/bomba-de-protons, DOI: 10.32749/nucleodoconhecimento.com.br/saude/bomba-de-protons
RESUMO
A associação dos inibidores de bomba de prótons (IBPs) ao câncer gástrico é uma informação facilmente encontrada na internet, na maioria das vezes em páginas sem caráter científico. Os IBPs são medicamentos amplamente utilizados nos distúrbios gastrointestinais, tendo o omeprazol como um dos seus representantes. Segundo o Instituto Nacional do Câncer – INCA, no Brasil, o câncer gástrico é o terceiro tipo de câncer mais frequente em homens e o quinto mais frequente em mulheres. O objetivo deste estudo é investigar à associação do uso de IBPs ao desenvolvimento de câncer gástrico. A metodologia consistiu em uma revisão integrativa da literatura seguindo a estratégia PICO na formulação da pergunta da pesquisa. O levantamento bibliográfico buscou artigos publicados que possuem como população-alvo indivíduos adultos, maiores de 18 anos, independente do sexo, que estiveram sob uso de IBPs, comparados com controles sem intervenção ou placebo, associados ao desenvolvimento do câncer gástrico. As bases de dados utilizadas foram PUBMED e BVS. Foram incluídos artigos em inglês e português, publicados entre 2017 a 2020. Esta pesquisa analisa que a relação entre os IBPs e o câncer gástrico ainda não está plenamente estabelecida. Nos casos em que se observou correlação positiva pode-se concluir, ao menos parcialmente, que o câncer gástrico é um evento de curto prazo, incluindo de menos de 1 ano de uso, suportando a ideia de que o câncer gástrico como um evento agudo.
Palavras-chaves: Inibidores de bomba de prótons, Câncer gástrico, Distúrbios gastrointestinais.
1. INTRODUÇÃO
Em uma época de notícias falsas, àquelas relacionadas à saúde humana implicam maiores riscos, pois alarmam a população para algo que cientificamente carece de comprovações.
A associação do omeprazol ao possível risco de causar câncer gástrico é facilmente encontrado na internet, em publicações de caráter duvidoso, trazendo confusão aos usuários destes inibidores de bombas protônicas. Isto constitui a motivação para este trabalho de revisão, buscando evidências científicas que confirmem ou refutem tal alegação.
Até a primeira quinzena do mês de julho de 2020, foram visualizadas no Google 464.000 resultados que associam a utilização do omeprazol ao desenvolvimento de câncer. Destaca-se que algumas das notícias que constam na primeira página de busca do Google, associam diretamente o uso do referido fármaco a esse risco.
Segundo o INCA (2020), no Brasil, o câncer gástrico é o terceiro tipo de câncer mais frequente em homens e o quinto mais frequente em mulheres. Hereditariedade, infecção pela bactéria Helicobacter Pylori, pelo vírus Epstein-Barr, idade avançada, sexo masculino, alimentação rica em sal, tabagismo, obesidade, consumo de conservantes alimentícios, anemia perniciosa, gastrite crônica atrófica, metaplasia gástrica, pólipos são as causas mais comuns de câncer gástrico (ZILBERSTEIN et al., 2013). A estimativa de novos casos para 2020 foi de 21.230 e o número de mortes em 2018 foi de 14.761.
Em 1989, por meio do omeprazol, os inibidores de bomba de prótons (IBPs) foram introduzidos na prática clínica para o tratamento de distúrbios relacionados à secreção gástrica. Quando comparados com os agentes anteriores usados para essa finalidade, como os anticolinérgicos, antagonistas de receptor de histamina 2 (H2RAs) e os análogos sintéticos de prostaglandinas, os IBPS se mostraram muito mais seguros, eficazes e tolerados pelos pacientes (STRAND; KIM; PEURA, 2017).
Aproximadamente 2 a 3 litros de secreções gástricas são produzidas diariamente, tendo a função de proteger contra patógenos externos, bem como auxiliar na digestão dos alimentos. Essa secreção é dividida em três fases (cefálica, gástrica e intestinal), sendo composta por ácido clorídrico (HCL), pepsinogênio, fator intrínseco, muco, gastrina e histamina (VANPUTTE et al., 2016).
A secreção de ácido gástrico, é realizada pelas células parietais das glândulas oxínticas localizadas nas superfícies internas do corpo e do fundo do estômago, através de uma regulação realizada por sinais endócrinos, nervosos e celulares. Quando estimuladas, as células parietais secretam solução ácida contendo cerca de 160mmol/L de HCL, com um pH ao redor de 0,8 e com uma concentração de íons hidrogênio cerca de 3 milhões de vezes maior do que a do sangue arterial. Para que ocorra a formação do ácido clorídrico nos canalículos intracelulares ramificados da célula parietal, é necessária uma sucessão de mecanismos químicos que tem como principal fonte de energia a bomba de hidrogênio-potássio (H+-K+-adenosina trifosfatase [ATPase]) (HALL, 2017).
As células parietais possuem receptores em sua membrana basolateral que respondem aos estímulos da gastrina, histamina e acetilcolina. A gastrina além de estimular a secreção ácida diretamente, ainda estimula células enterocromafínicas a secretarem histamina. Esses receptores ativados, induzem cascatas intracelulares através de segundos mensageiros. Quando a célula parietal é estimulada em resposta ao cheiro, visão ou ingestão dos alimentos, as membranas tubovesiculares onde a ATPase se encontra se fundem com a membrana dos canalículos secretórios, expondo a ATPase ao K+ extracelular, fazendo com que ela comece a secretar prótons (H+) (PELOSO, 2014).
A secreção de ácido em um indivíduo pode variar de acordo com inúmeros fatores: número de células parietais, sensibilidade das células parietais aos mecanismos regulatórios, alimentação, uso de medicamentos, hábito de fumar, estado emocional, dentre outros. O desequilíbrio da produção ácida, associado a diminuição dos mecanismos de defesa da mucosa do trato gastrointestinal, favorece o desenvolvimento de patologias como a úlcera gastroduodenal (ZATERKA; EISIG, 2016).
Os inibidores de bomba de prótons, são medicamentos amplamente utilizados para suprimir a secreção gástrica na terapêutica de distúrbios gastroesofágicos. Eles são pró–fármacos que se ativam no meio ácido do estômago, ligando-se de forma covalente aos grupos sulfidrila da H+-K+-adenosina trifosfatase [ATPase], inativando-a de forma irreversível, fazendo com que a secreção de ácido se normalize apenas com a síntese de novas ATPases (TANUS-SANTOS; PINHEIRO, 2019).
Os inibidores de bomba de prótons são capazes de manter o pH estomacal superior a 4 por 10 até 18 horas por dia. Embora a meia vida do omeprazol seja curta (até 2 horas), esses fármacos são capazes de inibir a secreção gástrica por até 4 dias, e após 5 dias de terapia continua é atingido um patamar estável de secreção ácida suprimida. Essa supressão ácida auxilia na recuperação de úlceras, inflamações da mucosa e sintomas relacionados a doença péptica (PELOSO, 2014).
Segundo Braga; Silva e Adams (2011), existem sete representantes da classe dos IBPS (omeprazol, lansoprazol, pantoprazol, rabeprazol, esomeprazol, dexlansoprazol, tenatoprazol). Todos compartilham da mesma estrutura principal e do mesmo mecanismo inibitório, sendo todos bases fracas protonáveis, variando em parte nas substituições dos grupos piridina ou benzimidazol.
Os inibidores da bomba de prótons (IBPS), classe ao qual o omeprazol pertence, têm sido vastamente utilizados no manejo terapêutico e patologias do Trato Gastrointestinal, apresenta um avanço no tratamento de úlceras pépticas Helicobacter pylori positiva ou negativa, da doença do refluxo gastroesofágico (DGRE), do esôfago de Barrett e da síndrome de Zollinger-Ellison. Tais drogas apresentam níveis satisfatórios de segurança e tolerância aos pacientes, com raros relatos de casos graves. Há relatos de nefrite intersticial que pode evoluir para insuficiência renal aguda (DELVE et al., 2003), hipomagnesia que pode levar a arritmias e convulsões e o aumento do risco de infecções (MOUCHANTAF, 2014)
Na doença do refluxo gastroesofágico as drogas de primeira escolha são os inibidores de bomba de prótons (IBP), promovendo a redução da agressão do esôfago proporcionada pelo ácido. O omeprazol é o IBP utilizado em larga escala no Brasil, sendo fornecido de forma gratuita pelo Ministério da Saúde. Vale ressaltar que os antagonistas dos receptores H2 da histamina e os procinéticos são considerados drogas de segunda escolha. Os IBPS em dose plena devem constituir o tratamento de escolha inicial por período de quatro a oito semanas. Se persistirem os sintomas nos pacientes, a dose deve ser dobrada, isto é, antes do desjejum e antes do jantar (HENRY, 2014).
É importante mencionar, o uso do omeprazol como protetor gástrico. Sartori et al. (2000) concluíram que o omeprazol se mostra efetivo na prevenção de lesões gastroduodenais, associadas ao tratamento quimioterápico contra o câncer. Regula et al. (2006) constataram que pacientes tomando anti-inflamatórios não esteroidais (AINES) continuamente, conseguem prevenir as lesões gastrointestinais, como a úlcera péptica, de forma segura e tolerada com o uso de omeprazol e pantoprazol.
Salgado et al. (2019) verificaram que 85 em cada 1.000 indivíduos tomam omeprazol ou algum derivado todos os dias na Espanha, já na Noruega 30 em cada 1.000, e 27 em cada 1.000 na Itália. Os autores também constataram que no Brasil faltam informações. A justificativa mais frequente para uso de um IBP fora dos protocolos, seria para a prevenção de gastrite em pacientes que fazem uso de vários medicamentos.
Araújo et al. (2017) comentam que os inibidores de bomba de prótons são a classe de medicamentos mais prescrita no mundo e que o uso inapropriado pode ocasionar eventos adversos a medicamentos, elevando taxas de morbidade e mortalidade, além de aumentar os custos da assistência à saúde.
Segundo um informativo do Ministério da Saúde (OMS, 1985), “[..] existe uso racional quando os pacientes recebem os medicamentos apropriados à sua condição clínica, em doses adequadas às suas necessidades individuais, por um período adequado e ao menor custo possível para eles e sua comunidade”.
2. OBJETIVO
Considerando a importância do uso racional de medicamentos, e que o omeprazol é um dos medicamentos mais utilizados no mundo, e ainda são veiculadas notícias sem evidência científica, esse estudo tem por objetivo, estabelecer à associação do uso de omeprazol, e outros IBPs, ao desenvolvimento de câncer gástrico.
3. METODOLOGIA
Foi realizada uma revisão integrativa da literatura, que possui uma abordagem metodológica mais ampla em relação aos outros tipos de revisão, sendo possível a inclusão de estudos metodologicamente. Essa metodologia foi desenvolvida para subsidiar a tomada de decisão e a melhoria da prática clínica (SOUZA et al., 2010).
Para a pesquisa foi formulada uma pergunta norteadora a partir da estratégia PICO: participantes, intervenção, comparação e resultados (outcomes). O levantamento bibliográfico buscou artigos publicados que possuem como população-alvo indivíduos adultos, maiores de 18 anos, independente do sexo, que estiveram sob uso de IBPs, comparados com controles sem intervenção, associados ao desenvolvimento do câncer gástrico.
As bases de dados utilizadas foram PUBMED e BVS. Foram incluídos artigo em inglês e português, publicados a partir de 2017 até 2020. Na estratégia de busca foram utilizados os seguintes descritores: “inibidores de bomba de prótons”, “câncer gástrico”, “próton pump inhibitors” e “gastric cancer” e seus correlatos em inglês. Relatos de caso, cartas de editores, artigos de opinião, textos de livros, trabalhos de conclusão de curso, teses e resumos em anais foram excluídos da amostra.
4. RESULTADOS E DISCUSSÃO
Pelo portal da BVS, inicialmente foram obtidos 127 artigos, foram descartados 40 estudos de revisão que não dispunham de dados objetivos, 9 duplicatas, 72 artigos sem relação aos propósitos deste estudo e 5 editoriais, restando apenas 1 artigo original, com dados objetivos de associação dos IBPs ao câncer gástrico.
Figura 1 – Estratégia de coleta de dados feita pela BVS
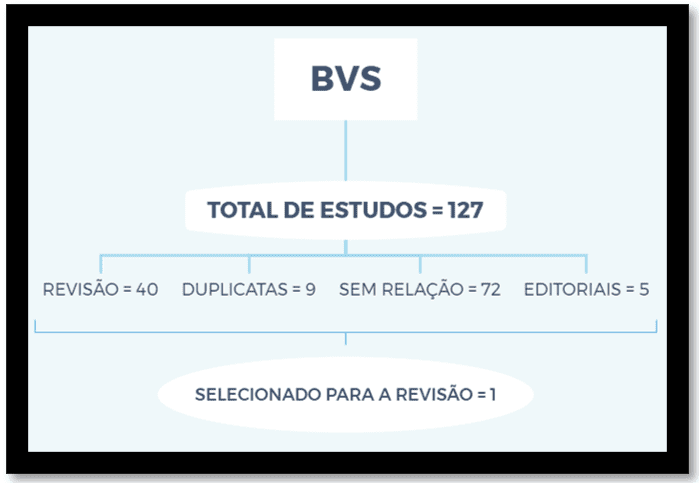
Utilizando-se da Pubmed, foram obtidos inicialmente 134 estudos, descartadas 31 revisões que não dispunham de dados objetivos, 9 relatos de caso, 13 editoriais, 72 artigos sem relação com os objetivos deste trabalho e 1 artigo em espanhol, restando 8 artigos.
Figura 2 – Estratégia de coleta de dados pela Pubmed

A amostra de artigos finalizada com 9 artigos, sendo três estudos coorte, dois estudos casos-controle, duas meta-análises, um estudo clínico retrospectivo e um estudo multicêntrico.
Os fatores de impactos das revistas foram coletados, todas com valores ao menos acima de 2.000, portanto, pode-se considerar que são revistas com grande número de citações em relação ao material publicado.
Apesar do número reduzido de artigos, retratam um quadro recente do uso de IBPs e somam em suas análises mais de 3 milhões de participantes de pesquisa.
Além de realizarem diversos métodos de estudos, os artigos também mostram diversidade da análise dos resultados, utilizando-se de Hazard Ratio (HR), taxa de incidência padronizada (SIR), Odds Ratio (OR) associados a estudos de prevalência. Em todos os estudos os dados são apresentados com intervalo de confiança de 90% e análise estatística com p menor que pelo menos 0,05.
Tabela 1 – Principais resultados dos artigos selecionados
| Referência | Fator de impacto | Tipo de estudo | Amostra | Resultados significantes |
| Cheung et al., 2017 | 19.819 | coorte | 63.397 | Uso contínuo 7,6 anos
Prevalência 0,24% HR IBP 2,44 (1,42 a 4,20) HR BH2 0,72 (0,48 a 1,07) |
| Brusselaers et al., 2019 | 2.179 | coorte | 796.425 | Uso contínuo ≥ 5 anos.
Prevalência 0,36% SIR 1 ano 7.22 (6.79–7.66) SIR 2.97 (2.83–3.10) |
| Brusselaers et al., 2017 | 2.496 | coorte | 797.067 | ³ 180 dias de uso
Prevalência 0,28% SIR = 3,38 (3,23 a 3,53). SIR £ 40 anos = 22,76, (15,94 a 31,52). |
| Lai et al., 2018 | 19.819 | caso-controle | 649 | IBP ≤ 6 anos OR 1.59 (1.24 a 2.05)
IBP > 6 OR 2.00 (1.36 a 2.95) BH2 OR 3.54 (1.91 to 6.55) |
| Lee et al., 2020 | 10.241 | caso-controle | 1.233 | IBP ³ 2 anos OR 1,07 (0,81-1,42) |
| Wan et al., 2018 | 19.819 | Metanálise | 926.386 | IBP £ 1 ano OR 4.13 (−1.80 a 10.07)
IBP ³ 3 anos 1.01 (0.51 a 1.50) |
| Jiang et al., 2019 | 3.437 | Metanálise | 943.070 | IBP ³ 36 meses OR 2,50 (1,74, 3,85) |
| Fukuda et al., 2019
|
3.626 | Retrospectivo
|
158 | Prevalência 58,6% de hiperplasia foveolar no grupo IBP vs 33,9% grupo não-IBP (p < 0,001) |
| Kiso et al., 2017
|
2.130 | Estudo multicêntrico | 1.007 | Lesões brancas. IBP OR 3.83 (1.67–8.27)
Metaplasia. IBP OR 13.72 (5.49–35.28) |
Fonte: Dos Autores, 2021
Os estudos epidemiológicos do tipo coorte descrevem a presença de eventos novos, como incidência dentro de uma população estudada durante um dado período de observação (MERCHÁN-HAMANN e TAUIL, 2021). Cheung et al., (2017) observaram uma incidência de 0,24% de câncer gástrico com o uso contínuo de IBPs por 7,6 anos. Nos estudos de Brusselaers et al., (2019), observou-se uma incidência relativamente maior de 0,36% e num intervalo de tempo inferior de uso contínuo de IBPs a partir de 5 anos. O mesmo grupo publicou em 2017 uma incidência semelhante de câncer gástrico (0,28%), porém, o surgimento do câncer gástrico foi avaliado a partir de 180 dias de uso de IBPs. Estes dados revelam que o câncer gástrico induzido por IBPs pode ser um evento de ocorrência precoce.
Cheung et al., (2017) analisaram os dados obtidos e expressaram em termos de Hazard Ratio (HR), que pode ser interpretado como o risco relativo da ocorrência do evento em função do tempo (MIOT, 2017) e obtiveram um HR de 2,44 (1,42 a 4,20). Deste modo, o uso de IBPs aumentam em 2,44 vezes o risco de desenvolver câncer gástrico. Interessante notar, que o uso dos antagonistas H2 da histamina apresentaram um HR de 0,72 (0,48 a 1,07), o que sugere efeito protetor em relação ao câncer gástrico, diminuindo o risco de ocorre-lo.
Brusselaers et al., (2017) e mais recentemente em 2019 utilizaram a metodologia taxa de incidência padronizada (SIR) que calcula a proporção de diagnósticos de câncer gástrico associado ao uso de IBPs em relação ao número de diagnósticos de câncer gástrico esperados na Suécia multiplicado por 100 (KELSEY, 1996). Em 2017 obtiveram um SIR de 3,38 (3,23 a 3,53). Assim, pode-se se dizer que com o uso de IBPs espera-se uma incidência 3,38 vezes maior de câncer gástrico. Neste mesmo estudo, considerou o cálculo de SIR para pessoas com menos de 40 anos e foi obtido um SIR de 22,76, (15,94 a 31,52), o que sugere que indivíduos mais novos podem ser mais susceptíveis ao câncer gástrico.
Em 2019 Brusselaers et al., (2019) obtiveram um SIR semelhante de 2.97 (2.83–3.10). Este estudo corrobora com o câncer gástrico induzido por IBPs ser um evento precoce, como sugere a publicação do mesmo grupo em 2017, pois foi obtido um SIR de 7.22 (6.79–7.66) no primeiro ano de uso de um IBP.
Para os demais estudos que se encontram na tabela 1, foi utilizado um modelo estatístico denominado Odds Ratio (OR). A razão de chances ou razão de possibilidades (OR), definida como a razão entre a chance de um evento ocorrer em um grupo e a chance de ocorrer em outro grupo. Chance ou possibilidade é a probabilidade de ocorrência deste evento dividida pela probabilidade da não ocorrência do mesmo evento (WAGNER e CALLEGARI-JACQUES, 1998).
No estudo de Lai et al., (2018), foi demonstrado que o uso de IBPs por 6 anos ou menos aumenta a chance de desenvolver câncer gástrico em 59%. Em contrapartida o uso por mais de 6 anos acarreta o dobro de chance de desenvolver câncer.
Um ponto peculiar no estudo de Lai et al., (2018) é que o uso dos antagonistas H2 da histamina geram mais que o triplo de chance de desenvolver o câncer, mostrando-se mais nocivo que os IBPS. Estes resultados conflitam com os estudos de Cheung et al., (2017), em que foi verificado um efeito protetor dos antagonistas H2 da histamina.
Lee et al., (2020), calcularam um Odds Ratio de 1.07 em 2 anos ou mais de uso dos IBPs, um resultado conflitante com os demais estudos de Odds Ratio, pois pode indicar que o uso de IBPs não modifica o risco de desenvolver câncer gástrico.
A grandiosa Metanálise de Wan et al, (2018), com mais de 900.000 participantes, trouxe um resultado muito curioso. Wan e colaboradores apresentaram um Odds Ratio de 4.13 quando o uso do IBP foi de 1 ano ou menos. Quando o uso do IBP se estende por 3 anos ou mais o Odds Ratio foi de 1.01.
Esses resultados significam que o uso durante um curto período gera um aumento significativo na probabilidade de desenvolver câncer gástrico. Segundo o Instituto Nacional do Câncer (INCA), o câncer é um processo multifatorial e os efeitos cumulativos dos diferentes agentes cancerígenos são responsáveis pelo início da doença, o que faz o resultado de Wan e seus colaboradores se mostrarem muito curiosos.
A também grandiosa metanálise de Jiang et al., (2019), com um número de participantes da pesquisa semelhante à pesquisa de Wan e colaboradores, mostram que o uso dos IBPs por um período de 3 anos ou mais aumenta os riscos de desenvolver a doença, com um Odds Ratio de 2.50. Novamente nota-se a tendência do câncer gástrico como um evento precoce.
Fukuda et al., (2019), realizou um estudo retrospectivo com 158 pacientes e percebeu uma prevalência maior de hiperplasia foveolar nos usuários de IBP (p<0,001). A hiperplasia foveolar é decorrente de uma regeneração da mucosa em resposta a uma agressão, porém o desenvolvimento de câncer a partir do pólipo hiperplásico é raro e por isso não é considerado como lesão pré-cancerosa (MORAIS, 2002). Mesmo assim, a hiperplasia foveolar pode ser, no futuro, um indicador de lesões induzidas por IBPs, o que auxiliaria a medicina na tomada de decisões.
Em um estudo multicêntrico, Kiso et al., (2017) identificaram lesões brancas associadas ao uso de IBP (OR 3,83) e metaplasia (OR 13,72).
A metaplasia é definida como uma alteração reversível na qual um tipo celular diferenciado (mesenquimal ou epitelial), é substituído por outro tipo celular de mesma linhagem e as influências que geram a metaplasia, quando persistentes, podem iniciar transformação maligna no epitélio metaplásico.
Da mesma forma que a hiperplasia foveolar, as lesões brancas podem ser futuros indicadores de lesões associadas aos IBPs. Porém o estudo de Kiso apresenta um intervalo de confiança demasiadamente grande e abre espaço para mais interpretações.
5. CONCLUSÕES
A relação entre os inibidores de bomba de prótons e o câncer gástrico ainda não está plenamente estabelecida, porém há estudos bem consolidados que indicam tal possibilidade. Os dados também sugerem que o câncer gástrico associado ao uso de IBPs possa ser um evento de curto prazo, diferente do que se diz sobre a história natural dos cânceres de forma geral.
Sabemos que os inibidores de bomba de prótons ajudam no combate de inúmeras condições patológicas, porém seu uso deve ser muito bem avaliado. Há a possibilidade de, no futuro, valer-se de lesões reversíveis associadas ao uso de IBPs como critério de decisão clínica para a suspensão do uso dos IBPs. Consideramos válida a sugestão de que estas pesquisas estejam em perspectivas futuras.
Convém lembrar a importância do uso racional de qualquer droga, inclusive dos inibidores de bomba de prótons. O balanço entre o risco e o benefício devem ser avaliados pelos profissionais de saúde, para que seja feito o melhor pelo paciente.
REFERÊNCIAS
BRAGA, M. P.; SILVA, C. B.; ADAMS, A. I. H. Inibidores da Bomba de Prótons: Revisão e Análise Farmacoeconômica. Ahead of Print, Rio Grande do Sul, v. 37, n. 2, p. 19-32, 2011.
BRUSSELAERS, N.; LAGERGREN, J.; ENGSTRAND, L. Duration of use of proton pump inhibitors and the risk of gastric and oesophageal cancer. Cancer Epidemiology. 62. 2019.
BRUSSELAERS, N.; WAHLIN, K.; ENGSTRAND, L.; LAGERGREN, J. Maintenance therapy with proton pump inhibitors and risk of gastric cancer: A nationwide population-based cohort study in Sweden. BMJ Open. 7. 2017.
CHEUNG, M.; WONG, A.; CHEN, L.; CHAN, E.; WONG, I.; LEUNG, W. Long-Term Use of Proton Pump Inhibitors and Risk of Gastric Cancer Development after Treatment for H. Pylori : A Population-Based Study. Gastroenterology. 152. S833, 2017.
DELVE, P.; LAU, M.; YUN, K.; WALKER, R. Omeprazole-induced acute interstitial nephritis. The New Zealand medical journal. 116. U332, 2003.
FUKUDA, M.; ISHIGAKI, H.; SUGIMOTO, M.; MUKAISHO, K.; MATSUBARA, A.; ISHIDA, H.; MORITANI, S.; ITOH, Y.; SUGIHARA, H.; ANDOH, A.; OGASAWARA, K.; MURAKAMI, K.; KUSHIMA, R. Histological analysis of fundic gland polyps secondary to PPI therapy. Histopathology. 75. 2019.
HALL, J. E. Guyton e Hall – Fundamentos de Fisiologia – 13ª Ed. Gen Guanabara Koogan, 2017.
HENRY, M. A. C. de A. Diagnóstico e tratamento da doença do refluxo gastroesofágico. ABCD, arq. bras. cir. dig., São Paulo, v. 27, n. 3, p. 210-215, Sept. 2014.
INCA. Tipos de câncer. Câncer de estômago. 2018. versão para Profissionais de Saúde. Disponível em: https://www.inca.gov.br/tipos-de-cancer/cancer-de-estomago/profissional-de-saude. Acesso em: 06 de fevereiro de 2020.
JIANG, K.; JIANG, X.; WEN, Y.; LIAO, L.; LIU, F. Relationship between long-term use of proton pump inhibitors and risk of gastric cancer: A systematic analysis. Journal of Gastroenterology and Hepatology. 34. 2019.
KELSEY J. L.; WHITTEMORE A.S.; EVANS A. S.; THOMPSON W. D. Methods in observational epidemiology. (2ª ed). Oxford University Press, Nova York, 1996.
KISO, M.; ITO, M.; BODA, T.; KOTACHI, T.; MASUDA, K.; HATA, K.; SASAKI, A.; KAWAMURA, T.; YOSHIHARA, M.; TANAKA, S.; CHAYAMA, K. Endoscopic findings of the gastric mucosa during long-term use of proton pump inhibitor – a multicenter study. Scandinavian Journal of Gastroenterology. 52. 2017.
LAI, S.; LAI, H.; LIN, C.; LIAO, K. Proton pump inhibitors and risk of gastric cancer in a case–control study. Gut. 68. 2018.
LEE, J.; MERCHANT, S.; SCHNEIDER, J.; JENSEN, C.; FIREMAN, B.; QUESENBERRY, C.; CORLEY, D. Proton Pump Inhibitor Use and Risk of Gastric, Colorectal, Liver, and Pancreatic Cancers in a Community-Based Population. The American Journal of Gastroenterology. 115. 2020.
MERCHÁN-HAMANN E.; TAUIL P. L. Proposta de classificação dos diferentes tipos de estudos epidemiológicos descritivos. Epidemiol Serv Saúde [preprint]. 2020.
MIOT H. A. Assessing normality of data in clinical and experimental trials. J Vasc Bras. 16(2):88-91. 2017.
MOUCHANTAF, R. Proton pump inhibitors: hypomagnesemia accompanied by hypocalcemia and hypokalemia. Canadian Adverse Reaction Newsletter. Volume 21, Issue 3, 2011.
PELOSO, L. J. A concentração sérica de tacrolimo após a ingestão de omeprazol: um estudo piloto. Dissertação de Mestrado em Ciências da Saúde. Faculdade de Medicina, Universidade Federal de Uberlândia, Uberlândia. MG, 2014.
RAUJO E. G. M. Riscos e benefícios do uso prolongado de Omeprazol. Revista Especialize On-line IPOG. Edição nº 14 Vol. 01, 2017.
REGULA, J.; BUTRUK, E.; DEKKERS, C.; BOER, S.; RAPS, D.; SIMON, L.; TERJUNG, A.; THOMAS, K.; LÜHMANN, R.; FISCHER, R. Prevention of NSAID-Associated Gastrointestinal Lesions: A Comparison Study Pantoprazole versus Omeprazole. The American journal of gastroenterology. 101. 1747-55, 2006.
SALGADO, A. L.; PALMA, A. L. R.; RAMOS, L. P.; et al. Uso indiscriminado de inibidores da bomba de prótons em receituários de medicamentos de uso contínuo. Brazilian Journal of health Review. São Paulo, 2019.
SARTORI, S.; TREVISANI, L.; NIELSEN, I.; TASSINARI, D.; PANZINI, I.; ABBASCIANO, V. Randomized Trial of Omeprazole or Ranitidine versus Placebo in the Prevention of Chemotherapy-induced Gastroduodenal Injury. Journal of Clinical Oncology, v. 18, n. 3, p. 463-467, 2000.
SCHLIOMA Z.; JAIME N. E. Tratado de gastroenterologia: da graduação à pós-graduação. 2. ed., São Paulo: Editora Atheneu, 2016.
SOUZA, M. T. de; SILVA, M. D. da; CARVALHO, R. de. Revisão integrativa: o que é e como fazer. Einstein (São Paulo), São Paulo, v. 8, n. 1, p. 102-106, Mar. 2010.
STRAND D. S.; KIM D.; PEURA D. A. 25 Years of Proton Pump Inhibitors: A Comprehensive Review. Gut Liver. Jan 15;11(1):27-37, 2017.
TANUS-SANTOS, J.; PINHEIRO, L. Proton pump inhibitors: New mechanisms of action. Basic & Clinical Pharmacology & Toxicology. 125, 2019.
VANPUTTE, C. L.; REGAN J.; RUSSO, A. Anatomia e fisiologia de Seeley. 10. ed. Porto Alegre: AMGH, 2016.
WAGNER, M. B.; CALLEGARI-JACQUES, S. M. Medidas de associação em estudos epidemiológicos: risco relativo e odds ratio. J Pediatr. 74. 247-251, 1998.
WAN, Q.; WU, X.; LI, N.; DU, L.; ZHOU, Y. Long-Term proton pump inhibitors use and risk of gastric cancer: A meta-analysis of 926 386 participants. Gut. 68, 2018.
WORLD HEALTH ORGANIZATION. The Rational use of drugs: report of the conference of experts. Nairóbi, 25-29 november 1985.
ZILBERSTEIN, B. et al. Consenso brasileiro sobre câncer gástrico: diretrizes para o câncer gástrico no Brasil. ABCD, arq. bras. cir. dig., São Paulo, v. 26, n. 1, p. 2-6, Mar. 2013.
[1] Discente do curso de Medicina do Centro Universitário das Américas – FAM.
[2] Mestre. Docente do curso de Medicina do Centro Universitário das Américas – FAM.
Enviado: Março, 2021.
Aprovado: Maio, 2021.