ARTIGO ORIGINAL
CORRÊA, Caroline de Paula Lopes [1], PIECHA, Camila Rios [2], ZANINI, Maria Luiza de Oliveira [3], DODE, Maria Teresa Bicca [4], RATMANN, Cristiane Wienke Raubach [5], DODE, Luciana Bicca [6], DIAZ, Patrícia Silva [7]
CORRÊA, Caroline de Paula Lopes. et al. Bioplástico colorido: corantes naturais como uma alternativa para coloração de poli(3-hidroxibutirato). Revista Científica Multidisciplinar Núcleo do Conhecimento. Ano. 08, Ed. 08, Vol. 04, pp. 25-49. Agosto de 2023. ISSN: 2448-0959, Link de acesso: https://www.nucleodoconhecimento.com.br/biologia/bioplastico-colorido, DOI: 10.32749/nucleodoconhecimento.com.br/biologia/bioplastico-colorido
RESUMO
Plásticos convencionais são grandes poluidores ambientais e, por consequência, há um interesse em materiais alternativos sustentáveis e biodegradáveis. Frente a isso, o Poli(3-hidroxibutirato) vem sendo estudado como um possível substituto. Neste trabalho, foram apresentados os resultados do desenvolvimento de filmes coloridos baseados em P(3HB) adicionados de corantes naturais comumente utilizados na indústria de alimentos, visando aumentar a variedade de aplicações do bioplástico. Os corantes páprica, urucum, mostarda e cúrcuma demonstraram capacidade em colorir o bioplástico nas diferentes concentrações testadas, permitindo uma gama de tonalidades disponíveis. Quando submetidos ao ensaio de fotodegradação, os filmes descoloriram sem, no entanto, perder a tonalidade das cores iniciais. A presença dos corantes protegeu as superfícies dos filmes, bem como sua inserção não afetou as propriedades térmicas do P(3HB). Os filmes de P(3HB) coloridos obtidos se mostram alinhados às novas concepções no desenvolvimento de materiais adequados à sustentabilidade.
Palavras-chave: Polihidroxialcanoatos, Plásticos biodegradáveis, Biopolímeros, Cores.
1. INTRODUÇÃO
Os plásticos de origem petroquímica são materiais consolidados em diversas aplicações e sua utilização inserida massivamente no cotidiano, tendo produção estimada em 390 Mt Plastics Europe (2022) sendo utilizados na produção de embalagens descartáveis e plásticos de uso único (GEYER; JAMBECK; LAW, 2017). Esse cenário de consumo acelerado, somados aos baixos índices de reciclagem e biodegradabilidade os torna um dos principais poluentes do planeta (AUTA et al., 2017; SILVA et al., 2020).
Os bioplásticos como materiais alternativos aos plásticos petroquímicos, têm contribuído para a evolução sustentável da indústria e sociedade Shamsuddin (2017), haja vista, já existirem opções que substituem itens plásticos convencionais (EUROPEAN BIOPLASTICS, 2022). Este mercado em expansão vai ao encontro da sexta onda de inovação baseada no princípio da sustentabilidade, na qual, empresas terão maior competitividade quando comprometidas com a readequação de seus produtos e processos (SILVA; DISERIO, 2015). Ainda, dados projetam aumento na produção de bioplásticos para 6.3 Mt em 2027, especialmente de Polihidroxialcanoatos e, dentre eles, o Poli(3-hidroxibutirato) (P(3HB)) (EUROPEAN BIOPLASTICS, 2022).
O P(3HB) se mostra atrativo ecologicamente, por apresentar características de biocompatibilidade e biodegradabilidade (ALVES et al., 2017). Possui várias aplicações descritas, como na área médica Israni et al. (2019) e agroindustrial Suave et al. (2005); Bhatia et al. (2019), bem como, na produção de filmes para embalagens que acondicionam alimentos (CHEA et al., 2016).
Além do apelo ambiental que dá destaque aos bioplásticos, outra maneira de torná-los atrativos é a aplicação de cores aos produtos. Corantes, quando utilizados na composição, atraem visualmente, tornando-os mais desejáveis e informativos (RABELLO, 2011; FDA, 2017). A adição de cores e o design diferenciam marcas ou indicam benefícios do produto, além de serem considerados fatores importante na decisão de compra (VEIGA, 2019).
Há também um interesse crescente na utilização de materiais ambientalmente amigáveis, a exemplo dos corantes naturais em substituição aos sintéticos. Essa mudança caminha junto ao aumento da consciência ambiental e do interesse público em produtos inovadores, ecologicamente sustentáveis e mais seguros ao consumidor (CARVALHO; SANTOS, 2015). Também, se apresentam como uma opção viável na coloração, sendo biodegradáveis, atóxicos e, na maioria, não alérgenos, não cancerígenos e obtidos de fontes renováveis (VERMA; GUPTA, 2017).
Ainda que o mercado de bioplásticos coloridos industrialmente já seja uma realidade (eeCOO SUSTENTABILIDADE©; BIO-ON®), a utilização de corantes naturais, especialmente na coloração de P(3HB), foi pouco estudada até o momento (HEREK et al., 2006; PAGNAN et al., 2017; LATOS-BROZIO; MASEK; ZABORSKI, 2019, LATOS-BROZIO; MASEK, 2019).
Nesse contexto, o presente trabalho utiliza uma metodologia inédita associada a corantes naturais comerciais na coloração de P(3HB), com o objetivo de demonstrar sua capacidade de adsorção ao bioplástico, avaliando seu potencial de coloração através de ensaios de degradação. Com isso, pretende-se contribuir na inserção dos corantes naturais à coloração de bioplásticos, ainda em desenvolvimento.
2. MATERIAIS E MÉTODOS
2.1 OBTENÇÃO DOS FILMES DE P(3HB) COLORIDOS
Os corantes naturais utilizados foram: páprica, urucum, mostarda, cúrcuma e hibisco (Sabão Glicerina®), previamente peneirados (Tyler 250 μm-60) e testados em quantidades entre 0,5 g e 0,25 g. Foi utilizado 0,25 g de P(3HB) (Biocycle®). Estes foram dissolvidos em clorofórmio, na proporção de 40:1 (v/m), em tubos de ensaio vedados a 58 ºC por 10 min com agitação (Vixar Mixer®) em intervalos de 5 min. O conteúdo dos frascos foi vertido em placas de Petri de vidro semi abertas (60mm x 1mm), sob agitação a 80 rpm (Kline, GT201BDU), conforme método de casting adaptado (MACAGNAN et al., 2017). Para amostra controle, foi usado um filme de 0,25 g de P(3HB) sem corante.
2.2 TESTE DE CONCENTRAÇÃO DOS CORANTES DOS FILMES DE P(3HB) COLORIDOS
A concentração foi registrada por análise macroestrutural visual e colorimétrica dos filmes circulares obtidos. A análise macroestrutural visual foi registrada por fotografia em Fotodocumentador (LPix Image HE – Loccus Biotechnology®).
Os dados colorimétricos foram registrados em coordenadas RGB utilizando Analisador de Cor (ACR-1023 Instrutherm®) e as médias e desvio padrão foram calculados no software Microsoft Office Excel 2016. O valor médio foi submetido à plataforma Easy RGB (http://www.easyrgb.com/en/convert.php) para obtenção da cor correspondente.
2.4 FOTODEGRADAÇÃO DOS FILMES DE P(3HB) COLORIDOS
O ensaio foi realizado em câmara de envelhecimento, de acordo com a norma Operação de Aparelhos de Lâmpadas Ultravioleta Fluorescente (UV) Para Exposição de Materiais Não Metálicos (ASTM G154-16), equipada com 4 lâmpadas UVA de 25W a 28 ºC. Os corpos de prova, em triplicata, (1,5 cm x 1,5 cm x 1 mm – Paquímetro Universal Wurth®), foram submetidos a períodos alternados de presença (8 h) e ausência de iluminação (16 h). As análises foram realizadas nos períodos de 0, 64, 128 e 192 h de ensaio.
A fotodegradação foi registrada por análise macroestrutural visual (Motorola© G8 Plus) e colorimétrica (ACR-1023 Instrutherm®). Os valores das triplicatas foram convertidos em coordenadas CIELab (COMMISSION INTERNATIONALE DE l’ECLAIRAGE.) na plataforma Easy RGB para o cálculo da variação de cor (ΔE) (VELHO, 2016). Os gráficos de (ΔE) foram produzidos no software GraphPad Prism 7. A análise estatística utilizou teste de Tukey (ANOVA) com p ≤ 0,05 no software Statistix 8. As médias e o desvio padrão foram calculados no software Microsoft Office Excel 2016.
2.5 ANÁLISE MICROESTRUTURAL DOS FILMES DE P(3HB) COLORIDOS
A superfície dos filmes de P(3HB) colorido na concentração de 0,15 g foi analisada através de micrografias das amostras antes (0 h) e após o ensaio de fotodegradação (192 h), em Microscópio Eletrônico de Varredura (MEV – Jeol, JSM – 6610 LV). As amostras foram recobertas com Au em metalizador (Denton Vacuum DESK V – voltagem 20 mA/ 300s e aceleração 15 kV).
2.6 ANÁLISE TERMOGRAVIMÉTRICA DOS FILMES DE P(3HB) COLORIDOS
Foram realizadas análises termogravimétricas (TGA) (SDT Q600- TA Instruments, TA60) nos filmes de concentração de 0,15 g. Amostras entre 0,1 a 0,5 mg foram colocadas em porta amostra de platina hermeticamente fechado, nas condições: temperatura entre 30 a 500 °C, fluxo de N2 (g) de 100 mL/min e aquecimento de 10 °C/min.
3. RESULTADOS E DISCUSSÃO
3.1 TESTE DE CONCENTRAÇÃO DOS CORANTES DOS FILMES DE P(3HB) COLORIDOS
Na análise macroestrutural visual dos filmes (Figura 1), observou-se que os corantes pigmentaram o P(3HB) em todas as concentrações, em comparação ao controle. As cores obtidas corresponderam à coloração esperada para os corantes utilizados. Ainda, houve progressão gradual da intensidade de coloração com aumento sucessivo na concentração em todos os corantes avaliados.
Figura 1. Filmes de P(3HB) coloridos nas diferentes concentrações de corantes naturais e amostra controle

Para todos os corantes, os filmes apresentaram coloração heterogênea, com a formação de espaços esbranquiçados nas concentrações de 0,05 g e 0,10 g. Esse comportamento tornou-se menos perceptível para a maioria na concentração de 0,15 g, com exceção do cúrcuma em que observou-se acúmulo desigual nas concentrações de 0,20 g e 0,25 g; além do hibisco, que apresentou coloração desigual em todas concentrações.
Os filmes coloridos com hibisco exibiram uma camada de cor superficial, na qual o corante parecia estar apenas depositado sobre o bioplástico. Também, apresentaram maior quantidade de pontos esbranquiçados independente do aumento na concentração, sugerindo pouca interação entre o corante e o bioplástico. O corante é composto por antocianinas, pigmentos solúveis em solventes polares Schiozer; Barata (2007), o que pode ter dificultado a interação durante o processo, já que na solubilização do P(3HB) é utilizado clorofórmio, um solvente apolar (NETO et al., 2010). Diante do exposto, as amostras de hibisco não tiveram continuidade nas demais análises.
De fato, a aplicação de corantes em pó em polímeros possui desvantagens relacionadas a dispersão que podem levar a variação de cor, ou a necessidade de grandes concentrações para obtenção de coloração sólida (NEUPLAST, 2018). A qualidade do corante também pode interferir na homogeneidade e intensidade da cor no filme de P(3HB) (PAGNAN et al., 2017). Assim, são utilizados ativadores de adesão para aumentar a fixação do corante ao polímero, diminuindo a formação de partículas não homogêneas (BURKHART; ULLMANN, 2017).
Os corantes avaliados foram utilizados em pó na sua versão primária, sendo submetidos apenas a peneiração prévia. Isso pode ter interferido na completa homogeneização durante o processo, da mesma forma, foram evitados quaisquer tipos de fixadores na formação dos filmes de P(3HB) coloridos para que estes tivessem a composição mais próxima a de um produto ambientalmente amigável.
Os resultados da análise colorimétrica das amostras (Tabela 1) foram comparados com as coleções de cores padrão disponíveis na plataforma Easy RGB (Figura 2).
Tabela 1. Valores médios de RGB das triplicatas de P(3HB) colorido nas diferentes concentrações de corantes naturais e amostra controle
| Corante | 0,05 g | 0,10 g | 0,15 g | 0,20 g | 0,25 g |
|
Páprica |
R:239 ±1,52
G:122 ± 2,08 B:44 ± 1,15 |
R:233 ±1,52
G:99 ± 0,577 B:22 ± 1,15 |
R:219 ± 1,52
G:76 ± 1,15 B:47 ± 1,52 |
R:220± 1,52
G:69 ± 1,15 B:39 ± 0,57 |
R:223± 2,08
G:71 ± 1,52 B:41 ± 1,15 |
|
Urucum |
R:239 ± 3,51
G:113 ± 2,08 B:68 ± 3,05 |
R:230 ± 4,16
G:116 ± 2,51 B:78 ± 3,51 |
R:230 ± 3,05
G:107 ± 2,51 B:70 ± 3,05 |
R:226 ± 3,21
G:95 ± 2,51 B:55 ± 3,05 |
R:223 ± 3,51
G:81 ± 2,51 B:37 ± 2,51 |
|
Mostarda |
R:246 ± 3,05
G:237 ± 3,51 B:156 ± 3,78 |
R:242 ± 2,51
G:230 ± 1,52 B:124 ± 2,64 |
R:239 ± 2,08
G:224± 3,05 B:88 ± 1,52 |
R:236 ± 3,05
G:213 ± 3,78 B:46 ± 1,52 |
R:229 ± 3,05
G:209 ± 4,04 B:29 ± 2,64 |
|
Cúrcuma |
R:225 ± 2,08
G:159 ± 1,52 B:66 ± 1,52 |
R:225 ± 3,51
G:155 ± 2,08 B:61 ± 1,52 |
R:206 ± 2
G:136 ± 3,05 B:45 ± 3,05 |
R:203 ± 1,73
G:130 ± 1,52 B:37 ± 2,08 |
R:200 ± 1,52
G:122 ± 2,08 B:22 ± 2,08 |
|
Controle 0,25 g |
R: 253 ± 1,24
G: 249 ± 1,24 B: 250 ± 2,94 |
Fonte: Elaborado pelos autores (2023).
Figura 2. Padrão de cores RGB obtidos na plataforma Easy RGB a partir do teste de concentração dos filmes de P(3HB) coloridos e amostra controle
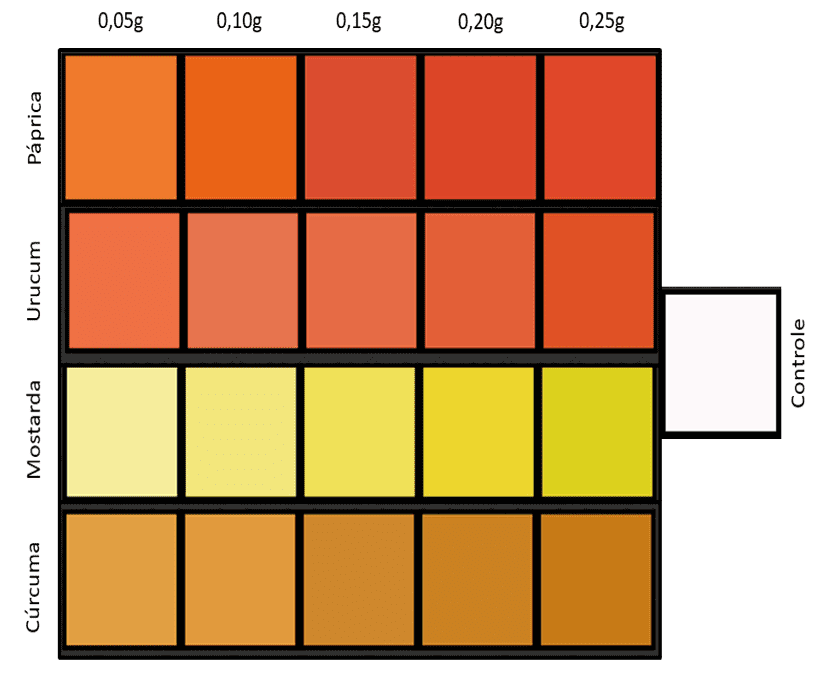
As imagens produzidas a partir dos dados colorimétricos corroboram com as cores observadas na análise visual. Da mesma forma, constata-se que houve diferença na coloração dos filmes de acordo com o aumento da concentração de corante para todas as amostras. Assim, a concentração de 0,15 g foi eleita para a continuidade das análises dos filmes de P(3HB) coloridos, devido a intensidade da cor e a concentração ser a intermediária entre as avaliadas.
3.2 FOTODEGRADAÇÃO DOS FILMES DE P(3HB) COLORIDOS
Visualmente, é possível inferir que todas as amostras dos filmes de P(3HB) coloridos sofreram degradação da cor a partir da incidência de luz UVA ao longo do teste (Figura 3). Os filmes de mostarda foram os que apresentaram maior despigmentação ao final das 196 h, sendo possível observar diferença na cor a partir de 64 h. Já para as amostras de urucum, a despigmentação foi perceptível com maior intensidade a partir de 128 h.
Para os filmes coloridos com páprica e cúrcuma houve despigmentação ao longo do teste, entretanto, apresentaram maior estabilidade de cor, seguidos da amostra controle que também não apresentou diferenças ao final da exposição.
Figura 3. Filmes de P(3HB) coloridos na concentração de 0,15 g dos corantes naturais e amostra controle submetidos a exposição a luz ultravioleta (UVA) artificial

A variação de cor (ΔE) (figura 4) evidencia que, de todos os filmes de P(3HB) coloridos, os de mostarda apresentaram maior alteração de cor ao longo do tempo, seguidos de urucum, páprica e cúrcuma, em relação à amostra controle. Ao final (192 h) foi realizada comparação estatística entre os corantes, que concordaram com os resultados ao longo do teste.
Figura 4. Variação de cor (ΔE) dos filmes de P(3HB) coloridos na concentração de 0,15 g dos corantes naturais e amostra controle submetidos a exposição a luz ultravioleta (UVA) artificial
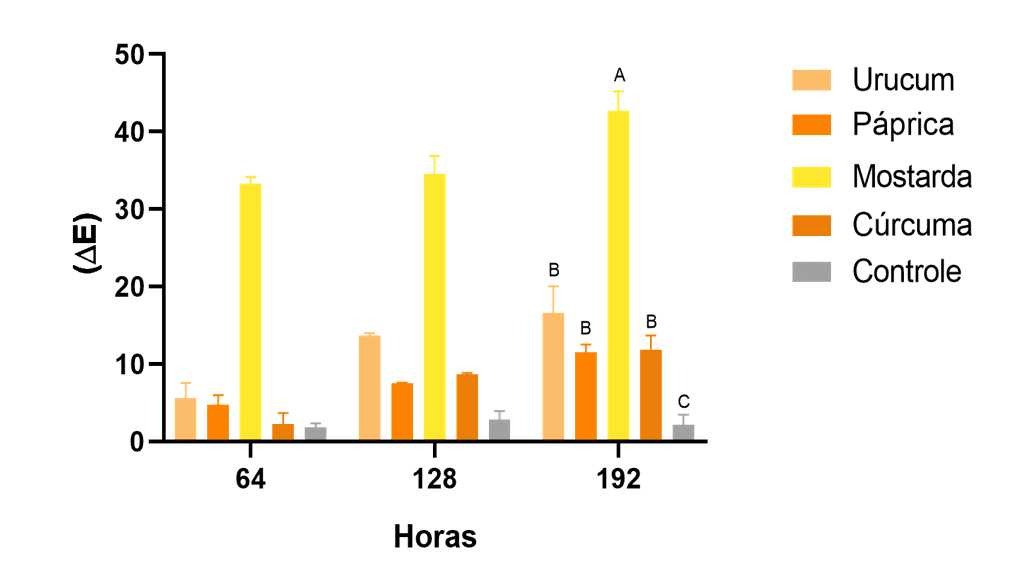
Do mesmo modo, os valores de RGB obtidos das amostras antes (0 h) e ao final da exposição (192 h) foram analisados no site Easy RGB para a obtenção das referidas cores, e, pode-se captar as diferenças em função da exposição a luz UVA (Figura 5) para cada corante e controle, corroborando aos demais resultados visuais (figura 2) e ΔE (figura 4).
Figura 5. Padrão de cores RGB obtidos na plataforma Easy RGB dos filmes de P(3HB) coloridos na concentração de 0,15 g dos corantes naturais e amostra controle submetidos a exposição a luz ultravioleta (UVA) artificial
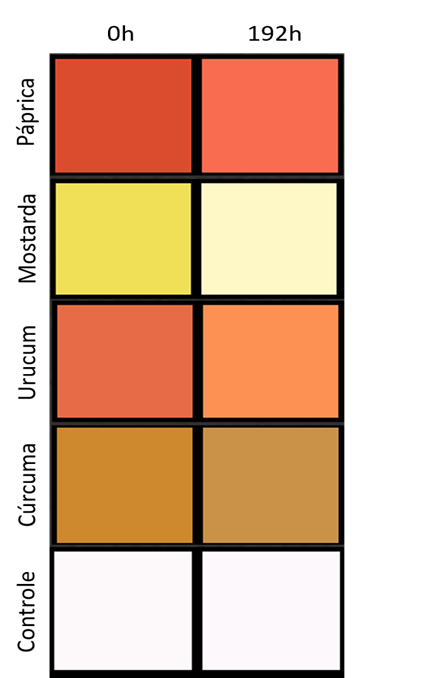
Os corantes utilizados neste estudo possuem em sua composição compostos carotenóides como a luteína (mostarda), capsantina e β-criptoxantina (páprica), bixina (urucum) e curcumina (cúrcuma). Uma das principais características dos carotenóides é a presença de ligações duplas conjugadas correspondentes aos cromóforos, permitindo absorverem a luz do espectro visível, conferindo cor aos carotenóides. Também, são pontos suscetíveis à isomerização e oxidação, pois acredita-se que exposição à luz induz a fotoisomerização trans-cis e a fotodestruição dos carotenóides, demonstrando a sensibilidade desses pigmentos a luz (SCHIOZER; BARATA, 2007).
A páprica é um corante natural de coloração avermelhada, obtido pela moagem de frutos desidratados de variedades de pimentões (Capsicum annuum L.), sendo um condimento muito popular (RIBEIRO, 2012). Embora os processos de degradação das cores dos carotenóides sejam aumentados na presença de luz e calor, alterando consideravelmente a estrutura do cromóforo Schiozer; Barata, (2007), nos filmes de P(3HB) deste estudo apresentou discreta despigmentação ao longo do teste.
Das sementes de Bixa orellana é extraído o corante urucum, de cor alaranjada, utilizado em diversas aplicações, além de apresentar propriedades repelentes e de proteção contra raios ultravioletas (BRANDÃO et al., 1992). A estrutura química da bixina, carotenóide que integra majoritariamente sua composição, é formada por moléculas de carbono com ligações duplas associadas a grupos carboxila. Essas estruturas formam sítios de interação com a luz UV, o que pode aumentar as reações de descoloração (SCOTTER, 2009; SOUZA et al., 2016). Pagnan et al. (2017) obteve filmes coloridos de P(3HB) com urucum em três concentrações, sendo submetidos a radiação UV artificial por 240 h. Seus resultados mostraram que todas as concentrações apresentaram aumento nos valores de ΔE ao final do teste.
A luteína dá coloração amarela ao corante mostarda extraído dos grãos secos da mostarda amarela (Sinapis alba L.) (STRINGHETA et al., 2006). O trabalho de Latos-Brozio e Masek (2019), que aplicaram luteína, beta caroteno, clorofila e cúrcumina em poli(ácido lático) (PLA) e P(3HB), avaliou a estabilidade das composições submetidas a radiação UV em períodos de 100 h a 300 h de exposição. Para as amostras de luteína no P(3HB), observou-se mudança de coloração, assim como para os resultados obtidos neste estudo. Ainda, houve degradação das cores durante todo o período do teste, entretanto, ocorreu perda abrupta da coloração nas composições com luteína entre 100 h e 200 h, diferentemente das amostras com o corante mostarda testadas neste estudo, sendo perceptível após 64 h de exposição. Os autores destacam a alta sensibilidade a radiação UV que os corantes beta caroteno, luteína e cúrcuma possuem quando expostos por mais de 100 h.
A curcumina é o pigmento componente majoritário nos rizomas de Curcuma longa e deles é extraído o corante cúrcuma na forma de pó seco, utilizado para coloração alimentícia devido à sua forte coloração amarela (SUETH-SANTIAGO et al., 2015). Latos-Brozio e Masek (2019), observaram o mesmo comportamento para o corante cúrcuma, isto é, modificação abrupta na coloração entre 100 h e 200 h. Neste trabalho o corante cúrcuma apresentou variação de cor (ΔE) ao longo do processo de fotodegradação.
3.3 ANÁLISE MICROESTRUTURAL DOS FILMES DE P(3HB) COLORIDOS
Na análise microestrutural dos filmes (Figura 6), identificou-se que a adição dos corantes ao P(3HB) modificou a superfície das amostras, reduzindo a porosidade, quando em comparação ao controle, para todos os corantes testados (0 h). Da mesma forma, tal comportamento se manteve para todos os corantes e controle após a exposição à fotodegradação por 192 h.
Figura 6. Microscopia Eletrônica de Varredura dos filmes de P(3HB) coloridos na concentração de 0,15 g dos corantes naturais e amostra controle submetidos a exposição a luz ultravioleta (UVA) artificial
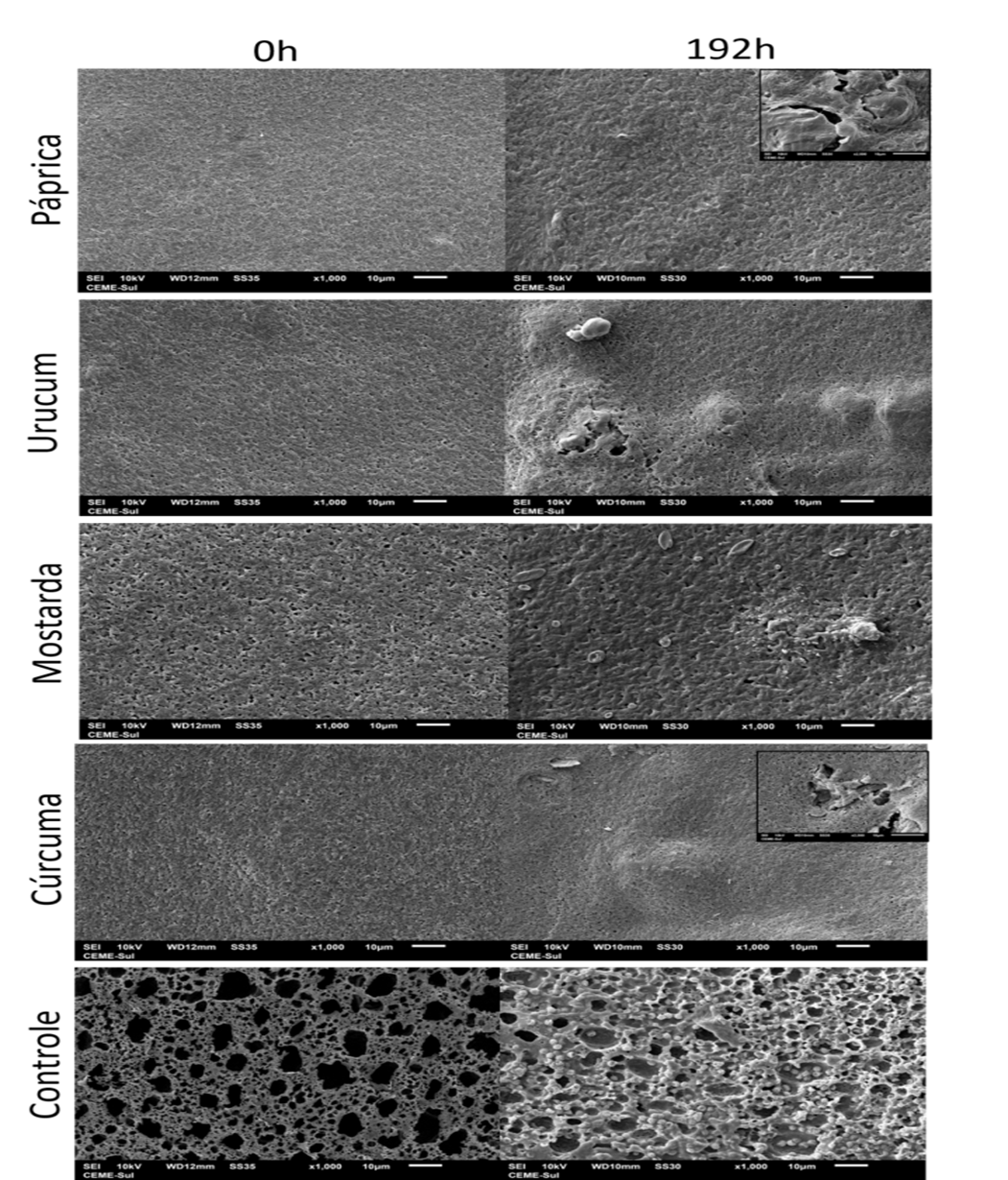
Nas imagens após 192 h (Figura 6), há existência de fissuras, em destaque no canto superior direito, e elevações nos filmes de páprica, urucum e cúrcuma, evidenciando que a fotodegradação foi capaz de produzir danos ao material, além da diminuição da coloração observada previamente (Figura 3). Entretanto, para o controle e os filmes de mostarda, se revelam rugosidades e modificações, não sendo perceptível se a exposição causou danos significativos à superfície. Ou seja, ainda que o mesmo tenha apresentado a maior diferença de perda de coloração entre as amostras (Figura 3), sua superfície não apresentou evidências de quebra do material.
Os mecanismos que envolvem a fotodegradação de polímeros são complexos e abrangem fatores que dependem não somente da estrutura química do corante, mas também das características do polímero, estando associados a interações diversas entre eles (RABELLO, 2011). Dessa forma, pode interagir em propriedades do P(3HB), dentre elas: mudança da coloração aumentando a opacidade e tornando o material esbranquiçado; redução da massa molar, promovendo a perda de material e tornando a superfície mais áspera e suscetível a fissuras; aumento da cristalinidade superficial do bioplástico, reduzindo as regiões porosas do material, como pode ser visualizado no controle (SANTOS et al., 2018).
Corantes podem participar ativamente nos processos de fotodegradação em polímeros, pois interferem diretamente na incidência da radiação, podendo diminuir, estabilizar ou acelerar o processo (SARON; FELISBERTI, 2006). No caso da mostarda, o mesmo parece atuar como um estabilizador, agindo como um filtro no bioplástico, reduzindo as reações que levam a formação de fissuras decorrentes do processo. Segundo Allen (1994), o comportamento de ação do corante à semelhança de um filtro torna-se mais influente de acordo com o aumento na concentração de corante utilizado no polímero. Dessa forma, Pagnan et al. (2017) também observou essas propriedades de proteção à radiação UVA em filmes de P(3HB) coloridos com maiores concentrações de urucum.
3.4 ANÁLISE TERMOGRAVIMÉTRICA DOS FILMES DE P(3HB) COLORIDOS
Os resultados de TGA dos filmes de P(3HB) coloridos e controle (Figura 7), mostram as curvas de degradação térmica do material comparando o efeito da adição dos corantes em relação ao controle.
Figura 7. Curvas termogravimétricas dos filmes de P(3HB) coloridos na concentração de 0,15 g dos corantes naturais e amostra controle
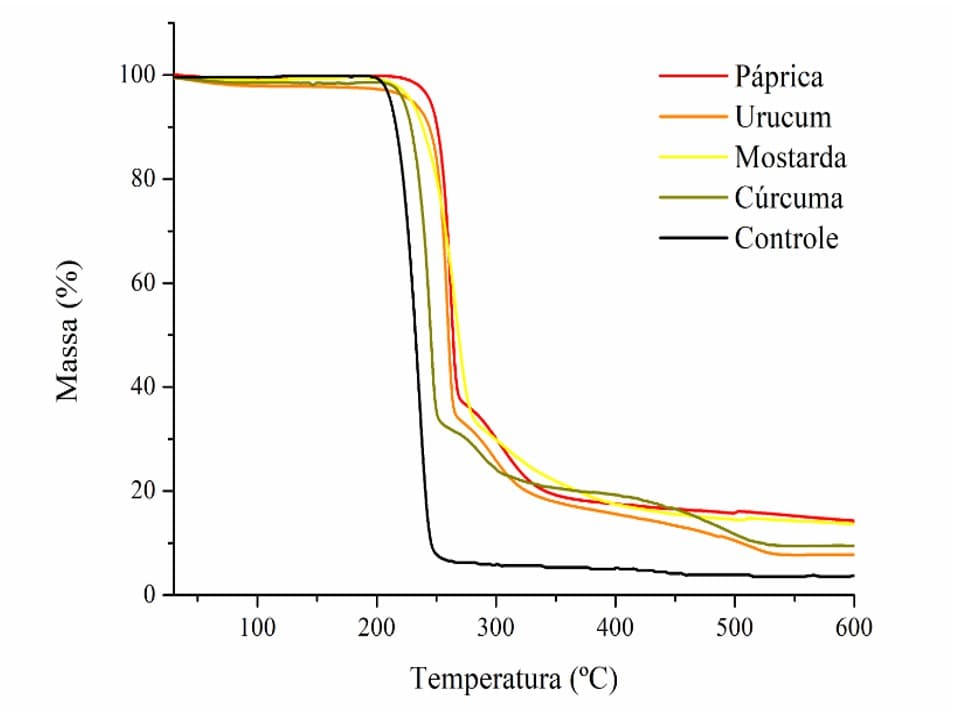
No gráfico da porcentagem de perda de massa pela temperatura (figura 7), as curvas apresentaram perfil de degradação semelhante entre os filmes coloridos e o controle, indicando que a concentração 0,15 g de corante inserida está abaixo da mínima para gerar alterações na estabilidade térmica no bioplástico, já que este apresenta temperaturas de degradação em torno de 240 ºC (ARAGOSA; SPECCHIA; FRIGIONE, 2021). Todas as amostras tiveram início da degradação em torno de 220 ºC e estabilização em 250 ºC, apresentando todo material volatilizado sem deixar resíduos, perda de massa de 90% e um ganho em estabilidade térmica de 30ºC. Ou seja, a degradação térmica dos filmes para todos os corantes ocorreu em um único processo de perda de massa sem diferenças no mecanismo, sugerindo que a inserção dos corantes não afetou o comportamento térmico do material, gerando apenas mais etapas de decomposição durante o processo.
4. CONCLUSÃO
Neste trabalho foi possível colorir filmes de P(3HB) com quatro corantes naturais (páprica, urucum, mostarda e cúrcuma) nas diferentes concentrações avaliadas com êxito, demonstrando que a metodologia de coloração empregada é eficiente para obtenção do P(3HB) colorido. Seu uso pode ser estudado futuramente para outros corantes e para possíveis aplicações do bioplástico.
Quando expostos ao ensaio de envelhecimento sujeitos à incidência de radiação UVA, os filmes de todos os corantes apresentaram variação de cor, resultando em perdas na coloração dos filmes. Todavia, mantiveram ao final do teste, coloração semelhante à cor natural do corante em pó, ou seja, não descaracterizando os filmes.
Nas micrografias foi observada a diminuição da porosidade dos filmes coloridos após a inserção dos corantes, e também os danos sofridos pelo material após a exposição à radiação UVA. Neste contexto, os filmes coloridos apresentaram maior integridade em relação ao controle.
A adição dos corantes naturais parece não interferir na degradação térmica dos filmes de P(3HB).
Esses resultados mostram que a utilização de corantes naturais comerciais em substituição aos corantes sintéticos se apresentam como uma alternativa sustentável para a coloração de filmes de P(3HB).
5. AGRADECIMENTOS
Este trabalho foi realizado com apoio do Conselho Nacional de Desenvolvimento Científico e Tecnológico (CNPq – Projeto 426266/2018) e Coordenação de Aperfeiçoamento de Pessoal de Nível Superior (CAPES – Código de Financiamento 001). As imagens de MEV foram realizadas pelo Centro de Microscopia Eletrônica do Sul (CEME-Sul) da Universidade Federal do Rio Grande.
REFERÊNCIAS
ALLEN, N. S. Photofading and light stability of dyed and pigmented polymers. Polymer degradation and stability, 44, p. 357-374, 1994. Disponível em: <https://doi.org/10.1016/0141-3910(94)90095-7>.
ALVES, M. et al. Poly(3-hydroxybutyrate) – P(3HB): Review of Production Process Technology. Industrial Biotechnology. v. 13, n. 4, p. 192-208, 2017. Disponível em: <https://doi.org/10.1089/ind.2017.0013>.
ARAGOSA, A.; SPECCHIA, V.; FRIGIONE, M.E. PHB Produced by Bacteria Present in the Argan Field Soil: A New Perspective for the Synthesis of the Bio-Based Polymer. Proceedings, v. 69(1), n. 5, p. 5-7, 2021. Disponível em: https://doi.org/10.3390/CGPM2020-07226.
ASTM G154-16. Standard Practice for Operating Fluorescent Ultraviolet (UV) Lamp Apparatus for Exposure of Nonmetallic Materials. Standard by ASTM International, 2016. Disponível em: https://asrecomposite.com/wp-content/uploads/2021/07/ASTM-G-154-2016.pdf. Acesso em: 12 mar. 2023.
AUTA, H. S.; EMINKE, C. U.; FAUZIAH, S. H. Distribution and importance of microplastics in the marine environment: a review of the sources, fate, effects, and potential solutions. Environment International. v. 102, p. 165-176, 2017. Disponível em: <https://doi.org/10.1016/j.envint.2017.02.013>.
BHATIA, S. K. et al. Lipase mediated functionalization of poly (3-hydroxybutyrate-co-3-hydroxyvalerate) with ascorbic acid into an antioxidant active biomaterial. International Journal of Biological Macromolecules, v. 123, p. 117-123, 2019. Disponível em: <https://doi.org/10.1016/j.ijbiomac.2018.11.052>.
BIO-ON®. Production – Essential data on “basic” PHAs production, 2023. Disponível em: <http://www.bio-on.it/production.php>. Acesso em: 12 mar. 2023.
BIOPLASTICS, EUROPEAN. Bioplastics market data, 2022. Disponível em: <https://www.european-bioplastics.org/market/>. Acesso em: 22 mar. 2023.
BRANDÃO, M. G. L. et al. Survey of medicinal plants used as antimalarials in the Amazon, Journal of Ethnopharmacology, v. 36(2), p. 175–182, 1992. Disponível em: <https://doi.org/10.1016/0378-8741(92)90018-m>.
BURKHART, C.; ULLMANN, K. Considerações sobre o uso de corantes líquidos. Revista Plástico Industrial, Ano 19, Aranda Editora, 2017. Disponível em: https://www.arandanet.com.br/assets/revistas/pi/2017/marco/index.php#page=18 Acesso em: 28 mar. 2023.
CARVALHO, C.; SANTOS, G. Global Communities, Biotechnology and Sustainable Design– Natural / Bio Dyes in Textiles. Procedia Manufacturing, v. 3, p. 6557-6564, 2015. Disponível em: <https://doi.org/10.1016/j.promfg.2015.07.956>.
CHEA V. et al. Poly(3-hydroxybutyrate-co-3-hydroxyvalerate) films for food packaging: Physical–chemical and structural stability under food contact conditions. Journal of Applied Polymer Science, v. 133, p. 1–8, 2016. Disponível em: <https://doi.org/10.1002/app.41850>.
COMMISSION INTERNATIONALE DE l’ECLAIRAGE. International Standards. Disponível em: <https://cie.co.at/publications/international-standards>. Acesso em: 28 mar. 2023.
SANTOS, A. J. et al. From Obtaining to Degradation of PHB: A Literature Review. Part II. Ingeniería y Ciencia, v.14, n. 27, p. 207–228, 2018. Disponível em: <https://doi.org/10.17230/ingciencia.14.27.9>.
eeCOO SUSTENTABILIDADE®. Produtos – Talheres, Colher sobremesa biodegradável Rosa ou Verde 15cm, 2023. Disponível em: https://www.eecoo.com.br/categoria-produto/talheres-biodegradaveis-e-compostaveis/. Acesso em: 20 mar. 2023.
FOOD AND DRUG ADMINISTRATION – FDA. Color Additives History, 2017. Disponível em: <https://www.fda.gov/industry/color-additives/color-additives-history>. Acesso em: 14 mar. 2023.
GEYER, R.; JAMBECK, J. R.; LAW, K. L. Production, use, and fate of all plastics ever made. Science Advances, v. 3, n. 7, e1700782, 2017. Disponível em: <https://doi.org/10.1126/sciadv.1700782>.
HEREK, L. C. S. et al. Impregnation of PET Films and PHB Granules with Curcumin in Supercritical CO2. Brazilian Journal of Chemical Engineering, v. 23, n. 2, p. 227 – 234, 2006. Disponível em: <https://doi.org/10.1590/S0104-66322006000200010>.
ISRANI, N; SHIVAKUMAR, S. Polyhydroxybutyrate: development and applications as a biodegradable biotextile, chapter 13, p. 405-444. Materials for Biomedical Engineering: Biopolymers Fibers. Elsevier, Amsterdan, Holand, 2019. Disponível em: <https://doi.org/10.1016/B978-0-12-816872-1.00014-5>.
LATOS, M.; MASEK, A.; ZABORSKI, M. The potential of juglone as natural dye and indicator for biodegradable polyesters. Proceedings of the Institution of Mechanical Engineers, Part L: Journal of Materials: Design and Applications, v.233, p. 276-285, 2019. Disponível em: <10.1177/1464420718804271>.
LATOS-BROZIO, M.; MASEK, A. The application of natural food colorants as indicator substances in intelligent biodegradable packaging materials. Food and Chemical Toxicology, v. 135, 110975, 2019. Disponível em: <https://doi.org/10.1016/j.fct.2019.110975>.
MACAGNAN, K. L. et al. Simplified recovery process of Ralstonia solanacearum-synthesized polyhydroxyalkanoates via chemical extraction complemented by liquid-liquid phase separation. Química Nova, v. 40, n. 2, p. 125-130, 2017. Disponível em: <https://doi.org/10.21577/0100-4042.20160162>.
NETO, J. O. et al. Metodologia para tratamento de clorofórmio comercial para uso em separações cromatográficas. Comunicado Técnico 164 Embrapa Agroindústria de Alimentos, Rio de Janeiro, RJ. ISSN 0103-5231, 2010. Disponível em: https://ainfo.cnptia.embrapa.br/digital/bitstream/item/74946/1/pub-145.pdf. Acesso em: 12 mar. 2023.
NEUPLAST, Pigmentos para plásticos: como funciona o processo de pigmentação?, 26 de julho de 2018. Disponível em: <https://www.neuplast.com.br/blog/pigmentos-para-plasticos-como-funciona-o-processo-de-pigmentacao/>. Acesso em: 17 de março de 2023.
PAGNAN, C. S. et al. Annatto-colored Poly(3-hydroxybutyrate): A Comprehensive Study on Photodegradation. Journal of Polymers and the Environment. v. 26, p. 1169–1178, 2017. Disponível em: <https://doi.org/10.1007/s10924-017-1026-1>.
PLASTICS EUROPE, Plastics – The Facts 2022, 2022. Disponível em: <https://plasticseurope.org/knowledge-hub/plastics-the-facts-2022/>. Acesso em: 14 abr. 2023.
RABELLO, M. Aditivação de Polímeros. Editora Artilber, 250 p, São Paulo, SP, 2011.
RIBEIRO, C. S. C. Qualidade de páprica, Anais do 52º Congresso Brasileiro de Olericultura, Salvador, Bahia. Revista Horticultura Brasileira v. 30, n. 2, 2012. Disponível em: <http://www.abhorticultura.com.br/eventosx2/eventosx/trabalhos/ev_6/PAL2.pdf>. Acesso em: 17 maio 2023.
SARON, C.; FELISBERTI, M. I. Ação de colorantes na degradação e estabilização de polímeros. Química Nova, v. 29, p. 124-128, 2006. Disponível em: <https://doi.org/10.1590/S0100-40422006000100022>.
SCHIOZER, A. L.; BARATA, L. E. S. Estabilidade de Corantes e Pigmentos de Origem Vegetal, Revista Fitos, v. 3, n. 2, p. 6-24, 2007. Disponível em: https://revistafitos.far.fiocruz.br/index.php/revista-fitos/article/view/71. Acesso em: 17 maio 2023.
SCOTTER, M. The chemistry and analysis of annatto food colouring: a review, Food Additives and Contaminants – Part A, v. 26, n. 8, p. 1123–1145, 2009. Disponível em: <https://doi.org/10.1080/02652030902942873>.
SHAMSUDDIN, I. M. Bioplastics as Better Alternative to Petroplastics and Their Role in National Sustainability: A Review. Advances in Bioscience and Bioengineering, v. 5, n. 4, p. 63-70, 2017. Disponível em:<https://doi: 10.11648/j.abb.20170504.13>.
SILVA, A. L. P. et al. Increased plastic pollution due to COVID-19 pandemic: Challenges and recommendations. Chemical Engineering Journal, v. 405, p. 126683, 2020. Disponível em: <https://doi.org/10.1016/j.cej.2020.126683>.
SILVA, G.; DISERIO, L. Sexta onda de inovação: Estamos preparados?, 2015. Disponível em: https://www.researchgate.net/publication/301543100_SEXTA_ONDA_DA_INOVACAO_ESTAMOS_PREPARADOS. Acesso em: 03 abr. 2023.
SOUZA, A. R. et al. Photodegradation of UHMWPE Compounded with Annatto and Beetroot Extracts. International Journal of Polymer Science, v. 2016, article ID 4346516, 2016. DOI: <https://doi.org/10.1155/2016/4346516>.
STRINGHETA, P. C. et al. Lutein: antioxidant properties and health benefits. Alimentos e Nutrição Araraquara, v. 17, n. 2, p. 229-238, 2006. Disponível em: https://www.researchgate.net/publication/49599824_LUTEINA_PROPRIEDADES_ANTIOXIDANTES_E_BENEFICIOS_A_SAUDE. Acesso em: 17 maio 2023.
SUAVE, J. et al. Microencapsulação do pesticida malathion em polímeros biodegradáveis: caracterização e ensaios de liberação. VIII Congresso Brasileiro de Polímeros, 2005. Disponível em: https://www.researchgate.net/publication/280076628_MICROENCANPSULACAO_DO_PESTICIDA_MALATHION_EM_POLIMEROS_BIODEGRADAVEIS_CARACTERIZACAO_E_ENSAIOS_DE_LIBERACAO. Acesso em: 17 maio 2023.
SUETH-SANTIAGO, V. et al. Curcumina, O Pó Dourado Do Açafrão-Da-Terra: Introspecções Sobre Química E Atividades Biológicas. Química Nova, v. 38, n. 4, p. 538-552, 2015. Disponível em: <https://doi.org/10.5935/0100-4042.20150035>.
VEIGA, M. P. A influência do Design na decisão de compra. (Trabalho de Conclusão de Curso) Graduação em Administração, Universidade de Caxias do Sul, Farroupilha, 2019. Disponível em: https://repositorio.ucs.br/xmlui/handle/11338/5908?locale-attribute=de Acesso em: 17 maio 2023.
VELHO, S. R. K. Desenvolvimento de corantes naturais estruturados para uso em plástico. (Tese). Programa de Pós-Graduação em Engenharia de Minas, Metalúrgica e de Materiais, Universidade Federal do Rio Grande do Sul, 2016. Disponível em: https://lume.ufrgs.br/handle/10183/150608. Acesso em: 17 maio 2023.
VERMA, S.; GUPTA, G. Natural dyes and its applications: A brief review. International Journal of Research and Analytical Reviews, v. 4, n. 4, 2017. Disponível em: http://ijrar.com/upload_issue/ijrar_issue_490.pdf. Acesso em: 18 maio 2023.
[1] Mestrado. ORCID: 0009-0003-9707-7599. Currículo Lattes: http://lattes.cnpq.br/3038246505868385.
[2] Mestrado. ORCID: 0000-0001-5511-7765.
[3] Graduação. ORCID: 0000-0002-7533-0341.
[4] Doutorado. ORCID: 0000-0002-8168-5771.
[5] Doutorado. ORCID: 0000-0002-1952-220X.
[6] Doutorado. ORCID: 0000-0002-5323-6311.
[7] Orientadora. Doutorado. ORCID: 0000-0001-9601-296X.
Enviado: 24 de maio, 2023.
Aprovado: 22 de junho, 2023.

